ARASAMILA
RITUXIMAB
Solución
1 Caja, 1 Frasco(s) ámpula, 10 mL, 100/10 mg/ml
1 Caja, 2 Frasco(s) ámpula, 10 mL, 100/10 mg/ml
1 Caja, 1 Frasco(s) ámpula, 50 mL, 500/50 mg/ml
1 Caja, 2 Frasco(s) ámpula, 50 mL, 500/50 mg/ml
FORMA FARMACÉUTICA Y FORMULACIÓN:
El frasco ámpula contiene:
Rituximab 100 mg, 500 mg
Vehículo cbp 10 mL, 50 mL
INDICACIONES TERAPÉUTICAS: ARASAMILA® está indicado para el tratamiento de pacientes con:
Linfoma no Hodgkin (LNH):
• Linfoma no Hodgkin indolente o folicular de linfocitos B, CD20 positivo, en recaída o quimiorresistente.
• Linfoma folicular en pacientes en fase III y IV sin tratamiento previo, en combinación con quimioterapia.
• Como terapia de mantenimiento en pacientes con linfoma folicular que hayan respondido a la terapia de inducción.
• Está indicado para el tratamiento de pacientes adultos con linfoma no Hodgkin difuso de células B grandes, CD20 positivo, en combinación con quimioterapia CHOP (ciclofosfamida, doxorrubicina, vincristina y prednisona).
Leucemia linfocítica crónica (LLC):
ARASAMILA® en combinación con quimioterapia está indicado para el tratamiento de leucemia linfocítica crónica (LLC) en pacientes sin tratamiento previo y en recaída/refractarios.
Granulomatosis con poliangeítis (Wegener) (GPA) y poliangeítis microscópica (PAM): ARASAMILA®, en combinación con glucocorticoides, está indicado para el tratamiento de pacientes con granulomatosis severamente activa con poliangeítis (GPA, también conocida como granulomatosis de Wegener) y poliangeítis microscópica.
FARMACOCINÉTICA Y FARMACODINAMIA:
Grupo farmacoterapéutico: Agentes antineoplásicos, anticuerpos monoclonales, código ATC: L01FA01.
ARASAMILA® (Rituximab) es un medicamento biológico desarrollado por vía de comparación (biosimilar).
El programa de desarrollo del producto fue diseñado para demostrar la comparabilidad entre ARASAMILA® y el fármaco comparador rituximab, conocido como Rituxan® (versión aprobada por los EE. UU.) o MabThera® (versión aprobada por la UE). De acuerdo con la información públicamente disponible, el siguiente estudio clínico sobre ARASAMILA® proporciona resultados de comparabilidad en eficacia:
• Estudio de eficacia clínica, seguridad, PK, EP e inmunogenicidad de fase III (GP13-301) para demostrar eficacia equivalente y seguridad, inmunogenicidad, PK y PD equivalentes de ARASAMILA® en comparación con el rituximab de origen (versión aprobada por la UE de MabTheraThe) en combinación con quimioterapia con ciclofosfamida, vincristina, prednisona (CVP) en pacientes con linfoma folicular avanzado (FL).
En la Tabla 1 se describe un breve resumen de los diseños de estudio y las poblaciones evaluadas:
|
ID Estudio |
Título de estudio |
Población de estudio |
Diseño y duración del estudio |
Dosis y vía de administración |
|
Estudio pivotal |
||||
|
GP13-301 |
Un ensayo aleatorizado, controlado, doble ciego de fase III para comparar la eficacia, la seguridad y la farmacocinética de GP2013 más ciclofosfamida, vincristina, prednisona frente a MabThera® más ciclofosfamida, vincristina, prednisona, seguido de terapia de mantenimiento GP2013 o MabThera® en pacientes con tratamiento previo linfoma folicular en estadio avanzado no tratado (ensayo ASSIST-FL) |
Pacientes con estadio FL avanzado no tratado previamente Fase de combinación: Total: 627 (350f, 277m) ARASAMILA®: N = 312 (181f, 131m) MabThera®: N = 315 (169f, 146m) Fase de mantenimiento: Total: 506 (294f, 212m) ARASAMILA®: N = 254 (151f, 103m) MabThera®: N = 252 (143f, 109m) |
Aleatorio, controlado, doble ciego, grupo paralelo Hasta 3 años 1 mes, incluido un periodo de detección de 28 días, aproximadamente 6 meses de tratamiento combinado y aproximadamente 2.5 años de tratamiento de mantenimiento y/o periodo de seguimiento |
Periodo de tratamiento combinado: 8 ciclos totales de ARASAMILA® o MabThera® 375 mg/m2 i.v. el día 1 de cada ciclo + CVP administrado cada 21 días (± 3 días) Periodo de tratamiento de mantenimiento (pacientes con PR o CR después de 8 ciclos de tratamiento combinado): 8 ciclos de tratamiento de ARASAMILA® o MabThera® 375 mg/m2 i.v. administrado cada 3 meses (± 14 días) por otros 2 años1. |
CR, respuesta completa; DMARD, fármacos antirreumáticos modificadores de la enfermedad; i.v., intravenoso (ly); f, femenino; m, masculino; MTX, metotrexato; N, número de pacientes o sujetos; TNF, factor de necrosis tumoral.
1 Sólo para Italia, consta de 12 ciclos de tratamiento de agente único ARASAMILA®/MabThera® administrado cada 2 meses (± 14 días) durante 2 años más.
Farmacodinamia:
Comparabilidad de los resultados de eficacia entre ARASAMILA® y rituximab de referencia:
Linfoma no Hodgkin: De acuerdo con la información públicamente disponible, la eficacia y la seguridad de ARASAMILA® se compararon con el medicamento de comparación en un estudio clínico aleatorizado pivotal doble ciego (GP13-301) en pacientes adultos con linfoma no Hodgkin folicular positivo para CD20 en estadio III/IV no tratado previamente.
El estudio consta de dos fases: terapia combinada con ciclofosfamida, vincristina y prednisona (CVP) durante 8 ciclos de tratamiento; seguido de una fase de mantenimiento donde los respondedores continuaron con ARASAMILA® o monoterapia con el medicamento de referencia durante 2 años.
Según los resultados de eficacia primarios y secundarios, se demostró la equivalencia entre ARASAMILA® y el medicamento de referencia en términos de tasa de respuesta general para la evaluación del tumor, respuesta completa, respuesta parcial, enfermedad estable y enfermedad progresiva, en pacientes con estadio avanzado no tratado previamente con linfoma folicular. Objetivo primario de evaluación: La tasa de respuesta global (ORR) al completar la fase de tratamiento de combinación, fue equivalente entre los dos tratamientos, como se muestra a continuación:
Tabla 2. Análisis primario de eficacia de ORR basado en los criterios de respuesta modificados para el linfoma maligno (PPS)
|
ARASAMILA® N = 311 n (%) [90% CI] |
MabThera® N = 313 n (%) [90% CI] |
Diferencia (ARASAMILA® y MabThera®) |
|
|
Tasa de respuesta global (CR or PR) |
271 (87.1%) [83.59, 90.15]1 |
274 (87.5%) [84.04, 90.49]1 |
-0.40% 95% CI: [-5.94, 5.14] 2 90% CI: [-5.10, 4.30] 2 |
1 Los IC del 90% de ORR son intervalos exactos derivados de la fórmula de Clopper-Pearson.
2 Los IC del 95% y 90% para las diferencias en las proporciones se basan en una aproximación normal a la distribución binomial.
PPS, por conjunto de protocolos; IC, intervalo de confianza; ORR, tasa de respuesta general; CR, respuesta completa; PR, respuesta parcial. El criterio de valoración secundario clave es la mejor respuesta general (BOR), definida como la mejor respuesta a la enfermedad registrada desde la aleatorización hasta la progresión, el inicio del nuevo tratamiento contra el cáncer o el final de la fase de combinación del estudio, lo que ocurra primero. Los resultados de BOR indican que la proporción de pacientes en cada una de las categorías de respuesta (Respuesta completa, Respuesta parcial, Enfermedad estable y Enfermedad progresiva), y sus intervalos de confianza del 90% asociados, para ARASAMILA® y el medicamento de referencia fueron similares a los mostrados abajo.
Tabla 3. Análisis secundario de eficacia de BOR basado en las evaluaciones de tumor cegado central (PPS)
|
Mejor respuesta global |
ARASAMILA® N = 311 n (%) [90% CI]1 |
MabThera® N = 313 n (%) [90% CI]1 |
|
Respuesta completa |
46 (14.8%) [11.6, 18.5] |
42 (13.4%) [10.4, 17.0] |
|
Respuesta parcial |
225 (72.3%) [67.9, 76.5] |
232 (74.1) [69.7, 78.2] |
|
Enfermedad estable |
20 (6.4%) [4.3, 9.2] |
20 (6.4%) [4.3, 9.1] |
|
Enfermedad progresiva |
1 (0.3%) [0.0, 1.5] |
3 (1.0%) [0.3, 2.5] |
|
Se desconoce/falta |
19 (6.1%) |
16 (5.1%) |
1 Los IC del 90% de ORR son intervalos exactos derivados de la fórmula de Clopper-Pearson.
PPS, por conjunto de protocolos; IC, intervalo de confianza.
Comparabilidad de la inmunogenicidad entre ARASAMILA® y el comparador rituximab:
En el estudio clínico aleatorizado, doble ciego (GP13-301) en pacientes adultos con linfoma no Hodgkin folicular CD20 positivo no tratado previamente, estadio III/IV, el número de pacientes con ADA detectables después del tratamiento fue bajo (5/274 pacientes [1.8%] en el grupo ARASAMILA® y 3/285 pacientes [1.1%] en el grupo MabThera®). Se detectaron NAbs en 2 de 274 (0.7%) pacientes en el grupo ARASAMILA® y 2 de 285 (0.7%) pacientes en el grupo MabThera®.
No se observaron diferencias relevantes en términos de seguridad general entre pacientes con y sin ADA/NAbs.
Rituximab se une específicamente al antígeno transmembrana, CD20, una tosfoproteína no glicosilada, ubicada en los linfocitos pre-By B maduros. El antígeno se expresa en > 95% de todos los linfomas no Hodgkin de células B.
El CD20 se encuentra tanto en las células B normales como en las malignas, pero no en las células madre hematopoyéticas, las células pro-B, las células plasmáticas normales u otros tejidos normales. Este antígeno no se internaliza tras la unión del anticuerpo y no se elimina de la superficie celular. CD20 no circula en el plasma como antígeno libre y, por lo tanto, no compite por la unión de anticuerpos.
El dominio Fab de rituximab se une al antígeno CD20 en los linfocitos B y el dominio Fc puede reclutar funciones efectoras inmunitarias para mediar en la lisis de las células B. Los posibles mecanismos de lisis celular mediada por efectores incluyen la citotoxicidad dependiente del complemento (CDC) resultante de la unión de C1q y la citotoxicidad celular dependiente de anticuerpos (ADCC) mediada por uno o más de los receptores Fc? en la superficie de granulocitos, macrófagos y células NK (natural killer). También se ha demostrado que la unión de rituximab al antígeno CD20 en los linfocitos B induce la muerte celular por apoptosis.
Los recuentos de células B periféricas disminuyeron por debajo de lo normal después de completar la primera dosis de rituximab. En pacientes tratados por neoplasias hematológicas malignas, la recuperación de células B comenzó dentro de los 6 meses posteriores al tratamiento y, en general, volvió a los niveles normales dentro de los 12 meses posteriores a la finalización de la terapia, aunque en algunos pacientes esto puede llevar más tiempo (hasta una mediana de tiempo de recuperación de 23 meses después de la finalización de la terapia de inducción). En pacientes con GPA o PAM, el número de células B en sangre periférica disminuyó a < 10 células/μL después de dos infusiones semanales de 375 mg/m2 de rituximab, y se mantuvo en ese nivel en la mayoría de los pacientes hasta el punto de tiempo de 6 meses. La mayoría de los pacientes (81%) mostró signos de retorno de células B, con recuentos > 10 células/μI en el mes 12, aumentando al 87% de los pacientes en el mes 18.
Experiencia clínica en linfoma no Hodgkin (LNH) y en leucemia linfocítica crónica (LLC):
Linfoma folicular:
Monoterapia:
Tratamiento inicial, semanalmente por 4 dosis:
En el ensayo fundamental, 166 pacientes con LNH de bajo grado o folicular de células B en recaída o quimiorresistente recibieron 375 mg/m2 de rituximab como una infusión intravenosa una vez por semana durante cuatro semanas. La tasa de respuesta general (ORR) en la población por intención de tratar (ITT) fue del 48% (IC 95% 41% 56%) con una tasa de respuesta completa (CR) del 6% y una tasa de respuesta parcial (RP) del 42%. El tiempo medio proyectado hasta la progresión (TTP) para los pacientes que respondieron fue de 13.0 meses. En un análisis de subgrupos, la ORR fue más alta en pacientes con subtipos histológicos de IWF B, C y D en comparación con el subtipo A de IWF (58% frente a 12%), más alta en pacientes cuya lesión más grande era < 5 cm frente a > 7 cm de diámetro mayor (53% frente a 38%) y mayor en pacientes con recaída quimiosensible en comparación con recaída quimiorresistente (definida como una duración de la respuesta < 3 meses) (50% frente a 22%). La ORR en pacientes tratados previamente con trasplante autólogo de médula ósea (ABMT) fue del 78% frente al 43% en pacientes sin ABMT. Ni la edad, el sexo, el grado del linfoma, el diagnóstico inicial, la presencia o ausencia de enfermedad voluminosa, la LDH normal o alta ni la presencia de enfermedad extraganglionar tuvieron un efecto estadísticamente significativo (prueba exacta de Fisher) sobre la respuesta a rituximab. Se observó una correlación estadísticamente significativa entre las tasas de respuesta y la afectación de la médula ósea. El 40% de los pacientes con compromiso de la médula ósea respondieron en comparación con el 59% de los pacientes sin compromiso de la médula ósea (p = 0.0186). Este hallazgo no fue respaldado por un análisis de regresión logística por pasos en el que se identificaron los siguientes factores como factores de pronóstico: tipo histológico, positividad de bcl-2 al inicio, resistencia a la última quimioterapia y enfermedad de Bulky.
Tratamiento inicial, semanalmente por 8 dosis:
En un ensayo multicéntrico de un solo grupo, 37 pacientes con LNH de células B foliculares, de bajo grado o quimiorresistentes en recaída recibieron 375 mg/m2 de rituximab en infusión intravenosa semanalmente en ocho dosis. El ORR fue del 57% (intervalo de confianza [IC] del 95%; 41% - 73%; CR 14%, PR 43%) con una TTP mediana proyectada para pacientes que respondieron de 19.4 meses (rango de 5.3 a 38.9 meses).
Tratamiento inicial, enfermedad bulky, semanalmente por 4 dosis:
En los datos agrupados de tres ensayos, 39 pacientes con enfermedad voluminosa recidivante o quimiorresistente (lesión única ≥ 10 cm de diámetro). LNH de células B foliculares o de bajo grado recibieron 375 mg/m2 de rituximab como infusión intravenosa semanalmente en cuatro dosis. El ORR fue del 36% (IC 95% 21% - 51%; CR 3%, PR 33%) con una mediana de TTP para los pacientes que respondieron de 9.6 meses (rango de 4.5 a 26.8 meses).
Re-tratamiento, semanalmente por 4 dosis:
En un ensayo multicéntrico de un solo brazo, 58 pacientes con LNH de bajo grado o de células B foliculares en recaída o quimiorresistentes, que habían logrado una respuesta clínica objetiva a un ciclo previo de rituximab, fueron tratados de nuevo con 375 mg/m2 de rituximab como infusión intravenosa semanal para cuatro dosis. Tres de los pacientes habían recibido dos cursos de rituximab antes de la inscripción y, por lo tanto, recibieron un tercer curso en el estudio. Dos pacientes fueron tratados nuevamente dos veces en el estudio. Para los 60 retratamientos en estudio, el ORR fue del 38% (IC 95% 26% - 51%; RC 10%, PR 28%) con una TTP mediana proyectada para pacientes que respondieron de 17.8 meses (rango 5.4 - 26.6). Esto se compara favorablemente con el TTP logrado después del curso anterior de rituximab (12.4 meses).
Tratamiento inicial, en combinación con quimioterapia:
En un ensayo aleatorizado abierto, un total de 322 pacientes con linfoma folicular no tratados previamente se aleatorizaron para recibir quimioterapia CVP (ciclofosfamida 750 mg/m2, vincristina 1.4 mg/m2 hasta un máximo de 2 mg el día 1, y prednisolona 40 mg/m2/día los días 1 - 5) cada 3 semanas durante 8 ciclos o rituximab 375 mg/m2 en combinación con CVP (R-CVP). Rituximab se administró el primer día de cada ciclo de tratamiento. Un total de 321 pacientes (162 R-CVP, 159 CVP) recibieron terapia y se analizó su eficacia. La mediana de seguimiento de los pacientes fue de 53 meses. R-CVP condujo a un beneficio significativo sobre CVP para el criterio principal de valoración, el tiempo hasta el fracaso del tratamiento (27 meses frente a 6.6 meses, p < 0.0001, prueba de rango logarítmico). La proporción de pacientes con respuesta tumoral (CR, CRu, PR) fue significativamente mayor (p < 0.0001 prueba Chi-Square) en el grupo R-CVP (80.9%) que en el grupo CVP (57.2%). El tratamiento con R-CVP prolongó significativamente el tiempo hasta la progresión de la enfermedad o la muerte en comparación con CVP, 33.6 meses y 14.7 meses, respectivamente (p < 0.0001, prueba de rango logarítmico). La mediana de duración de la respuesta fue de 37.7 meses en el grupo de R-CVP y de 13.5 meses en el grupo de CVP (p < 0.0001, prueba de rango logarítmico).
La diferencia entre los grupos de tratamiento con respecto a la supervivencia global mostró una diferencia clínica significativa (p = 0.029, prueba de rango logarítmico estratificada por centro): las tasas de supervivencia a los 53 meses fueron del 80.9% para los pacientes del grupo R-CVP frente al 71.1% para los pacientes del grupo CVP.
Los resultados de otros tres ensayos aleatorios que utilizaron rituximab en combinación con un régimen de quimioterapia diferente a CVP (CHOP, MCP, CHVP/interferón-α) también demostraron mejoras significativas en las tasas de respuesta, los parámetros dependientes del tiempo y la supervivencia general. Los resultados clave de los cuatro estudios se resumen en la Tabla 4.
Tabla 4. Resumen de resultados clave de cuatro estudios aleatorizados de fase III que evalúan el beneficio de rituximab con diferentes regímenes de quimioterapia en el linfoma folicular
|
Estudiar |
Tratamiento, N |
FU mediana, meses |
TRG, % |
CR, % |
Mediana de TTF/PFS/EFS, meses |
Tasas de SG, % |
|
M39021 |
CVP, 159 R-CVP, 162 |
53 |
57 81 |
10 41 |
TTP mediana: 14.7 33.6 p < 0.0001 |
53 meses 71.1 80.9 p = 0.029 |
|
GLSG’00 |
CHOP, 205 R-CHOP, 223 |
18 |
90 96 |
17 20 |
TTF medio: 2.6 años No alcanzado p < 0.001 |
18 meses 90 95 p = 0.016 |
|
OSHO-39 |
PCM, 96 R-MCP, 105 |
47 |
75 92 |
25 50 |
SLP mediana: 28.8 No alcanzado p < 0.0001 |
48 meses 74 87 p = 0.0096 |
|
FL2000 |
CHVP-IFN, 183 R-CHVP-IFN, 175 |
42 |
85 94 |
49 76 |
SLE mediana: 36 No alcanzado p < 0.0001 |
42 meses 84 91 p = 0.029 |
EFS: Supervivencia libre de eventos.
TTP: tiempo hasta la progresión o la muerte.
PFS: supervivencia sin progresión.
TTF: tiempo hasta el fracaso del tratamiento.
Tasas de SG: tasas de supervivencia en el momento de los análisis.
Terapia de mantenimiento:
Linfoma folicular no tratado previamente:
En un ensayo de fase III prospectivo, abierto, internacional, multicéntrico, 1,193 pacientes con linfoma folicular avanzado sin tratamiento previo recibieron terapia de inducción con R-CHOP (n = 881), R-CVP (n = 268) o R-FCM (n = 44), según elección de los investigadores. Un total de 1,078 pacientes respondieron a la terapia de inducción, de los cuales 1,018 fueron aleatorizados a terapia de mantenimiento con rituximab (n = 505) u observación (n = 513). Los dos grupos de tratamiento estaban bien equilibrados con respecto a las características iniciales y el estado de la enfermedad. El tratamiento de mantenimiento con rituximab consistió en una infusión única de rituximab a 375 mg/m2 de superficie corporal administrada cada 2 meses hasta la progresión de la enfermedad o por un periodo máximo de dos años.
El análisis primario preespecificado se realizó en una mediana de tiempo de observación de 25 meses desde la aleatorización, la terapia de mantenimiento con rituximab resultó en una mejora clínicamente relevante y estadísticamente significativa en el criterio principal de valoración de la supervivencia libre de progresión evaluada por el investigador (PFS) en comparación con la observación en pacientes con linfoma folicular no tratado previamente (Tabla 5).
También se observó un beneficio significativo del tratamiento de mantenimiento con rituximab para las variables secundarias de supervivencia libre de eventos (SSC), tiempo hasta el próximo tratamiento antilinfoma (TNLT), tiempo hasta la siguiente quimioterapia (TNCT) y tasa de respuesta general (ORR) en el análisis primario. (Tabla 5).
Los datos del seguimiento prolongado de los pacientes del estudio (mediana de seguimiento de 9 años) confirmaron el beneficio a largo plazo de la terapia de mantenimiento con rituximab en términos de PFS, EFS, TNLT y TNCT (Tabla 5).
Tabla 5. Resumen de los resultados de eficacia para el mantenimiento con rituximab frente a la observación en el análisis primario definido por el protocolo y después de una mediana de seguimiento de 9 años (análisis final)
|
Análisis primario (mediana de FU: 25 meses) |
Análisis final (mediana FU: 9.0 años) |
|||
|
Observación N = 513 |
Rituximab N = 505 |
Observación N = 513 |
Rituximab N = 505 |
|
|
Eficacia primaria Supervivencia libre de progresión (mediana) valor p de rango logarítmico cociente de riesgos instantáneos (IC del 95 %) la reducción de riesgos |
NR NR < 0.0001 0.50 (0.39, 0.64) 50% |
4.06 años 10.49 años < 0.0001 0.61 (0.52, 0.73) 39% |
||
|
Eficacia secundaria Supervivencia global (mediana) valor p de rango logarítmico cociente de riesgos instantáneos (IC del 95%) la reducción de riesgos |
NR NR 0.7246 0.89 (0.45, 1.74) 11% |
NR NR 0.7948 1.04 (0.77, 1.40) -6% |
||
|
Supervivencia libre de eventos (mediana) valor p de rango logarítmico cociente de riesgos instantáneos (IC del 95 %) la reducción de riesgos |
38 meses NR < 0.0001 0.54 (0.43, 0.69) 46% |
4.04 años 9.25 años < 0.0001 0.64 (0.54, 0.76) 36% |
||
|
TNLT (mediana) valor p de rango logarítmico cociente de riesgos instantáneos (IC del 95%) la reducción de riesgos |
NR NR 0.0003 0.61 (0.46, 0.80) 39% |
6.11 años NR < 0.0001 0.66 (0.55, 0.78) 34% |
||
|
TNCT (mediana) valor p de rango logarítmico cociente de riesgos instantáneos (IC del 95%) la reducción de riesgos |
NR NR 0.0011 0.60 (0.44, 0.82) 40% |
9.32 años NR 0.0004 0.71 (0.59, 0.86) 39% |
||
|
Tasa de respuesta general* prueba chi-cuadrado p valor razón de probabilidades (IC del 95%) |
55% 74% < 0.0001 2.33 (1.73, 3.15) |
61% 79% <0.0001 2.43 (1.84, 3.22) |
||
|
Tasa de respuesta completa (CR/CRu)* prueba chi-cuadrado p valor razón de probabilidades (IC del 95%) |
48% 67% < 0.0001 2.21 (1.65, 2.94) |
53% 67% < 0.0001 2.34 (1.80, 3.03) |
||
* Al final del mantenimiento/observación; resultados del análisis final basados en una mediana de seguimiento de 73 meses.
FU: seguimiento; NR: no alcanzado en el momento del corte clínico, TNCT: tiempo hasta el próximo tratamiento de quimioterapia; TNLT: tiempo hasta el próximo tratamiento antilinfoma.
El tratamiento de mantenimiento con rituximab brindó un beneficio constante en todos los subgrupos predefinidos probados: sexo (masculino, femenino), edad (< 60 años, >= 60 años), puntuación FLIPI (<= 1, 2 o >= 3), terapia de inducción (R CHOP, R-CVP o R-FCM) e independientemente de la calidad de la respuesta al tratamiento de inducción (CR, CRu o PR). Los análisis exploratorios del beneficio del tratamiento de mantenimiento mostraron un efecto menos pronunciado en pacientes de edad avanzada (> 70 años), sin embargo, los tamaños de muestra fueron pequeños.
Linfoma folicular en recaída/refractario:
En un ensayo prospectivo, abierto, internacional, multicéntrico, de fase III, 465 pacientes con linfoma folicular en recaída/refractario fueron aleatorizados en un primer paso para recibir terapia de inducción con CHOP (ciclofosfamida, doxorrubicina, vincristina, prednisolona; n = 231) o rituximab más CHOP (R CHOP, n = 234). Los dos grupos de tratamiento estaban bien equilibrados con respecto a las características iniciales y el estado de la enfermedad. Un total de 334 pacientes que lograron una remisión completa o parcial después de la terapia de inducción fueron aleatorizados en un segundo paso para recibir terapia de mantenimiento con rituximab (n = 167) u observación (n = 167). El tratamiento de mantenimiento con rituximab consistió en una infusión única de rituximab a 375 mg/m2 de superficie corporal administrada cada 3 meses hasta la progresión de la enfermedad o por un periodo máximo de dos años.
El análisis de eficacia final incluyó a todos los pacientes asignados aleatoriamente a ambas partes del estudio. Después de una mediana de tiempo de observación de 31 meses para los pacientes asignados al azar a la fase de inducción, R-CHOP mejoró significativamente el resultado de los pacientes con linfoma folicular en recaída/resistente al tratamiento en comparación con CHOP (consulte la Tabla 6).
Tabla 6. Fase de inducción: descripción general de los resultados de eficacia para CHOP frente a R-CHOP (mediana de tiempo de observación de 31 meses)
|
PICAR |
R-CHOP |
valor p |
Reducción de riesgos 1) |
|
|
Eficacia primaria |
||||
|
TRQ2) |
74% |
87% |
0.0003 |
N/A |
|
CR2) |
16% |
29% |
0.0005 |
N/A |
|
PR2) |
58% |
58% |
0.9449 |
N/A |
1) Las estimaciones se calcularon mediante cocientes de riesgo.
2) Última respuesta tumoral evaluada por el investigador. La prueba estadística “primaria” para la “respuesta” fue la prueba de tendencia de CR frente a PR frente a la falta de respuesta (p < 0,0001).
Abreviaturas: NA, no disponible; TRO: tasa de respuesta global; CR: respuesta completa; PR: respuesta parcial.
Para los pacientes aleatorizados a la fase de mantenimiento del ensayo, la mediana del tiempo de observación fue de 28 meses desde la aleatorización de mantenimiento. El tratamiento de mantenimiento con rituximab condujo a una mejora clínicamente relevante y estadísticamente significativa en el criterio principal de valoración, la SLP (tiempo desde la aleatorización de mantenimiento hasta la recaída, la progresión de la enfermedad o la muerte) en comparación con la observación sola (p < 0.0001 prueba de rango logarítmico). La mediana de SLP fue de 42.2 meses en el brazo de mantenimiento con rituximab en comparación con 14.3 meses en el brazo de observación. Usando un análisis de regresión de Cox, el riesgo de experimentar enfermedad progresiva o muerte se redujo en un 61% con el tratamiento de mantenimiento con rituximab en comparación con la observación (95% IC; 45% - 72%). Las tasas sin progresión estimadas por Kaplan-Meier a los 12 meses fueron del 78% en el grupo de mantenimiento con rituximab frente al 57% en el grupo de observación. Un análisis de la supervivencia global confirmó el beneficio significativo del mantenimiento con rituximab sobre la observación (p = 0.0039 prueba de rango logarítmico). El tratamiento de mantenimiento con rituximab redujo el riesgo de muerte en un 56% (IC 95%; 22% - 75%).
Tabla 7. Fase de mantenimiento: descripción general de los resultados de eficacia rituximab frente a observación (mediana de tiempo de observación de 28 meses)
|
Parámetro de eficacia |
Estimación de Kaplan-Meier de tiempo medio hasta el evento (meses) |
Riesgo reducción |
||
|
Observación (N = 167) |
Rituximab (N = 167) |
Valor p de rango logarítmico |
||
|
Supervivencia libre de progresión (PFS) |
14.3 |
42.2 |
< 0.0001 |
61% |
|
Sobrevivencia promedio |
NR |
NR |
0.0039 |
56% |
|
Tiempo para un nuevo tratamiento del linfoma |
20.1 |
38.8 |
< 0.0001 |
50% |
|
Supervivencia libre de enfermedada |
16.5 |
53.7 |
0.0003 |
67% |
|
Análisis de subgrupos SLP |
||||
|
PICAR |
11.6 |
37.5 |
< 0.0001 |
71% |
|
R-CHOP |
22.1 |
51.9 |
0.0071 |
46% |
|
RC |
14.3 |
52.8 |
0.0008 |
64% |
|
relaciones públicas |
14.3 |
37.8 |
< 0.0001 |
54% |
|
Sistema operativo |
||||
|
PICAR |
NR |
NR |
0.0348 |
55% |
|
R-CHOP |
NR |
NR |
0.0482 |
56% |
NR: no alcanzado; a: sólo aplicable a pacientes que logran una RC.
El beneficio del tratamiento de mantenimiento con rituximab se confirmó en todos los subgrupos analizados, independientemente del régimen de inducción (CHOP o R-CHOP) o la calidad de la respuesta al tratamiento de inducción (CR o PR) (Tabla 7). El tratamiento de mantenimiento con rituximab prolongó significativamente la mediana de SLP en pacientes que respondieron a la terapia de inducción con CHOP (mediana de SLP de 37.5 meses frente a 11.6 meses, p < 0.0001), así como en los que respondieron a la inducción de R-CHOP (mediana de SLP de 51.9 meses frente a 22.1 meses, p = 0.0071). Aunque los subgrupos eran pequeños, el tratamiento de mantenimiento con rituximab brindó un beneficio significativo en términos de supervivencia general tanto para los pacientes que respondieron a CHOP como para los pacientes que respondieron a R-CHOP, aunque se requiere un seguimiento más prolongado para confirmar esta observación.
Linfoma no Hodgkin difuso de células B grandes en adultos:
En un ensayo aleatorizado, abierto, un total de 399 pacientes de edad avanzada (de 60 a 80 años de edad) sin tratamiento previo con linfoma difuso de células B grandes recibieron quimioterapia CHOP estándar (ciclofosfamida 750 mg/m2, doxorrubicina 50 mg/m2, vincristina (1.4 mg/m2 hasta un máximo de 2 mg el día 1 y prednisolona 40 mg/m2/día los días 1-5) cada 3 semanas durante 8 ciclos o bien recibieron rituximab 375 mg/m2 más CHOP (R-CHOP). Rituximab se administró el primer día del ciclo de tratamiento.
El análisis de eficacia final incluyó a todos los pacientes aleatorizados (197 CHOP, 202 R-CHOP) y tuvo una mediana de seguimiento de aproximadamente 31 meses. Los dos grupos de tratamiento estaban bien equilibrados en cuanto a las características basales de la enfermedad y el estado de la enfermedad. El análisis final confirmó que el tratamiento con R-CHOP se asoció con una mejora clínicamente relevante y estadísticamente significativa en la duración de la supervivencia libre de eventos (el parámetro principal de eficacia; donde los eventos fueron muerte, recaída o progresión del linfoma, o instauración de un nuevo tratamiento antilinfoma) (p = 0.0001). Las estimaciones de Kaplan Meier de la mediana de duración de la supervivencia sin eventos fueron de 35 meses en el brazo R-CHOP en comparación con 13 meses en el brazo CHOP, lo que representa una reducción del riesgo del 41%. A los 24 meses, las estimaciones de supervivencia general fueron del 68.2% en el brazo R-CHOP en comparación con el 57.4% en el brazo CHOP. Un análisis posterior de la duración de la supervivencia general, realizado con una mediana de seguimiento de 60 meses, confirmó el beneficio de R-CHOP sobre el tratamiento con CHOP (p = 0.0071), lo que representa una reducción del riesgo del 32%.
El análisis de todos los parámetros secundarios (tasas de respuesta, supervivencia libre de progresión, supervivencia libre de enfermedad, duración de la respuesta) verificó el efecto del tratamiento con R-CHOP en comparación con CHOP. La tasa de respuesta completa después del ciclo 8 fue del 76.2% en el grupo R-CHOP y del 62.4% en el grupo CHOP (p = 0.0028). El riesgo de progresión de la enfermedad se redujo en un 46% y el riesgo de recaída en un 51%. En todos los subgrupos de pacientes (sexo, edad, IPI ajustado por edad, estadio de Ann Arbor, ECOG, microglobulina β2, LDH, albúmina, síntomas B, enfermedad bulky, sitios extraganglionares, afectación de la médula ósea), los cocientes de riesgo para la supervivencia libre de eventos y la supervivencia (R-CHOP en comparación con CHOP) fue inferior a 0.83 y 0.95 respectivamente. R-CHOP se asoció con mejoras en los resultados para pacientes de alto y bajo riesgo según el IPI ajustado por edad.
Hallazgos de laboratorio clínico:
De 67 pacientes evaluados para anticuerpos humanos anti-ratón (HAMA), no se observaron respuestas. De 356 pacientes evaluados para anticuerpos antidrogas (ADA), el 1.1% (4 pacientes) fueron positivos.
Leucemia linfocítica crónica (LLC):
En dos ensayos abiertos, aleatorizados, un total de 817 pacientes sin tratamiento previo y 552 pacientes con LLC recidivante/refractaria para recibir quimioterapia FC (25 mg/m2 de fludarabina, 250 mg/m2 de ciclofosfamida, días 1-3) cada 4 semanas en 6 ciclos o rituximab en combinación con FC (R-FC). Se administró rituximab a una dosis de 375 mg/m2 durante el primer ciclo un día antes de la quimioterapia y a una dosis de 500 mg/m2 el día 1 de cada ciclo de tratamiento posterior. Los pacientes fueron excluidos del estudio sobre LLC recidivante/refractaria si habían tenido tratamiento previo con anticuerpos monoclonales o si eran refractarios (definidos como no lograr una remisión parcial durante al menos 6 meses) a fludarabina o cualquier análogo de nucleósido. Se analizó con respecto a eficacia un total de 810 pacientes (403 R-FC, 407 FC) para el estudio de primera línea (Tabla 8 y Tabla 9) y 552 pacientes (276 R-FC, 276 FC) para el estudio recidivante/refractario (Tabla 10).
En el estudio de primera línea, después de una mediana de tiempo de observación de 48.1 meses, la mediana de SLP fue de 55 meses en el grupo de R-FC y 33 meses en el grupo de FC (p < 0.0001, prueba de rango logarítmico). El análisis de supervivencia global mostró beneficio significativo del tratamiento con R-FC sobre la quimioterapia FC (p = 0.0319, prueba de rango logarítmico) (Tabla 8). El beneficio en términos de SLP se observó de forma consistente en la mayoría de los subgrupos de pacientes analizados de acuerdo con el riesgo de enfermedad en la línea base (es decir, etapas de Binet A-C) (Tabla 9).
Tabla 8. Tratamiento de primera línea de la leucemia linfocítica crónica Resumen de los resultados de eficacia de rituximab más FC frente a FC solo: mediana de tiempo de observación de 48.1 meses
|
Parámetro de eficacia |
Estimación de Kaplan-Meier de tiempo medio hasta el evento (meses) |
Riesgo reducción |
||
|
FC (N = 409) |
R-FC (N = 408) |
Valor p de rango logarítmico |
||
|
Supervivencia libre de progresión (PFS) |
32.8 |
55.3 |
< 0.0001 |
45% |
|
Sobrevivencia promedio |
NR |
NR |
0.0319 |
27% |
|
Supervivencia libre de eventos |
31.3 |
51.8 |
< 0.0001 |
44% |
|
Tasa de respuesta (CR, nPR o PR) tasas CR |
72.6% 16.9% |
85.8% 36.0% |
< 0.0001 < 0.0001 |
n / A n / A |
|
Duración de la respuesta* |
36.2 |
57.3 |
< 0.0001 |
44% |
|
Supervivencia libre de enfermedad (DFS)** |
48.9 |
60.3 |
0.0520 |
31% |
|
Tiempo para un nuevo tratamiento |
47.2 |
69.7 |
< 0.0001 |
42% |
Tasa de respuesta y tasas de RC analizadas mediante la prueba de chi-cuadrado. NR: no alcanzado; na: no aplicable.
* Solo aplicable a pacientes que logran un CR, nPR, PR.
** Solo aplicable a pacientes que logran una RC.
Tabla 9. Tratamiento de primera línea de leucemia linfocítica crónica Relaciones de riesgo de supervivencia libre de progresión según la etapa de Binet (ITT) - 48.1 meses de tiempo medio de observación
|
Supervivencia libre de progresión (PFS) |
Número de pacientes |
Cociente de riesgo (95% IC) |
Valor p (prueba de Wald, no ajustada) |
|
|
FC |
R-FC |
|||
|
Binet etapa A |
22 |
18 |
0.39 (0.15; 0.98) |
0.0442 |
|
Binet etapa B |
259 |
263 |
0.52 (0.41; 0.66) |
< 0.0001 |
|
Binet etapa C |
126 |
126 |
0.68 (0.49; 0.95) |
0.0224 |
IC: Intervalo de confianza.
En el estudio de LLC recidivante/refractario, la mediana de supervivencia libre de progresión (criterio de valoración primario) fue de 30.6 meses en el grupo R-FC y 20.6 meses en el grupo FC (p- 0.0002, prueba rango logarítmico). El beneficio en términos de SLP se observó en casi todos los subgrupos de pacientes analizados de acuerdo con el riesgo de enfermedad al inicio. Se reportó una ligera pero no significativa mejora en la supervivencia global en el R-FC en comparación con el brazo del FC.
Tabla 10. Tratamiento de la leucemia linfocítica crónica recidivante/refractaria - visión general de los resultados de eficacia para rituximab más FC vs. FC solo (mediana de tiempo de observación de 25.3 meses)
|
Parámetro de eficacia |
Estimación de Kaplan-Meier de tiempo medio hasta el evento (meses) |
Riesgo reducción |
||
|
FC (N = 276) |
R-FC (N = 276) |
Valor p de rango logarítmico |
||
|
Supervivencia libre de progresión (PFS) |
20.6 |
30.6 |
0.0002 |
35% |
|
Sobrevivencia promedio |
51.9 |
NR |
0.2874 |
17% |
|
Supervivencia libre de eventos |
19.3 |
28.7 |
0.0002 |
36% |
|
Tasa de respuesta (CR, nPR o PR) |
58.0% |
69.9% |
0.0034 |
n / A |
|
Tasas CR |
13.0% |
24.3% |
0.0007 |
n / A |
|
Duración de la respuesta* |
27.6 |
39.6 |
0.0252 |
31% |
|
Supervivencia libre de enfermedad (DFS)** |
42.2 |
39.6 |
0.8842 |
-6% |
|
Tiempo hasta un nuevo tratamiento para la LLC |
34.2 |
NR |
0.0024 |
35% |
Respuesta índice y_ RC tarifas analizado __ usando chi - cuadrado Prueba.
* Sólo aplicable a pacientes que logran un CR, nPR, PR; NR: no alcanzado: n/a no aplicable.
** Sólo aplicable a pacientes que logran una RC.
Los resultados de otros estudios de apoyo con rituximab en combinación con otros regímenes de quimioterapia (incluyendo CHOP, FCM, PCM, bendamustina y cladribina) para el tratamiento de pacientes con LLC previamente no tratados y/o recidivantes/refractarios también han demostrado tasas altas de respuesta globales con beneficios en términos de tasas de SLP, aunque con toxicidad moderadamente mayor (en especial mielotoxicidad). Estos estudios apoyan el uso de rituximab con cualquier quimioterapia.
Los datos realizados en aproximadamente 180 pacientes pretratados con rituximab han demostrado beneficios clínicos (incluida RC) y son de apoyo para el retratamiento de rituximab.
Granulomatosis con poliangeítis (Wegener) (GPA) y poliangeítis microscópica:
Un total de 197 pacientes con vasculitis con granulomatosis con poliangitis (Wegener) (GPA) y poliangitis microscópica (PAM) graves y activas asociada a ANCA fueron incluidos y tratados en un estudio activo, controlado, aleatorio, doble-ciego, multicéntrico, de no inferioridad. Los pacientes fueron de 15 años de edad o mayores, con diagnóstico de granulomatosis con poliangitis (Wegener) activa (75% de pacientes) o poliangitis microscópica (PAM) (24% de pacientes) de acuerdo con los criterios del consenso de la conferencia de Chapel Hill (1% de pacientes tenía GPA y PAM de tipo desconocido).
Los pacientes fueron aleatorizados con tasa 1:1 a recibir ciclofosfamida oral diariamente (2 mg/kg/día) por 3-6 meses, seguido de azatioprina o rituximab (375 mg/m2) una vez a la semana por 4 semanas. Los pacientes de ambos brazos recibieron un pulso intravenoso (IV) de 1,000 mg de metilprednisolona (u otro glucocorticoide a dosis equivalente) por día por 1 a 3 días, seguido de prednisona oral (1 mg/kg/día, sin exceder 80 mg/día). La titulación de prednisona se completó en el mes 6 desde el inicio del tratamiento de estudio.
La medida de desenlace primaria fue lograr la remisión completa a los 6 meses, definida por el puntaje de actividad de vasculitis de Birmingham para granulomatosis de Wegener (BVAS/WG) de 0, sin terapia con glucocorticoides. El margen preespecificado de no inferioridad para la diferencia de tratamiento fue 20%. El estudio demostró la no inferioridad rituximab con respecto a ciclofosfamida para remisión completa a 6 meses (Tabla 11). Adicionalmente, la tasa de remisión completa en el brazo con rituximab fue significativamente mayor que la tasa estimada de remisión completa en pacientes con GPA y PAM grave no tratados o tratados únicamente con glucocorticoides, con base en los datos de control histórico.
Se observó eficacia para ambos tipos de pacientes, para los pacientes con GPA y PAM de reciente diagnóstico y para pacientes con recaída de la enfermedad (Tabla 12).
Tabla 11. Porcentaje de pacientes que lograron remisión completa en el mes 6 (población de intención de tratamiento)
|
Rituximab (n = 99) |
Ciclofosfamida (n = 98) |
Diferencia de tratamiento (rituximab-ciclofosfamida) |
|
|
Tasa |
63.6% |
53.1% |
10.6% |
|
IC 95.1%b |
(54.1%, 73.2%) |
(43.1%, 63.0%) |
(-3.2%, 24.3%)a |
IC = Intervalo de confianza.
a La no inferioridad fue demostrada con la unión más baja (-3.2%) que fue más alta que el margen predeterminado de no inferioridad (-20%).
b El intervalo de confianza de 95.1% refleja un alfa adicional de 0.001 encontrado en el análisis interino de eficacia.
Tabla 12. Remisión completa a los 6 meses por estado de la enfermedad
|
Rituximab |
Ciclofos-famida |
Diferencia (IC 95%) |
|
|
Todos los pacientes Recién diagnosticado Reincidente |
n = 99 n = 48 n = 51 |
n = 98 n = 48 n = 50 |
|
|
Remisión completa |
|||
|
Todos los pacientes |
63.6% |
53.1% |
10.6% (-3.2, 24.3) |
|
Recién diagnosticado |
60.4% |
64.6% |
-4.2% (-23.6, 15.3) |
|
Reincidente |
66.7% |
42.0% |
24.7% (5.8, 43.6) |
La imputación del peor de los casos se aplica a los pacientes con datos faltantes.
Remisión completa a los 12 y 18 meses:
En el grupo de rituximab, el 48% de los pacientes lograron RC a los 12 meses y el 39% de los pacientes lograron RC a los 18 meses. En pacientes tratados con ciclofosfamida (seguida de azatioprina para el mantenimiento de la remisión completa), el 39% de los pacientes lograron RC a los 12 meses y el 33% de los pacientes lograron RC a los 18 meses. Del mes 12 al mes 18, se observaron 8 recaídas en el grupo de rituximab en comparación con cuatro en el grupo de ciclofosfamida.
Evaluaciones de laboratorio:
Un total de 23/99 (23%) de los pacientes tratados con rituximab del ensayo de inducción de la remisión dieron positivo para ADA a los 18 meses. Ninguno de los 99 pacientes tratados con rituximab fue ADA positivo en la selección. No hubo una tendencia aparente o un impacto negativo de la presencia de ADA sobre la seguridad o la eficacia en el ensayo de inducción de la remisión.
Tratamiento de mantenimiento en adultos:
Un total de 117 pacientes (88 con GPA, 24 con PAM y 5 con vasculitis renal limitada asociada a ANCA) en remisión de la enfermedad fueron aleatorizados para recibir azatioprina (59 pacientes) o rituximab (58 pacientes) en un estudio prospectivo multicéntrico, controlado, abierto. Los pacientes incluidos tenían entre 21 y 75 años de edad y tenían una enfermedad recién diagnosticada o recidivante en remisión completa después del tratamiento combinado con glucocorticoides y pulsos de ciclofosfamida. La mayoría de los pacientes eran ANCA positivos al momento del diagnóstico o durante el curso de su enfermedad; tenían vasculitis necrotizante de vasos pequeños histológicamente confirmada con un fenotipo clínico de GPA o PAM, o vasculitis renal limitada asociada a ANCA; o ambos.
La terapia de inducción a la remisión incluyó prednisona IV, administrada a discreción del investigador, precedida en algunos pacientes por pulsos de metilprednisolona y pulsos de ciclofosfamida hasta que se alcanzó la remisión después de 4 a 6 meses. En ese momento, y dentro de un máximo de 1 mes después del último pulso de ciclofosfamida, los pacientes fueron asignados al azar para recibir rituximab (dos infusiones intravenosas de 500 mg separadas por dos semanas [el día 1 y el día 15] seguidas de 500 mg IV cada 6 meses durante 18 meses) o azatioprina (administrada por vía oral a dosis de 2 mg/kg/día durante 12 meses, luego 1.5 mg/kg/día durante 6 meses y finalmente 1 mg/kg/día durante 4 meses [suspensión del tratamiento tras estos 22 meses]). El tratamiento con prednisona se redujo gradualmente y luego se mantuvo en una dosis baja (aproximadamente 5 mg por día) durante al menos 18 meses después de la aleatorización. La reducción gradual de la dosis de prednisona y la decisión de interrumpir el tratamiento con prednisona después del mes 18 quedaron a criterio del investigador.
Todos los pacientes fueron seguidos hasta el mes 28 (10 o 6 meses, respectivamente, después del último tratamiento con rituximab, infusión o dosis de azatioprina). Se requirió profilaxis de neumonía por Pneumocystis jirovecii para todos los pacientes con recuentos de linfocitos T CD4+ inferiores a 250 por milímetro cúbico.
La medida de resultado primaria fue la tasa de recaída mayor en el mes 28.
Resultados:
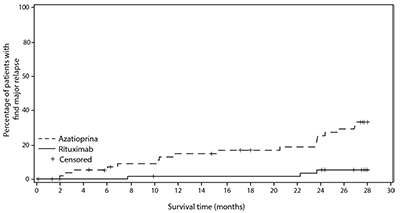
En el mes 28, se produjo una recaída mayor (definida por la reaparición de signos clínicos y/o de laboratorio de actividad de vasculitis ([BVAS] > 0) que podrían provocar insuficiencia o daño orgánico o poner en peligro la vida) en 3 pacientes (5%) en el grupo de rituximab y 17 pacientes (29%) en el grupo de azatioprina (p = 0.0007). Se produjeron recaídas menores (que no ponen en peligro la vida y no involucran daño orgánico importante) en siete pacientes en el grupo de rituximab (12%) y ocho pacientes en el grupo de azatioprina (14%).
Las curvas de tasa de incidencia acumulada mostraron que el tiempo hasta la primera recaída mayor fue mayor en pacientes con rituximab a partir del mes 2 y se mantuvo hasta el mes 28 (Figura 1).
|
Número de sujetos con recaída mayor |
|||||||||||||||
|
Azatioprina |
0 |
0 |
3 |
3 |
5 |
5 |
8 |
8 |
9 |
9 |
9 |
10 |
13 |
15 |
17 |
|
Rituximab |
0 |
0 |
0 |
0 |
1 |
1 |
1 |
1 |
1 |
1 |
1 |
1 |
3 |
3 |
3 |
|
Número de sujetos en riesgo |
|||||||||||||||
|
Azatioprina |
59 |
56 |
52 |
50 |
47 |
47 |
44 |
44 |
42 |
41 |
40 |
39 |
36 |
34 |
0 |
|
Rituximab |
58 |
56 |
56 |
56 |
55 |
54 |
54 |
54 |
54 |
54 |
54 |
54 |
52 |
50 |
0 |
Nota: Los pacientes fueron censurados al mes 28 si no presentaban ningún evento.
Evaluaciones de laboratorio:
Un total de 6/34 (18%) de los pacientes tratados con rituximab del ensayo clínico de terapia de mantenimiento desarrollaron ADA. No hubo una tendencia aparente o impacto negativo de la presencia de ADA en la seguridad o eficacia en el ensayo clínico de terapia de mantenimiento.
Farmacocinética:
Linfoma no Hodgkin del adulto (LNH):
Con base en un análisis farmacocinético poblacional en 298 pacientes con LNH que recibieron infusiones únicas o múltiples de rituximab como agente único o en combinación con terapia CHOP (las dosis de rituximab aplicadas oscilaron entre 100 y 500 mg/m2), las estimaciones típicas de la población de aclaramiento no especifico (CL 1), el aclaramiento específico (CL 2) probablemente contribuido por las células B o la carga tumoral, y el volumen de distribución del compartimento central (V1) fueron 0.14 L/día, 0.59 L/día y 2.7 L, respectivamente. La mediana estimada de la vida media de eliminación terminal de rituximab fue de 22 días (rango, 6.1 a 52 días). Los recuentos iniciales de células CD19 positivas y el tamaño de las lesiones tumorales medibles contribuyeron a parte de la variabilidad en CL 2 de rituximab en los datos de 161 pacientes que recibieron 375 mg/m2 como infusión intravenosa durante 4 dosis semanales. Los pacientes con recuentos de células positivas para CD19 más altos o lesiones tumorales tenían un CL 2 más alto. Sin embargo, un gran componente de la variabilidad interindividual se mantuvo para CL 2 después de la corrección de los recuentos de células positivas para CD19 y el tamaño de la lesión tumoral. V 1 varió según el área de superficie corporal (BSA) y la terapia CHOP. Esta variabilidad en V 1 (27.1% y 19.0%) contribuida por el rango en BSA (1.53 a 2.32 m2) y la terapia CHOP concurrente, respectivamente, fue relativamente pequeña. La edad, el sexo y el estado funcional de la OMS no tuvieron efecto sobre la farmacocinética de rituximab. Este análisis sugiere que no se espera que el ajuste de dosis de rituximab con cualquiera de las covariables probadas resulte en una reducción significativa en su variabilidad farmacocinética. Rituximab, administrado como una infusión intravenosa a una dosis de 375 mg/m2 a intervalos semanales durante 4 dosis a 203 pacientes con LNH que nunca habían recibido rituximab, produjo una Cmáx media después de la cuarta infusión de 486 μg/mL (rango, 77.5 a 996.6 μg/mL). Rituximab fue detectable en el suero de pacientes de 3 a 6 meses después de completar el último tratamiento.
Tras la administración de 8 dosis de rituximab a una dosis de 375 mg/m2 como infusión intravenosa a intervalos semanales a 37 pacientes con LNH, la Cmáx media aumentó con cada infusión sucesiva, desde una media de 243 μg/ml (rango, 16 - 582 μg/mL) después de la primera infusión a 550 μg/mL (rango, 171-1.177 μg/mL) después de la octava infusión.
El perfil farmacocinético de rituximab cuando se administró en 6 infusiones de 375 mg/m2 en combinación con 6 ciclos de quimioterapia CHOP fue similar al observado con rituximab solo.
Leucemia linfocítica crónica (LLC):
Rituximab se administró como infusión intravenosa a una dosis del primer ciclo de 375 mg/m2 aumentada a 500 mg/m2 en cada ciclo durante 5 dosis en combinación con fludarabina y ciclofosfamida en pacientes con LLC. La Cmáx media (N = 15) fue de 408 μg/mL (rango, 97 - 764 μg/mL) después de la quinta infusión de 500 mg/m2 y la semivida terminal media fue de 32 días (rango, 14 - 62 días).Granulomatosis con poliangeítis (GPA) y poliangeítis microscópica (MPA):
Población adulta:
Con base en el análisis farmacocinético poblacional de los datos de 97 pacientes con GPA y PAM que recibieron 375 mg/m2 de rituximab una vez a la semana durante cuatro dosis, la vida media de eliminación terminal estimada fue de 23 días (rango, 9 - 49 días).
El aclaramiento medio y el volumen de distribución de rituximab fueron 0.313 L/día (rango, 0.116 - 0.726 L/día) y 4.50 L (rango 2.25 - 7.39 L), respectivamente. La concentración máxima durante los primeros 180 días (Cmax), la concentración mínima en el día 180 (C180) y el área bajo la curva acumulada durante 180 días (ABC180) fueron (mediana (rango]) 372.6 (252.3-533.5) μg/mL, 2.1 (0-29.3) μg/mL y 10,302 (3,653-2,1874) μg/mL*días, respectivamente.
CONTRAINDICACIONES:
Hipersensibilidad al principio activo o a cualquiera de sus excipientes o a las proteínas murinas. Pacientes con estado inmunocomprometido grave. Infecciones graves y activas. Insuficiencia cardíaca grave (clase IV de la New York Heart Association) o enfermedades cardíacas graves no controladas. Embarazo, lactancia y menores de 18 años.
RESTRICCIONES DE USO DURANTE EL EMBARAZO Y LA LACTANCIA:
Mujeres en edad fértil/Anticoncepción en mujeres: Debido al largo tiempo de permanencia de Rituximab en el organismo en pacientes con depleción de células B, las mujeres en edad fértil deben usar métodos anticonceptivos eficaces durante el tratamiento y hasta 12 meses después del tratamiento con ARASAMILA®.
Uso durante el embarazo: Se sabe que las inmunoglobulinas lgG atraviesan la barrera placentaria. No se han determinado los niveles de linfocitos B en recién nacidos de madres expuestas a Rituximab en ensayos clínicos. No existen datos suficientes ni controlados en mujeres embarazadas, sin embargo, se han notificado depleción transitoria de células B y linfocitopenia en algunos niños nacidos de madres expuestas a Rituximab durante el embarazo. Se han observado efectos similares en los estudios realizados en animales (ver sección Precauciones en relación con efectos de carcinogénesis, mutagénesis, teratogénesis y sobre la fertilidad). Por estos motivos ARASAMILA® no debe administrarse durante el embarazo.
Uso durante la lactancia:
Los datos limitados sobre la excreción de Rituximab en la leche materna sugieren niveles muy bajos en la leche (dosis infantil relativa inferior al 0.4%). Pocos casos de seguimiento de lactantes alimentados con leche materna describen un crecimiento y desarrollo normales hasta el año y medio.
Sin embargo, como estos datos son limitados, los resultados a largo plazo de los bebés amamantados siguen siendo desconocidos. No se recomienda la lactancia materna durante el tratamiento con Rituximab y, de forma óptima, durante los 12 meses siguientes al tratamiento con Rituximab.
REACCIONES SECUNDARIAS Y ADVERSAS:
Experiencia del linfoma no Hodgkin y la leucemia linfocítica crónica en adultos:
Resumen del perfil de seguridad: De acuerdo con la información públicamente disponible del medicamento innovador, el perfil de seguridad global de Rituximab en linfoma no Hodgkin y leucemia linfocítica crónica se basa en los datos de pacientes de ensayos clínicos y de los estudios de postcomercialización. Estos pacientes fueron tratados con Rituximab en monoterapia (como tratamiento de inducción o como tratamiento de mantenimiento tras el tratamiento de inducción) o en combinación con quimioterapia.
En pacientes que recibieron Rituximab, las reacciones al medicamento observadas con mayor frecuencia fueron las RRI y en la mayoría de los pacientes ocurrieron durante la primera infusión. La incidencia de los síntomas relacionados con la infusión disminuyó sustancialmente con las posteriores infusiones y fue menor del 1% después de ocho dosis de Rituximab.
Durante los ensayos clínicos en pacientes con LNH, aproximadamente el 30-55% de los pacientes experimentaron reacciones infecciosas (en su mayoría bacterianas y virales) y el 30-50% de pacientes con LCC.
Las reacciones adversas al medicamento (RAM) graves notificadas u observadas con mayor frecuencia fueron:
• RRI (incluyendo síndrome de liberación de citocinas, síndrome de lisis tumoral, ver sección Precauciones generales).
• Infecciones (ver sección Precauciones generales).
• Acontecimientos cardiovasculares (ver sección Precauciones generales).
Otras RAM graves notificadas incluyen reactivación de la hepatitis B y LMP (ver sección Precauciones generales). Lista tabulada de reacciones adversas:
En la Tabla 13 están incluidas las frecuencias de las RAM notificadas con Rituximab tanto solo como en combinación con quimioterapia. Las reacciones adversas se enumeran en orden decreciente de gravedad dentro de cada intervalo de frecuencia. Las frecuencias se definen como muy frecuentes (≥ 1/10), frecuentes (≥ 1/100 a < 1/10), poco frecuentes ( ≥ 1/1,000 a < 1/100), raras (≥ 1/10,000 a < 1/1,000), muy raras (< 1/10,000) y desconocidas (no pueden estimarse a partir de los datos disponibles). Dentro de cada grupo de frecuencias, las reacciones adversas se presentan en orden decreciente de gravedad.
Las RAM identificadas sólo durante los estudios de postcomercialización, y cuya frecuencia no puede ser estimada, se definen como “frecuencia no conocida”.
Tabla 13. Resumen de las RAM notificadas en pacientes con LNH y LCC tratados con Rituximab en monoterapia/mantenimiento en los ensayos clínicos o durante los estudios clínicos
|
MedDRA Sistema de clasificación de órganos |
Muy común |
Común |
Poco común |
Raro |
Muy raro |
No conocida |
|
Infecciones e infestaciones |
Infecciones bacterianas, infecciones virales, +bronquitis |
Sepsis, +neumonía, +infección febril, +herpes zóster, +infección del tracto respiratorio, infecciones fúngicas, infecciones de etiología desconocida, +bronquitis aguda, +sinusitis, hepatitis B1 |
Infección viral grave2, Pneumocystis jirovecii |
LMP |
||
|
Trastornos de la sangre y del sistema linfático |
Neutropenia, leucopenia, +neutropenia febril, +trombocitopenia |
Anemia, +pancitopenia, +granulocitopenia |
Trastornos de la coagulación, anemia aplásica, anemia hemolítica, linfadenopatía |
Aumento transitorio de los niveles séricos de IgM3 |
Neutropenia tardía3 |
|
|
Trastornos del sistema inmunológico |
Reacciones relacionadas con la perfusión4, angioedema |
Hipersensibilidad |
Anafilaxia |
Síndrome de lisis tumoral, síndrome de liberación de citoquinas4, enfermedad del suero |
Trombocitopenia aguda reversible relacionada con la infusión4 |
|
|
Trastornos del metabolismo y de la nutrición |
Hiperglucemia, pérdida de peso, edema periférico, edema facial, aumento de LDH, hipocalcemia |
|||||
|
Desórdenes psiquiátricos |
Depresión, nerviosismo |
|||||
|
Trastornos del sistema nervioso |
Parestesia, hipoestesia, agitación, insomnio, vasodilatación, vértigo, ansiedad |
Disgeusia |
Neuropatía periférica, parálisis del nervio facial5 |
Neuropatía craneal, pérdida de otros sentidos5 |
||
|
Trastornos oculares |
Trastorno de lagrimeo, conjuntivitis |
Pérdida severa de visión5 |
||||
|
Trastornos de oído y del laberinto |
Tinnitus, dolor de oído |
Pérdida de audición5 |
||||
|
Trastornos cardiacos |
+Infarto de miocardio4,6, arritmia, +fibrilación auricular, taquicardia, +trastorno cardiaco |
+Insuficiencia ventricular izquierda, +taquicardia supraventricular, +taquicardia ventricular, +angina, +isquemia miocárdica, bradicardia |
Trastornos cardiacos graves4,6 |
Insuficiencia cardiaca4,6 |
||
|
Trastornos vasculares |
Hipertensión, hipotensión ortostática, hipotensión |
Vasculitis (predominantemente cutánea), vasculitis leucocitoclástica |
||||
|
Trastornos respiratorios, torácicos y mediastínicos |
Broncoespasmo4, enfermedad respiratoria, dolor torácico, disnea, aumento de la tos, rinitis |
Asma, bronquiolitis obliterante, trastorno pulmonar, hipoxia |
Enfermedad pulmonar intersticial7 |
Insuficiencia respiratoria4, |
Infiltración pulmonar |
|
|
Desórdenes gastrointestinales |
Náuseas |
Vómito, diarrea, dolor abdominal, disfagia, estomatitis, estreñimiento, dispepsia, anorexia, irritación de garganta |
Distensión abdominal |
Perforación gastrointestinal7 |
||
|
Trastornos de la piel y del tejido subcutáneo |
Prurito, erupción cutánea, +alopecia |
Urticaria, sudoración, sudores nocturnos, +trastorno de la piel |
Reacciones cutáneas ampollosas graves, Síndrome de Stevens-Johnson, necrólisis epidérmica tóxica (Síndrome de Lyell)7 |
|||
|
Trastornos musculoesqueleticos y del tejido conjuntivo |
Hipertonía, mialgia, artralgia, dolor de espalda, dolor de cuello, dolor |
|||||
|
Trastornos renales y urinarios |
Insuficiencia renal4 |
|||||
|
Desordenes generales y condiciones administrativas del sitio |
Fiebre, escalofríos, astenia, dolor de cabeza |
Dolor tumoral, rubefacción, malestar general, síndrome catarral, +fatiga, +escalofríos, +fallo multiorgánico4 |
Dolor en el lugar de la infusión |
|||
|
Investigación |
Disminución en los niveles de IgG |
Para cada término, el conteo de frecuencia se basó en las reacciones de todos los grados (desde leves a graves), excepto para los términos marcados con “+”, en los que el conteo de frecuencia se basó sólo en reacciones graves (≥ grado 3 del criterio de toxicidad común del NCI). Sólo se informa la frecuencia más alta observada en los ensayos.
1 Incluye reactivación e infecciones primarias; frecuencia basada en el régimen R-FC en la LLC en recaída/refractaria.
2 Véase también la sección de infección a continuación.
3 Ver también la sección de reacciones adversas hematológicas a continuación.
4 Consulte también la sección reacciones relacionadas con la perfusión a continuación. Casos raramente fatales reportados.
5 Signos y síntomas de neuropatía craneal. Ocurrió en varios momentos hasta varios meses después de completar la terapia con rituximab.
6 Se observaron principalmente en pacientes con afección cardíaca previa y/o quimioterapia cardiotóxica y se asociaron principalmente con reacciones relacionadas con la infusión.
7 Incluye casos fatales.
De acuerdo con la información públicamente disponible del medicamento innovador, los siguientes acontecimientos han sido notificados como acontecimientos adversos durante los ensayos clínicos, sin embargo, fueron notificados con una incidencia menor o similar en el brazo de Rituximab comparado con el brazo control: hematotoxicidad, neutropenia, infección en el tracto urinario, trastorno sensorial, fiebre.
De acuerdo con la información públicamente disponible del medicamento innovador los signos y síntomas indican que más del 50% de los pacientes en los ensayos clínicos sufrieron reacciones relacionadas con la infusión, que en su mayoría se observaron durante la primera infusión, generalmente durante las primeras dos horas. Estos síntomas incluyeron principalmente fiebre, escalofríos y rigidez. Otros síntomas incluyeron rubor, angioedema, broncoespasmo, vómitos, náuseas, urticaria/rash, fatiga, cefalea, irritación de garganta, rinitis, prurito, dolor, taquicardia, hipertensión, hipotensión, disnea, dispepsia, astenia y características del síndrome de lisis tumoral. Las reacciones graves relacionadas con la infusión (como broncoespasmo, hipotensión) ocurrieron en hasta el 12% de los casos. Además, en algunos casos las reacciones notificadas fueron infarto de miocardio, fibrilación auricular, edema pulmonar y trombocitopenia aguda reversible. Se notificaron con menor frecuencia o frecuencia desconocida, exacerbación de las patologías cardiacas preexistentes, tales como angina de pecho o insuficiencia cardiaca congestiva o trastornos cardiacos graves (insuficiencia cardiaca, infarto de miocardio, fibrilación auricular), edema pulmonar, insuficiencia multiorgánica, síndrome de lisis tumoral, síndrome de liberación de citocinas, insuficiencia renal e insuficiencia respiratoria. La incidencia de síntomas relacionados con la infusión disminuye considerablemente en las infusiones siguientes y es menor al 1% de los pacientes en el octavo ciclo del tratamiento de Rituximab.
Descripción de reacciones adversas seleccionadas: Infecciones: De acuerdo con la información públicamente disponible del medicamento innovador, rituximab indujo la depleción de células B en el 70-80% de los pacientes, pero se asoció con una disminución de las inmunoglobulinas séricas solamente en una minoría de pacientes.
En los ensayos aleatorizados en el brazo de Rituximab se notificó una mayor incidencia en las infecciones localizadas de Candida, así como de herpes zóster. Se notificaron infecciones graves en aproximadamente el 4% de los pacientes tratados con Rituximab en monoterapia. Comparando un tratamiento de mantenimiento con Rituximab de hasta dos años de duración con el brazo de observación, se notificaron frecuencias más elevadas de las infecciones globales, incluyendo infecciones de grado 3 o 4. No se observó toxicidad acumulada en términos de infecciones notificadas durante los dos años del periodo de mantenimiento. Además, en los pacientes tratados con Rituximab se han notificado otras infecciones virales graves, ya sean nuevas, reactivaciones o exacerbaciones, algunas de las cuales fueron mortales. La mayoría de los pacientes habían recibido Rituximab en combinación con quimioterapia o como parte de un trasplante de células madre hematopoyéticas. Ejemplos de estas infecciones virales graves son las causadas por los virus de la familia herpes (citomegalovirus, virus de la varicela zóster y virus herpes simple), virus JC (leucoencefalopatía multifocal progresiva [LMP]) y el virus de la hepatitis C. Se han notificado en ensayos clínicos casos de muerte por LMP tras progresión de la enfermedad y retratamiento. Se han notificado casos de reactivación de la hepatitis B, la mayoría de los cuales aparecieron en pacientes que recibieron Rituximab en combinación con quimioterapia citotóxica. En pacientes con LLC recidivante/refractaria, la incidencia de infección por hepatitis B de grado 3/4 (reactivación e infección primaria) fue del 2% en R-FC frente al 0% de FC. Se ha observado progresión del sarcoma de Kaposi en pacientes expuestos a rituximab con sarcoma de Kaposi preexistente. Estos casos ocurrieron en indicaciones no aprobadas y la mayoría de los pacientes eran VIH positivos.
Reacciones adversas de tipo hematológico: De acuerdo con la información públicamente disponible del medicamento innovador, en los ensayos clínicos con Rituximab en monoterapia administrado durante 4 semanas, las anomalías hematológicas que aparecieron en una minoría de pacientes fueron, en general, leves y reversibles. Se notificaron casos graves de neutropenia (grado 3/4) en un 4.2%, anemia en un 1.1% y trombocitopenias en el 1.7% de los pacientes. Durante el tratamiento de mantenimiento con Rituximab de hasta dos años se notificó una mayor incidencia de casos de leucopenia (grado 3/4, 5% vs. 2%) y neutropenia grado 3/4, (10% vs. 4%) comparado con el brazo de observación. La incidencia de trombocitopenia fue baja (< 1. grado 3/4) y no hubo diferencias entre los brazos del tratamiento. Durante el ciclo de tratamiento en estudios con rituximab en combinación con quimioterapia, leucopenia grado 3/4 (R CHOP 88% vs. CHOP 79%, R-FC 23% vs. FC 12%), neutropenia (R-CVP 24% vs. CVP 14%, RCHOP 97% frente a CHOP 88%, R-FC 30% frente a FC 19% en CLL no tratada previamente), pancitopenia (RFC 3% frente a FC 1% en CLL no tratada previamente) generalmente se informaron con frecuencias más altas en comparación con la quimioterapia sola. Sin embargo, la mayor incidencia de neutropenia en pacientes tratados con rituximab y quimioterapia no se asoció con una mayor incidencia de infecciones e infestaciones en comparación con los pacientes tratados con quimioterapia sola. Los estudios en LLC no tratada previamente y en recaída/refractaria han establecido que hasta en el 25% de los pacientes tratados con R-FC la neutropenia fue prolongada (definida como el recuento de neutrófilos que permanece por debajo de 1 x 109/L entre los días 24 y 42 después de la última dosis) o se produjo con un inicio tardío (definido como un recuento de neutrófilos por debajo de 1 x 109/L más tarde de 42 días después de la última dosis en pacientes sin neutropenia prolongada previa o que se recuperaron antes del día 42) después del tratamiento con rituximab más FC. No se informaron diferencias para la incidencia de anemia. Se informaron algunos casos de neutropenia tardía que ocurrieron más de cuatro semanas después de la última infusión de rituximab. En el estudio de primera línea de CLL, los pacientes en estadio C de Binet experimentaron más eventos adversos en el grupo R-FC en comparación con el grupo FC (R-FC 83% frente a FC 71%). En el estudio de LLC recidivante/refractaria, se notificó trombocitopenia de grado 3/4 en el 11% de los pacientes del grupo R-FC en comparación con el 9% de los pacientes del grupo FC.
En ensayos de Rituximab en pacientes con macroglobulinemia de Waldenstrom se han observado aumentos transitorios de los niveles séricos de lgM tras el inicio del tratamiento que pueden estar asociados con hiperviscosidad y síntomas relacionados. El aumento transitorio de lgM generalmente descendió hasta al menos el nivel basal en un periodo de 4 meses.
Reacciones adversas cardiovasculares: De acuerdo con la información públicamente disponible del medicamento innovador, durante los ensayos clínicos con Rituximab en monoterapia, se notificaron reacciones cardiovasculares en el 18.8% de los pacientes, siendo hipotensión e hipertensión las reacciones más frecuentemente notificadas. Se notificaron casos de arritmia de grado 3 o 4 (incluyendo taquicardia ventricular y supraventricular) y de angina de pecho durante la infusión. Durante el tratamiento de mantenimiento, la incidencia de los trastornos cardiacos de grado 3/4 fue comparable entre los pacientes tratados con Rituximab y el brazo de observación. Los acontecimientos cardiacos se notificaron como reacciones adversas graves (fibrilación auricular, infarto de miocardio, fallo del ventrículo izquierdo, isquemia miocárdica) en el 3% de los pacientes tratados con Rituximab en comparación con < 1% de los pacientes del brazo de observación. En estudios que evaluaron rituximab en combinación con quimioterapia, la incidencia de arritmias cardiacas de grado 3 y 4, predominantemente arritmias supraventriculares como taquicardia y aleteo/fibrilación auricular, fue mayor en el grupo R-CHOP (14 pacientes, 6.9%) en comparación con el grupo CHOP (3 pacientes, 1.5%). Todas estas arritmias ocurrieron en el contexto de una infusión de rituximab o se asociaron con condiciones predisponentes como fiebre, infección, infarto agudo de miocardio o enfermedad respiratoria y cardiovascular preexistente. No se observaron diferencias entre los grupos R-CHOP y CHOP en la incidencia de otros eventos cardiacos de grado 3 y 4, como insuficiencia cardiaca, enfermedad del miocardio y manifestaciones de enfermedad arterial coronaria. En LLC, la incidencia global de trastornos cardiacos de grado 3 o 4 fue baja tanto en el estudio de primera línea (4% R-FC, 3% FC) como en el estudio en recaída/refractario (4% R-FC, 4% FC).
Sistema respiratorio: De acuerdo con la información públicamente disponible del medicamento innovador, se han notificado casos de enfermedad pulmonar intersticial con resultado de muerte.
Trastornos neurológicos:
Durante el periodo de tratamiento (fase de tratamiento de inducción que comprende R-CHOP durante un máximo de ocho ciclos), cuatro pacientes (2%) tratados con R-CHOP, todos con factores de riesgo cardiovascular, experimentaron accidentes cerebrovasculares tromboembólicos durante el primer ciclo de tratamiento. No hubo diferencia entre los grupos de tratamiento en la incidencia de otros eventos tromboembólicos. En contraste, tres pacientes (1.5%) tuvieron eventos cerebrovasculares en el grupo CHOP, todos los cuales ocurrieron durante el periodo de seguimiento. En LLC, la incidencia general de trastornos del sistema nervioso de grado 3 o 4 fue baja tanto en el estudio de primera línea (4% R-FC, 4% FC) como en el estudio en recaída/refractario (3% R-FC, 3% FC).
De acuerdo con la información públicamente disponible del medicamento innovador, han sido notificados casos de síndrome de encefalopatía posterior reversible (PRES)/síndrome leucoencefalopatía posterior reversible (RPLS). Los signos y síntomas incluyen alteraciones en la visión, dolor de cabeza, convulsiones y alteración del estado mental con o sin hipertensión asociada. El diagnóstico de PRES/RPLS debe confirmarse mediante técnicas de imagen cerebral. En los casos notificados se han reconocido factores de riesgo para PRES/RPLS, incluyendo enfermedad subyacente, hipertensión, terapia inmunosupresora y/o quimioterapia.
Trastornos gastrointestinales: De acuerdo con la información públicamente disponible del medicamento innovador, en pacientes tratados con Rituximab para el linfoma no Hodgkin se han observado casos de perforación gastrointestinal, que en algunos casos causaron la muerte. En la mayoría de estos casos se administró Rituximab en combinación con quimioterapia.
Niveles de lgG: En los ensayos clínicos que evaluaban el tratamiento de mantenimiento con Rituximab en pacientes con linfoma folicular en recaída o refractario, después del tratamiento de inducción, la mediana de los niveles de lgG estaba por debajo del límite inferior de la normalidad (LLN) (< 7 g/L) en ambos grupos, tanto en el de observación como en el de Rituximab. En el grupo de observación, la mediana del nivel de lgG aumentó posteriormente por encima de LLN, pero se mantuvo constante en el grupo de Rituximab. La proporción de pacientes con niveles lgG por debajo de LLN fue aproximadamente del 60% en el grupo de Rituximab durante los 2 años de tratamiento, mientras que en el grupo de observación descendió (36% después de 2 años).
En pacientes pediátricos tratados con Rituximab se han observado un número pequeño de casos espontáneos; y, en la bibliografía, de hipogammaglobulinemia, en algunos casos grave que requiere terapia prolongada de reemplazo de inmunoglobulinas. No se conocen las consecuencias de la depleción prolongada de células B en pacientes pediátricos.
Trastornos de la piel y del tejido subcutáneo: De acuerdo con la información públicamente disponible del medicamento innovador se han notificado muy raramente casos de necrólisis epidérmica tóxica (síndrome de Lyell) y síndrome de Stevens-Johnson, alguno con desenlace mortal.
Subpoblaciones de pacientes - Rituximab en monoterapia: De acuerdo con la información públicamente disponible del medicamento innovador:
Pacientes de edad avanzada (≥ 65 años): La incidencia de RAM de todos los grados y las RAM grado 3/4 fueron similares en pacientes de edad avanzada en comparación con pacientes más jóvenes (< 65 años).
Enfermedad voluminosa o Bulky:
Hubo una mayor incidencia de RAM de grado 3/4 en pacientes con enfermedad voluminosa que en pacientes sin enfermedad voluminosa (25.6% frente a 15.4%). La incidencia de RAM de cualquier grado fue similar en estos dos grupos.
Retratamiento: El porcentaje de pacientes que notificaron RAM en el retratamiento con ciclos posteriores de Rituximab fue similar al porcentaje de pacientes que notificaron RAM de cualquier grado y RAM de grado 3/4 para el tratamiento inicial.
Subpoblaciones de pacientes: tratamiento combinado con rituximab:
Ancianos (≥ 65 años):
La incidencia de eventos adversos sanguíneos y linfáticos de grado 3/4 fue mayor en pacientes de edad avanzada en comparación con pacientes más jóvenes(< 65 años), con LLC no tratada previamente o en recaída/refractaria.
Experiencia en granulomatosis con poliangeítis (GPA) y poliangeítis microscópica (PAM):
Inducción de la remisión en adultos (Estudio 1 de GPA/MPA):
En el Estudio 1 de GPA/MPA, 99 pacientes adultos fueron tratados para inducir la remisión de GPA y PAM con rituximab (375 mg/m2, una vez a la semana durante 4 semanas) y glucocorticoides.
Las RAM enumeradas en la Tabla 14 fueron todas las reacciones adversas que ocurrieron con una incidencia de ≥ 5% en el grupo de rituximab y con una frecuencia mayor que en el grupo de comparación.
Tabla 14. Reacciones adversas que ocurrieron a los 6 meses en ≥ 5% de los pacientes adultos que recibieron rituximab en el Estudio 1 de GPA/MPA (Rituximab n = 99 con mayor frecuencia que el grupo de comparación) o durante la vigilancia posterior a la comercialización
|
Clasificación de órganos del sistema MedDRA Reacción adversa |
Frecuencia |
|
Infecciones e infestaciones |
|
|
Infección del tracto urinario |
7% |
|
Bronquitis |
5% |
|
Infección de herpes |
5% |
|
Nasofaringitis |
5% |
|
Infección viral grave1 |
No conocida |
|
Trastornos de la sangre y del sistema linfático |
|
|
Trombocitopenia |
7% |
|
Trastornos del sistema inmunológico |
|
|
Síndrome de liberación de citoquinas |
5% |
|
Trastornos del metabolismo y de la nutrición |
|
|
Hiperpotasemia |
5% |
|
Desórdenes psiquiátricos |
|
|
Insomnio |
14% |
|
Trastornos del sistema nervioso |
|
|
Mareo |
10% |
|
Temblor |
10% |
|
Trastornos vasculares |
|
|
Hipertensión |
12% |
|
Enrojecimiento |
5% |
|
Trastornos respiratorios, torácicos y mediastínicos |
|
|
Tos |
12% |
|
Disnea |
11% |
|
Epistaxis |
11% |
|
Congestión nasal |
6% |
|
Desórdenes gastrointestinales |
|
|
Diarrea |
18% |
|
Dispepsia |
6% |
|
Estreñimiento |
5% |
|
Trastornos de la piel y del tejido subcutáneo |
|
|
Acné |
7% |
|
Trastornos musculoesqueléticos y del tejido conjuntivo |
|
|
Espasmos musculares |
18% |
|
Artralgia |
15% |
|
Dolor de espalda |
10% |
|
Debilidad muscular |
5% |
|
Dolor musculoesquelético |
5% |
|
Dolor en las extremidades |
5% |
|
Desordenes generales y condiciones administrativas del sitio |
|
|
Edema periférico |
16% |
|
Investigaciones |
|
|
Hemoglobina disminuida |
6% |
1 Observado durante la vigilancia posterior a la comercialización. Consulte también la sección infecciones a continuación.
Tratamiento de mantenimiento para adultos (estudio 2 de GPA/MPA):
En el Estudio 2 de GPA/MPA, un total de 57 pacientes adultos con GPA y PAM activos graves fueron tratados con rituximab para el mantenimiento de la remisión.
Tabla 15. Reacciones adversas que ocurrieron en ≥ 5% de los pacientes adultos que recibieron rituximab en el Estudio 2 de GPA/MPA (Rituximab n = 57), y con mayor frecuencia que el grupo de comparación, o durante la vigilancia posterior a la comercialización
|
Clasificación de órganos del sistema MedDRA Reacción adversa |
Frecuencia |
|
Infecciones e infestaciones |
|
|
Bronquitis |
14% |
|
Rinitis |
5% |
|
Infección viral grave1 |
No conocida |
|
Trastornos respiratorios, torácicos y mediastínicos |
|
|
Disnea |
9% |
|
Desórdenes gastrointestinales |
|
|
Diarrea |
7% |
|
Desordenes generales y condiciones administrativas del sitio |
|
|
Pirexia |
9% |
|
Enfermedad similar a la influenza |
5% |
|
Edema periférico |
5% |
|
Lesiones, intoxicaciones y complicaciones de procedimientos |
|
|
Reacciones relacionadas con la perfusión2 |
12% |
1 Observado durante la vigilancia posterior a la comercialización. Consulte también la sección infecciones a continuación.
2 Los detalles sobre las reacciones relacionadas con la perfusión se proporcionan en la descripción de la sección de reacciones adversas seleccionadas.
El perfil de seguridad general fue consistente con el perfil de seguridad bien establecido para rituximab en indicaciones autoinmunes aprobadas, incluidas GPA y PAM. En general, el 4% de los pacientes en el brazo de rituximab experimentaron eventos adversos que llevaron a la suspensión. La mayoría de los eventos adversos en el brazo de rituximab fueron de intensidad leve o moderada. Ningún paciente en el brazo de rituximab tuvo eventos adversos fatales.
Los eventos notificados con mayor frecuencia considerados RAM fueron reacciones e infecciones relacionadas con la perfusión.
Seguimiento a largo plazo (estudio 3 de GPA/MPA):
En un estudio observacional de seguridad a largo plazo, 97 pacientes con GPA y PAM recibieron tratamiento con rituximab (media de 8 infusiones [rango 1-28]) durante hasta 4 años, según la práctica habitual y el criterio de su médico. El perfil de seguridad general fue consistente con el perfil de seguridad bien establecido de rituximab en GPA y PAM y no se informaron nuevas reacciones adversas.
Descripción de reacciones adversas seleccionadas:
Reacciones relacionadas con la infusión: De acuerdo con la información públicamente disponible del medicamento innovador, las RRI en el ensayo clínico de GPA y PAM se definieron como cualquier evento adverso que ocurra dentro de las 24 horas tras la infusión y que los investigadores las considerasen relacionadas con la infusión en la población de seguridad. Se trataron noventa y nueve pacientes con Rituximab y el 12% experimentaron al menos una RRI. Todas las RRI fueron de Grado 1 o 2. Las RRI más frecuentes incluyeron el síndrome de liberación de citocinas, enrojecimiento, irritación de garganta y temblor. Rituximab se administró en conjunto con glucocorticoides por vía intravenosa los cuales reducen la incidencia y gravedad de estos eventos.
En el Estudio 2 de GPA/MPA (estudio de mantenimiento en adultos), 7/57 (12%) pacientes en el brazo de rituximab experimentaron al menos una reacción relacionada con la infusión. La incidencia de síntomas de RRI fue máxima durante o después de la primera infusión (9%) y disminuyó con las infusiones posteriores (< 4%). Todos los síntomas de RRI fueron leves o moderados y la mayoría de ellos se informaron en los SOC Trastornos respiratorios, torácicos y mediastínicos y trastornos de la piel y del tejido subcutáneo.
Infecciones: De acuerdo con la información públicamente disponible del medicamento innovador, en los 99 pacientes de Rituximab, la tasa global de infección fue aproximadamente del 210 por 100 años-paciente (IC del 95%: 173-256). Las infecciones fueron predominantemente de leves a moderadas y afectaron mayoritariamente al tracto respiratorio superior, herpes zóster y al tracto urinario. La incidencia de infecciones graves fue aproximadamente del 25 por 100 años-paciente. La infección grave notificada más frecuentemente en el grupo de Rituximab fue neumonía con una frecuencia del 4%.
En el Estudio 2 de GPA/MPA, 30/57 (53%) pacientes en el brazo de rituximab experimentaron infecciones. La incidencia de infecciones de todos los grados fue similar entre los brazos. Las infecciones fueron predominantemente de leves a moderadas. Las infecciones más comunes en el brazo de rituximab incluyeron infecciones del tracto respiratorio superior, gastroenteritis, infecciones del tracto urinario y herpes zóster. La incidencia de infecciones graves fue similar en ambos brazos (aproximadamente 12%). La infección grave notificada con mayor frecuencia en el grupo de rituximab fue la bronquitis leve o moderada.
En el entorno posterior a la comercialización, se informaron infecciones virales graves en pacientes con GPA/MPA tratados con rituximab.
Tumores: De acuerdo con la información públicamente disponible del medicamento innovador, la incidencia de tumores en pacientes con granulomatosis con poliangeítis y poliangeítis microscópica tratados con Rituximab en el ensayo clínico fue 2.00 por 100 años-paciente en la fecha de cierre común del ensayo (cuando el último paciente ha terminado el periodo de seguimiento). Basándose en las tasas de incidencia estandarizadas, la incidencia de tumores parece ser similar a la que ya se ha notificado en pacientes con vasculitis asociada a ANCA.
Reacciones adversas cardiovasculares:
De acuerdo con la información públicamente disponible del medicamento innovador, se han notificado caso de eventos cardiacos graves. En el Estudio 1 de GPA/MPA, los eventos cardiacos ocurrieron a una tasa de aproximadamente 273 por 100 años-paciente (IC del 95%: 149 - 470) en el punto final primario de 6 meses. La tasa de eventos cardiacos graves fue de 2.1 por 100 años-paciente (IC del 95%: 3 a 15). Los acontecimientos notificados con mayor frecuencia fueron taquicardia (4%) y fibrilación auricular (3%) (ver sección Precauciones generales).
Acontecimientos neurológicos: De acuerdo con la información públicamente disponible del medicamento innovador, se han notificado casos de síndrome de encefalopatía posterior reversible (SEPR)/síndrome de leucoencefalopatía posterior reversible (SLPR). Los signos y síntomas incluyeron alteraciones visuales, cefalea, convulsiones y alteración del estado mental, con o sin hipertensión asociada. El diagnóstico de SEPR/SLPR requiere confirmación mediante estudios de imagen cerebral. Los casos notificados de SEPR/SLPR tenían factores de riesgo reconocidos, incluyendo las enfermedades subyacentes del paciente, hipertensión, terapia de inmunosupresión y/o quimioterapia.
Reactivación de Hepatitis B: De acuerdo con la información públicamente disponible del medicamento innovador, se ha notificado un pequeño número de casos de reactivación de hepatitis B, algunos con resultado de muerte, en pacientes con granulomatosis con poliangeítis y poliangeítis microscópica que habían recibido Rituximab en la experiencia postcomercialización.
Hipogammaglobulinemia:
Se ha observado hipogammaglobulinemia (lgA, lgG o lgM por debajo del límite inferior de la normalidad) en pacientes adultos y pediátricos con GPA y PAM tratados con rituximab.
En el Estudio 1 de GPA/MPA, a los 6 meses en el grupo de rituximab el 27%, 58% y 51% de los pacientes con niveles normales de inmunoglobulina al inicio tenían niveles bajos de lgA, lgG e lgM, respectivamente, en comparación con el 25%, 50% y 46% en el grupo ciclofosfamida. La tasa de infecciones generales e infecciones graves no aumentó después del desarrollo de niveles bajos de lgA, lgG o lgM.
En el Estudio 2 de GPA/MPA, no se observaron diferencias clínicamente significativas entre los dos brazos de tratamiento ni disminuciones en los niveles de inmunoglobulina total, lgG, lgM o lgA durante todo el ensayo.
Neutropenia:
En el Estudio 1 de GPA/MPA, el 24% de los pacientes en el grupo de rituximab (ciclo único) y el 23% de los pacientes en el grupo de ciclofosfamida desarrollaron neutropenia de grado 3 o mayor según los CTC. La neutropenia no se asoció con un aumento observado de infecciones graves en pacientes tratados con rituximab.
En el estudio 2 de GPA/MPA, la incidencia de neutropenia de todos los grados fue del 0% para los pacientes tratados con rituximab frente al 5% para los pacientes tratados con azatioprina.
Trastornos de la piel y del tejido subcutáneo: De acuerdo con la información públicamente disponible del medicamento innovador, se han notificado muy raramente casos de necrólisis epidérmica tóxica (síndrome de Lyell) y síndrome de Stevens-Johnson, alguno con desenlace mortal.
Comparabilidad de ARASAMILA® con Mabthera®: De acuerdo con la información públicamente disponible, las frecuencias generales de eventos adversos comunes y eventos adversos graves fueron comparables entre ambos grupos de tratamiento en el linfoma folicular no Hodgkin (fases de combinación y mantenimiento). Los perfiles de seguridad, incluida la inmunogenicidad de ARASAMILA® en las poblaciones fundamentales, son consistentes con el perfil de seguridad conocido del medicamento de referencia informado en ensayos clínicos y vigilancia posterior a la comercialización.
A continuación, se presenta una discusión de los eventos adversos informados en los estudios individuales.
Estudio GP13-301 (Linfoma no Hodgkin folicular): Durante la fase de tratamiento combinado y la fase de tratamiento de mantenimiento en curso del estudio GP13-301, la incidencia general de eventos adversos, eventos adversos graves, interrupciones del tratamiento debido a eventos adversos y muertes fueron similares en el ARASAMILA® y los grupos de medicamentos de referencia. La Tabla 7 a continuación resume los eventos adversos informados con mayor frecuencia con sospecha de causalidad al fármaco del estudio en la fase de combinación.
Tabla 16. Eventos adversos con sospecha de relación causal con el tratamiento informados en al menos el 5% de los pacientes con FL - Fase de combinación
|
GP2013 - CVP (N = 312) |
Medicamento de referencia-CVP (N = 315) |
|||
|
Término preferido |
Todos los grados n (%) |
Grado 3/4 n (%) |
Todos los grados n (%) |
Grado 3/4 n (%) |
|
Número total de pacientes con EA’s con sospecha de relación con el medicamento del estudio |
229 (73.4) |
88 (28.2) |
223 (70.8) |
98 (31.1) |
|
Neutropenia |
65 (20.8) |
44 (14.1) |
77 (24.4) |
51 (16.2) |
|
Constipación |
43 (13.8) |
3 (1.0) |
33 (10.5) |
1 (0.3) |
|
Relacionados con la infusión |
41 (13.1) |
3 (1.0) |
37 (11.7) |
2 (0.6) |
|
Náusea |
34 (10.9) |
0 |
35 (11.1) |
0 |
|
Neuropatía peripheral |
34 (10.9) |
4 (1.3) |
25 (7.9) |
2 (0.6) |
|
Fatiga |
26 (8.3) |
0 |
18 (5.7) |
1 (0.3) |
|
Paraestesia |
21 (6.7) |
1 (0.3) |
30 (9.5) |
1 (0.3) |
|
Astenia |
21 (6.7) |
0 |
22 (7.0) |
1 (0.3) |
|
Leucopenia |
21 (6.7) |
7 (2.2) |
24 (7.6) |
13 (4.1) |
|
Alopecia |
20 (6.4) |
1 (0.3) |
17 (5.4) |
1 (0.3) |
|
Neuropatía sensorial periférica |
21 (6.7) |
0 |
17 (5.4) |
0 |
|
Vómito |
16 (5.1) |
0 |
14 (4.4) |
0 |
|
Pirexia |
11 (3.5) |
1 (0.3) |
16 (5.1) |
0 |
EA= Evento Adverso; CVP= ciclofosfamida, vincristina, prednisona; LF= Linfoma Folicular; n= número de pacientes en la respectiva categoría; N= Número de pacientes por grupo de tratamiento.
En la fase de mantenimiento, el único evento adverso informado con una frecuencia superior al 5% fue neutropenia (todos los grados: ARASAMILA® 7.9%, medicamento de referencia 5.2%; grado 3 o 4: ARASAMILA® 5.1%, medicamento de referencia 3.6%). La neutropenia febril no se informó en ninguno de los pacientes de ARASAMILA® y en el 1.2% en el medicamento de referencia (todos de Grado 3/4). Se notificaron infecciones de grado 3/4 en el 1.6% en ARASAMILA® y en el 0.4% en el medicamento de referencia, y las infecciones graves en el 6-7% en ARASAMILA® y en el 6.7% en el medicamento de referencia.
INMUNOGENICIDAD: De acuerdo con la información públicamente disponible, la inmunogenicidad se evaluó para 559 pacientes con linfoma folicular en el estudio GP13-301. En general, el número de pacientes con anticuerpos antidrogas (ADA) detectables después de la dosis fue bajo (8 pacientes, 1.4%), sin diferencias clínicamente significativas entre ARASAMILA® (5 de 274 pacientes, 1.8%) y grupos de medicamentos de referencia (3 de 285 pacientes, 1.1%). Se detectaron anticuerpos neutralizantes (NAb) en el 0.7% de los pacientes en ambos grupos de tratamiento.
En resumen, los resultados de inmunogenicidad evaluados por la formación de ADA y NAb y al evaluar posibles signos clínicos de inmunogenicidad no revelaron diferencias clínicamente relevantes entre ARASAMILA® y el medicamento de referencia y la incidencia observada fue comparable con la incidencia de ADA informada previamente para el medicamento de referencia.
PRECAUCIONES EN RELACIÓN CON EFECTOS DE CARCINOGÉNESIS, MUTAGÉNESIS, TERATOGÉNESIS Y SOBRE LA FERTILIDAD: De acuerdo con la información públicamente disponible del medicamento innovador se ha demostrado que Rituximab posee una alta especificidad para el antígeno CD20 de las células B. Durante los ensayos de toxicidad en monos cinomólogos no se observó ningún otro efecto además de la depleción de células B en la sangre periférica y en el tejido linfático, previsible por el mecanismo farmacológico.
De acuerdo con la información públicamente disponible del medicamento innovador, se han realizado estudios de toxicidad en el desarrollo en monos cinomólogos que recibieron dosis de hasta 100 mg/kg (tratamiento durante los días 20-50 de la gestación); no se apreciaron evidencias de toxicidad fetal debidos a Rituximab. No obstante, se observó, de forma dosis-dependiente y mediada por el mecanismo farmacológico, una depleción de células B en los órganos linfáticos de los fetos, que persistió después del nacimiento; la depleción se acompañó de una disminución de los niveles de lgG de los animales recién nacidos afectados. El recuento de células B de estos animales se normalizó en los 6 primeros meses de vida y no afectó negativamente a la reacción a la vacunación.
De acuerdo con la información públicamente disponible reportada por el medicamento innovador, no se han llevado a cabo pruebas estándar para investigar la mutagenicidad, ya que esas pruebas no son relevantes para esta molécula. No se han realizado estudios a largo plazo en animales para establecer el potencial carcinogénico de Rituximab.
De acuerdo con la información públicamente disponible reportada por el medicamento innovador, no se han realizado estudios específicos para determinar los efectos de Rituximab en la fertilidad. En general, en ensayos de toxicidad en monos cinomolgos no se observó efecto dañino en los órganos reproductores en hombres o mujeres.
Fertilidad:
Los estudios en animales no revelaron efectos nocivos de rituximab en los órganos reproductivos.
INTERACCIONES MEDICAMENTOSAS Y DE OTRO GÉNERO: Actualmente existen datos limitados sobre las posibles interacciones con otros medicamentos y con Rituximab.
La administración de rituximab con fludarabina, ciclofosfamida o metotrexato parece no tener impacto en la farmacocinética de estos. Además, no hubo un efecto aparente de fludarabina y ciclofosfamida en la farmacocinética de rituximab.
Los pacientes con títulos de anticuerpos humanizados, anti-murinos o anti-fármaco (HAMA/ADA) pueden sufrir reacciones alérgicas o de hipersensibilidad al ser tratados con otros anticuerpos monoclonales terapéuticos o de diagnóstico.
ALTERACIONES EN LOS RESULTADOS DE PRUEBAS DE LABORATORIO:
Linfoma no Hodgkin: De acuerdo con la información públicamente disponible, se notificaron algunos casos de neutropenia tardía ocurridas tras más de 4 semanas después de la última infusión de Rituximab.
En ensayos de Rituximab en pacientes con macroglobulinemia de Waldenstrom se han observado aumentos transitorios de los niveles séricos de lgM tras el inicio del tratamiento que pueden estar asociados con hiperviscosidad y síntomas relacionados. El aumento transitorio de lgM generalmente descendió hasta al menos el nivel basal en un periodo de 4 meses.
Pacientes con granulomatosis con poliangeítis (Wegener) (GPA) y poliangeítis microscópica (PAM): Hipogammaglobulinemia: De acuerdo con la información públicamente disponible, se ha observado hipogammaglobulinemia (lgA, lgG o lgM por debajo del límite inferior normal) en pacientes con granulomatosis con poliangeítis y poliangeítis microscópica tratados con Rituximab. A los 6 meses, en el ensayo de no inferioridad, con comparador activo, aleatorizado, doble ciego, multicéntrico controlado con placebo, en el grupo de Rituximab el 27%, 58% y 51% de los pacientes con niveles de inmunoglobulinas normales al inicio del ensayo, tuvieron bajos niveles de lgA, lgG e lgM respectivamente en comparación con el 25%, 50% y 46% en el grupo de ciclofosfamida. No hubo un incremento en la incidencia de las infecciones generales o infecciones graves en pacientes con bajos niveles de lgA, lgG e lgM.
Neutropenia: De acuerdo con la información públicamente disponible, en el ensayo de Rituximab de no inferioridad, con comparador activo, aleatorizado, doble ciego, multicéntrico controlado con placebo, en granulomatosis con poliangeítis y poliangeítis microscópica, el 24% de los pacientes en el grupo de Rituximab (ciclo único) y el 23% de los pacientes en el grupo de ciclofosfamida desarrollaron neutropenia de grado 3 o superior. La neutropenia no se asoció a un incremento observado en la infección grave en los pacientes tratados con Rituximab. El efecto de múltiples ciclos de Rituximab en el desarrollo de neutropenia en pacientes con granulomatosis con poliangeítis y poliangeítis microscópica no se ha estudiado en ensayos clínicos.
PRECAUCIONES GENERALES:
La solución contiene hasta 23.06 mmol de sodio.
Anticuerpo monoclonal quimérico murino/humano lgG1 de origen ADN recombinante expresado en células de ovario de hámster chino (CHO).
Trazabilidad:
Para mejorar la trazabilidad de los medicamentos biológicos, debe consignarse claramente el nombre del medicamento administrado en la historia clínica del paciente, así como el número de lote.
Leucoencefalopatía multifocal progresiva (LMP): Todos los pacientes tratados con Rituximab para GPA, PAM deben recibir la tarjeta de alerta para el paciente con cada infusión. La tarjeta de alerta contiene información de seguridad importante para los pacientes con respecto al posible aumento del riesgo de infecciones, LMP.
De acuerdo con la información públicamente disponible, han notificado casos muy raros de muerte por leucoencefalopatía multifocal progresiva (LMP) tras el uso de Rituximab. Los pacientes deben ser monitorizados a intervalos regulares para detectar cualquier nuevo signo o síntoma neurológico, así como cualquier empeoramiento que pueda indicar LMP. Si se llegara a sospechar que el paciente sufre LMP, debe suspenderse la administración de Rituximab hasta que se haya descartado dicha posibilidad. El médico debe evaluar a los pacientes para determinar si los síntomas son indicativos de alteración neurológica, y si es así, si estos síntomas son indicativos de LMP. Se debe considerar si esta clínicamente indicada la consulta con un neurólogo.
Si existe alguna duda, además de la evaluación, deberá considerarse un estudio de imagen de resonancia magnética preferiblemente con contraste, un análisis del líquido cefalorraquídeo (LCR) para detectar ADN del virus JC y repetir las evaluaciones neurológicas.
El médico debe estar especialmente alerta a los síntomas indicativos de LMP que el paciente pueda no advertir (p. ej. síntomas cognitivos, neurológicos o psiquiátricos). Se le debe aconsejar al paciente que informe a su pareja o a la persona que le cuide acerca de su tratamiento, ya que ellos puedan detectar síntomas de los que el paciente no es consciente. Si el paciente desarrolla LMP, se debe suspender el tratamiento con Rituximab permanentemente.
En pacientes inmunodeprimidos con LMP, se ha observado la estabilización o mejora del desenlace clínico tras la reconstitución del sistema inmune. Se desconoce si la detección precoz de LMP y la suspensión del tratamiento con Rituximab pueden llevar a una estabilización similar o a una mejoría del desenlace clínico.
Linfoma no Hodgkin y leucemia linfocítica crónica: Reacciones relacionadas con la infusión: De acuerdo con la información públicamente disponible, Rituximab se asocia con reacciones relacionadas con la infusión que pueden estar relacionadas con la liberación de citocinas y/u otros mediadores químicos (Doesseger L et al., 2015). El síndrome de liberación de citocinas puede ser clínicamente indistinguible de las reacciones de hipersensibilidad aguda.
Las reacciones descritas a continuación incluyen el síndrome de liberación de citocinas, el síndrome de lisis tumoral y reacciones anafilácticas y de hipersensibilidad.
Se han reportado casos de reacciones relacionadas con la infusión graves, con resultado de muerte, durante el uso postcomercialización de la formulación de Rituximab intravenoso, con un inicio entre los 30 minutos y 2 horas después del comienzo de la primera infusión intravenosa de Rituximab. Incluyeron acontecimientos pulmonares y en algunos casos incluyeron lisis tumoral rápida y características del síndrome de lisis tumoral además de fiebre, escalofríos, rigidez, hipotensión, urticaria, angioedema y otros síntomas (ver sección Reacciones secundarias y adversas).
El síndrome de liberación de citocinas grave se presenta por disnea grave, frecuentemente acompañada de broncoespasmo e hipoxia, además de fiebre, escalofríos, rigidez, urticaria y angioedema. Este síndrome puede estar asociado con algunas características del síndrome de lisis tumoral tales como hiperuricemia, hiperpotasemia, hipocalcemia, hiperfosfatemia, fallo renal agudo, aumento de la lactato-deshidrogenasa (LDH) y puede asociarse con fallo respiratorio agudo y muerte. El fallo respiratorio agudo puede estar acompañado de infiltración intersticial o edema pulmonar, visibles a la exploración radiológica torácica. El síndrome se manifiesta frecuentemente dentro de la primera o segunda hora después de iniciar la primera infusión. Los pacientes con antecedentes de insuficiencia pulmonar o con infiltración tumoral pulmonar pueden tener un riesgo mayor de mal pronóstico y deben aumentarse las precauciones durante su tratamiento. En aquellos pacientes que desarrollen síndrome de liberación de citocinas grave (ver sección Dosis y vía de administración) se debe interrumpir la infusión inmediatamente y administrar tratamiento sintomático de choque. Dado que a la mejoría inicial de los síntomas clínicos puede seguir una recidiva, se debe monitorizar estrechamente a estos pacientes hasta que el síndrome de lisis tumoral y la infiltración pulmonar se hayan resuelto o hayan sido descartados. Una vez resueltos completamente los signos y síntomas, raramente se repite el síndrome de liberación de citocinas en tratamientos posteriores.
Los pacientes con un elevado número de células tumorales circulantes (≥ 25 × 109/L) que pueden tener un riesgo mayor de desarrollar un síndrome de liberación de citocinas especialmente grave, se deben tratar extremando las precauciones. Estos pacientes se deben monitorizar muy estrechamente durante la primera infusión. En estos pacientes se debe considerar reducir la velocidad de la primera infusión o un fraccionamiento de la dosis durante más de dos días durante el primer ciclo y algún ciclo posterior si el recuento de linfocitos es aún > 25 × 109/L.
En el 77% de los pacientes tratados con Rituximab se han detectado todo tipo de reacciones adversas relacionadas con la infusión (incluyendo síndrome de liberación de citocinas acompañado de hipotensión y broncoespasmo en el 10% de los pacientes, ver sección Reacciones secundarias y adversas). Generalmente, estos síntomas son reversibles tras la interrupción de la infusión de Rituximab y la administración de un antipirético, un antihistamínico, y ocasionalmente, oxígeno, solución salina intravenosa o broncodilatadores, y, en caso de necesidad, glucocorticoides. Para reacciones graves, ver síndrome de liberación de citocinas.
Se han reportado casos de reacciones de hipersensibilidad, incluyendo anafilácticas, después de la administración intravenosa de proteínas. A diferencia del síndrome de liberación de citocinas, las reacciones de hipersensibilidad verdaderas se presentan típicamente durante los primeros minutos de la infusión. Se debe contar de forma inmediata con medicamentos utilizados para combatir las reacciones de hipersensibilidad, es decir, adrenalina, antihistamínicos y glucocorticoides, por si ocurriera una reacción alérgica durante la administración de Rituximab. Clínicamente las manifestaciones de anafilaxia pueden parecerse a las manifestaciones del síndrome de liberación de citocinas (previamente descrito). Las reacciones atribuibles a la hipersensibilidad se han notificado con menor frecuencia que las atribuidas a la liberación de citocinas.
Además, se notificaron casos de infarto de miocardio, fibrilación auricular, edema pulmonar y trombocitopenia reversible aguda.
Debido a que durante la administración de Rituximab puede desarrollarse hipotensión, se debe considerar interrumpir los medicamentos antihipertensivos 12 horas antes de la infusión de ARASAMILA®.
Trastornos cardiacos: De acuerdo con la información públicamente disponible, se han reportado casos de angina de pecho, arritmias cardiacas tales como flutter y fibrilación auricular, fallo cardiaco y/o infarto de miocardio en pacientes tratados con Rituximab. Por lo tanto, se deben monitorizar estrictamente los pacientes con antecedentes de enfermedad cardiaca y/o cardiotoxicidad asociada a la quimioterapia.
Toxicidad hematológica: De acuerdo con la información públicamente disponible, aunque Rituximab en monoterapia no tiene efecto mielosupresor, se debe tener precaución en pacientes con un recuento de neutrófilos < 1.5 × 109/L y/o plaquetas < 75 × 109/L, puesto que la experiencia clínica en esta población es limitada. Rituximab se ha utilizado en 21 pacientes sometidos a trasplante autólogo de médula ósea y en otros grupos de riesgo con una función de la médula ósea presumiblemente reducida, sin que haya inducido mielotoxicidad.
Se deben realizar recuentos de sangre total de forma regular, incluyendo recuentos de neutrófilos y de plaquetas, durante el tratamiento con ARASAMILA®. Infecciones: De acuerdo con la información públicamente disponible en el tratamiento con Rituximab pueden presentarse infecciones graves e incluso mortales (ver sección Reacciones secundarias y adversas). ARASAMILA® no debe ser administrado a pacientes con infecciones graves activas (ej. tuberculosis, sepsis e infecciones oportunistas, ver sección Contraindicaciones).
El médico debe tener especial precaución cuando considere el uso de ARASAMILA® en pacientes con historial de infecciones crónicas o recurrentes o en unas condiciones subyacentes que puedan provocar una mayor predisposición a infecciones (ver sección Reacciones secundarias y adversas).
Durante el uso postcomercialización de rituximab en LNH se han notificado casos muy raros de leucoencefalopatía multifocal progresiva (LMP) (ver sección Reacciones secundarias y adversas). La mayoría de los pacientes habían recibido Rituximab en combinación con quimioterapia o como parte de un trasplante de células madre hematopoyéticas.
Inmunizaciones: De acuerdo con la información públicamente disponible, no se ha estudiado la seguridad de la inmunización con vacunas de virus vivos después de recibir tratamiento con Rituximab en pacientes con LNH, por tanto, no se recomienda la vacunación con virus vivos. Los pacientes tratados con ARASAMILA® pueden recibir vacunas inactivadas, sin embargo, con las vacunas inactivadas los porcentajes de respuesta pueden ser menores. En un estudio no aleatorizado de pacientes con LNH de bajo grado con recidivas, que recibieron Rituximab en monoterapia cuando se comparó con el grupo control no tratado sano, el porcentaje de respuesta a la vacunación fue menor con el antígeno de memoria del Tétanos (16% vs. 81%), y con neoantígeno Keyhole Limpet Haemocyanin (KLH) (4% vs.76% cuando se determinó un incremento > de 2 en el título de anticuerpo).
Los títulos de anticuerpos medios antes del tratamiento frente antígenos como Streptococcus pneumoniae, gripe A, paperas, rubéola y varicela, se mantuvieron hasta al menos 6 meses después del tratamiento con Rituximab.
Reacciones de la piel: De acuerdo con la información públicamente disponible, se han notificado casos de reacciones cutáneas graves tales como necrólisis epidérmica tóxica (síndrome de Lyell) y síndrome de Stevens-Johnson, algunas con desenlace mortal (ver sección Reacciones secundarias y adversas). En caso de que aparezcan tales reacciones con una sospecha de relación con Rituximab, el tratamiento debe suspenderse permanentemente.
Granulomatosis con poliangeítis (GPA), poliangeítis microscópica (MPA):
Reacciones Relacionadas con la Infusión (RRI): De acuerdo con la información públicamente disponible, Rituximab se asocia con reacciones relacionadas con la infusión (RRI) que pueden estar mediadas por la liberación de citocinas y/u otros mediadores químicos. Siempre antes de cada infusión de ARASAMILA® se debe administrar premedicación consistente en un analgésico/antipirético y un antihistamínico.
Se han notificado durante la comercialización de Rituximab RRI graves con resultado de muerte en pacientes. La mayoría de los eventos relacionados con la infusión notificados en los ensayos clínicos fueron de leves a moderados en cuanto a gravedad. Los síntomas reportados con mayor frecuencia fueron reacciones alérgicas como cefalea, prurito, irritación de garganta, enrojecimiento, erupciones, urticaria, hipertensión y fiebre. En general, el porcentaje de pacientes que experimenta alguna reacción a la infusión es más alto después de la primera infusión que tras la segunda en cualquier ciclo de tratamiento. La incidencia de RRI disminuye con las sucesivas infusiones (ver sección Reacciones secundarias y adversas). Las reacciones notificadas revirtieron, por lo general, tras disminuir la velocidad de infusión de Rituximab o suspender la infusión y administrar un antipirético, un antihistamínico y, en ocasiones, oxígeno, una solución intravenosa de cloruro de sodio 9 mg/ml (0.9%) o broncodilatadores, y en caso de necesidad, glucocorticoides. Los pacientes con afecciones cardiacas preexistentes o que han tenido una reacción cardiopulmonar adversa previa se deben vigilar estrechamente. Dependiendo de la gravedad de la RRI y de las intervenciones necesarias se suspenderá el tratamiento con ARASAMILA® de forma temporal o permanente. En la mayoría de los casos, la infusión se pudo reanudar al 50% de la velocidad anterior (p. ej., de 100 mg/h a 50 mg/h) una vez resueltos completamente todos los síntomas.
Deben estar disponibles para su uso inmediato medicamentos para tratar las reacciones de hipersensibilidad, como la adrenalina, los antihistamínicos y los glucocorticoides, por si ocurre una reacción alérgica durante la administración de ARASAMILA®.
Trastornos cardiacos: De acuerdo con la información públicamente disponible, no se tienen datos sobre la seguridad de Rituximab en pacientes con insuficiencia cardiaca moderada (clase III de la NYHA) o enfermedad cardiovascular grave no controlada. En pacientes con isquemia miocárdica preexistente se ha notificado con Rituximab su exacerbación sintomática, resultando en angina de pecho, así como fibrilación auricular y flutter. Por lo tanto, si el paciente refiere antecedentes de cardiopatía, y en los que han experimentado previamente reacciones cardiopulmonares adversas, se deberá considerar el riesgo de complicaciones cardiovasculares derivadas de las reacciones a la infusión antes de administrar ARASAMILA® y se monitorizará rigurosamente a los pacientes durante el tratamiento. Debido a que se puede producir hipotensión durante la infusión de Rituximab, se evaluará la necesidad de interrumpir temporalmente cualquier medicamento antihipertensivo 12 horas antes de la infusión de ARASAMILA®.
Se han reportado casos de angina de pecho, arritmias cardiacas, así como aleteo auricular y fibrilación, insuficiencia cardiaca y/o infarto de miocardio en pacientes que recibieron Rituximab. Por lo tanto, los pacientes con antecedentes de enfermedad cardiaca deben ser vigilados estrechamente (ver más arriba reacciones relacionadas con la infusión).
Infecciones: Debido al mecanismo de acción de Rituximab y funciones de las células B, los pacientes tratados con ARASAMILA® pueden tener un mayor riesgo de infección. Se han presentado infecciones graves, incluyendo casos mortales (ver sección Reacciones secundarias y adversas) durante el tratamiento con Rituximab. No debe administrarse ARASAMILA® a pacientes con una infección activa grave (es decir tuberculosis, sepsis e infecciones oportunistas, ver sección Contraindicaciones) ni a aquéllos con inmunodeficiencia grave (p. ej., pacientes con niveles de CD4 o CD8 muy bajos). Se debe tener cuidado antes de administrar Rituximab a pacientes con antecedentes de infecciones recidivantes o crónicas o con patologías subyacentes que puedan predisponer a infecciones graves p. ej., hipogammaglobulinemia (ver sección Reacciones secundarias y adversas). Se recomienda cuantificar los niveles de inmunoglobulina antes de iniciar el tratamiento con ARASAMILA®.
Los pacientes que manifiesten signos y síntomas de infección después del tratamiento con ARASAMILA® deben recibir atención y tratamiento inmediato. Antes de administrar los ciclos siguientes del tratamiento con ARASAMILA®, se debe reevaluar el riesgo potencial de infecciones.
Infecciones hepatitis B: De acuerdo con la información públicamente disponible, en pacientes en tratamiento con Rituximab para granulomatosis con poliangeítis y poliangeítis microscópica se han notificado casos de reactivación de hepatitis B, con resultado mortal.
Antes de iniciar el tratamiento con ARASAMILA® en todos los pacientes se debe llevar a cabo la detección del virus de la Hepatitis B (VHB). Al menos debe incluir HBsAg y HBcAc. Esto puede ser complementado con otros marcadores apropiados de acuerdo a las guías locales. Los pacientes con actividad clínica de hepatitis B no deben ser tratados con Rituximab. En pacientes con serología positiva de hepatitis B (bien HBsAg o HBcAc) se debe consultar con un especialista en enfermedades hepáticas antes de iniciar el tratamiento y deben ser monitorizados y tratados siguiendo los estándares médicos locales para prevenir la reactivación de la hepatitis B.
Neutropenia tardía: De acuerdo con la información públicamente disponible, se deben cuantificar los neutrófilos en sangre antes de cada ciclo con ARASAMILA® y regularmente hasta 6 meses tras la finalización del tratamiento y si hay signos o síntomas de infección (ver sección Reacciones secundarias y adversas).
Reacciones de la piel: De acuerdo con la información públicamente disponible se han reportado casos de reacciones cutáneas graves tales como necrólisis epidérmica tóxica (síndrome de Lyell) y síndrome de Stevens-Johnson, algunas con desenlace mortal (ver sección Reacciones secundarias y adversas). En caso de que aparezcan tales reacciones, con una sospecha de relación con ARASAMILA® el tratamiento debe suspenderse permanentemente.
Inmunizaciones: Antes de iniciar el tratamiento con Rituximab se debe verificar el estado de vacunación de los pacientes y deben estar al día con todas las vacunas de acuerdo con las guías actuales de vacunación antes del tratamiento con ARASAMILA®. La vacunación debe haberse completado al menos cuatro semanas antes de iniciar el tratamiento con ARASAMILA®.
No se ha estudiado la seguridad de la inmunización con vacunas de virus vivos después de recibir tratamiento con Rituximab. Por lo tanto, no está recomendada la vacunación con vacunas de virus vivos durante el tratamiento con ARASAMILA® o mientras haya reducción de células B periféricas.
Los pacientes tratados con ARASAMILA® pueden recibir vacunas inactivadas, sin embargo, con las vacunas inactivadas el porcentaje de respuesta puede ser menor. Si se requiriese vacunación con virus inactivados durante el tratamiento con Rituximab, esta vacunación debe haberse completado como mínimo cuatro semanas antes de comenzar el siguiente ciclo de tratamiento con Rituximab.
Sodio: Este medicamento contiene hasta 23.06 mmol (o 530.1 mg) de sodio por dosis, por lo tanto, se debe tomar en cuenta en pacientes con dietas bajas en sodio: Efectos sobre la capacidad para conducir y utilizar máquinas: De acuerdo con la información públicamente disponible, la influencia de Rituximab sobre la capacidad para conducir y utilizar máquinas es pequeña. Se pueden producir mareos tras la administración de Rituximab (ver sección Reacciones secundarias y adversas).
Malignidad:
Los medicamentos inmunomoduladores pueden aumentar el riesgo de malignidad. Sin embargo, los datos disponibles no sugieren un mayor riesgo de malignidad para el rituximab utilizado en indicaciones autoinmunes más allá del riesgo de malignidad ya asociado a la enfermedad autoinmune subyacente.
Excipientes:
Este medicamento contiene 2.3 mmol (o 52.6 mg) de sodio por frasco ámpula de 10 mL y 11.5 mmol (o 263.2 mg) de sodio por frasco ámpula de 50 mL equivalente al 2.6% (por frasco ámpula de 10 mL) y al 13.2% (por frasco ámpula de 50 mL). La OMS recomienda una ingesta diaria máxima de 2 g de sodio para un adulto.
DOSIS Y VÍA DE ADMINISTRACIÓN:
Vía de administración: Intravenosa.
De acuerdo con la información públicamente disponible reportada por el medicamento innovador, ARASAMILA® se debe administrar bajo la estrecha supervisión de un profesional sanitario con experiencia y en un entorno que disponga de forma Inmediata de un equipo completo de reanimación (ver sección Precauciones generales).
Premedicación y medicamentos profilácticos:
Siempre se debe administrar premedicación consistente en un antipirético y un antihistamínico, por ejemplo, paracetamol y difenhidramina, antes de cada administración de ARASAMILA®.
En pacientes adultos con LNH y LLC tratados con ARASAMILA®, a una velocidad de infusión de 90 minutos, se debe considerar la premedicación con glucocorticoides si ARASAMILA® no se va a administrar en combinación con quimioterapia que incluya glucocorticoides.
Se recomienda la profilaxis con hidratación adecuada y la administraciónde uricostáticos desde 48 horas antes del inicio de la terapia para pacientes con CLL para reducir el riesgo de síndrome de lisis tumoral. Para los pacientes con LLC cuyo recuento de linfocitos es > 25 × 109/L,se recomienda administrar 100 mg de prednisona/prednisolona por vía intravenosa poco antes de la infusión con ARASAMILA® para disminuir la velocidad y la gravedad de las reacciones agudas a la infusión y/o el síndrome de liberación de citoquinas.
En pacientes con GPA o PAM, la premedicación con 100 mg de metilprednisolona intravenosa debe completarse 30 minutos antes de cada infusión de rituximab para disminuir la incidencia y la gravedad de las reacciones relacionadas con la infusión (RRP).
En pacientes con GPA o PAM antes de la primera infusión de ARASAMILA®, se recomienda administrar metilprednisolona por vía intravenosa de 1 a 3 días, a una dosis de 1,000 mg al día (la última dosis de metilprednisolona se puede administrar el mismo día que la primera infusión de ARASAMILA®). Esto se debe continuar con prednisona por vía oral a una dosis de 1 mg/kg/día (sin exceder los 80 mg/día, y reducir la dosis tan rápido como sea posible, basándose en la necesidad clínica) durante y después del tratamiento con ARASAMILA®.
Se recomienda la profilaxis de la neumonía por Pneumocystis jirovecii (PJP) para pacientes adultos con GPA/PAM durante y después del tratamiento, según corresponda de acuerdo con las guías de práctica clínica locales.
Dosis:
Es importante comprobar las etiquetas de los medicamentos para asegurarse de que se está administrando la formulación adecuada al paciente, según lo prescrito.
Linfoma no Hodgkin:
Linfoma no Hodgkin folicular:
Terapia combinada: De acuerdo con la información públicamente disponible reportada por el medicamento innovador, para el tratamiento de inducción en pacientes con linfoma folicular en recidiva o refractario o que no hayan sido previamente tratados, la dosis recomendada de ARASAMILA® en combinación con quimioterapia es de 375 mg/m2 de superficie corporal por ciclo, hasta 8 ciclos.
ARASAMILA® debe ser administrado el día 1 de cada ciclo de quimioterapia, después de la administración intravenosa del componente glucocorticoide de la quimioterapia, si procede.
Terapia de mantenimiento:
• Linfoma folicular previamente no tratado.
De acuerdo con la información públicamente disponible reportada por el medicamento innovador, la dosis recomendada de ARASAMILA®, cuando se utiliza para el tratamiento de mantenimiento en pacientes con linfoma folicular no previamente tratados que han respondido a la terapia de inducción es de 375 mg/m2 de superficie corporal una vez cada 2 meses (empezando dos meses después de la última dosis de la terapia de inducción) hasta progresión de la enfermedad o hasta un periodo máximo de dos años (12 infusiones en total).
• Linfoma folicular en recaída o refractario.
De acuerdo con la información públicamente disponible reportada por el medicamento innovador, la dosis recomendada de ARASAMILA® cuando se utiliza para el tratamiento de mantenimiento en pacientes con linfoma folicular que están en recaída o son refractarios, que han respondido a la terapia de inducción, es de 375 mg/m2 de superficie corporal una vez cada 3 meses (empezando 3 meses después de la última dosis de la terapia de inducción) hasta progresión de la enfermedad o hasta un periodo máximo de dos años (8 infusiones en total). Monoterapia:
• Linfoma folicular en recaída o refractario.
De acuerdo con la información públicamente disponible reportada por el medicamento innovador, la dosis recomendada de ARASAMILA® en monoterapia usado como tratamiento de inducción en pacientes adultos con linfoma folicular estadio III-IV que sean quimiorresistentes o estén en su segunda o subsiguientes recidivas tras quimioterapia es de 375 mg/m2 de superficie corporal administrada en forma de infusión intravenosa una vez por semana durante cuatro semanas.
La dosis recomendada para repetir el tratamiento con ARASAMILA® en monoterapia en pacientes con linfoma no Hodgkin folicular en recidiva o refractario que ya habían respondido a un tratamiento previo con Rituximab en monoterapia es de 375 mg/m2 de superficie corporal administrada en forma de infusión intravenosa una vez por semana durante cuatro semanas.
Linfoma no Hodgkin difuso de células B grandes en adultos:
Debe usarse en combinación con quimioterapia CHOP. La dosis recomendada es de 375 mg/m2 de superficie corporal, administrada el día 1 de cada ciclo de quimioterapia durante 8 ciclos después de la infusión intravenosa del componente glucocorticoide de CHOP. No se ha establecido la seguridad y eficacia de rituximab en combinación con otras quimioterapias en el LNH difuso de células B grandes.
Ajustes de dosis durante el tratamiento:
No se recomiendan reducciones de dosis de rituximab. Cuando rituximab se administre en combinación con quimioterapia, se deben aplicar las reducciones de dosis estándar para los medicamentos quimioterapéuticos.
Leucemia linfocítica crónica:
La dosis recomendada de rituximab en combinación con quimioterapia para pacientes sin tratamiento previo y recidivantes/refractarios es de 375 mg/m2 de superficie corporal administrada el día 0 del primer ciclo de tratamiento seguida de 500 mg/m2 de superficie corporal administrada el día 1 de cada ciclo subsiguiente durante 6 ciclos en total. La quimioterapia se debe administrar después de la perfusión de rituximab.
Granulomatosis con poliangeítis (GPA) y poliangeítis microscópica (PAM):
Los pacientes tratados con rituximab deben recibir la tarjeta de alerta para el paciente con cada infusión.
Inducción de la remisión en adultos:
De acuerdo con la información públicamente disponible del medicamento innovador, la dosis recomendada de ARASAMILA® para el tratamiento para la inducción de la remisión de GPA y PAM es de 375 mg/m2 de superficie corporal, administrada en forma de infusión intravenosa una vez por semana durante 4 semanas (cuatro infusiones en total).
Se recomienda profilaxis para la neumonía por Pneumocystis jirovecii en pacientes con granulomatosis con poliangeítis o con poliangeítis microscópica durante y tras el tratamiento con ARASAMILA®, según sea apropiado.
Tratamiento de mantenimiento en adultos:
Después de la inducción de la remisión con rituximab, el tratamiento de mantenimiento en pacientes adultos con GPA y PAM no debe iniciarse antes de las 16 semanas posteriores a la última perfusión de rituximab.
Después de la inducción de la remisión con otros inmunosupresores estándar de atención, se debe iniciar el tratamiento de mantenimiento con rituximab durante el período de 4 semanas que sigue a la remisión de la enfermedad.
ARASAMILA® se debe administrar en dos infusiones intravenosas de 500 mg separadas por dos semanas, seguidas de una infusión intravenosa de 500 mg cada 6 meses a partir de entonces. Los pacientes deben recibir ARASAMILA® durante al menos 24 meses después de lograr la remisión (ausencia de signos y síntomas clínicos). Para los pacientes que pueden tener un mayor riesgo de recaída, los médicos deben considerar una duración más prolongada de la terapia de mantenimiento con rituximab, hasta 5 años.
Poblaciones especiales:
Población pediátrica: No se ha establecido todavía la seguridad y eficacia de Rituximab en niños menores de 18 años. No se dispone de datos.
Pacientes de edad avanzada: No se requiere ajustar la dosis en los pacientes de edad avanzada (> 65 años). Forma de administración: De acuerdo con la información públicamente disponible reportada por el medicamento innovador, ARASAMILA® se administra por vía intravenosa. La solución preparada de ARASAMILA® se debe administrar como infusión intravenosa empleando una vía específica. Las soluciones preparadas no se deben administrar en infusión rápida o en bolo intravenoso.
De acuerdo con la información públicamente disponible, para la preparación de ARASAMILA® se deberá hacer lo siguiente:
• Lavado cuidadoso de manos antes de la colocación de guantes y bata.
• Se deberá preparar en condiciones estériles.
• Es preferible que la preparación se lleve a cabo por paciente.
• Llevar a cabo la desinfección alcohol del tapón del medicamento, dejándolo evaporar.
• Introducir la aguja con ángulo de 45° con bisel hacia arriba.
• Evitar la sobrepresión en el interior del frasco ámpula, manteniéndola siempre negativa.
• Se debe diluir en solución salina al 0.9% o en solución de glucosa al 5% con un volumen necesario para generar una concentración máxima de 1 mg/ml y debe ser administrada mediante infusión intravenosa a través de un filtro de 0.22 micrones. La solución debe ser preparada para administración ambulatoria utilizando vía venosa periférica o central.
De acuerdo con la información públicamente disponible, los pacientes deben ser estrechamente monitorizados para detectar el inicio de un síndrome de liberación de citocinas (ver sección Precauciones generales). Se debe interrumpir inmediatamente la infusión en aquellos pacientes que muestren evidencia de reacciones graves, especialmente disnea grave, broncoespasmo o hipoxia. En los pacientes con linfoma no Hodgkin se debe evaluar posteriormente la evidencia de síndrome de lisis tumoral incluyendo pruebas de laboratorio adecuadas y la evidencia de infiltración pulmonar por radiología torácica. En ningún paciente se debe reiniciar la infusión hasta la remisión completa de todos los síntomas y la normalización de los valores de laboratorio y de los resultados de la radiología torácica. A partir de ese momento, la infusión se puede reiniciar, inicialmente, como máximo a la mitad de la velocidad de la infusión previa. Si se presentasen por segunda vez las mismas reacciones adversas graves, se debe considerar seriamente, y analizar por caso, la decisión de interrumpir el tratamiento.
Las reacciones relacionadas con la infusión (RRI) de grado leve o moderado (ver sección Reacciones secundarias y adversas) se resuelven generalmente reduciendo la velocidad de infusión. La velocidad de infusión se puede incrementar cuando mejoren los síntomas.
Primera infusión: La velocidad inicial recomendada de la infusión es de 50 mg/h, y después de los primeros 30 minutos se puede aumentar, en incrementos de 50 mg/h cada 30 minutos, hasta un máximo de 400 mg/h.
Infusiones posteriores: Las infusiones posteriores de ARASAMILA® se pueden comenzar con una velocidad de 100 mg/h, y aumentar en incrementos de 100 mg/h cada 30 minutos, hasta un máximo de 400 mg/h.
Pacientes adultos: sólo linfoma no Hodgkin (LNH) y leucemia linfocítica crónica (LCC):
Si los pacientes no experimentaron una reacción adversa a la infusión de grado 3 o 4 durante el primer ciclo, se puede administrar una infusión de 90 minutos durante el segundo ciclo con un régimen de quimioterapia que incluya glucocorticoides. La infusión se debe iniciar a una velocidad del 20% del total de la dosis administrado en los primeros 30 minutos y el 80% restante de la dosis total en los 60 minutos siguientes. Si se tolera la infusión de 90 minutos en el segundo ciclo, se puede utilizar la misma velocidad durante la administración del régimen de tratamiento restante (hasta los ciclos sexto u octavo).
En pacientes con enfermedades cardiovasculares clínicamente significativas, incluyendo arritmias, o reacciones graves a la infusión previa a cualquier terapia biológica anterior o a rituximab, no se debe administrar la infusión más rápida.
MANIFESTACIONES Y MANEJO DE LA SOBREDOSIFICACIÓN O INGESTA ACCIDENTAL: De acuerdo con la información públicamente disponible, existe una experiencia limitada, disponible en ensayos clínicos en humanos, con dosis mayores a la aprobada para la formulación de Rituximab intravenoso. La dosis intravenosa más alta de Rituximab evaluada hasta la fecha en humanos es 5,000 mg (2,250 mg/m2), probada en un estudio de escalado de dosis en leucemia linfocítica crónica. No se identificaron señales adicionales de seguridad.
En los pacientes que experimenten sobredosis se debe interrumpir inmediatamente la infusión y se deben monitorizar estrechamente.
Tras la comercialización, se notificaron cinco casos de sobredosis de Rituximab. En tres de los casos no se notificaron reacciones adversas. En los otros dos que se notificaron efectos adversos fueron síntomas gripales, con una dosis de 1.8 g de Rituximab e insuficiencia respiratoria mortal, con una dosis de 2 g de Rituximab.
PRESENTACIONES:
Caja con 1 frasco ámpula con 10 mL (100 mg/10 mL).
Caja con 2 frascos ámpula con 10 mL (100 mg/10 mL).
Caja con 1 frasco ámpula con 50 mL (500 mg/50 mL)
Caja con 2 frascos ámpula con 50 mL (500 mg/50 mL).
Todas las presentaciones con instructivo anexo.
RECOMENDACIONES SOBRE ALMACENAMIENTO: Consérvese en refrigeración entre 2 °C y 8 °C. No se congele.
Tras dilución aséptica en una solución de cloruro de sodio al 0.9%, ARASAMILA® se mantiene estable durante 30 días entre 2 °C y 8 °C, y posteriormente durante 24 horas a no más de 25 °C. Una vez transcurrido este periodo, el producto deberá desecharse.
Tras dilución aséptica en una solución de glucosa al 5% durante 24 horas entre 2 °C y 8 °C, y posteriormente durante 24 horas a no más de 25 °C. Una vez transcurrido este periodo, el producto deberá desecharse.
Desde un punto de vista microbiológico, la solución para perfusión preparada debe usarse inmediatamente.
Las condiciones de preparación antes del uso y manipulación son responsabilidad del usuario. A menos que la dilución se haya realizado en condiciones asépticas controladas y validadas, los tiempos de almacenamiento en uso normalmente no excederían las 24 horas a 2 ºC y 8 ºC.
Consérvese la caja bien cerrada. Protéjase de la luz.
Consérvese en su envase original, una vez fuera de refrigeración a no más de 30 ºC durante 7 días.
LEYENDAS DE PROTECCIÓN:
Literatura exclusiva para el médico. Este medicamento deberá ser prescrito y administrado únicamente por médicos especialistas en Hematología, Oncología o Reumatología, con experiencia en quimioterapia antineoplásica y/o anticuerpos monoclonales. No se administre si la solución no es transparente, si contiene partículas en suspensión o sedimentos. Si no se administra todo el producto, deséchese el sobrante. No se administre si el cierre ha sido violado. No se deje al alcance de los niños. Su venta requiere receta médica. No se use durante el embarazo ni lactancia. No se use en menores de 18 años. Este medicamento puede producir mareo y afectar el estado de alerta, por lo que no deberá conducir vehículos automotores ni maquinaria pesada durante su uso.
Reporte las sospechas de reacción adversa al correo: farmacovigilancia@cofepris.gob.mx
Titular del registro:
Sandoz GmbH
Biochemiestraße 10, 6250 Kundl
Austria
Representante Legal:
SANDOZ, S.A. de C.V.
La Candelaria No. 186,
Col. Atlántida, C.P. 04370, Coyoacán,
Ciudad de México, México.
Reg. Núm. 015M2020 SSA IV
®Marca Registrada