
BERODUAL
FENOTEROL, IPRATROPIO
Suspensión
1 Frasco(s), 10 mL, 200 Dosis
FORMA FARMACÉUTICA Y FORMULACIÓN:
Frasco presurizado con válvula dosificadora
Cada g contiene:
Bromuro de Ipratropio 0.394 mg
Fenoterol 0.938 mg
Vehículo cbp 1 g
10 ml = 200 dosis.
Cada dosis proporciona:
Bromuro de Ipratropio 21 μg
Fenoterol 50 μg
INDICACIONES TERAPÉUTICAS: Broncodilatador útil para la prevención y tratamiento de los síntomas de enfermedades que cursen con obstrucción crónica de la vía aérea con broncoespasmo reversible como el asma bronquial y especialmente, la bronquitis crónica con o sin enfisema pulmonar. Debe considerarse un tratamiento concomitante anti-inflamatorio para pacientes con asma bronquial y en aquellos pacientes con enfermedad obstructiva crónica que responde a la administración de esteroides.
FARMACOCINÉTICA Y FARMACODINAMIA: El efecto terapéutico de BERODUAL® es producido por un efecto tópico en la vía aérea. Investigaciones farmacocinéticas muestran que la formulación HFA y la formulación convencional CFC pueden ser consideradas como equivalentes.
Tras ser administrado mediante inhalación, se deposita en el tracto respiratorio en un 16% de la dosis, la porción remanente es deglutida.
Los ingredientes activos (bromuro de ipratropio y bromhidrato de fenoterol) son absorbidos rápidamente por el tracto respiratorio, minutos después de la inhalación se obtiene el pico en la concentración plasmática.
No existe evidencia de que la farmacocinética de ambos ingredientes en combinación difiera de la dada por las dos sustancias por separado.
Bromhidrato de fenoterol: La porción ingerida se metaboliza principalmente a conjugados de sulfato. La biodisponibilidad absoluta seguida de la administración oral es baja (aproximadamente de 1.5%).
Después de la administración intravenosa se observaron tres fases, siendo así que la vida media terminal fue de aproximadamente 3 horas. El fenoterol así como sus conjugados son excretados rápidamente a través de la vía renal (depuración renal 267 mL/min). Alrededor del 40% del principio activo está unido a las proteínas plasmáticas. En su estado no metabolizado, el bromhidrato de fenoterol puede lentamente atravesar la placenta, además de incorporarse a la leche materna.
El bromuro de ipratropio tras ser administrado mediante inhalación tiene una biodisponibilidad baja (aproximadamente 2%). Seguido de su administración intravenosa existe una rápida declinación bifásica plasmática.
Su vida media final fue de 1.6 horas con una eliminación total de su ingrediente activo de 23 L/min. Aproximadamente el 40% de la eliminación es por vía renal (0.9 L/min) y el 60% restante no es renal (metabolismo hepático). Los principales metabolitos encontrados en la orina tienen una unión deficiente a los receptores muscarínicos. 46% de ingrediente activo es excretado por vía renal después de la administración intravenosa, 4.4%, 1.6% después de la inhalación es excretada sin cambios a través de la orina. Existe una unión mínima a proteínas plasmáticas (menor al 20%). El ion de ipratropio no cruza la barrera hematoencefálica, se desconoce si cruza la barrera placentaria.
Los estudios clínicos con duración de tratamiento mayor de 3 meses involucran pacientes adultos asmáticos y con EPOC y niños asmáticos en los que la formulación HFA y la formulación CFC han sido comparadas, las dos formulaciones son terapéuticamente equivalentes.
BERODUAL® contiene dos ingredientes activos con efecto broncodilatador, el bromuro de ipratropio que presenta un efecto anticolinérgico y el bromhidrato de fenoterol un agente β-adrenérgico.
El bromuro de ipratropio es un compuesto cuaternario de amonio con propiedades anticolinérgicas (parasimpaticolítico). En estudios preclínicos, inhibió el reflejo vagal por la acción antagonista de la acetilcolina, el agente transmisor liberado por el nervio vago. Los anticolinérgicos previenen del incremento de la concentración intracelular del monofosfato cíclico de guanosina (GMPc) causado por la interacción de la acetilcolina con el receptor muscarínico del músculo liso bronquial.
La broncodilatación seguida de la inhalación del bromuro de ipratropio es el inicio local, con efecto sitio-específico y no sistémico.
En estudios controlados hasta de 90 días, en pacientes con broncoespasmo asociado con la enfermedad pulmonar obstructiva crónica (bronquitis crónica y enfisema) se observó una mejoría significativa en la función pulmonar (FEV; y FEF25-75% con incremento del 15% o mayor) ocurrió dentro de los primeros 15 minutos, alcanzando el pico máximo en 1-2 horas, y persistiendo en la mayoría de los pacientes hasta 6 horas después de su administración.
En estudios controlados hasta 90 días, en pacientes con broncoespasmo asociado con asma se observó una mejoría significativa en la función pulmonar (FEV1) con un incremento del 15% o más, lo cual ocurrió en el 40% de los pacientes.
Evidencia preclínica y clínica sugiere que no hay efecto dañino del bromuro de ipratropio en la mucosa de la vía aérea, depuración mucociliar e intercambio gaseoso.
El bromhidrato de fenoterol es un agente simpaticomimético directo, en el rango de dosis terapéuticas es estimulante selectivo de los β1-receptores. La estimulación de los β1-receptores se da en rangos de administración de dosis mayores. La ocupación de los β2-receptores activa la adenilatociclasa por medio de la estimulación de la proteína Gs. El incremento del AMPc activa a la proteína cinasa A la cual fosforila proteínas blanco de las células del músculo liso. Esto a su vez da como resultado la fosforilación de cadenas ligeras de miosina en la cinasa, inhibición del hidrólisis del fosfoinositol y la apertura de canales de calcio de alta conductancia a su vez activados por potasio.
El fenoterol relaja los bronquios y el músculo liso vascular y protege contra el estímulo broncoconstrictor como los causados por la histamina, metacolina, aire frío y alergenos (respuesta temprana). Después de su administración se inhibe a los mediadores broncoconstrictores y pro-inflamatorios de los mastocitos. Además, se ha demostrado que a dosis altas de fenoterol se da un incremento en la depuración mucociliar.
Posterior a la administración oral, es donde frecuentemente se alcanzan las concentraciones más altas en plasma y aún más después de la administración intravenosa que inhibe la motilidad uterina. Incluso a dosis más altas, se observan efectos metabólicos como lipólisis, glucogenólisis, hiperglucemia e hipokalemia, esta última a causa de un incremento en la recaptura del potasio dada primeramente por el músculo esquelético. Los efectos beta-adrenérgicos en el corazón tales como un incremento en el ritmo cardiaco y la propiedad para contraerse se deben a los efectos vasculares del fenoterol, en cambio, la estimulación de los β-receptores, se da a dosis supraterapéuticas y ocasiona estimulación de los β2-receptores. Se han reportado prolongaciones del segmento QTc, como es el caso de otros agentes β-adrenérgicos, sin embargo, para las soluciones presurizadas para inhalar de fenoterol éstas fueron discretas y se observaron a dosis más altas de las recomendadas. El significado clínico no se ha establecido. El temblor es un efecto frecuentemente observado de los β-agonistas. A diferencia de los efectos en el músculo liso bronquial, los efectos sistémicos de los β-agonistas están sujetos al desarrollo de la tolerancia.
En estudios clínicos, el fenoterol demostró una alta eficacia en manifestaciones que se caracterizan por broncoespasmo. Previene la broncoconstricción seguida de la exposición a varios estímulos como son el ejercicio, la exposición al aire frío y la respuesta temprana resultado de la exposición a agentes alergenos.
El uso concurrente de estos dos ingredientes activos dilata los bronquios debido a que afecta diferentes sitios de acción farmacológicos. Los ingredientes activos se complementan mutuamente en la acción espasmolítica que ejercen sobre el músculo liso bronquial y permiten un uso terapéutico amplio en el campo de los desórdenes broncopulmonares asociados con la constricción del tracto respiratorio. La acción complementaria es tal, que sólo se requiere una muy baja proporción del componente β-adrenérgico para obtener el efecto deseado, facilitando la adecuación de dosis individuales para cada paciente con un mínimo de reacciones adversas.
En pacientes con asma y con EPOC, BERODUAL® ha demostrado ser tan eficaz como una doble dosis de fenoterol sin ipratropio, pero fue mejor tolerado en estudios de dosis acumulativa.
En estudios realizados en pacientes con asma y EPOC se demostró mayor eficacia comparado con sus componentes ipratropio o fenoterol.
En casos que cursen con broncoconstricción aguda, BERODUAL® es efectivo de tal manera que resulta una elección adecuada para el tratamiento de crisis agudas de asma.
CONTRAINDICACIONES: BERODUAL® está contraindicado en pacientes con hipersensibilidad conocida al fenoterol o a sustancias similares a la atropina o a cualquier otro componente de la fórmula.
BERODUAL® está contraindicado en pacientes con cardiomiopatía hipertrófica obstructiva y taquiarritmia.
RESTRICCIONES DE USO DURANTE EL EMBARAZO Y LA LACTANCIA: Datos preclínicos combinados con la experiencia disponible en humanos, han demostrado que no hay evidencia de efectos indeseables en el embarazo durante la administración de fenoterol o ipratropio. Sin embargo, deberán observarse las precauciones normales, en cuanto al uso de los medicamentos durante el embarazo, especialmente durante el primer trimestre.
Deberá tomarse en cuenta el efecto del fenoterol en la inhibición de las contracciones uterinas.
Estudios no clínicos demuestran que el bromuro de fenoterol es excretado por la leche materna. Se desconoce si el ipratropio se excreta por la leche materna. Siendo poco probable que el ipratropio llegue en cantidades considerables al producto, especialmente cuando se administra en aerosol. Sin embargo, debido a que muchos medicamentos son excretados en la leche materna, se debe tener especial precaución al administrar BERODUAL® a madres que están lactando.
REACCIONES SECUNDARIAS Y ADVERSAS: BERODUAL® puede ocasionar nerviosismo, xerostomía, cefalea, mareo y temblor fino de músculo esquelético. Taquicardia y palpitaciones. Alteraciones en la motilidad gastrointestinal (vómito, constipación y diarrea) y retención urinaria que se ha reportado como reversible.
Pueden ocurrir efectos secundarios a nivel ocular (incluyendo trastornos en la acomodación y glaucoma). Se han reportado reacciones en la piel o de tipo alérgico del tipo exantema, angioedema lingual, labial y facial, urticaria, laringoespasmo y reacciones anafilácticas.
Durante la terapia con β2-agonistas puede presentarse hipokalemia potencialmente grave.
Así como con otros productos que contienen β-agonistas se pueden presentar náuseas, vómito, diaforesis, astenia, mialgias y calambres musculares.
Se ha observado una disminución en la presión diastólica e incremento en la presión sistólica. Pueden ocurrir arritmias (particularmente después de dosis altas), fibrilación auricular, isquemia miocárdica y traquicardia supraventricular.
En casos individuales donde se da tratamiento de inhaloterapia con productos que contienen β-agonistas, se han reportado alteraciones psicológicas.
Con el uso de la inhaloterapia se han reportado tos, irritación local (faringitis e irritación de la garganta) y broncoespasmo inducido por inhalación.
PRECAUCIONES EN RELACIÓN CON EFECTOS DE CARCINOGÉNESIS, MUTAGÉNESIS, TERATOGÉNESIS Y SOBRE LA FERTILIDAD: No han sido desarrollados estudios de genotoxicidad y carcinogenicidad. Sin embargo, en estudios in vivo e in vitro revelaron que ni el fenoterol ni el ipratropio tienen potencial mutagénico.
Asimismo, los estudios de carcinogenicidad llevados a cabo durante dos años con la administración por vía inhalada de fenoterol y administración oral de ipratropio en ratas y ratones, revelaron que no existen efectos patológicos oncogénicos.
INTERACCIONES MEDICAMENTOSAS Y DE OTRO GÉNERO: Otros β-adrenérgicos, anticolinérgicos y derivados de la xantina (como teofilina) pueden incrementar el efecto broncodilatador. La administración conjunta con otros betamiméticos, anticolinérgicos y derivados de la xantina (p. ej. teofilina) puede incrementar las reacciones adversas.
Durante la administración concurrente de β-bloqueadores, puede ocurrir una potencial y severa reducción de la broncodilatación.
La hipokalemia inducida por los β2-agonistas puede verse incrementada con el tratamiento concomitante con derivados de la xantina, corticosteroides y diuréticos. Esto debe tenerse en cuenta particularmente en pacientes con obstrucción grave de la vía aérea.
La hipokalemia puede dar lugar a un incremento en la susceptibilidad a arritmias en pacientes que se encuentran recibiendo dioxina. Adicionalmente, la hipoxia puede agravar los efectos de la hipokalemia en el ritmo cardiaco. Se recomienda la vigilancia de los niveles de potasio sérico en dichas situaciones.
Los fármacos que contienen β2-agonistas deben ser administrados con precaución en pacientes tratados con inhibidores de la MAO o antidepresivos tricíclicos, debido a que puede aumentar la acción de los β-agonistas adrenérgicos.
La susceptibilidad a los efectos cardiovasculares de los β-agonistas, puede verse incrementada durante la inhalación de anestésicos de hidrocarburo halogenados tales como el halotano, tricloroetileno y enflurano.
ALTERACIONES EN LOS RESULTADOS DE PRUEBAS DE LABORATORIO: Tras la administración de BERODUAL® puede producirse una reducción dosis-dependiente transitoria del potasio en suero.
PRECAUCIONES GENERALES: Cuando se usa la nueva formulación de BERODUAL® por primera vez, algunos pacientes pueden observar que el sabor es ligeramente diferente de la formulación que contiene CFC.
Se debe advertir a los pacientes de esto cuando cambien de una a otra formulación. También deben ser informados que ambas formulaciones son intercambiables para propósitos prácticos y que la diferencia en el sabor no tiene consecuencias en términos de la seguridad o la eficacia de la nueva formulación.
En caso de disnea aguda o empeoramiento del cuadro deberá consultarse inmediatamente al médico.
Uso prolongado:
– En pacientes con asma bronquial y con EPOC leve se debe administrar a libre demanda en lugar de un uso en forma regular.
– Debe considerarse agregar o aumentar el tratamiento anti-inflamatorio para el control de la inflamación de las vías respiratorias y para prevenir el deterioro del control de la enfermedad en pacientes con asma bronquial y en pacientes con EPOC que responden al uso de esteroides.
El incremento en el uso de productos β2-adrenérgicos tales como BERODUAL® en una base regular como control de síntomas de obstrucción bronquial puede sugerir un descontrol clínico. Si la obstrucción bronquial empeora, el simple incremento en el uso de β2-adrenérgicos tales como BERODUAL® más allá de la dosis recomendada por períodos extensos de tiempo no es apropiado e incluso puede ser peligroso.
En esta situación, el plan de tratamiento y, en particular, el adecuado tratamiento anti-inflamatorio con corticoides inhalados, deberá revisarse con la finalidad de prevenir deterioro potencialmente amenazante de la vida en el control de la enfermedad.
El uso de otros broncodilatadores simpaticomiméticos en conjunto con BERODUAL® únicamente deberá realizarse bajo supervisión médica.
Bajo las siguientes condiciones, debe utilizarse BERODUAL® sólo tras haber evaluado los riesgos y beneficios, especialmente cuando se están utilizando mayores dosis de las recomendadas. Diabetes mellitus descontrolada, infarto miocárdico reciente, alteraciones cardiacas o vasculares graves, hipertiroidismo o feocromocitoma.
Pueden detectarse efectos cardiovasculares con los medicamentos simpaticomiméticos, incluyendo BERODUAL® /Duovent®. Existe evidencia de la información post-comercialización y de la literatura publicada, de raros episodios de isquemia miocárdica asociada con beta-agonistas. Debe alertarse a los pacientes con cardiopatía subyacente grave (p.ej. Cardiopatía isquémica, arritmia o insuficiencia cardiaca grave) quienes estén recibiendo BERODUAL® /Duovent® para que acudan a buscar consejo médico si experimentan dolor torácico u otros síntomas de empeoramiento de la cardiopatía. Debe prestarse atención a la evaluación de síntomas tales como disnea y dolor torácico tanto si tienen origen respiratorio o cardiaco.
Puede presentarse hipokalemia como resultados del uso de β2-adrenérgicos.
BERODUAL® deberá usarse con precaución en pacientes con hiperplasia prostática e inflamación del cuello vesical. O bien, predisposición al glaucoma de ángulo estrecho.
Se han presentado casos aislados de complicaciones oculares (p. ej. Midriasis, hipertensión intraocular, glaucoma de ángulo cerrado, dolor ocular) cuando fue rociado bromuro de ipratropio aerolizado o en combinación con un agonista β2-adrenérgico en los ojos. Se debe de instruir a los pacientes acerca del uso correcto del BERODUAL® en aerosol.
El dolor ocular o el malestar en los ojos, visión borrosa, halos visuales o imágenes coloreadas en asociación con ojos rojos, con congestión conjuntival y edema corneal pueden ser signos de glaucoma de ángulo estrecho. En caso de que alguna combinación de estos síntomas se desarrolle, debe iniciarse tratamiento con gotas oftálmicas que produzcan miosis y se deberá acudir a revisión oftalmológica inmediatamente.
Los pacientes con fibrosis quística pueden ser más propensos a la motilidad gastrointestinal.
Reacciones de hipersensibilidad inmediatas pueden presentarse después de la administración de BERODUAL® demostradas por casos raros de urticaria, angioedema, exantema, broncoespasmo, edema orofaríngeo y anafilaxia.
DOSIS Y VÍA DE ADMINISTRACIÓN: La dosis debe ser adaptada al requerimiento individual. A menos de que se prescriba de otra manera, las dosis recomendadas para adultos y niños mayores de 6 años son las siguientes:
Episodios agudos de asma:
• Dos disparos son suficientes para aliviar con los síntomas en la mayoría de los casos. En casos más severos, si la respiración no ha mejorado notablemente después de 5 minutos, pueden administrarse dos disparos más.
• Si un episodio no ha sido aliviado después de 4 disparos, pueden requerirse disparos adicionales. En dichos casos, los pacientes deberán consultar con su médico y/o trasladarlos al hospital más cercano.
Tratamiento a largo plazo o intermitente: En niños mayores a 6 años y adultos, se recomiendan de 1 a 2 inhalaciones del aerosol tres veces al día (Máximo 8 disparos al día).
En los niños BERODUAL® solo debe adminisrarse por prescripción mediante dispositivo médico y siempre bajo la supervisión de un adulto.
Instrucciones de uso: Los pacientes deben ser instruidos en la correcta administración de los aerosoles como medio para garantizar el éxito del tratamiento.
Presione la válvula dos veces antes de usar el aparato por primera vez.
Debe seguir los siguientes pasos antes de cada uso:
1. Retire la tapa protectora.
2. Exhale profundamente.
3. Sostenga el aerosol como se muestra en la figura 1, posteriormente cierre los labios alrededor de la boquilla.
La flecha y el fondo del recipiente deben estar hacia arriba.
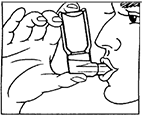
(Fig. 1)
4. Respire profundamente, presionando la base del contenedor firmemente al mismo tiempo, esto libera una dosis medida o disparo. Sostenga la respiración durante unos segundos, entonces retire la boquilla de la boca y exhale.
La misma acción debe repetirse para la segunda inhalación.
5. Coloque la tapa protectora después de su uso.
6. Si el aerosol no ha sido utilizado por más de tres días la válvula tiene que ser activada nuevamente.
El contenedor no es transparente. Por lo tanto no es posible ver si está vacío.
El aerosol proporciona 200 dosis (inhalaciones). Cuando éstas han sido utilizadas los aerosoles todavía parecen contener una pequeña cantidad de fluido. El aerosol debe; sin embargo, sustituirse porque no puede conseguir la cantidad adecuada de tratamiento.
La cantidad del aerosol para su tratamiento se puede comprobar de la siguiente manera:
Quitar el aerosol de la boquilla de plástico y poner el aerosol en un recipiente con agua. El contenido de los aerosoles puede ser estimado mediante la observación de su posición en el agua (figura 2).
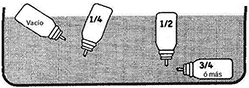
La boquilla siempre debe mantenerse limpia y puede lavarse con agua tibia. Si se emplea jabón o detergente, la boquilla debe enjuagarse con agua limpia.
Advertencia: La boquilla plástica se ha diseñado especialmente para usar con BERODUAL® para asegurar que usted siempre reciba la cantidad adecuada del medicamento. La boquilla nunca debe usarse con otro aerosol dosificador ni el aerosol dosificador BERODUAL® debe usarse con cualquier otra boquilla que no sea la proporcionada con el producto.
El contenedor está bajo presión y no debe abrirse a la fuerza o exponerse a temperaturas superiores a los 50°C.
PRESENTACIÓN: BERODUAL® Aerosol dosificador (10 mL = 200 dosis aerosol). Envase metálico con dispositivo bucal, para inhalación mediante dispositivo especial.
RECOMENDACIONES SOBRE ALMACENAMIENTO: Consérvese a temperatura ambiente a no más de 30°C.
LEYENDAS DE PROTECCIÓN:
Literatura exclusiva para médicos. No se deje al alcance de los niños. Su venta requiere receta médica. Léase instructivo anexo. Agítese bien antes de usarse. No se deje al alcance de los niños. No se use cerca del fuego o flama. No fume o encienda flama cuando se aplique. No exponga el envase a los rayos del sol o lugares excesivamente calientes, no perfore o los arroje al fuego. Evite el contacto con los ojos. El empleo de este medicamento durante el embarazo y la lactancia queda bajo la responsabilidad del médico. Durante el empleo dirigir la válvula hacia abajo.
PELIGRO INFLAMABLE.
Hecho en Alemania por:
Boehringer Ingelheim Pharma GmbH & Co. KG.
Binger Straβe 173,
55216 Ingelheim am Rhein, Alemania.
Distribuido por:
BOEHRINGER INGELHEIM PROMECO, S.A. de C.V.
Calle del Maíz No. 49, Col. Barrio Xaltocán,
C.P. 16090, Deleg, Xochimilco, D.F., México.
Reg. Núm. 023M86, SSA IV
®Marca Registrada