
HIGROTON BLOK
ATENOLOL, CLORTALIDONA
Tabletas
1 Caja, 100 Tabletas, 100/25 Miligramos
1 Caja, 100 Tabletas, 50/12.5 Miligramos
1 Caja, 28 Tabletas, 100/25 mg
1 Caja, 28 Tabletas, 50/12.5 mg
1 Caja, 30 Tabletas, 100/25 Miligramos
1 Caja, 30 Tabletas, 50/12.5 Miligramos
1 Caja, 50 Tabletas, 100/25 Miligramos
1 Caja, 50 Tabletas, 50/12.5 Miligramos
1 Caja, 28 Tabletas, 50 mg, 12.5 mg
1 Caja, 28 Tabletas, 100 mg, 25 mg
FORMA FARMACÉUTICA Y FORMULACIÓN:
Cada TABLETA contiene:
Atenolol 50 mg, 100 mg
Clortalidona 12.5 mg, 25 mg
Excipiente cbp 1 tableta
INDICACIONES TERAPÉUTICAS:
Hipertensión.
HIGROTON BLOK® está indicado en pacientes cuya presión arterial no pudo reducirse de manera suficiente con Atenolol o Clortalidona solo.
FARMACOCINÉTICA Y FARMACODINAMIA:
Farmacocinética:
Atenolol:
Después de la aplicación oral, Atenolol se resorbe en aprox. 50% del tracto gastrointestinal. Debido a que Atenolol no está sujeto a un metabolismo de primer paso, la disponibilidad sistémica es también de aprox. 50%. Los niveles máximos de plasma se alcanzan después de 2-4 horas. El enlace a la proteína plasmática es de aprox. 3%; el volumen de distribución relativo es de 0.7 l/kg.
Atenolol se metaboliza en un grado muy reducido. No se producen metabolitos activos con relevancia clínica.
Aproximadamente el 90% del Atenolol sistémicamente disponible se elimina a través de los riñones en el transcurso de 48 horas de forma inalterada. La vida media de eliminación de Atenolol es, con una función renal normal, de 6-10 horas. Con una insuficiencia renal terminal, la vida media de eliminación puede incrementar hasta 140 horas.
Clortalidona:
Clortalidona se absorbe relativamente despacio en el tracto gastrointestinal (t50 de absorción aprox. 2.6 h). La disponibilidad sistémica es de aprox. 64 ± 10% después de la ingestión oral. El enlace a la proteína plasmática es de 75%, el volumen de distribución es 4 l/kg.
Clortalidona es eliminada predominantemente a través de los riñones en forma de sustancia inalterada. La vida media de eliminación es de aprox. 50 horas.
Biodisponibilidad:
HIGROTON BLOK®:
Un estudio de biodisponibilidad comparativo realizado en 24 sujetos en 1992 mostró los siguientes resultados en comparación con la preparación de referencia:
Para Atenolol:
|
Preparación de prueba |
Preparación de referencia |
|
|
Cmax [ng/ml] concentración plasmática máxima |
563.3 ± 164.94 |
519.50 ± 193.30 |
|
tmax [h] tiempo de concentración plasmática máxima |
3.15 ± 0.98 |
3.02 ± 1.22 |
|
AUC(0-48 h) [ng/ml*h] área debajo de la curva de concentración-tiempo |
5512.24 ± 1137.40 |
4964.92 ± 1448.28 |
|
AUC(0-∞) [ng/ml*h] área debajo de la curva de concentración-tiempo |
6150.19 ± 1057.91 |
5477.43 ± 1408.34 |
Los valores se indican como medias aritméticas y rango de dispersión (desviación estándar).
Para Clortalidona
|
Preparación de prueba |
Preparación de referencia |
|
|---|---|---|
|
Cmax [ng/ml] concentración plasmática máxima |
1.85 ± 0.36 |
1.75 ± 0.37 |
|
tmax [h] tiempo de concentración plasmática máxima |
11.62 ± 3.26 |
10.17 ± 2.71 |
|
AUC(0-240 h) [μg/ml*h] área debajo de la curva de concentración-tiempo |
159.41 ± 33.56 |
152.11 ± 25.36 |
|
AUC(0-∞) [μg/ml*h] área debajo de la curva de concentración-tiempo |
169.00 ± 37.44 |
161.23 ± 28.63 |
Los valores se indican como medias aritméticas y rango de dispersión (desviación estándar).
La curva de la concentración plasmática media en comparación con la preparación de referencia en un diagrama de concentración contra tiempo:
Para Atenolol:
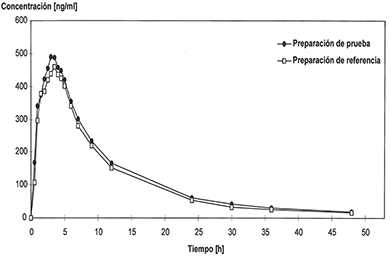
Para Clortalidona:
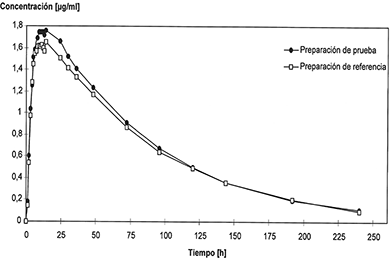
Farmacodinamia:
HIGROTON BLOK® es una preparación combinada que contiene Atenolol y Clortalidona como constituyentes eficaces.
Atenolol:
Atenolol es un bloqueador de receptores beta hidrófilo con relativa selectividad de beta1 (“cardioselectividad”), sin actividad simpaticomimética intrínseca (ISA) y sin efecto estabilizador de membrana.
La sustancia reduce, en función del nivel del tono simpático, la frecuencia y la fuerza contractiva del corazón, la velocidad de conducción AV y la actividad de renina en el plasma. Atenolol puede originar un aumento del tono de la musculatura lisa a través de la inhibición de receptores de beta2.
Clortalidona:
Clortalidona es un derivado de benzotiadiazina con eficacia de acción prolongada.
Las tiazidas actúan directamente en los riñones al aumentar el cloruro sódico y, por consiguiente, la excreción de fluidos relacionada. Su sitio objetivo principal clínicamente relevante es el túbulo distal. Allí, inhiben el co-transporte electroneutral de Na-Cl en la membrana celular luminar. Potasio y magnesio se excretan a un mayor grado, calcio en menor medida.
Debido a altas dosis de Clortalidona, el bicarbonato puede excretarse cada vez más como consecuencia de la inhibición de anhidrasa carbónica, de modo que se alcalice la orina.
La acidosis o alcalosis no influye de manera sustancial en el efecto salurético o diurético de Clortalidona.
Durante la terapia a largo plazo de Clortalidona, se reduce la excreción de calcio a través de los riñones, de modo que se pueda originar una hipercalcemia.
El equilibrio de sodio alterado, la reducción del volumen de fluido y plasma extracelular, una alteración de la resistencia vascular renal, así como una menor respuesta a norepinefrina y angiotensina II se consideran mecanismos del efecto antihipertensivo de Clortalidona.
Clortalidona no es eficaz en pacientes que sufren de insuficiencia renal crónica (aclaramiento de creatinina de menos de 30 ml/min y/o creatinina sérica de más de 1.8 mg/100 ml).
CONTRAINDICACIONES:
No debe administrarse en pacientes con las siguientes condiciones:
• Hipersensibilidad conocida al atenolol y clortalidona (o a productos farmacéuticos derivados de la sulfonamida) o cualquier otro componente de la fórmula.
• Bloqueo cardiaco de segundo o tercer grado.
• Síndrome del nodo enfermo.
• Bradicardia (pulso en reposo menor a 50 palpitaciones por minuto antes del inicio del tratamiento).
• Acidosis metabólica.
• Embarazo y lactancia.
• Insuficiencia cardiaca no controlada.
• Hipotensión.
• Trastornos arteriales periféricos severos.
• Choque cardiogénico.
• Insuficiencia renal severa (insuficiencia renal con oliguria o anuria; aclaramiento de creatinina de menos de 30 ml/min y/o creatinina sérica de más de 1.8 mg/100 ml).
• Feocromocitoma no tratado.
• Hipersensibilidad Bronquial, por ejemplo, en el asma.
• Disfunción hepática severa.
• Trastornos de electrólitos clínicamente relevantes (hipokalemia, hiponatremia, hipercalcemia).
• Gota.
• En niños, debido a la falta de experiencia.
La administración intravenosa de antagonistas del calcio de tipo verapamilo y diltiazem u otros antiarrítmicos (tales como disopiramida) está contraindicada en pacientes tratados con HIGROTON BLOK® (excepto en la medicina de cuidados intensivos).
RESTRICCIONES DE USO DURANTE EL EMBARAZO Y LA LACTANCIA:
Uso durante el embarazo y lactancia:
HIGROTON BLOK® no debe administrarse durante el embarazo, ni lactancia.
REACCIONES SECUNDARIAS Y ADVERSAS:
En estudios clínicos, las reacciones adversas posibles son usualmente atribuibles a las acciones farmacológicas de sus componentes.
Los siguientes efectos no deseados, enlistados por sistema corporal, se han reportado con las siguientes frecuencias:
Muy común (≥1/10), común (≥1/100 a <1/10), no común (≥1/1,000 a <1/100), poco común (≥1/10,000 a <1/1,000), muy poco común (<1/10,000), desconocido (no puede estimarse a partir de los datos disponibles).
Trastornos de la sangre y del sistema linfático:
Poco común: Púrpura, trombocitopenia, leucopenia (relacionada a clortalidona).
Trastornos psiquiátricos:
No común: Alteraciones del sueño del tipo observado con otros betabloqueadores.
Poco común: Cambios de humor, pesadillas, confusión, psicosis y alucinaciones.
Trastornos del sistema nervioso:
Poco común: Mareo, cefalea, parestesia.
Trastornos oculares:
Poco común: Ojos secos, trastornos visuales.
No conocidos: Derrame coroideo.
Trastornos cardiacos:
Común: Bradicardia.
Poco común: Deterioro de falla cardiaca, precipitación del bloqueo cardiaco.
Trastornos vasculares:
Común: Extremidades frías.
Poco común: Hipotensión ortostática que puede asociarse con síncope, la claudicación intermitente puede aumentar si ya está presente, en pacientes susceptibles al fenómeno de Raynaud.
Trastornos respiratorios, torácicos y del mediastino:
Poco común: Puede presentarse broncoespasmo en pacientes con asma bronquial o antecedentes de dolencias asmáticas.
Trastornos gastrointestinales:
Común: Trastornos gastrointestinales (incluyendo náusea relacionada a clortalidona).
Poco común: Sequedad de boca.
Desconocido: Constipación.
Trastornos hepatobiliares:
Poco común: Toxicidad hepática incluyendo colestasis intrahepática, pancreatitis (relacionada a clortalidona).
Trastornos de la piel y del tejido subcutáneo:
Poco común: Alopecia, reacción cutánea psoriasiforme, exacerbación de psoriasis, erupciones cutáneas.
Trastornos musculoesqueléticos y del tejido conjuntivo:
Desconocido: Síndrome parecido al lupus.
Trastornos del sistema reproductor y de la mama:
Poco común: Impotencia.
Muy poco común: Trastorno de la libido**
Trastornos generales y condiciones del sitio de administración:
Común: Fatiga.
Investigaciones:
Común (relacionado a clortalidona): Hiperuricemia, hiponatremia, hipopotasemia, tolerancia alterada a glucosa.
No común: Aumento en la concentración sérica de transaminasas.
Muy poco común: Se ha observado aumento de los anticuerpos antinucleares (ANA); sin embargo, la relevancia clínica de este fenómeno no ha sido dilucidada.
Se debe considerar la suspensión de atenolol/clortalidona si, de acuerdo con el juicio clínico, el bienestar del paciente se ve afectado negativamente por cualquiera de las reacciones anteriores.
PRECAUCIONES EN RELACIÓN CON EFECTOS DE CARCINOGÉNESIS, MUTAGÉNESIS, TERATOGÉNESIS Y SOBRE LA FERTILIDAD:
No existe información acerca de los efectos sobre la carcinogénesis, mutagénesis y teratogénesis.
Potencial mutagénico y tumorigénico:
Clortalidona in vitro induce mutaciones cromosomales en células de mamíferos. Experimentos in vivo en ratones no produjeron esta evidencia en la médula ósea y en hepatocitos. La importancia de los resultados in vitro positivos no se ha aclarado de forma suficiente. No existen estudios a largo plazo en animales acerca de un potencial tumorigénico de la Clortalidona.
Atenolol no se ha sometido a una prueba de mutagenicidad detallada. Hasta la fecha, las pruebas han producido resultados negativos. Estudios a largo plazo en ratas y ratones no revelaron ninguna evidencia de un potencial tumorigénico de Atenolol.
INTERACCIONES MEDICAMENTOSAS Y DE OTRO GÉNERO:
Debido a su componente betabloqueador (Atenolol):
El uso combinado de betabloqueadores y bloqueadores de canales de calcio con efectos inotrópicos negativos por ejemplo, verapamil, diltiazem, puede llevar a una exacerbación de estos efectos particularmente en pacientes con función ventricular afectada y/o propiedades atípicas de la conducción sinoatrial o sinoventricular.3 Esto puede resultar en hipotensión severa, bradicardia e insuficiencia cardiaca.
Los betabloqueadores y los bloqueadores de los canales de calcio no deben administrarse por vía intravenosa dentro de las 48 horas de la suspensión de cualquiera de ellos.
Los medicamentos antiarrítmicos clase I como disopiramida y amiodarona pueden potencializar el efecto en el tiempo de conducción atrial e inducir negativamente el efecto inotrópico.
Los glucósidos digitálicos, en asociación con beta bloqueadores, pueden aumentar el tiempo de conducción atrioventricular.
Los betabloqueadores pueden exacerbar la hipertensión de rebote que puede presentarse tras la suspensión de la clonidina. Si los dos principios activos se administran conjuntamente, el betabloqueador debe suspenderse varios días antes de suspender la clonidina. Si se reemplaza la clonidina por betabloqueantes, la introducción de los betabloqueadores se debe retrasar por varios días después de que la administración de clonidina se ha suspendido.
El uso concomitante de agentes simpaticomiméticos, por ejemplo adrenalina, puede contrarrestar el efecto de beta bloqueadores.
El uso concomitante de sustancias activas inhibidoras de la prostaglandina sintetasa, (por ejemplo, ibuprofeno, indometacina) puede disminuir los efectos hipotensores de los betabloqueantes.
Se debe tener precaución cuando se utilicen agentes anestésicos con atenolol/clortalidona (vea la sección Precauciones generales).
Debido a su componente tiazídico (Clortalidona):
El componente de la clortalidona puede reducir el aclaramiento renal de litio que conduce a un aumento de su concentración sérica. Por lo tanto, pueden ser necesarios ajustes de dosis de litio.
Debido a la combinación de fármacos:
La terapia concomitante con dihidropiridinas, por ejemplo, nifedipino, puede aumentar el riesgo de hipotensión e insuficiencia cardiaca; puede ocurrir en pacientes con insuficiencia cardiaca latente.
El uso concomitante de baclofeno puede aumentar el efecto antihipertensivo, por lo que se hace necesario realizar ajustes de dosis.
ALTERACIONES EN LOS RESULTADOS DE PRUEBAS DE LABORATORIO:
Durante la administración continua, a largo plazo de HIGROTON BLOK®, frecuentemente pueden ocurrir trastornos del equilibrio de fluidos y electrólitos, especialmente hipocalemia e hiponatremia, además, hipomagnesemia e hipocloremia, así como hipercalcemia.
Es posible que haya niveles elevados de transaminasa, en casos raros íctero colestásico (ictericia), valores elevados de amilasa y pancreatitis durante el tratamiento con HIGROTON BLOK®.
PRECAUCIONES GENERALES:
Debido a su componente betabloqueador:
• Aunque está contraindicado en la insuficiencia cardiaca no controlada (véase sección de Contraindicaciones), puede ser usado en pacientes cuyos signos de insuficiencia cardiaca hayan sido controlados. Se deberá tener precaución en pacientes con pobre reserva cardiaca.
• Pueden incrementarse el número y duración de los ataques de angina de pecho en pacientes con angina de Prinzmetal, debido a la falta de oposición del receptor alfa, que es el mediador de la vasoconstricción arterial coronaria. Atenolol es un bloqueador beta1 selectivo; y, por lo tanto, el uso combinado de atenolol/clortalidona puede ser considerado, aunque se debe tener precaución extrema.
• Aunque contraindicado en trastornos arteriales periféricos severos (ver sección Contraindicaciones) atenolol/clortalidona también puede agravar trastornos circulatorios arteriales periféricos menos graves.
• Debido a su efecto negativo sobre el tiempo de conducción, se debe tener precaución si se administra a pacientes con bloqueo cardiaco de primer grado.
• Puede modificar los signos clínicos de hipoglucemia como taquicardia, palpitaciones y sudoración.
• Puede enmascarar los signos cardiovasculares de la tirotoxicosis.
• Los betabloqueadores, gracias a su acción farmacológica, reducen el ritmo y frecuencia cardiacas, presión arterial y contractilidad. En casos raros en que un paciente con este tratamiento desarrolle síntomas que pueden ser atribuibles a una frecuencia cardiaca baja, la dosis puede ser reducida.
• No se debe interrumpir el tratamiento de manera abrupta en pacientes con cardiopatía isquémica.
• Puede provocar una reacción más severa a diversos alérgenos, cuando se administra en pacientes con antecedentes de reacción anafiláctica a dichos alérgenos. Estos pacientes pueden no responder a las dosis usuales de adrenalina utilizadas para tratar las reacciones alérgicas.
• En general, los pacientes con enfermedad broncoespástica no deben recibir beta bloqueadores debido al aumento en la resistencia de las vías aéreas. Atenolol es un bloqueador beta1 selectivo; sin embargo, esta selectividad no es absoluta. Por lo tanto, debe utilizarse la dosis más baja posible de atenolol / clortalidona y se debe tener precaución extrema. Si sucede un aumento en la resistencia de las vías aéreas, se debe descontinuar atenolol/clortalidona y se debe administrar tratamiento con un broncodilatador (por ejemplo, salbutamol), en caso de ser necesario.
• Los efectos sistémicos de los betabloqueadores orales pueden potenciarse cuando se usa concomitantemente con beta bloqueadores oftálmicos, debido a que estos pueden tener acceso a la circulación sistémica a través del sistema lagrimal, la mucosa nasal y los vasos conjuntivales.
• En pacientes que padecen feocromocitoma, pueden utilizar atenolol/ clortalidona sólo si se ha establecido un bloqueo de los receptores alfa. Se debe monitorear de cerca la presión sanguínea.
• Se debe tener precaución cuando se utilicen agentes anestésicos en forma concomitante con atenolol/clortalidona. Se debe informar al anestesiólogo y se recomienda que el anestésico de elección sea un agente con actividad inotrópica tan pequeña como sea posible. El uso de betabloqueadores con anestésicos puede provocar una atenuación de taquicardia refleja y aumentar el riesgo de hipotensión. Es mejor evitar agentes anestésicos que provocan depresión del miocardio.
Debido a su componente tiazídico (Clortalidona):
• Periódicamente, debe determinarse el electrólito plasmático en intervalos adecuados para detectar un posible desequilibrio electrolítico, especialmente hipopotasemia e hiponatremia.
• Se recomienda la medición de electrólitos, especialmente en el paciente de mayor edad, aquellos que reciben fármacos digitálicos para el tratamiento de la insuficiencia cardiaca, en aquellos que tienen una dieta anormalmente baja en potasio o quienes sufren trastornos gastrointestinales. La hipopotasemia puede predisponer a arritmias en pacientes que reciben digitálicos.
• Ya que clortalidona puede alterar la tolerancia a la glucosa, los pacientes diabéticos deben estar conscientes de la posibilidad de un aumento de la concentración de glucosa en sangre. Se recomienda un monitoreo frecuente de la glucosa sanguínea, principalmente en la fase inicial de la terapia. En terapias de largo plazo deben realizarse pruebas de glucosa en orina a intervalos regulares.
• En pacientes con insuficiencia hepática o que padecen enfermedad hepática progresiva, alteraciones mínimas en el equilibrio de los líquidos y electrólitos pueden desencadenar un coma hepático.
• Puede suceder hiperuricemia. Sólo un aumento mínimo en el ácido úrico sérico sucede usualmente en casos de elevación prolongada, el uso concurrente de un agente uricosúrico revertirá la hiperuricemia.
Derrame coroideo, miopía aguda y glaucoma agudo de ángulo cerrado secundario:
Los fármacos sulfonamida o derivados de sulfonamida pueden causar una reacción idiosincrásica que da como resultado un derrame coroideo con defecto del campo visual, miopía transitoria y glaucoma agudo de ángulo cerrado. Los síntomas incluyen la aparición aguda de disminución de la agudeza visual o dolor ocular y, por lo general, ocurren entre horas y semanas después del inicio del fármaco. El glaucoma agudo de ángulo cerrado no tratado puede provocar una pérdida permanente de la visión. El tratamiento principal consiste en interrumpir la ingesta de fármacos lo más rápidamente posible. Es posible que deban considerarse tratamientos médicos o quirúrgicos rápidos si la presión intraocular permanece incontrolada. Los factores de riesgo para desarrollar glaucoma agudo de ángulo cerrado pueden incluir antecedentes de alergia a la sulfonamida o la penicilina.
Los atletas deben estar conscientes de que este medicamento puede provocar una reacción positiva a pruebas de ‘antidoping’.
Efecto sobre la capacidad para manejar y utilizar maquinaria:
Es poco probable que su uso resulte en cualquier disminución en la capacidad de los pacientes para manejar u operar maquinaria.
Sin embargo, debe tomarse en cuenta que puede presentarse mareo y fatiga ocasionalmente.
DOSIS Y VÍA DE ADMINISTRACIÓN:
Vía de Administración: Oral.
En principio, el tratamiento de la hipertensión debe iniciarse con un solo principio activo a bajas dosis (gradualmente).
La adición de la combinación fija de HIGROTON BLOK® sólo se recomienda después de un ajuste de dosis individual previo con los principios activos (es decir, Atenolol y Clortalidona). Si se justifica clínicamente, se puede considerar la conversión directa de la monoterapia a la combinación fija.
HIGROTON BLOK® 50/12.5 mg:
La dosis usual es de 1 tableta recubierta una vez al día (equivalente a 50 de Atenolol/12.5 mg de Clortalidona) en pacientes para los que el tratamiento combinado está indicado.
HIGROTON BLOK® 100/25 mg:
La dosis usual es de 1 tableta recubierta una vez al día (equivalente a 100 de Atenolol/25 mg de Clortalidona) en pacientes para los que el tratamiento combinado está indicado.
Duración de la administración:
El medicamento debe tomarse sin masticar junto con abundante líquido antes de una comida.
La duración de la administración es determinada por el médico tratante.
El tratamiento puede interrumpirse o terminarse únicamente por orden del médico.
Especialmente en pacientes con enfermedades de las arterias coronarias, la terapia con HIGROTON BLOK® no debe descontinuarse de manera abrupta, sino de forma gradual.
MANIFESTACIONES Y MANEJO DE LA SOBREDOSIFICACIÓN O INGESTA ACCIDENTAL:
Sobredosis:
Los síntomas de sobredosis pueden incluir bradicardia, hipotensión, insuficiencia cardiaca aguda y broncoespasmo.
El tratamiento general debe incluir: una supervisión frecuente, tratamiento en una sala de cuidados intensivos (terapia de choques), el uso de lavado gástrico, carbón activado y un laxante para prevenir la absorción de una sustancia activa todavía presente en el tracto gastrointestinal, la utilización de sustitutos del plasma o plasma para el tratamiento de la hipotensión y el shock. Puede ser considerado el uso de hemodiálisis o la hemoperfusión.
La bradicardia excesiva puede ser contrarrestada con atropina en dosis de 1 a 2 mg por vía intravenosa y/o un marcapasos cardiaco. Si es necesario, esto puede ser seguido por una dosis en bolo de 10 mg por vía intravenosa de glucagón. Si se requiere, se puede repetir o puede ser seguido de una infusión intravenosa de glucagón en dosis de 1 a 10 mg/hora dependiendo de la respuesta. Si no hay respuesta al glucagón o éste no se encuentra disponible, se puede administrar un estimulante beta-adrenérgico como dobutamina en dosis de 2.5 a 10 microgramos/kg/minuto mediante infusión intravenosa.
La Dobutamina, debido a sus efectos inotrópicos positivos, puede utilizarse para tratar la hipotensión y la insuficiencia cardiaca aguda. Es probable que estas dosis no sean suficientes para revertir los efectos cardiacos de los beta-bloqueadores si se ha consumido una sobredosis. Por lo tanto, la dosis de dobutamina debe aumentar de ser necesario para alcanzar la respuesta requerida de acuerdo a la condición clínica del paciente.
El broncoespasmo puede ser revertido casualmente mediante broncodilatadores.
La diuresis excesiva debe contrarrestarse manteniendo un balance normal de fluidos y electrólitos.
PRESENTACIONES:
Caja de cartón con 28, 30, 50 o 100 tabletas de 100 mg/25 mg en envase burbuja.
Caja de cartón con 28, 30, 50 o 100 tabletas de 50 mg/12.5 mg en envase burbuja
RECOMENDACIONES SOBRE ALMACENAMIENTO:
Consérvese o manténgase a no más de 25 °C.
Consérvese la caja bien cerrada.
LEYENDAS DE PROTECCIÓN:
Literatura exclusiva para médicos. Su venta requiere receta médica. No se deje al alcance de los niños. Prohibida la venta fraccionada del producto. No se use en el embarazo ni lactancia.
Reporte las sospechas de reacción adversa al correo:
farmacovigilancia@cofepris.gob.mx
Propiedad de:
Sandoz GmbH
Biochemiestraße 10, 6250 Kundl
Austria
Representante Legal:
SANDOZ, S.A. de C.V.
La Candelaria No. 186
Col. Atlántida, C.P. 04370
Coyoacán, Ciudad de México, México
Reg. Núm. 386M2008 SSA IV
193300001T0102/19Mar2021/IPPA_DRA-Sandoz
®Marca Registrada