JANUMET® - Comprimidos
Sustancia(s):
- Metformina, Sitagliptina
Presentaciones:
- 1 Caja, 14 Comprimidos, 50/500 mg/mg
- 1 Caja, 28 Comprimidos, 50/500 mg/mg
- 1 Caja, 56 Comprimidos, 50/500 mg/mg
- 1 Caja, 14 Comprimidos, 50/850 mg/mg
- 1 Caja, 28 Comprimidos, 50/850 mg/mg
- 1 Caja, 56 Comprimidos, 50/850 mg/mg
- 1 Caja, 14 Comprimidos, 50/1000 mg/mg
- 1 Caja, 28 Comprimidos, 50/1000 mg/mg
- 1 Caja, 56 Comprimidos, 50/1000 mg/mg
III. FORMA FARMACÉUTICA Y FORMULACIÓN
Comprimido.
Fórmula (50 mg/500 mg)
Cada comprimido contiene:
Fosfato de Sitagliptina Monohidratada equivalente a 50 mg de Sitagliptina
Clorhidrato de Metformina 500 mg
Excipiente cbp 1 comprimido
Fórmula (50 mg/ 850 mg)
Cada comprimido contiene:
Fosfato de Sitagliptina Monohidratada equivalente a 50 mg de Sitagliptina
Clorhidrato de Metformina 850 mg
Excipiente cbp 1 comprimido
Fórmula (50 mg/1,000 mg)
Cada comprimido contiene:
Fosfato de Sitagliptina Monohidratada equivalente a 50 mg de Sitagliptina
Clorhidrato de Metformina 1,000 mg
Excipiente cbp 1 comprimido
XIX. NÚMERO DE REGISTRO DEL MEDICAMENTO ANTE LA SECRETARÍA
Reg. No. 134M2007 SSA IV
Versión: S-WPC-MK0431A-T-052020
RCN: 000013428-MX
IV. INDICACIONES TERAPÉUTICAS
JANUMET está indicado como tratamiento inicial en pacientes con diabetes mellitus tipo 2 para mejorar el control glucémico cuando la dieta y el ejercicio no brindan un control adecuado de la glucemia.
JANUMET está indicado como complemento de la dieta y el ejercicio para mejorar el control glucémico en pacientes con diabetes mellitus tipo 2 inadecuadamente controlados con metformina o sitagliptina solas o en los que ya están siendo tratados con la combinación de sitagliptina y metformina.
JANUMET está indicado como parte del tratamiento combinado triple con una sulfonilurea como complemento de la dieta y el ejercicio, en pacientes con diabetes mellitus tipo 2 inadecuadamente controlados con cualquiera de dos de los tres medicamentos: metformina, sitagliptina o una sulfonilurea.
JANUMET está indicado como parte del tratamiento combinado triple con un agonista del PPARℽ (p. ej., tiazolidinedionas) como complemento de la dieta y el ejercicio, en pacientes con diabetes mellitus tipo 2 inadecuadamente controlados con cualquiera de dos de los tres medicamentos: metformina, sitagliptina o un agonista del PPARℽ.
JANUMET está indicado en pacientes con diabetes mellitus tipo 2 como complemento a la dieta y el ejercicio, para mejorar el control de la glucemia en combinación con insulina.
V. FARMACOCINÉTICA Y FARMACODINAMIA
Mecanismo de acción
JANUMET
JANUMET combina dos agentes hipoglucemiantes con mecanismos de acción complementarios, para mejorar el control de la glucemia en pacientes con diabetes tipo 2: Fosfato de sitagliptina, que es un inhibidor de la dipeptidil peptidasa 4 (DPP-4), y clorhidrato de metformina, que es un miembro de las biguanidas.
Los comprimidos de JANUMET contienen sitagliptina y una formulación de metformina de liberación inmediata.
Fosfato de sitagliptina
El fosfato de sitagliptina es un miembro de una clase de agentes hipoglucemiantes llamados inhibidores de la dipeptidil peptidasa 4 (DPP-4), que mejoran el control glucémico en pacientes con diabetes tipo 2, aumentando las concentraciones de las hormonas incretinas activas. Estas hormonas, que incluyen el péptido-1 similar al glucagón (GLP-1, por las siglas en inglés para glucagon-like peptide-1) y el péptido insulinotrópico dependiente de la glucosa (GIP, por las siglas en inglés para glucose-dependent insulinotropic polypeptide), son liberadas por el intestino durante todo el día y sus niveles aumentan en respuesta a la ingestión de alimentos. Las incretinas forman parte de un sistema endógeno que participa en la regulación fisiológica de la homeostasis de la glucosa. Cuando la glucemia está normal o elevada, el GLP-1 y el GIP aumentan la síntesis y la liberación de insulina por las células beta del páncreas a través de vías de señalización intracelulares en las que interviene el monofosfato de adenosina cíclico (cAMP, por las siglas en inglés para cyclic adenosine monophosphate). Se ha demostrado que el tratamiento con inhibidores del GLP-1 o de la DPP-4 en modelos animales de diabetes tipo 2 mejora la capacidad de respuesta de las células beta a la glucosa y estimula la biosíntesis y la liberación de insulina. Con concentraciones mayores de insulina, aumenta la captación tisular de glucosa. Además, el GLP-1 disminuye la secreción de glucagón por las células alfa del páncreas. Las concentraciones disminuidas de glucagón y el aumento de las concentraciones de insulina hacen que disminuya la producción hepática de glucosa, lo cual da por resultado la disminución de la concentración de glucosa en la sangre. Los efectos del GLP-1 y del GIP son dependientes de la glucosa, de tal manera que cuando la glucemia está baja no se observa estimulación de la liberación de insulina ni la inhibición de la secreción de glucagón por el GLP-1. La estimulación de liberación de insulina, tanto por GLP-1 como por GIP, se potencializa cuando los niveles de glucosa están por arriba de las concentraciones normales. Más aún, GLP-1 no afecta la respuesta normal del glucagón a la hipoglucemia. La actividad de GLP-1 y de GIP está limitada por la enzima DPP-4, que hidroliza rápidamente las incretinas y las transforma en productos inactivos. La sitagliptina impide esa hidrólisis de las incretinas por la DPP-4, por lo que aumentan las concentraciones plasmáticas de las formas activas del GLP-1 y del GIP. Al aumentar los niveles de las incretinas, la sitagliptina aumenta la liberación de insulina y disminuye la concentración de glucagón de manera dependiente de la glucosa. En los pacientes con diabetes tipo 2 con hiperglucemia, esos cambios en las concentraciones de insulina y de glucagón hacen que disminuyan las concentraciones de hemoglobina A1c (HbA1c) y la glucemia en ayunas y postprandial. El mecanismo dependiente de glucosa de sitagliptina es diferente al mecanismo de sulfonilureas, las cuales incrementan la secreción de insulina aun cuando los niveles de glucosa estén bajos, lo que puede causar hipoglucemia en pacientes con diabetes tipo 2 y en sujetos normales. La sitagliptina es un inhibidor potente y sumamente selectivo de la enzima DPP-4 y no inhibe las enzimas estrechamente relacionadas DPP-8 y DPP-9, a concentraciones terapéuticas.
Clorhidrato de metformina
La metformina es un agente hipoglucemiante que mejora la tolerancia a la glucosa en pacientes con diabetes tipo 2, disminuyendo tanto la glucosa plasmática basal como la postprandial. Sus mecanismos de acción farmacológicos son diferentes de los de otras clases de hipoglucemiantes orales. La metformina disminuye la producción hepática y la absorción intestinal de glucosa, y mejora la sensibilidad a la insulina aumentando la captación y la utilización periférica de glucosa. A diferencia de las sulfonilureas, la metformina no produce hipoglucemia ni en los pacientes con diabetes tipo 2 ni en los sujetos normales (excepto en circunstancias especiales; ver VII. PRECAUCIONES GENERALES, Clorhidrato de metformina), y no causa hiperinsulinemia. El tratamiento con metformina no modifica la secreción de insulina, mientras que puede disminuir los niveles de insulina en ayunas y la respuesta de la insulina plasmática durante todo el día.
FARMACOCINÉTICA
JANUMET
Los resultados de un estudio de bioequivalencia definitivo en sujetos sanos demostraron que los comprimidos combinados de JANUMET (Sitagliptina/Clorhidrato de metformina) con 50 mg/500 mg y con 50 mg/1,000 mg son bioequivalentes a la administración concomitante de esas mismas dosis de fosfato de sitagliptina (JANUVIA®) y clorhidrato de metformina en comprimidos individuales.
Debido a que se demostró bioequivalencia a las dosis más baja y más alta de comprimido combinados, se confirió bioequivalencia al comprimido de combinación fija (FDC, por las siglas en inglés para fixed dose combination) de 50 mg/850 mg (sitagliptina/metformina).
Absorción
JANUMET
Posterior a la ingesta de los comprimidos de JANUMET con un desayuno alto en grasas, el grado total de exposición (AUC, por las siglas en inglés para area under the curve) y la tasa de absorción (Cmáx y Tmáx) para sitagliptina no se alteraron en comparación con el estado de ayuno. Posterior a la ingesta de comprimidos de JANUMET con un desayuno alto en grasas, el AUC y Cmáx de metformina disminuyeron en 6% y 28% respectivamente, y el Tmáx ocurrió aproximadamente 1.5 horas más tarde, en relación con el estado de ayuno.
Fosfato de sitagliptina
La biodisponibilidad absoluta de la sitagliptina es de 87% aproximadamente. La administración concomitante de una comida alta en grasas con fosfato de sitagliptina no tuvo ningún efecto sobre la farmacocinética de la sitagliptina.
Clorhidrato de metformina
La biodisponibilidad absoluta de un comprimido de 500 mg de clorhidrato de metformina administrado en ayunas es de 50-60%, aproximadamente. Los estudios con dosis orales únicas de comprimidos de clorhidrato de metformina de 500 mg a 1,500 mg y de 850 mg a 2,550 mg indican que el efecto no es proporcional al incremento de las dosis, lo cual se debe a una disminución de la absorción y no a una alteración en la eliminación. La presencia de alimentos disminuye y retarda ligeramente la absorción de la metformina, como muestran una disminución de 40% aproximadamente en su concentración plasmática máxima promedio (Cmáx), una disminución de 25% del AUC de concentración plasmática versus tiempo y un aumento de 35 minutos del tiempo para alcanzar la concentración máxima plasmática (Tmáx) tras la administración de un solo comprimido de 850 mg de metformina con alimentos, en comparación con la administración de esa misma dosis en ayunas. Se desconoce la importancia clínica de estas disminuciones.
Los alimentos bajos y altos en grasa incrementaron la exposición sistémica (medido por el AUC) de las tabletas de GLUMETZA alrededor de un 38% y 73%, respectivamente, en relación con el ayuno. Ambos alimentos prolongaron el Tmáx de metformina en aproximadamente 3 horas, pero la Cmáx no fue afectada.
Distribución
Fosfato de sitagliptina
El volumen de distribución promedio en estado de equilibrio tras una dosis única intravenosa de sitagliptina a personas sanas es de 198 litros (L) aproximadamente. La porción de sitagliptina que se une reversiblemente a las proteínas plasmáticas es baja (38%).
Clorhidrato de metformina
El volumen aparente de distribución (V/F) de la metformina tras la administración oral única de comprimidos con 850 mg de clorhidrato de metformina fue en promedio de 654 ± 358 L. A diferencia de las sulfonilureas, que se unen en más de 90% a las proteínas plasmáticas, la metformina se une escasamente a éstas. Parte de la metformina penetra en los eritrocitos, muy probablemente en función del tiempo. A las dosis clínicas y horarios de administración usuales de los comprimidos de clorhidrato de metformina, las concentraciones plasmáticas de metformina en el estado de equilibrio se alcanzan en 24-48 horas y son generalmente <1 μg/mL. Durante los estudios clínicos controlados de metformina, sus concentraciones plasmáticas máximas no fueron mayores de 5 μg/mL, aun con las dosis máximas.
Metabolismo
Fosfato de sitagliptina
La sitagliptina es eliminada principalmente sin cambio en la orina, y su transformación metabólica es una vía menor. Aproximadamente 79% es excretada sin cambio en la orina.
Después de una dosis oral de sitagliptina marcada con 14C, aproximadamente 16% de la radiactividad fue excretada como metabolitos de la sitagliptina. Se detectaron sólo trazas de seis metabolitos, y no se prevé que éstos contribuyan a la actividad inhibidora de la sitagliptina sobre la DPP-4 plasmática. Los estudios in vitro indicaron que la principal enzima causante del metabolismo limitado de la sitagliptina fue CYP3A4, secundada por CYP2C8.
Clorhidrato de metformina
Los estudios con dosis únicas por vía intravenosa en sujetos normales demostraron que la metformina es excretada sin cambio en la orina y no es metabolizada en el hígado (no se ha identificado ningún metabolito en los seres humanos) ni excretada con la bilis.
Eliminación
Fosfato de sitagliptina
Tras la administración de una dosis oral de [14C] sitagliptina a sujetos sanos, aproximadamente 100% de la radiactividad administrada fue eliminada en las heces (13%) o la orina (87%) durante la semana siguiente. Después de una dosis oral de 100 mg, la t½ terminal aparente de la sitagliptina fue de 12.4 horas aproximadamente, y su depuración renal fue de unos 350 mL/min.
La eliminación de la sitagliptina ocurre principalmente por excreción renal, por secreción tubular activa. La sitagliptina es un sustrato para el transportador 3 de aniones orgánicos humano (hOAT-3, por las siglas en inglés para human organic anion transporter-3), el cual podría intervenir en su eliminación renal. No se ha determinado la importancia clínica del hOAT-3 en el transporte de la sitagliptina. Ésta es también un sustrato de la glucoproteína-p, que también puede mediar en su eliminación renal. Sin embargo, la ciclosporina, que es un inhibidor de la glucoproteína-p, no disminuyó la depuración renal de la sitagliptina.
Clorhidrato de metformina
La depuración renal de la metformina es aproximadamente 3.5 veces mayor que la depuración de la creatinina, lo cual indica que la secreción tubular es la principal vía de eliminación de la metformina. Tras la administración por vía oral, aproximadamente 90% del medicamento absorbido es eliminado por la vía renal en las primeras 24 horas, con una vida media de eliminación plasmática de 6.2 horas aproximadamente. En la sangre, la vida media de eliminación es de unas 17.6 horas aproximadamente, lo cual sugiere que la masa eritrocitaria puede ser un compartimiento de distribución del fármaco.
Características de los pacientes
Diabetes tipo 2
Fosfato de sitagliptina
La farmacocinética de la sitagliptina es generalmente similar en los pacientes con diabetes tipo 2 y en los sujetos sanos.
Clorhidrato de metformina
Si la función renal es normal, no hay ninguna diferencia en la farmacocinética de la metformina administrada en dosis únicas o múltiples entre los pacientes con diabetes tipo 2 y los sujetos sanos, y a las dosis clínicas usuales no ocurre ninguna acumulación del medicamento en ninguno de esos dos grupos.
Insuficiencia renal
Fosfato de sitagliptina
En comparación con los sujetos con función renal normal, el AUC plasmática de la sitagliptina aumentó aproximadamente 2 veces en los pacientes con insuficiencia renal moderada con una Tasa de Filtración Glomerular estimada (eGFR, por las siglas en inglés para estimated Glomerular Filtration Rate) de 30 a <45 mL/min/1.73 m2 y aproximadamente 4 veces en los pacientes con insuficiencia renal grave (eGFR <30 mL/min/1.73 m2) incluyendo a los pacientes con nefropatía terminal (ESRD, por las siglas en inglés para end-stage renal disease) bajo tratamiento con hemodiálisis.
Clorhidrato de metformina
En los pacientes con disminución de la función renal, aumenta la vida media plasmática y sanguínea de la metformina y disminuye su depuración renal (ver CONTRAINDICACIONES y PRECAUCIONES GENERALES).
Insuficiencia hepática
Fosfato de sitagliptina
En los pacientes con insuficiencia hepática moderada (puntuación de Child-Pugh de 7 a 9), tras la administración de una dosis única de 100 mg de fosfato de sitagliptina, los promedios de AUC y de Cmáx de sitagliptina fueron aproximadamente 21% y 13% mayores, respectivamente, comparado con sujetos sanos. Esas diferencias no se consideran clínicamente importantes.
No se tiene ninguna experiencia clínica en pacientes con insuficiencia hepática grave (puntuación de Child-Pugh > 9). Sin embargo, como la sitagliptina se elimina principalmente por vía renal, no se prevé que la insuficiencia hepática grave afecte la farmacocinética de la sitagliptina.
Clorhidrato de metformina
No se han hecho estudios sobre la farmacocinética de la metformina en pacientes con insuficiencia hepática.
Sexo
Fosfato de sitagliptina
Basándose en un análisis compuesto de los datos farmacocinéticos de la Fase I y en un análisis farmacocinético de población de los datos de las Fases I y II, el sexo no tuvo ningún efecto de importancia clínica sobre la farmacocinética de la sitagliptina.
Clorhidrato de metformina
Los parámetros farmacocinéticos de la metformina no difirieron significativamente entre sujetos normales y los pacientes con diabetes tipo 2 cuando se analizaron según el sexo, igualmente, en los estudios clínicos controlados en pacientes con diabetes tipo 2 el efecto hipoglucemiante de la metformina fue similar en los hombres y en las mujeres.
Pacientes de edad avanzada
Fosfato de sitagliptina
Según un análisis farmacocinético de población de los datos de las Fases I y II, la edad no tuvo un efecto de importancia clínica sobre la farmacocinética de la sitagliptina. Las personas de edad avanzada (65 a 80 años) tuvieron concentraciones plasmáticas de sitagliptina aproximadamente 19% mayores que en sujetos de menor edad.
Clorhidrato de metformina
Datos limitados de estudios farmacocinéticos controlados de metformina en personas de edad avanzada sanas sugieren que en éstas está disminuida la depuración plasmática total de la metformina y aumentadas su vida media y su Cmáx en comparación con personas jóvenes sanas. Según estos datos, el cambio en la farmacocinética de la metformina al aumentar la edad es debido principalmente al cambio en la función renal (ver la información para prescribir de GLUCOPHAGE1).
1 GLUCOPHAGE es una marca registrada de Merck Sante S.A.S, asociada de Merck KGaA of Darmstadt, Alemania. Licenciada a Bristol-Myers Squibb Company.
Niños
Se investigó la farmacocinética de sitagliptina (dosis única de 50 mg, 100 mg o 200 mg) en pacientes pediátricos (de 10 a 17 años de edad) con diabetes tipo 2. En esta población, el AUC ajustado a la dosis de sitagliptina en plasma fue aproximadamente un 18% menor en comparación con los pacientes adultos con diabetes tipo 2 para una dosis de 100 mg. Esto no se considera una diferencia clínicamente significativa basada en la relación plana de farmacocinética/ farmacodinamia (PK / PD) entre la dosis de 50 mg y 100 mg en adultos.
No se ha hecho ningún estudio con sitagliptina en niños <10 años de edad.
Raza
Fosfato de sitagliptina
Basándose en un análisis compuesto de los datos farmacocinéticos de la Fase I y en un análisis farmacocinético de población de los datos de las Fases I y II que incluyeron sujetos de razas blanca, hispanos, negros, asiáticos y de otros grupos raciales, la raza no tuvo ningún efecto de importancia clínica sobre la farmacocinética de la sitagliptina.
Clorhidrato de metformina
No se han hecho estudios de los parámetros farmacocinéticos de la metformina según la raza. En estudios clínicos controlados de metformina en pacientes con diabetes tipo 2, su efecto hipoglucemiante fue similar en blancos (n=249), negros (n=51) e hispanos (n=24).
Índice de masa corporal (IMC o BMI, por las siglas en inglés para Body Mass Index)
Fosfato de sitagliptina
Basándose en un análisis compuesto de los datos farmacocinéticos de la Fase I y en un análisis farmacocinético de población de los datos de las Fases I y II, el índice de masa corporal (IMC) no tuvo ningún efecto de importancia clínica sobre la farmacocinética de la sitagliptina.
FARMACODINAMIA
Fosfato de sitagliptina
General
En pacientes con diabetes tipo 2, la administración de dosis orales únicas de sitagliptina inhibe la actividad de la enzima DPP-4 durante un periodo de 24 horas, resultando en un incremento de 2 a 3 veces las concentraciones circulantes de GLP-1 y GIP activos, aumento de las concentraciones plasmáticas de insulina y de péptido C, y disminución de las concentraciones de glucagón, disminución de la glucemia en ayunas y disminución del margen de variación de la glucemia después de la ingestión de glucosa o de una comida.
En estudios clínicos Fase III de 18 y 24 semanas de duración, el tratamiento con 100 mg diarios de sitagliptina en pacientes con diabetes tipo 2 mejoró significativamente el funcionamiento de las células beta evaluado mediante varios marcadores, que incluyeron la Evaluación Modelo β de Homeostasis (HOMA-β, por las siglas en inglés para Homeostasis Model Assessment-β), la relación proinsulina/insulina y las mediciones de la sensibilidad de las células beta según las muestras múltiples de la prueba de tolerancia a la ingestión de alimentos. En estudios de Fase II, la eficacia sobre la glucemia de la dosificación de 50 mg de sitagliptina dos veces al día fue similar a la de 100 mg una vez al día.
En un estudio doble ciego de dos días, cruzado, de cuatro periodos, aleatorizado y controlado, de doble enmascaramiento en adultos sanos, se compararon los efectos de la administración concomitante de sitagliptina y metformina sobre las concentraciones de GLP-1 plasmático activo y total y la glucemia postprandiales con los de la administración de sitagliptina sola, metformina sola o placebo, cada uno administrado por dos días. El aumento del promedio ponderado de las concentraciones de GLP-1 activo 4 horas después de la comida fue aproximadamente dos veces mayor con la sitagliptina sola o la metformina sola que con el placebo. La administración concomitante de sitagliptina y metformina tuvo un efecto aditivo sobre el efecto en las concentraciones de GLP-1 activo, que aumentaron 4 veces más que con el placebo. La sitagliptina sola también aumentó sólo las concentraciones de GLP-1 activo, debido muy probablemente a la inhibición de la DPP-4, mientras que la metformina sola aumentó en grado similar las concentraciones de GLP-1 activo y total, lo cual refleja un mecanismo diferente para el aumento del GLP-1 activo, debido principalmente a un aumento del GLP-1 total. Estos datos son consistentes con diferentes mecanismos de acción para incrementar las concentraciones de GLP-1 activo. Los resultados de ese estudio también demostraron que la sitagliptina, pero no la metformina, aumenta las concentraciones de GIP activo.
En estudios con sujetos sanos, la sitagliptina no disminuyó la glucemia ni provocó hipoglucemia, lo cual sugiere que sus acciones insulinotrópica y supresora del glucagón son dependientes de la glucosa.
Efectos sobre la presión arterial
En un estudio cruzado, controlado con placebo y aleatorizado en pacientes hipertensos tratados con uno o más antihipertensivos (incluyendo inhibidores de la enzima convertidora de angiotensina [ECA o ACE por las siglas en inglés para angiotensin-converting enzyme], antagonistas de la angiotensina II, bloqueadores de canales de calcio, beta-bloqueadores y diuréticos), la administración concomitante con sitagliptina fue generalmente bien tolerada. En esos pacientes, la sitagliptina tuvo un modesto efecto reductor de la presión arterial; 100 mg diarios disminuyó 2 mmHg en promedio la presión sistólica ambulatoria en comparación con el placebo. No se han observado disminuciones en personas normotensas.
Electrofisiología cardiaca
En un estudio cruzado, controlado con placebo y aleatorizado, se administró a 79 sujetos sanos una dosis oral única de 100 mg de sitagliptina, de 800 mg de sitagliptina (8 veces mayor que la dosis recomendada), y placebo. La dosis recomendada de 100 mg no tuvo ningún efecto sobre el intervalo QTc obtenido durante la concentración plasmática máxima o en cualquier otro momento del estudio. Con la dosis de 800 mg, el aumento máximo del promedio de cambio del QTc inicial corregido respecto al placebo fue de sólo 8.0 mseg 3 horas después de la administración. Este pequeño aumento no se consideró clínicamente importante. Con la dosis de 800 mg, las concentraciones plasmáticas máximas de sitagliptina fueron aproximadamente 11 veces mayores que las producidas por la dosis de 100 mg.
En los pacientes con diabetes tipo 2 que recibieron sitagliptina a dosis de 100 mg diarios (N=81) o de 200 mg diarios (N=63) no hubo cambios importantes del intervalo QTc en los electrocardiogramas (EKG) obtenidos en el momento de la concentración plasmática máxima esperada.
ESTUDIOS CLÍNICOS
Estudios clínicos de la administración concomitante de sitagliptina y metformina demostraron mejorías significativas en el control glucémico en pacientes adultos con diabetes tipo 2. Ninguno de los estudios clínicos de eficacia descritos en adultos abajo se realizaron con JANUMET comprimidos; sin embargo, se ha demostrado la bioequivalencia de JANUMET comprimidos con la administración concomitante de sitagliptina y clorhidrato de metformina de liberación inmediata para todas las concentraciones de las tabletas.
En un estudio comparativo, la administración una vez al día de metfomina de liberación prolongada ha tenido una eficacia similar a la de la formulación de metformina de liberación inmediata dos veces al día, en todas las medidas de control de la glucemia.
Sitagliptina y metformina como tratamiento inicial en pacientes con diabetes tipo 2
Un total de 1,091 pacientes con diabetes tipo 2 y control inadecuado de la glucemia con dieta y ejercicio, participaron en un estudio factorial de 24 semanas, aleatorizado, doble ciego, controlado con placebo, diseñado para evaluar la eficacia y seguridad del tratamiento inicial con la combinación de sitagliptina y metformina. Se aleatorizó a un número aproximadamente equivalente de pacientes para recibir tratamiento inicial con placebo; 100 mg de sitagliptina una vez al día; 500 ó 1,000 mg de metformina dos veces al día; o 50 mg de sitagliptina dos veces al día combinada con metformina 500 ó 1,000 mg dos veces al día.
El tratamiento inicial con la combinación de sitagliptina y metformina produjo mejorías significativas en HbA1C, en glucosa plasmática en ayunas (FPG, por las siglas en inglés para fasting plasma glucose) y en glucosa plasmática postprandial (PPG, por las siglas en inglés para post-prandial glucose) a las 2 horas en comparación con placebo, con metformnina sola y con sitagliptina sola (p<0.001; Tabla 1, Figura 1). A las 3 semanas (el primer punto de evaluación después de iniciar el tratamiento), se logró una mejoría en FPG cercana a la máxima reducción de FPG y se mantuvo durante las 24 semanas del estudio. Las mediciones de la función de las células beta, HOMA-β y la relación proinsulina a insulina también mostraron mayor mejoría con la administración concomitante de sitagliptina y metformina en comparación con la monoterapia de ambos medicamentos. En general, los efectos en los lípidos fueron neutrales. La disminución en el peso corporal en el grupo de la combinación de sitagliptina y metformina fue similar al de los grupos de metformina sola o de placebo. Las reducciones promedio respecto al inicio en HbA1C comparado con placebo fueron generalmente mayores en los pacientes con valores basales más altos de HbA1C. La mejoría en HbA1C fue generalmente consistente entre los sub-grupos definidos por sexo, edad, raza o IMC basal. Las reducciones promedio respecto al inicio en HbA1c de los pacientes que no estaban bajo tratamiento hipoglucemiante al inicio del estudio fueron: sitagliptina 100 mg una vez al día, -1.06%; metformina 500 mg dos veces al día, -1.09%; metformina 1,000 mg dos veces al día, -1.24%; sitagliptina 50 mg dos veces al día más metformina 500 mg dos veces al día, -1.59%; sitagliptina 50 mg dos veces al día más metformina 1,000 mg dos veces al día, -1.94% y; para quienes recibieron placebo, -0.17%.
Figura 1. Cambios promedio del valor basal de HbA1C durante 24 semanas con sitagliptina y metformina, solas y en combinación, como tratamiento inicial en pacientes con diabetes tipo 2†
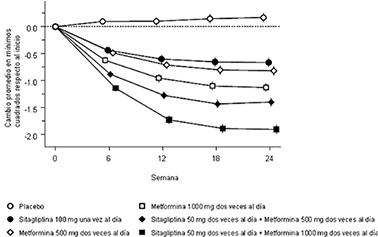
† Todos los mínimos cuadrados de la Población de Pacientes Tratados ajustados para tratamiento hipoglucemiante y valor basal previos.
Tabla 1. Parámetros de glucemia y peso corporal en la visita final (estudio de 24 semanas) para sitagliptina y metformina, solos o en combinación como tratamiento inicial†
|
Placebo |
Sitagliptina 100 mg una vez al día |
Metformina 500 mg dos veces al día |
Sitagliptina 50 mg una vez al día + Metformina 500 mg dos veces al día |
Metformina 1,000 mg dos veces al día |
Sitagliptina 50 mg dos veces al día + Metformina 1,000 mg dos veces al día |
|
|
HbA1c (%) |
n = 165 |
n = 175 |
n = 178 |
n = 183 |
n = 177 |
n = 178 |
|
Basal (promedio) |
8.68 |
8.87 |
8.90 |
8.79 |
8.68 |
8.76 |
|
Cambio respecto al valor basal (promedio ajustado‡) |
0.17 |
-0.66 |
-0.82 |
-1.40 |
-1.13 |
-1.90 |
|
Diferencia respecto a placebo promedio ajustado ‡) |
- |
-0.83§ |
-0.99§ |
-1.57§ |
-1.30§ |
-2.07§ |
|
Pacientes (%) que alcanzaron HbA1c <7% |
15 (9.1%) |
35 (20.0%) |
41 (23.0%) |
79 (43.2%) |
68 (38.4%) |
118 (66.3%) |
|
FPG (mg/dL) |
n = 169 |
n = 178 |
n = 179 |
n = 183 |
n = 179 |
n = 180 |
|
Basal (promedio) |
196.3 |
201.4 |
205.2 |
203.9 |
197.0 |
196.7 |
|
Cambio respecto al valor basal (promedio ajustado‡) |
5.8 |
-17.5 |
-27.3 |
-47.1 |
-29.3 |
-63.9 |
|
Diferencia respecto a placebo (promedio ajustado ‡) |
- |
-23.3§ |
-33.1§ |
-52.9§ |
-35.1§ |
-69.7§ |
|
PPG a las 2 horas (mg/dL) |
n = 129 |
n = 136 |
n = 141 |
n = 147 |
n = 138 |
n = 152 |
|
Basal (promedio) |
276.8 |
285.4 |
292.7 |
291.8 |
283.4 |
286.9 |
|
Cambio respecto al valor basal (promedio ajustado‡) |
0.3 |
-51.9 |
-53.4 |
-92.5 |
-78.0 |
-116.9 |
|
Diferencia respecto a placebo (promedio ajustado ‡) |
-52.2§ |
-53.7§ |
-92.8§ |
-78.3§ |
-116.9§ |
|
|
Peso corporal (kg)% |
n = 167 |
n = 175 |
n = 179 |
n = 184 |
n = 175 |
n = 178 |
|
Basal (promedio) |
90.1 |
85.9 |
88.1 |
90.0 |
89.4 |
88.2 |
|
Cambio respecto al valor basal (promedio ajustado‡) |
-0.9 |
0.0 |
-0.9 |
-0.6 |
-1.1 |
-1.3 |
|
Diferencia respecto a placebo (promedio ajustado‡) |
0.9¶ |
0.1# |
0.4# |
-0.1# |
-0.3# |
† Población de todos los pacientes tratados (análisis con intención de tratar).
‡ Promedio de mínimos cuadrados ajustado según el tratamiento hipoglucemiante anterior y el nivel basales.
§ p<0.001 comparado con placebo.
% Población de todos los pacientes tratados, excluyendo datos posteriores al tratamiento glucémico de rescate.
¶ p=0.005 comparado con placebo.
# Sin significancia estadística (p≥0.05) comparado con placebo.
Además, este estudio incluyó pacientes (n=117) con hiperglucemia más severa (HbA1C >11%) o glucosa sanguínea (>280 mg/dL) que fueron tratados en forma abierta con sitagliptina 50 mg más metformina 1,000 mg dos veces al día. En este grupo de pacientes, el valor basal de HbA1C era 11.15%, FPG era 314.4 mg/dL y PPG a las 2 horas era 441.0 mg/dL. Después de 24 semanas se observaron disminuciones de -2.94% para HbA1C, -126.7 mg/dL para FPG y -207.9 mg/dL para PPG a las dos horas. En esta cohorte abierta se observó un modesto incremento del peso corporal de 1.3 kg a las 24 semanas.
Adición de sitagliptina en pacientes controlados inadecuadamente con metformina sola:
La seguridad y la eficacia de la combinación de sitagliptina y metformina se evaluó en dos estudios clínicos doble ciego, controlados con placebo en pacientes con diabetes mellitus tipo 2. En ambos estudios se aleatorizó a pacientes en los que dosis estables de ≥1,500 mg de metformina con control inadecuado de la glucemia, para recibir 100 mg diarios de sitagliptina o placebo añadidos a su tratamiento con metformina.
En un estudio, 701 pacientes recibieron 100 mg de sitagliptina o placebo una vez al día durante 24 semanas. En comparación con el placebo, la adición de sitagliptina al tratamiento con metformina mejoró significativamente la concentración de HbA1c (-0.65%), la FPG (-25.4 mg/dL) y la PPG a las dos horas (-50.6 mg/dL) (ver Figura 2 y Tabla 2). En esa mejoría de la HbA1c respecto a placebo, no influyeron su valor basal, el tratamiento hipoglucemiante previo, el sexo, la edad, el IMC basal, el tiempo transcurrido desde que se diagnosticó la diabetes, la presencia de síndrome metabólico, ni los índices estándares de resistencia a la insulina (HOMA-IR) o de secreción de insulina (HOMA-β). Comparado con los pacientes que tomaron placebo, los pacientes que recibieron sitagliptina presentaron ligeras disminuciones en colesterol total, colesterol no-HDL y en los triglicéridos. En los dos grupos de tratamiento se observó una disminución similar del peso corporal.
Figura 2. Cambio promedio del valor basal de HbA1c en el transcurso de 24 semanas con dosis totales diarias de 100 mg de sitagliptina más metformina o con placebo más metformina en pacientes con diabetes tipo 2†,‡
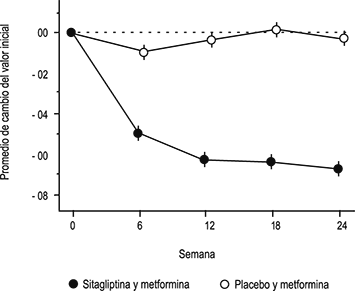
† Pacientes con control glucémico inadecuado con la monoterapia con metformina.
‡ Los Mínimos cuadrados de la Población de Todos los Pacientes Tratados ajustados para tratamiento hipoglucemiante y valor basal previos.
Tabla 2. Parámetros glucémicos y peso corporal en la visita final (Estudio de 24 semanas). Sitagliptina añadida a tratamiento actual con metformina en pacientes con control inadecuado de la glucemia†
|
Sitagliptina 100 mg + metformina una vez al día |
Placebo + metformina |
|
|
HbA1c (%) |
n = 453 |
n = 224 |
|
Basal (promedio) |
7.96 |
8.03 |
|
Cambio del valor basal (promedio ajustado‡) |
-0.67 |
-0.02 |
|
Diferencia con el placebo+metformina (promedio ajustado‡) |
-0.65§ |
|
|
% de pacientes que llegaron a HbA1c <7% |
213 (47.0) |
41 (18.3) |
|
FPG (mg/dL) |
N = 454 |
N = 226 |
|
Basal (promedio) |
170.0 |
173.5 |
|
Cambio respecto al valor basal (promedio ajustado‡) |
-16.9 |
8.5 |
|
Diferencia respecto a placebo+metformina (promedio ajustado‡) |
-25.4§ |
|
|
PPG a las 2 horas (mg/dL) |
N = 387 |
N = 182 |
|
Basal (promedio) |
274.5 |
272.4 |
|
Cambio respecto al valor basal (promedio ajustado‡) |
-62.0 |
-11.4 |
|
Diferencia respecto a placebo+metformina (promedio ajustado‡) |
-50.6§ |
|
|
Peso corporal (kg) * |
N = 399 |
N = 169 |
|
Basal (promedio) |
86.9 |
87.6 |
|
Cambio respecto al valor basal (promedio ajustado‡) |
-0.7 |
-0.6 |
|
Diferencia respecto a placebo+metformina (promedio ajustado‡) |
-0.1¶ |
† Todos los pacientes tratados (análisis con la intención de tratar).
‡ Promedios de los mínimos cuadrados ajustados según el tratamiento hipoglucemiante y el valor basal previos.
§ p<0.001 comparado con placebo + metformina.
* Todos los pacientes tratados, excluyendo datos posteriores al tratamiento hipoglucemiante de rescate.
¶ Sin significancia estadística (p≥0.05) comparado con placebo + metformina.
En otro estudio se midió la glucemia durante las 24 horas del día. Veintiocho pacientes recibieron 50 mg de sitagliptina o placebo dos veces al día durante cuatro semanas además de su tratamiento con metformina dos veces al día. Al cabo de esas cuatro semanas se determinó la diferencia en la eficacia reductora de la glucemia según el promedio ponderado de la glucemia (WMG, por las siglas en inglés para weighted mean glucose) en 24 horas, basándose en la toma de múltiples muestras de sangre, incluyendo las obtenidas antes y después de las comidas y por la noche. En comparación con el placebo más metformina, la administración concomitante de 50 mg de sitagliptina dos veces al día con metformina disminuyó significativamente (-32.8 mg/dL) el WMG en 24 horas. Además, la sitagliptina administrada con metformina, en comparación con el placebo administrado con metformina, disminuyó considerablemente la glucemia en ayunas, y causó menores variaciones de la glucemia después de las tres comidas del día (Figura 3). En las mediciones de la glucemia hechas por los pacientes, el tratamiento con sitagliptina más metformina también disminuyó significativamente en comparación con el placebo más metformina el promedio de glucemia en ayunas (-20.3 mg/dL), el promedio de siete mediciones de la glucemia (-28.0 mg/dL) y la glucemia postprandial a las dos horas (-36.6 mg/dL).
Figura 3. Perfil de glucemia plasmática durante 24 horas después de cuatro semanas de tratamiento con 50 mg diarios dos veces al día de sitagliptina y metformina o con placebo y metformina en pacientes con diabetes tipo 2†
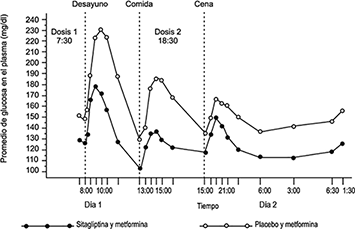
† Pacientes con inadecuado control de la glucemia bajo monoterapia con metformina.
Tratamiento de adición de sitagliptina a pacientes controlados inadecuadamente con la combinación de glimepirida y metformina:
Un total de 441 pacientes con diabetes tipo 2 participaron en un estudio de 24 semanas, doble ciego, aleatorizado, controlado con placebo, que se diseñó para evaluar la eficacia de sitagliptina 100 mg una vez al día comparado con placebo en combinación con glimepirida (sola o en combinación con metformina). En este estudio, 220 pacientes estuvieron en la combinación de glimepirida (≥4 mg diarios) y metformina (≥1,500 mg diarios); los resultados de los puntos finales de glucemia, incluyendo HbA1c y FPG, se describen a continuación.
La combinación de sitagliptina, glimepirida y metformina produjo, respecto al nivel basal, reducciones significativas en HbA1c (-0.89%) y FPG (-20.7 mg/dL) en comparación con placebo (ver Tabla 3). Las reducciones promedio respecto al nivel basal en HbA1C comparado con placebo en general fueron mayores en quienes tenían valores mayores de HbA1C al inicio. Los pacientes tratados con sitagliptina tuvieron un modesto incremento en el peso corporal respecto a quienes recibieron placebo.
Tabla 3. Parámetros glucémicos y peso corporal en la visita final (Estudio de 24 semanas) para sitagliptina en combinación con glimepirida con metformina†
|
Sitagliptina 100 mg + Glimepirida + Metformina |
Placebo + Glimepirida + Metformina |
|
|
HbA1c (%) |
N = 115 |
N = 105 |
|
Basal (promedio) |
8.27 |
8.28 |
|
Cambio respecto al valor basal (promedio ajustado‡) |
-0.59 |
0.30 |
|
Diferencia con placebo (promedio ajustado‡) |
-0.89§ |
|
|
Pacientes (%) que alcanzó HbA1C <7% |
26 (22.6) |
1 (1.0) |
|
FPG (mg/dL) |
N = 115 |
N = 109 |
|
Basal (promedio) |
179.3 |
178.9 |
|
Cambio respecto al valor basal (promedio ajustado‡) |
-7.8 |
12.9 |
|
Diferencia con placebo (promedio ajustado‡) |
-20.7§ |
|
|
Peso corporal (kg)% |
N = 102 |
N = 74 |
|
Basal (promedio) |
86.5 |
84.6 |
|
Cambio respecto al valor basal (promedio ajustado‡) |
0.4 |
-0.7 |
|
Diferencia con placebo (promedio ajustado‡) |
1.1†† |
† Todos los pacientes tratados (análisis con intención de tratar).
‡ Promedios de los mínimos cuadrados ajustados según el tratamiento hipoglucemiante y el valor basal previos.
§ p<0.001 comparado con placebo.
% Todos los pacientes tratados, excluyendo datos posteriores al tratamiento hipoglucemiante de rescate.
†† p = 0.007 comparado con placebo.
Tratamiento combinado de adición en pacientes controlados inadecuadamente con metformina más rosiglitazona:
Un total de 262 pacientes con diabetes tipo 2 participaron en un estudio controlado con placebo, de 54 semanas, doble ciego, aleatorizado diseñado para evaluar la eficacia de sitagliptina en combinación con metformina y rosiglitazona. Pacientes con control glucémico inadecuado con un esquema estable de metformina (≥1,500 mg diarios) y rosiglitazona (≥4 mg diarios) fueron aleatorizados a la adición de 100 mg de sitagliptina o de placebo administrados una vez al día. Los parámetros glucémicos fueron evaluados en el primer punto en el tiempo de la Semana 18 y a la Semana 54.
En combinación con metformina y rosiglitazona, sitagliptina brindó mejorías significativas en HbA1c, FPG y PPG de 2 horas en comparación a placebo con metformina y rosiglitazona (Tabla 4, Figura 4) a la Semana 18, con mejorías sostenidas hasta el final del estudio. Los efectos en los lípidos fueron generalmente neutrales. No hubo diferencias significativas entre sitagliptina y placebo en el cambio en el peso corporal.
Figura 4: Cambio promedio del valor basal de HbA1c (%) durante 54 semanas en un estudio de adición de sitagliptina al tratamiento de pacientes controlados inadecuadamente con metformina y rosiglitazona†
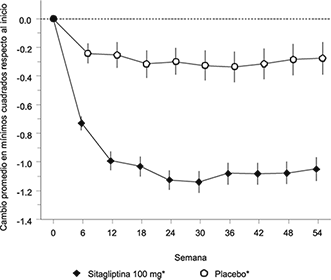
† Población de todos los pacientes tratados; Promedio de mínimos cuadrados ajustado según el tratamiento y el valor inicial basales (barras de error = error estándar).
* Adición al tratamiento en curso con metformina y rosiglitazona.
Tabla 4: Parámetros glucémicos y peso corporal en las semanas 18 y 54 (visita final) para sitagliptina en tratamiento combinado de adición a metformina y rosiglitazona†
|
Semana 18 |
Semana 54 |
|||
|
Sitagliptina 100 mg + Metformina + Rosiglitazona |
Placebo + Metformina + Rosiglitazona |
Sitagliptina 100 mg + Metformina + Rosiglitazona |
Placebo + Metformina + Rosiglitazona |
|
|
HbA1c (%) |
N = 168 |
N = 88 |
N = 168 |
N = 88 |
|
Basal (promedio) |
8.81 |
8.73 |
8.81 |
8.73 |
|
Cambio respecto al valor basal (promedio ajustado‡) |
-1.03 |
-0.31 |
-1.05 |
-0.28 |
|
Diferencia con placebo + rosiglitazona + metformina (promedio ajustado ‡) |
-0.72§ |
-0.77§ |
||
|
Pacientes (%) que lograron A1C <7% |
37 (22%) |
8 (9%) |
44 (26%) |
12 (14%) |
|
FPG (mg/dL) |
N = 169 |
N = 89 |
N = 169 |
N = 89 |
|
Basal (promedio) |
182.1 |
183.5 |
182.1 |
183.5 |
|
Cambio respecto al valor basal (promedio ajustado‡) |
-30.7 |
-11.7 |
-28.0 |
-10.7 |
|
Diferencia con placebo + rosiglitazona + metformina (promedio ajustado ‡) |
-19.0§ |
-17.4§ |
||
|
PPG 2 horas (mg/dL) |
N = 142 |
N = 75 |
N = 147 |
N = 77 |
|
Basal (promedio) |
257.8 |
249.5 |
256.6 |
247.7 |
|
Cambio respecto al valor basal (promedio ajustado‡) |
-59.9 |
-22.0 |
-50.7 |
-16.6 |
|
Diferencia con placebo + rosiglitazona + metformina (promedio ajustado ‡) |
-37.9§ |
-34.1§ |
||
|
Peso corporal (kg)% |
N = 157 |
N = 79 |
N = 115 |
N = 40 |
|
Basal (promedio) |
82.1 |
87.0 |
82.0 |
85.6 |
|
Cambio respecto al valor basal (promedio ajustado‡) |
0.5 |
0.2 |
1.9 |
1.3 |
|
Diferencia con placebo + rosiglitazona + metformina (promedio ajustado ‡) |
0.3¶ |
0.6¶ |
||
† Población de todos los pacientes tratados (análisis con intención de tratar).
‡ Promedio de mínimos cuadrados ajustado según el tratamiento hipoglucemiante y el valor basal previos.
§ p<0.001 comparado con placebo + metformina + rosiglitazona.
% Todos los pacientes tratados, excluyendo datos posteriores al tratamiento glucémico de rescate.
¶ Sin diferencia estadísticamente significativa (p≥0.05) comparado con placebo + metformina + rosiglitazona.
Tratamiento combinado de adición de sitagliptina en pacientes controlados inadecuadamente con la combinación de metformina e insulina:
Un total de 641 pacientes con diabetes tipo 2 participaron en un estudio controlado con placebo, doble ciego, con distribución al azar, de 24 semanas diseñado para evaluar la eficacia de sitagliptina 100 mg una vez al día en combinación con una dosis estable de insulina. Aproximadamente 75% de los pacientes estaban también tomando metformina. Pacientes con insulina premezclada, de acción larga o de acción intermedia (con o sin metformina), fueron distribuidos al azar para que se les añadiera sitagliptina 100 mg o placebo. Los puntos finales glucémicos incluyeron HbA1c, glucosa en ayunas y glucosa postprandial de 2 horas.
La combinación de sitagliptina, metformina e insulina proporcionó mejorías significativas en HbA1c, glucosa en ayunas y glucosa postprandial de 2 horas comparado con placebo (Tabla 5). La mejoría en HbA1c comparado con placebo fue generalmente consistente entre los subgrupos definidos por sexo, edad, raza, IMC inicial, tiempo desde el diagnóstico de diabetes, presencia de síndrome metabólico, e índices estándar de resistencia la insulina (HOMA-IR) y de secreción de insulina (HOMA-β). No hubo diferencias importantes en el peso corporal respecto al inicio entre los grupos.
Tabla 5: Parámetros glucémicos y peso corporal en la Visita Final (Estudio de 24 semanas) para sitagliptina en tratamiento combinado de adición con metformina y una dosis estable de insulina†
|
Sitagliptina 100 mg + Insulina + Metformina |
Placebo + Insulina + Metformina |
|
|
HbA1c (%) |
N = 223 |
N = 229 |
|
Basal (promedio) |
8.73 |
8.60 |
|
Cambio respecto al valor basal (promedio ajustado‡) |
-0.66 |
-0.13 |
|
Diferencia vs. placebo (promedio ajustado‡,§) |
-0.53% |
|
|
Pacientes (%) que lograron la meta HbA1c <7% |
32 (14.3) |
12 (5.2) |
|
FPG (mg/dL) |
N = 225 |
N = 229 |
|
Basal (promedio) |
173.5 |
175.6 |
|
Cambio respecto al valor basal (promedio ajustado‡) |
-22.2 |
-3.9 |
|
Diferencia vs. placebo (promedio ajustado‡) |
-18.3% |
|
|
PPG a las 2 horas (mg/dL) |
N = 182 |
N = 189 |
|
Basal (promedio) |
280.7 |
280.6 |
|
Cambio respecto al valor basal (promedio ajustado‡) |
-39.0 |
1.5 |
|
Diferencia vs. placebo (promedio ajustado‡) |
-40.4% |
|
|
Peso corporal (kg) ¶ |
N = 201 |
N = 200 |
|
Basal (promedio) |
87.9 |
88.0 |
|
Cambio respecto al valor basal (promedio ajustado‡) |
-0.1 |
0.0 |
|
Diferencia vs. placebo (promedio ajustado‡) |
-0.1# |
† Población de todos los pacientes tratados (análisis con intención de tratar).
‡ Promedio de mínimos cuadrados ajustado a uso de insulina en la Visita 1 (premezclada vs. no premezclada [acción intermedia o larga]), y valor basal.
§ El tratamiento por interacción de estratos con insulina no fue significativo (p>0.10).
% p<0.001 comparado con placebo.
¶ Todos los pacientes tratados, excluyendo datos posteriores al tratamiento glucémico de rescate.
# Sin diferencia estadística significativa (p≥0.05) comparado con placebo.
En otro estudio de 24-semanas, aleatorizado, doble-ciego, controlado con placebo, diseñado para evaluar la eficacia de la sitagliptina añadida a la insulina como terapia combinada, 660 pacientes con control glicémico inadecuado usando insulina glargina con o sin metformina (≥1,500 mg diarios) fueron aleatorizados a la adición ya sea de 100 mg de sitagliptina (N=330) o placebo (N=330), administrados una vez al día mientras experimentaban intensificación de la terapia con insulina. Entre los pacientes que tomaban metformina, el valor basal de HbA1c fue de 8.70% y la dosis basal de insulina era 37 UI/día. Los pacientes recibieron instrucciones para calibrar su dosis de insulina glargina con base en los valores obtenidos de glucosa en ayuno con prueba por punción capilar. Los puntos finales glucémicos medidos incluyeron HbA1c y a FPG.
Entre los pacientes que tomaban metformina, en la Semana 24, el aumento en la dosis diaria de insulina fue 21% menor en los pacientes tratados con sitagliptina (19 UI/día, N=285) que en los pacientes tratados con placebo (24 UI/día, N=283). La diferencia en la dosis de insulina (-5 UI/día) fue estadísticamente significativa (p=0.007). La reducción de HbA1c para pacientes tratados con sitagliptina, metformina, e insulina fue -1.35% comparado con -0.90% para pacientes tratados con placebo, metformina, e insulina, una diferencia de -0.45% [95% CI (por las siglas en inglés para Confidence Interval): -0.62, -0.29]. La reducción de FPG para pacientes tratados con sitagliptina, metformina, e insulina fue -54.8 mg/dL comparada con -43.0 mg/dL para pacientes tratados con placebo, metformina, e insulina, una diferencia de -11.8 mg/dL [95% CI: -18.7, -4.9]. La incidencia de hipoglucemia fue 24.9% para pacientes tratados con sitagliptina, metformina, e insulina y 37.8% para pacientes tratados con placebo, metformina e insulina. La diferencia en la incidencia de hipoglucemia (-12.9%) fue estadísticamente significativa (p<0.001).
Estudio controlado con activo (glipizida) en combinación con metformina
El efecto del tratamiento de mantenimiento a largo plazo se evaluó en un estudio de 52 semanas, doble ciego, controlado con glipizida en pacientes con diabetes tipo 2 inadecuadamente controlados con monoterapia de metformina ≥1,500 mg/día. En este estudio los pacientes fueron aleatorizados a la adición de sitagliptina 100 mg diarios (N=588) o glipizida (N=584) por 52 semanas. Los pacientes que recibieron glipizida iniciaron con una dosis de 5 mg al día y después se les ajustó la dosis a criterio del investigador hasta alcanzar una FPG objetivo de <110 mg/dL, sin hipoglucemia significativa durante las siguientes 18 semanas. Como dosis máxima se permitió una dosificación de 20 mg al día para optimizar el control glucémico. Después, la dosis de glipizida debía mantenerse constante. La dosis promedio de glipizida después del periodo de ajuste fue de 10.3 mg.
Ambos tratamientos mejoraron significativamente el control de la glucemia respecto al valor basal. Después de 52 semanas, la reducción en HbA1c respecto al valor basal fue -0.67% con sitagliptina 100 mg diarios y -0.67% con glipizida, lo cual confirmó una eficacia comparable de estos dos medicamentos. La reducción en FPG fue -10.0 mg/dL con sitagliptina y -7.5 mg/dL con glipizida. En un análisis post hoc, los pacientes con una HbA1c basal mayor (≥9%), tuvieron mayores reducciones en ambos grupos respecto al valor basal en HbA1c (sitagliptina, -1.68%; glipizida, -1.76%). En este estudio, la relación proinsulina a insulina, un marcador de eficiencia en la síntesis y liberación de insulina, mejoró con sitagliptina y se deterioró con el tratamiento con glipizida. La incidencia de hipoglucemia en el grupo tratado con sitagliptina (4.9%) fue significativamente menor que con el grupo con glipizida (32.0%). Los pacientes tratados con sitagliptina presentaron una disminución de peso promedio significativa, comparado con el aumento significativo de peso en los pacientes que recibieron glipizida (-1.5 kg vs. +1.1 kg).
Clorhidrato de metformina
El estudio prospectivo con distribución al azar UKPDS (por las siglas en inglés para United Kingdom Prospective Diabetes Study) ha demostrado el beneficio a largo plazo del control intensivo de la glucemia en la diabetes tipo 2. El análisis de los resultados obtenidos en pacientes obesos tratados con metformina después de haber fracasado el tratamiento con dieta sola mostró:
• una disminución significativa del riesgo absoluto de cualquier complicación relacionada con diabetes en el grupo de metformina (29.8 casos/1,000 años-paciente) en comparación con la dieta sola (43.3 casos/1,000 años-paciente), p=0.0023 y en comparación con los grupos de monoterapia con sulfonilurea y con insulina combinados (40.1 casos/1,000 años-paciente) (p=0.0034).
• una disminución significativa del riesgo absoluto de mortalidad relacionada con diabetes: metformina, 7.5 muertes/1,000 años-paciente; dieta sola, 12.7 muertes/1,000 años-paciente (p=0.017).
• una disminución significativa del riesgo absoluto de mortalidad total: Metformina, 13.5 muertes/1,000 años-paciente, en comparación con la dieta sola (20.6 muertes/1,000 años-paciente) (p=0.011), y en comparación con los grupos de monoterapia con sulfonilurea y con insulina combinados 18.9 muertes/1,000 años-paciente) (p=0.021).
• una disminución significativa del riesgo absoluto de infarto al miocardio: Metformina, 11 casos/1,000 años-paciente; dieta sola, 18 casos/1,000 años-paciente (p=0.01).
Estudio de Seguridad Cardiovascular TECOS
El Estudio de Evaluación de Desenlaces Cardiovasculares (TECOS, por las siglas en inglés para Trial Evaluating Cardiovascular Outcomes with Sitagliptin) fue un estudio aleatorizado en 14,671 pacientes en la población con intención de tratar con una HbA1c de ≥6.5 a 8.0% con enfermedad cardiovascular (CV) establecida, que recibieron sitagliptina (7,332), 100 mg diarios (o 50mg diarios si la eGFR basal era ≥30 y <50 mL/min/1.73 m2) o placebo (7,339) añadidos al cuidado usual, apuntando a estándares regionales para HbA1c y factores de riesgo CV. No se incluyeron en el estudio pacientes con una eGFR <30 mL/min/1.73 m2. La población de estudio incluyó a 2,004 pacientes ≥75 años de edad y 3,324 pacientes con insuficiencia renal (eGFR <60 mL/min/1.73 m2).
Durante el curso del estudio, la diferencia promedio global estimada (SD) en HbA1c entre los grupos sitagliptina y placebo fue de 0.29% (0.01), 95% IC (-0.32, -0.27); p<0.001. Los pacientes en el grupo sitagliptina recibieron menos agentes hipoglucemiantes que los del grupo placebo (razón de riesgo 0.72, 95% IC, 0.68 a 0.77; p≤0.001) y, entre los pacientes sin insulina a la entrada al estudio, hubo menor probabilidad de iniciar tratamiento crónico con insulina (razón de riesgo 0.70, 95% IC, 0.63 a 0.79; p<0.001).
El punto final cardiovascular primario fue una composición de la primera ocurrencia de muerte cardiovascular, infarto al miocardio no fatal, apoplejía no fatal, u hospitalización por angina inestable. Los puntos finales cardiovasculares secundarios incluyeron la primera ocurrencia de muerte cardiovascular, infarto al miocardio no fatal, o apoplejía no fatal, la primera ocurrencia de los componentes individuales de composición primaria; mortalidad por cualquier causa y admisiones hospitalarias por insuficiencia cardíaca congestiva.
Después de un seguimiento mediano de hasta 3 años, añadir sitagliptina al cuidado usual, no incrementó el riesgo de eventos adversos cardiovasculares mayores, o el riesgo de hospitalización por insuficiencia cardíaca, comparado con el cuidado usual sin sitagliptina en pacientes con diabetes tipo 2 (Tabla 6).
Tabla 6: Tasas de Desenlaces Cardiovasculares Compuestos y Desenlaces Secundarios Clave
|
Sitagliptina 100 mg |
Placebo |
Razón de Riesgo (95% CI) |
Valor de p† |
|||
|
N (%) |
Tasa de Incidencia por 100 Pacientes-Años* |
N (%) |
Tasa de Incidencia por 100 Pacientes-Años* |
|||
|
Análisis en la Población por Protocolo |
||||||
|
Número de Pacientes |
7,257 |
7,266 |
0.98 (0.88-1.09) |
<0.001 |
||
|
Punto Final Primario Compuesto |
||||||
|
(Muerte cardiovascular, infarto al miocardio no fatal, apoplejía no fatal, u hospitalización por angina inestable) |
695 (9.6) |
3.7 |
695 (9.6) |
3.8 |
||
|
Punto Final Secundario Compuesto |
||||||
|
(Muerte cardiovascular, infarto al miocardio no fatal, o apoplejía no fatal) |
609 (8.4) |
3.2 |
602 (8.3) |
3.3 |
0.99 (0.89-1.11) |
<0.001 |
|
Análisis en la Población con Intención de Tratar |
||||||
|
Número de Pacientes |
7,332 |
7,339 |
0.98 (0.89-1.08) |
<0.001 |
||
|
Punto Final Primario Compuesto |
||||||
|
(Muerte cardiovascular, infarto al miocardio no fatal, apoplejía no fatal, u hospitalización por angina inestable) |
839 (11.4) |
4.1 |
851 (11.6) |
4.2 |
||
|
Punto Final Secundario Compuesto |
0.99 (0.89-1.10) |
<0.001 |
||||
|
(Muerte cardiovascular, infarto al miocardio no fatal, o apoplejía no fatal) |
745 (10.2) |
3.6 |
746 (10.2) |
3.6 |
||
|
Desenlace Secundario |
||||||
|
Muerte cardiovascular |
380 (5.2) |
1.7 |
366 (5.0) |
1.7 |
1.03 (0.89-1.19) |
0.711 |
|
Todos los infartos al miocardio (fatales y no fatales) |
300 (4.1) |
1.4 |
316 (4.3) |
1.5 |
0.95 (0.81-1.11) |
0.487 |
|
Todas las apoplejías (fatales y no fatales) |
178 (2.4) |
0.8 |
183 (2.5) |
0.9 |
0.97 (0.79-1.19) |
0.760 |
|
Hospitalización por angina inestable |
116 (1.6) |
0.5 |
129 (1.8) |
0.6 |
0.90 (0.70-1.16) |
0.419 |
|
Muerte por cualquier causa |
547 (7.5) |
2.5 |
537 (7.3) |
2.5 |
1.01 (0.90-1.14) |
0.875 |
|
Hospitalización por insuficiencia cardíaca‡ |
228 (3.1) |
1.1 |
229 (3.1) |
1.1 |
1.00 (0.83-1.20) |
0.983 |
* Tasa de incidencia por 100 años-paciente calculada como 100 x (número total de pacientes con ≥1 evento durante el periodo de exposición elegible por total de años-paciente de seguimiento).
† Basado en un modelo estratificado de Cox por región. Para puntos finales compuestos, el valor de p corresponde a una prueba de no inferioridad que buscó mostrar que la razón de riesgo es menor de 1.3. Para los demás puntos finales, los valores de p corresponden a una prueba de diferencias en las razones de riesgo.
‡ El análisis de hospitalización por insuficiencia cardíaca se ajustó por antecedentes de insuficiencia cardíaca a nivel basal.
Terapia complementaria de sitagliptina en pacientes pediátricos controlados inadecuadamente con metformina con o sin insulina:
Un total combinado de 220 pacientes pediátricos de 10 a 17 años con diabetes tipo 2 y control glucémico inadecuado con metformina con o sin insulina participaron en dos estudios aleatorizados, doble ciego, controlados con placebo, de grupos paralelos durante 54 semanas. La adición de 100 mg de sitagliptina (administrada como JANUMET) se comparó con la adición de placebo a la metformina.
La superioridad de la reducción de HbA1c se demostró para JANUMET sobre la metformina en la semana 20 en el análisis combinado de estos dos estudios. La reducción de la HbA1c en los pacientes tratados con JANUMET (N = 107) fue del -0,6% en comparación con el -0,1% en los pacientes tratados con metformina (N = 113), una diferencia del -0,5% (IC del 95%: -0,9, -0,1 ). Sin embargo, los resultados de los estudios individuales fueron inconsistentes y no se observó la eficacia de JANUMET sobre metformina en la semana 54. Estos resultados no apoyan el uso de JANUMET en pacientes pediátricos (de 10 a 17 años) con diabetes tipo 2.
VI. CONTRAINDICACIONES
JANUMET (sitagliptina/ metformina) está contraindicado en pacientes con:
1. Insuficiencia renal grave (eGFR < 30 mL/min/1.73 m2) (ver PRECAUCIONES GENERALES, Vigilancia de la función renal).
2. Hipersensibilidad conocida al fosfato de sitagliptina, clorhidrato de metformina o a cualquier otro componente de JANUMET (ver PRECAUCIONES GENERALES, Fosfato de sitagliptina, Reacciones de hipersensibilidad y REACCIONES SECUNDARIAS Y ADVERSAS, Experiencia Posterior a la Comercialización).
3. Acidosis metabólica aguda o crónica, incluyendo cetoacidosis diabética, con o sin coma.
Se debe suspender temporalmente la administración de JANUMET en los pacientes que serán sometidos a estudios radiológicos con administración intravascular de medios de contraste yodados, porque el uso de estos productos pueden causar alteraciones agudas de la función renal (ver PRECAUCIONES GENERALES, Clorhidrato de metformina).
VII. PRECAUCIONES GENERALES
No se debe usar JANUMET en pacientes con diabetes tipo 1 ni para tratar la cetoacidosis diabética.
Pancreatitis: en pacientes que toman sitagliptina ha habido reportes de pancreatitis aguda, incluyendo pancreatitis necrotizante o hemorrágica fatal y no fatal (ver REACCIONES SECUNDARIAS Y ADVERSAS). Se debe advertir a los pacientes sobre los síntomas característicos de la pancreatitis aguda: dolor abdominal persistente y severo. Se ha observado que la pancreatitis se resuelve tras la suspensión de sitagliptina. Si se sospecha pancreatitis, se debe descontinuar JANUMET o cualquier otro medicamento que se sospeche pueda causarla.
Vigilancia de la función renal: Se sabe que la metformina y la sitagliptina son excretadas en gran parte por vía renal. El riesgo de acumulación de metformina y acidosis láctica aumenta con el grado de insuficiencia renal. JANUMET esta contraindicado en insuficiencia renal grave, pacientes con una eGFR < 30 mL/min/1.73 m2 (ver DOSIS Y VÍA DE ADMINISTRACIÓN, CONTRAINDICACIONES y PRECAUCIONES GENERALES, Clorhidrato de Metformina, Acidosis Láctica).
Antes de iniciar el tratamiento con JANUMET, y después por lo menos cada año, se debe evaluar la función renal. Si se prevé el desarrollo de insuficiencia renal, se debe medir la función renal con mayor frecuencia y suspender la administración de JANUMET si aparecen signos de insuficiencia renal.
Hipoglucemia en combinación con una sulfonilurea o con insulina: Como es típico con otros medicamentos hipoglucemiantes, se ha observado hipoglucemia en pacientes que son tratados con sitagliptina y metformina en combinación con insulina o una sulfonilurea (ver REACCIONES SECUNDARIAS Y ADVERSAS). Por ello, para reducir el riesgo de hipoglucemia inducida por sulfonilurea o por insulina, se debe considerar una dosis menor de la sulfonilurea o de la insulina (ver DOSIS Y VÍA DE ADMINISTRACIÓN).
Fosfato de sitagliptina
Hipoglucemia en combinación con una sulfonilurea o con insulina: En los estudios clínicos de sitagliptina como monoterapia o como parte del tratamiento combinado con medicamentos que se sabe causan hipoglucemia (p. ej. metformina o un agonista del PPARℽ [tiazolidinediona]), las tasas de hipoglucemia fueron similares a las observadas en los pacientes que recibieron placebo. Como es típico con otros medicamentos hipoglucemiantes, se ha observado hipoglucemia en pacientes que son tratados con sitagliptina en combinación con insulina o una sulfonilurea (ver REACCIONES SECUNDARIAS Y ADVERSAS). Por ello, para reducir el riesgo de hipoglucemia inducida por sulfonilurea o por insulina, se debe considerar una dosis menor de la sulfonilurea o de la insulina (ver DOSIS Y VÍA DE ADMINISTRACIÓN).
Reacciones de hipersensibilidad: Ha habido reportes posteriores a la comercialización de reacciones de hipersensibilidad graves en pacientes tratados con sitagliptina, uno de los componentes de JANUMET. Estas reacciones incluyen anafilaxis, angioedema, y condiciones cutáneas exfoliativas, incluyendo el síndrome de Stevens-Johnson. Como estas reacciones se reportan voluntariamente de una población de tamaño incierto, en general no es posible estimar de manera confiable su frecuencia o establecer una relación causal a la exposición al fármaco. El inicio de estas reacciones ocurrió dentro de los primeros 3 meses después del inicio del tratamiento con sitagliptina, algunos reportes ocurrieron después de la primera dosis. Si se sospecha una reacción de hipersensibilidad, suspenda JANUMET, evalúe otras causas potenciales del evento e inicie un tratamiento alternativo para la diabetes (ver CONTRAINDICACIONES y REACCIONES SECUNDARIAS Y ADVERSAS, Experiencia Posterior a la Comercialización).
Penfigoide ampolloso: Se han reportado casos posteriores a la comercialización de penfigoide ampolloso que requirieron hospitalización con el uso de inhibidores de la DPP-4. En estos casos reportados, los pacientes típicamente se recuperaron con tratamiento inmunosupresor tópico o sistémico y suspendiendo el tratamiento con el inhibidor de la DPP-4. Pida a sus pacientes reportar la aparición de ampollas o erosiones cuando estén bajo tratamiento con JANUMET. En caso de sospecha de penfigoide ampolloso se debe suspender el tratamiento con JANUMET y se debe considerar referir al paciente con el dermatólogo para diagnóstico y tratamiento apropiado.
Clorhidrato de metformina
Acidosis láctica: La acidosis láctica es una complicación metabólica rara, pero grave, que puede ocurrir debido a la acumulación de metformina durante el tratamiento con JANUMET (fosfato de sitagliptina/clorhidrato de metformina); es mortal en aproximadamente 50% de los casos. También puede ocurrir en varios estados fisiopatológicos, incluyendo diabetes mellitus, y cuando hay hipoperfusión e hipoxemia tisulares importantes. La acidosis láctica se caracteriza por concentraciones sanguíneas elevadas de lactato (>5 mmol/L), disminución del pH sanguíneo, trastornos electrolíticos con aumento de la brecha aniónica, y aumento de la relación lactato/piruvato. Cuando la metformina está implicada como causa de la acidosis láctica, generalmente sus concentraciones plasmáticas son mayores de 5 μg/mL.
La incidencia reportada de acidosis láctica en pacientes que están recibiendo clorhidrato de metformina es muy baja (aproximadamente 0.03 casos/1,000 años-paciente y aproximadamente 0.015 casos mortales por cada 1,000 años-paciente). En más de 20,000 años-paciente de exposición a la metformina en los estudios clínicos, no hubo ningún reporte de acidosis láctica. Los casos reportados han ocurrido principalmente en pacientes diabéticos con insuficiencia renal significativa, incluyendo tanto nefropatía intrínseca como hipoperfusión renal, a menudo en un cuadro de múltiples problemas médicos/quirúrgicos concomitantes y múltiples medicamentos concomitantes (ver DOSIS Y VÍA DE ADMINISTRACIÓN, Recomendaciones de uso para pacientes con Insuficiencia Renal). Los pacientes con insuficiencia cardiaca congestiva que necesitan tratamiento farmacológico, en particular aquéllos con insuficiencia cardiaca congestiva inestable o aguda que están en riesgo de hipoperfusión e hipoxemia, tienen mayor riesgo de presentar acidosis láctica. El riesgo de acidosis láctica aumenta con el grado de insuficiencia renal y con la edad del paciente. Por lo tanto, el riesgo de acidosis láctica podría disminuir significativamente vigilando regularmente la función renal de los pacientes que reciben metformina y usando la dosis mínima efectiva de la metformina. En particular, los pacientes de edad avanzada (se debe realizar una vigilancia cuidadosa de la función renal (ver más abajo Empleo en Pacientes de Edad Avanzada, Clorhidrato de metformina). Además, se debe suspender enseguida la administración de metformina si aparece cualquier trastorno asociado con hipoxemia, deshidratación o sepsis. Debido a que el deterioro de la función hepática puede limitar significativamente la capacidad para depurar lactato, generalmente se debe evitar administrar metformina a pacientes con signos clínicos o de laboratorio de hepatopatía. Los pacientes que están tomando metformina deben evitar el consumo excesivo agudo o crónico de alcohol, porque éste potencia los efectos de la metformina sobre el metabolismo del lactato. Además, se debe suspender temporalmente la administración de metformina antes de cualquier estudio radiológico con un medio de contraste intravascular o de cualquier intervención quirúrgica.
En muchos casos la acidosis láctica inicia sutilmente, acompañada sólo por síntomas inespecíficos como malestar general, mialgias, disnea, incremento de la somnolencia y malestar abdominal inespecífico. Con una acidosis mayor se pueden asociar hipotermia, hipotensión y bradiarritmias resistentes. El paciente y su médico deben tener presente la posible importancia de esos síntomas, se debe indicar al paciente que informe inmediatamente a su médico si aparecen. Se debe suspender la administración de metformina hasta aclarar la situación. Puede ser útil medir los electrólitos, cetonas séricos, glucemia y, si está indicado, el pH sanguíneo, el nivel de lactato y la concentración sanguínea de metformina. Una vez que se ha estabilizado a un paciente con determinada dosificación de metformina, es improbable que los síntomas gastrointestinales, que son comunes durante el inicio del tratamiento, estén relacionados con el medicamento. La aparición posterior de síntomas gastrointestinales puede ser debida a acidosis láctica o a otra enfermedad grave.
Las concentraciones de lactato en plasma venoso en ayunas mayores que el límite superior normal pero menores de 5 mmol/L en pacientes que están tomando metformina no indican necesariamente una inminente acidosis láctica, sino que pueden ser debidas a otros mecanismos, como diabetes mal controlada, obesidad, actividad física intensa o problemas técnicos en el manejo de las muestras.
Se debe sospechar acidosis láctica en cualquier paciente diabético con acidosis metabólica pero sin signos de cetoacidosis (cetonuria y cetonemia).
La acidosis láctica es una urgencia médica que se tiene que tratar en un hospital. En el caso de un paciente con acidosis láctica que está tomando metformina, se debe suspender inmediatamente la administración del medicamento e iniciar enseguida medidas de sostén. Dado que el clorhidrato de metformina es dializable (con una depuración de hasta 170 mL/min con buenas condiciones hemodinámicas), se recomienda una pronta hemodiálisis para corregir la acidosis y extraer la metformina acumulada. En muchos casos ese tratamiento corrige rápidamente los síntomas y acelera la recuperación (ver CONTRAINDICACIONES).
Hipoglucemia: En las circunstancias usuales de uso, los pacientes que reciben metformina sola no presentan hipoglucemia, pero ésta puede ocurrir cuando el ingreso calórico es deficiente, cuando la actividad física intensa no es compensada por complementos calóricos, o durante el uso concomitante de otros agentes que disminuyen la glucemia (como las sulfonilureas y la insulina) o de etanol. Los pacientes de edad avanzada, debilitados, desnutridos, con insuficiencia suprarrenal o hipofisiaria o con intoxicación alcohólica son particularmente propensos a los efectos hipoglucemiantes. La hipoglucemia puede ser difícil de identificar en los pacientes de edad avanzada y en las personas que están tomando bloqueadores β-adrenérgicos.
Uso concomitante de medicamentos que pueden afectar la función renal o la disposición de la metformina: Se deben usar con precaución medicamentos concomitantes que pueden afectar la función renal, causar cambios hemodinámicos significativos o interferir con la disposición de la metformina, como medicamentos catiónicos que son eliminados por secreción tubular (ver INTERACCIONES MEDICAMENTOSAS, Clorhidrato de metformina).
Estudios radiológicos con medios de contraste yodados intravasculares (p. ej. urografía o colangiografía intravenosas, angiografía, y tomografía computarizada (CT por las siglas en inglés para computed tomography) con medio de contraste intravascular: Los medios de contraste intravasculares yodados pueden causar alteraciones agudas de la función renal, y se han asociado con acidosis láctica en pacientes que recibían metformina (ver CONTRAINDICACIONES). Por lo tanto, en pacientes con una eGFR de ≥ 30 a < 60 mL/min/1.73 m2, en pacientes con antecedente de insuficiencia hepática, alcoholismo o insuficiencia cardiaca, o en pacientes que recibirán contraste yodado intra-arterial, se debe suspender temporalmente la administración de JANUMET antes o al momento y durante 48 horas después de hacer cualquiera de esos estudios, y continuarla sólo después de reevaluar la función renal y comprobar que es aceptable.
Estados hipóxicos: El colapso cardiovascular (choque) de cualquier causa, la insuficiencia cardiaca congestiva aguda, el infarto agudo al miocardio y otros trastornos caracterizados por hipoxemia se han asociado con acidosis láctica y también pueden causar hiperazoemia prerrenal. Si ocurren en pacientes bajo tratamiento con JANUMET, se debe suspender enseguida la administración de este medicamento.
Intervenciones quirúrgicas: Se debe suspender temporalmente la administración de JANUMET antes de cualquier intervención quirúrgica (excepto en operaciones menores en las que no se restringe la ingestión de alimentos y líquidos), y no se debe reiniciar hasta que el paciente haya vuelto a alimentarse por vía oral y se haya comprobado que su función renal es aceptable (ver DOSIS Y VÍA DE ADMINISTRCIÓN).
Ingestión de alcohol: Se sabe que el alcohol potencia el efecto de la metformina sobre el metabolismo del lactato. Por lo que se debe advertir a los pacientes que deben evitar el consumo excesivo agudo o crónico de alcohol mientras están recibiendo JANUMET.
Deterioro de la función hepática: Como el deterioro de la función hepática se ha asociado con algunos casos de acidosis láctica, generalmente se debe evitar administrar JANUMET a pacientes con signos clínicos o de laboratorio de hepatopatía.
Concentraciones de vitamina B12: En estudios clínicos controlados de metformina de 29 semanas de duración se observó en aproximadamente 7% de los pacientes una disminución hasta valores subnormales de las concentraciones séricas previamente normales de vitamina B12, sin manifestaciones clínicas. Sin embargo, esa disminución, debida posiblemente a la interferencia de la absorción de esa vitamina a partir del complejo B12-factor intrínseco, muy rara vez se acompaña de anemia y cesa rápidamente al suspender la administración de metformina o al administrar vitamina B12. Se recomienda medir los parámetros hematológicos cada año en los pacientes tratados con JANUMET, para investigar y tratar apropiadamente cualquier anormalidad que se encuentre.
Algunas personas (con ingestión o absorción insuficiente de vitamina B12 o de calcio) tienden a presentar concentraciones subnormales de vitamina B12 en el suero. Puede ser útil medir esas concentraciones cada dos a tres años en esos pacientes.
Cambios en el estado clínico de pacientes con diabetes tipo 2 previamente controlada: Un paciente con diabetes tipo 2 que ya estaba controlada con JANUMET y presenta anormalidades de laboratorio o datos clínicos de enfermedad (especialmente si sus trastornos son vagos y mal definidos) debe ser evaluado pronto en busca de signos de cetoacidosis o de acidosis láctica. Esta evaluación debe incluir medición de electrólitos y cetonas séricos, glucemia y, si está indicado, pH sanguíneo, concentraciones de lactato, piruvato y metformina. Si hay acidosis, se debe suspender inmediatamente la administración de JANUMET e iniciar las medidas correctivas apropiadas.
Pérdida del control de la glucemia: Cuando un paciente que está controlado con cualquier régimen antidiabético se ve expuesto a estrés como fiebre, traumatismo, infección o cirugía, se puede perder durante cierto tiempo el control de la glucemia. Puede ser necesario suspender la administración de JANUMET y administrar insulina temporalmente. Una vez resuelto ese episodio agudo, se puede reanudar el tratamiento con JANUMET.
Efectos sobre la Capacidad de Conducir y utilizar Maquinaria
No se han realizado estudios de los efectos de JANUMET sobre la capacidad para conducir y utilizar máquinas. Sin embargo, no se espera que JANUMET afecte la capacidad de conducir y usar máquinas.
Empleo en niños
La seguridad y eficacia de la adición de sitagliptina en pacientes pediátricos de 10 a 17 años con diabetes tipo 2 y control inadecuado de la glucemia con metformina con o sin insulina se evaluó en dos estudios durante 54 semanas. La adición de sitagliptina (administrada como JANUMET) se comparó con la adición de placebo a metformina.
Si bien se demostró la superioridad de la reducción de HbA1c para JANUMET sobre la metformina en la semana 20 en el análisis agrupado de estos dos estudios, los resultados de los estudios individuales fueron inconsistentes. Además, la eficacia de JANUMET sobre metformina no se observó en la semana 54. Por lo tanto, estos resultados no apoyan el uso de JANUMET en sujetos pediátricos (de 10 a 17 años) con diabetes tipo 2.
En pacientes pediátricos de 10 a 17 años con diabetes tipo 2, el perfil de efectos secundarios fue comparable al observado en adultos.
JANUMET no se ha estudiado en pacientes pediátricos menores de 10 años.
Empleo en pacientes de edad avanzada
JANUMET
Como la sitagliptina y la metformina son excretadas en gran parte por los riñones y el envejecimiento se puede asociar con una disminución de la función renal, JANUMET se debe usar con precaución conforme se envejece. Se debe escoger con cuidado la dosificación, basándose en una vigilancia cuidadosa y regular de la función renal (ver arriba Vigilancia de la función renal).
Fosfato de sitagliptina
En los estudios clínicos, la seguridad y la eficacia de la sitagliptina en pacientes de edad avanzada (≥65 años) fueron similares a las observadas en los de menor edad (<65 años).
Clorhidrato de metformina
Los estudios clínicos controlados de metformina no incluyeron suficientes pacientes de edad avanzada para determinar si responden de modo diferente de como lo hacen los de menor edad, aunque en otra experiencia clínica reportada no se han identificado diferencias en las respuestas entre los dos grupos de edad.
VIII. RESTRICCIONES DE USO DURANTE EL EMBARAZO Y LA LACTANCIA
EMBARAZO
No hay estudios suficientes y bien controlados en mujeres embarazadas con JANUMET o con sus componentes individuales; por lo tanto, no se conoce la seguridad de JANUMET en ellas. Como otros agentes hipoglucemiantes orales, no se recomienda emplear JANUMET durante el embarazo.
No se han hecho estudios en animales con los componentes combinados de JANUMET para evaluar sus efectos sobre la reproducción. Los datos siguientes están basados en los resultados de estudios realizados con sitagliptina o metformina individualmente.
Fosfato de sitagliptina
La sitagliptina no fue teratogénica en ratas a dosis orales de hasta 250 mg/kg ni en conejas que recibieron hasta 125 mg/kg durante la organogénesis (dosis hasta 32 y 22 veces mayores, respectivamente, que la exposición en humanos, basándose en la dosis diaria recomendada en adultos de 100 mg diarios). En las ratas aumentó ligeramente la incidencia de malformaciones costales en los fetos (costillas ausentes, hipoplásicas u onduladas) con la dosificación de 1,000 mg/kg/día (aproximadamente 100 veces la exposición en seres humanos, basándose en la dosis diaria recomendada en adultos de 100 mg diarios). En las crías de las ratas que recibieron dosis orales de 1,000 mg/kg/día se observó una pequeña disminución del promedio de peso corporal antes del destete en ambos sexos y del promedio de aumento de peso después del destete en los machos. Sin embargo, los estudios de reproducción en animales no siempre pronostican la respuesta en los seres humanos.
Clorhidrato de metformina
La metformina no fue teratogénica en ratas y conejas a dosificaciones de hasta 600 mg/kg/día. Esto representa una exposición aproximadamente 2 y 6 mayor, respectivamente, que la dosis diaria máxima recomendada en los seres humanos de 2,000 mg, basándose en el área de superficie corporal. Las concentraciones en los fetos demostraron una barrera placentaria parcial contra la metformina.
LACTANCIA
No se han hecho estudios en hembras lactantes con los componentes combinados de JANUMET. En estudios realizados con los componentes individuales, tanto la sitagliptina como la metformina fueron secretadas en la leche de las ratas lactantes. No se sabe si la sitagliptina es secretada en la leche humana. Por lo tanto, no se debe administrar JANUMET a una mujer que está amamantando.
IX. REACCIONES SECUNDARIAS Y ADVERSAS
En estudios clínicos controlados con placebo en pacientes con diabetes mellitus tipo 2, la combinación de sitagliptina y metformina generalmente fue bien tolerada. La incidencia general de reacciones secundarias reportada en los pacientes que recibieron la combinación de sitagliptina y metformina fue similar a la reportada en los pacientes que recibieron la combinación de placebo y metformina.
Tratamiento Combinado con Sitagliptina y Metformina
Tratamiento Inicial
En un estudio factorial de 24 semanas, controlado con placebo, de tratamiento inicial con sitagliptina 50 mg dos veces al día en combinación con metformina 500 ó 1,000 mg dos veces al día, los eventos adversos relacionados con el medicamento reportados en ≥1% de los pacientes que recibieron el tratamiento combinado (y mayor a los que recibieron placebo) se muestran en la Tabla 7.
Tabla 7: Tratamiento Inicial con la Combinación de Sitagliptina y Metformina: Reacciones Adversas Relacionadas con el Medicamento Reportadas en ≥1% de los Pacientes que recibieron el Tratamiento Combinado (y mayor a los que recibieron Placebo)†
|
Número de Pacientes (%) |
||||
|
Placebo |
Sitagliptina 100 mg una vez al día |
Metformina 500 o 1,000 mg b.i.d.†† |
Sitagliptina 50 mg b.i.d. + Metformina 500 o 1,000 mg b.i.d.†† |
|
|
N = 176 |
N = 179 |
N = 364 |
N = 372 |
|
|
Diarrea |
2 (1.1) |
0 (0.0) |
12 (3.3) |
13 (3.5) |
|
Náusea |
1 (0.6) |
0 (0.0) |
9 (2.5) |
6 (1.6) |
|
Dispepsia |
0 (0.0) |
0 (0.0) |
4 (1.1) |
5 (1.3) |
|
Flatulencia |
0 (0.0) |
0 (0.0) |
2 (0.5) |
5 (1.3) |
|
Vómito |
0 (0.0) |
0 (0.0) |
1 (0.3) |
4 (1.1) |
|
Cefalea |
0 (0.0) |
1 (0.6) |
4 (1.1) |
5 (1.3) |
|
Hipoglucemia |
0 (0.0) |
1 (0.6) |
2 (0.5) |
4 (1.1) |
† Población con intención de tratar
†† Datos combinados de los pacientes que recibieron las dosis menores y máximas de metformina
Tratamiento Combinado de Adición a Metformina
En un estudio de 24 semanas, controlado con placebo, en el que se añadió sitagliptina a tratamiento en curso con metformina, 464 pacientes recibieron metformina y 100 mg una vez al día de sitagliptina y 237 recibieron placebo y metformina. La única reacción adversa reportada relacionada con el medicamento que ocurrió con una incidencia ≥1% y mayor que con placebo en los que recibieron sitagliptina y metformina fue náusea (1.1% con 100 mg de sitagliptina y metformina, 0.4% con placebo y metformina).
Hipoglucemia y Reacciones Adversas Gastrointestinales
En los estudios controlados con placebo de tratamiento combinado con sitagliptina y metformina, la incidencia de hipoglucemia (independientemente de la causalidad atribuida por el investigador) reportada en los pacientes que recibieron la combinación de sitagliptina y metformina fue similar a la reportada para los pacientes tratados con metformina y placebo. La incidencia de reacciones adversas gastrointestinales preespecificadas en pacientes tratados con la combinación de sitagliptina y metformina fue similar a la reportada para los pacientes tratados con metformina sola. Ver Tabla 8.
Tabla 8: Hipoglucemia y reacciones adversas gastrointestinales preespecificadas (independientemente de la causalidad atribuida por el investigador) reportadas en los pacientes que recibieron tratamiento combinado†
|
Número de pacientes (%) |
||||||
|
Estudio de sitagliptina y metformina como tratamiento inicial |
Estudio de adición de sitagliptina a tratamiento actual con metformina |
|||||
|
Placebo |
Sitagliptina 100 mg una vez al día |
Metformina 500 ó 1,000 mg dos veces al día†† |
Sitagliptina 50 mg dos veces al día + Metformina 500 ó 1,000 mg dos veces al día†† |
Placebo y Metformina ≥1,500 mg diarios |
Sitagliptina 100 mg diarios y Metformina ≥1,500 mg diarios |
|
|
N = 176 |
N = 179 |
N = 364 |
N = 372 |
N = 237 |
N = 464 |
|
|
Hipoglucemia |
1 (0.6) |
1 (0.6) |
3 (0.8) |
6 (1.6) |
5 (2.1) |
6 (1.3) |
|
Diarrea |
7 (4.0) |
5 (2.8) |
28 (7.7) |
28 (7.5) |
6 (2.5) |
11 (2.4) |
|
Náusea |
2 (1.1) |
2 (1.1) |
20 (5.5) |
18 (4.8) |
2 (0.8) |
6 (1.3) |
|
Vómito |
1 (0.6) |
0 (0.0) |
2 (0.5) |
8 (2.1) |
2 (0.8) |
5 (1.1) |
|
Dolor abdominal |
4 (2.3) |
6 (3.4) |
14 (3.8) |
11 (3.0) |
9 (3.8) |
10 (2.2) |
† En el estudio de tratamiento inicial, el malestar abdominal fue incluido en dolor abdominal
†† Datos combinados de los pacientes que recibieron las dosis menores y máximas de metformina
En todos los estudios las reacciones adversas de hipoglucemia se basaron en todos los reportes de hipoglucemia sintomática; no se requirió hacer una medición de la glucosa.
Sitagliptina en Combinación con Metformina y una Sulfonilurea
En un estudio controlado con placebo de 24 semanas de sitagliptina 100 mg diarios añadidos a la combinación con glimepirida ≥4 mg diarios y metformina ≥1,500 mg diarios, las reacciones adversas relacionadas con el medicamento reportadas en ≥1% de los pacientes tratados con sitagliptina (n=116) y más común que en los pacientes tratados con placebo (n=113) fueron hipoglucemia (sitagliptina 13.8%, placebo 0.9%) y estreñimiento (1.7%, 0.0%).
Sitagliptina en Combinación con Metformina y un Agonista PPARℽ
En un estudio controlado con placebo de sitagliptina 100 mg diarios añadidos al tratamiento combinado en curso de metformina y rosiglitazona, las reacciones adversas relacionadas con el medicamento reportadas durante el punto de tiempo primario a la semana 18 en ≥1% de los pacientes tratados con sitagliptina (n=170) y más comúnmente que en los pacientes tratados con placebo (n=92) fueron: cefalea (sitagliptina, 2.4%; placebo, 0.0%), diarrea (1.8%, 1.1%), náusea (1.2%, 1.1%), hipoglucemia (1.2%, 0.0%), y vómito (1.2%, 0.0%). A la semana 54, las reacciones adversas relacionadas con el medicamento reportadas en ≥1% de los pacientes tratados con sitagliptina y más comúnmente que en los pacientes tratados con placebo fueron: cefalea (2.4%, 0.0%), hipoglucemia (2.4%, 0.0%), infección del tracto respiratorio superior (1.8%, 0.0%), náusea (1.2%, 1.1%), tos (1.2%, 0.0%), infecciones fúngicas cutáneas (1.2%, 0.0%), edema periférico (1.2%, 0.0%), y vómito (1.2%, 0.0%).
Sitagliptina en Combinación con Metformina e Insulina
En un estudio controlado con placebo de 24 semanas con sitagliptina 100 mg añadida en combinación al tratamiento en curso con metfomina ≥1,500 mg diarios y una dosis estable de insulina, la única reacción adversa relacionada con el medicamento reportada en ≥1% de los pacientes tratados con sitagliptina (n=229) y más comúnmente que en los pacientes tratados con placebo (n=233) fue hipoglucemia (sitagliptina, 10.9%; placebo, 5.2%). En otro estudio de 24 semanas los pacientes recibieron sitagliptina como tratamiento adicional mientras se intensificaba la isulina (con o sin metformina), la única reacción adversa relacionada con el fármaco reportada en ≥1% de los pacientes tratados con sitagliptina y metformina y con mayor frecuencia que en los pacientes tratados con placebo y metformina fue el vómito (sitagliptina y metformina, 1.1% , placebo y metformina 0.4%)
Pancreatitis
En un análisis combinado de 19 estudios clínicos doble ciego que incluyó datos de 10,246 pacientes aleatorizados a recibir sitagliptina 100 mg/día (N= 5,429) o el correspondiente control (tratamiento activo o placebo), (N= 4,817), la incidencia de eventos no adjudicados de pancreatitis aguda fue 0.1 por 100 años-paciente en cada grupo (4 pacientes con un evento en 4,708 años-paciente para sitagliptina y 4 pacientes con un evento en 3,942 años-paciente para el grupo control). Ver también más adelante Estudio de Seguridad Cardiovascular TECOS (Ver PRECAUCIONES GENERALES, Pancreatitis).
Con la combinación de sitagliptina y metformina no se observaron cambios clínicamente significativos en los signos vitales o en el EKG (incluyendo el intervalo QT).
Reacciones Adversas Reportadas con Sitagliptina
No hubo reportes de reacciones adversas relacionadas con el medicamento con una incidencia ≥1% en los pacientes que recibieron sitagliptina.
Reacciones Adversas Reportadas con Metformina
Las reacciones adversas reportadas (independientemente de la causalidad) en más del 5% de los pacientes tratados con metformina y con más frecuencia que en los pacientes tratados con placebo son diarrea, náusea/vómito, flatulencia, astenia, indigestión, malestar abdominal y cefalea.
Estudio de Seguridad Cardiovascular TECOS
El Estudio para Evaluar los Desenlaces Cardiovasculares con Sitagliptina (TECOS) incluyó a 7,332 pacientes tratados con sitagliptina, a 100 mg diarios (o 50 mg diarios si la tasa de filtración glomerular basal estimada (eGFR) era ≥30 y <50 mL/min/1.73 m2), y 7,339 pacientes tratados con placebo en la población con intención de tratar. Ambos tratamientos se añadieron al cuidado usual, apuntando a estándares regionales para HbA1c y factores de riesgo CV. La población de estudio incluyó un total de 2,004 pacientes ≥75 años de edad (970 tratados con sitagliptina y 1,034 tratados con placebo). La incidencia global de reacciones adversas graves en los pacientes que recibieron sitagliptina fue similar a la de los pacientes que recibieron placebo. La evaluación de complicaciones relacionadas con la diabetes preespecificadas reveló incidencias similares entre los grupos, incluyendo infecciones (18.4% de los pacientes tratados con sitagliptina y 17.7% de los pacientes tratados con plabeo) e insuficiencia renal (1.4% de los pacientes tratados con sitagliptina y 1.5% de los pacientes tratados con plabeo). El perfil de eventos adversos en los pacientes ≥75 años de edad fue generalmente similar al de la población general.
En la población con intención de tratar, entre los pacientes que estaban usando insulina y/o una sulfonilurea a nivel basal, la incidencia de hipoglucemia grave fue de 2.7% en los pacientes tratados con sitagliptina y 2.5% en los pacientes tratados con placebo, entre los pacientes que no estaban usando insulina y/o una sulfonilurea a nivel basal, la incidencia de hipoglucemia grave fue de 1.0% en los pacientes tratados con sitagliptina y de 0.7% en los pacientes tratados con placebo. La incidencia de eventos de pancreatitis con adjudicación confirmada fue de 0.3% en los pacientes tratados con sitagliptina y de 0.2% en los pacientes tratados con placebo. La incidencia de eventos de malignidad con adjudicación confirmada fue de 3.7% en los pacientes tratados con sitagliptina y de 4.0% en los pacientes tratados con placebo.
Población pediátrica
En un análisis agrupado de dos ensayos clínicos controlados con placebo con JANUMET en pacientes pediátricos de 10 a 17 años con diabetes tipo 2, las reacciones adversas relacionadas con el medicamento notificadas durante el período de tratamiento de 54 semanas en ≥1% de los pacientes en el grupo de JANUMET (N = 107) y con mayor frecuencia que en los pacientes del grupo de metformina (N = 113) fue diarrea (2.8%; Metformin, 0.9%)), náuseas (2.8%, 0.9%), e hipoglucemia (6.5%, 3.5%).
El perfil de las reacciones adversas fue comparable al observado en adultos. No hubo diferencias clínicamente relevantes entre los grupos de JANUMET y metformina hasta la semana 54 en los criterios de valoración de seguridad de laboratorio, signos vitales, índices de adiposidad o criterios de valoración de crecimiento y desarrollo.
Experiencia Posterior a la Comercialización
Durante el uso posterior a la comercialización de JANUMET o sitagliptina, uno de los componentes de JANUMET se ha identificado reacciones adversas adicionales. Estas reacciones han sido reportadas cuando JANUMET o sitagliptina se utilizaron como monoterapia o en combinación con otros medicamentos hipoglucemiantes. Como estas reacciones se reportaron voluntariamente de una población de tamaño incierto, generalmente no es posible estimar de manera confiable su frecuencia o establecer una relación causal a la exposición del medicamento.
Reacciones de hipersensibilidad incluyendo anafilaxis, angioedema, erupción cutánea, urticaria, vasculitis cutánea, y condiciones cutáneas exfoliativas incluyendo el síndrome de Stevens-Johnson (ver CONTRAINDICACIONES y PRECAUCIONES GENERALES, Fosfato de sitagliptina, Reacciones de hipersensibilidad); pancreatitis aguda, incluyendo pancreatitis necrotizante o hemorrágica fatal y no fatal (ver PRECAUCIONES GENERALES, Pancreatitis); deterioro de la función renal, incluyendo insuficiencia renal aguda (algunas veces requiriendo diálisis); penfigoide ampolloso (ver PRECAUCIONES GENERALES, penfigoide ampolloso); infección de vías respiratorias superiores; nasofaringitis; estreñimiento, vómito, cefalea; artralgia, mialgia, dolor en las extremidades, dolor de espalda, prurito.
X. INTERACCIONES MEDICAMENTOSAS Y DE OTRO GÉNERO
Sitagliptina y Metformina
La coadministración de dosis múltiples de sitagliptina (50 mg dos veces al día) y metformina (1,000 mg dos veces al día) no alteró significativamente la farmacocinética de sitagliptina o metformina en pacientes con diabetes tipo 2.
No se han hecho estudios de interacción farmacocinética con JANUMET, pero sí se han hecho estudios con los componentes individuales de JANUMET (fosfato de sitagliptina y clorhidrato de metformina).
Fosfato de sitagliptina
En los estudios de interacciones farmacológicas, la sitagliptina no tuvo efectos de importancia clínica sobre la farmacocinética de los siguientes medicamentos: metformina, rosiglitazona, gliburida, simvastatina, warfarina y anticonceptivos orales. Según esos datos, la sitagliptina no inhibe las isoenzimas 3A4, 2C8 o 2C9 del citocromo P-450 (CYP). Basándose en los datos in vitro, no es de esperarse que inhiba las isoenzimas CYP2D6, 1A2, 2C19 Y 2B6, ni que induzca a CYP3A4.
Se han realizado análisis de farmacocinética de población en pacientes con diabetes tipo 2. Los medicamentos administrados concomitantemente no tuvieron un efecto clínicamente importante en la farmacocinética de sitagliptina. Los medicamentos evaluados fueron aquellos que comúnmente se administran a pacientes con diabetes tipo 2, incluyendo reductores de colesterol (p. ej., estatinas, fibratos, ezetimiba), antiplaquetarios (p. ej., clopidogrel), antihipertensivos (p. ej., inhibidores de la ECA, bloqueadores de los receptores de angiotensina, beta-bloqueadores, antagonistas de canales de calcio, hidroclorotiazida), analgésicos y anti-inflamatorios no esteroideos (p. ej., naproxeno, diclofenaco, celecoxib), antidepresivos (p. ej., bupropión, fluoxetina, sertralina), antihistamínicos (p. ej., cetrizina), inhibidores de la bomba de protones (p. ej., omeprazol, lansoprazol) y medicamentos para disfunción eréctil (p. ej., sildenafil).
Al administrar concomitantemente sitagliptina y digoxina, aumentaron ligeramente el área bajo la curva de concentración (AUC, 11%) y el promedio de concentración máxima (Cmáx, 18%) de la digoxina. No se considera que esos aumentos tengan importancia clínica. Se debe vigilar apropiadamente a los pacientes que estén recibiendo digoxina. El AUC y la Cmáx de la sitagliptina aumentaron aproximadamente 29% y 68%, respectivamente, al administrar concomitantemente dosis orales únicas de 100 mg de JANUVIA® y de 600 mg de ciclosporina, que es un potente inhibidor de prueba de la glucoproteína-p. No se considera que esos cambios observados en la farmacocinética de la sitagliptina tengan importancia clínica.
Clorhidrato de metformina
Gliburida: En un estudio sobre interacción de dosis únicas en pacientes con diabetes tipo 2, la administración concomitante de metformina y gliburida no causó ningún cambio en la farmacocinética o la farmacodinámica de la metformina. Se observaron disminuciones del AUC y de la Cmáx de la gliburida, pero esas disminuciones fueron muy variables. Debido a que fue un estudio con dosis únicas y a la falta de correlación entre las concentraciones sanguíneas de gliburida y los efectos farmacodinámicos, es incierta la importancia clínica de esta interacción.
Furosemida: Un estudio sobre la interacción de dosis únicas de metformina y furosemida en sujetos sanos demostró que la administración concomitante afectó los parámetros farmacocinéticos de ambos compuestos. La furosemida aumentó 22% la Cmáx plasmática y sanguínea y 15% el AUC sanguínea de la metformina, sin ningún cambio significativo en la depuración renal de metformina. Cuando se administró concomitantemente con metformina, la Cmáx y el AUC de la furosemida fueron 31% y 12% menores, respectivamente, que cuando se administró sola, y su vida media terminal disminuyó 32%, sin ningún cambio significativo en su depuración renal de furosemida. No hay información disponible acerca de la interacción de la metformina y la furosemida cuando se administran concomitantemente por tiempo prolongado.
Nifedipina: Un estudio sobre la interacción de dosis únicas de metformina y nifedipina en sujetos sanos demostró que la administración concomitante de nifedipina aumentó 20% la Cmáx y 9% el ABC de la metformina, así como la cantidad de metformina excretada en la orina. Su Tmáx y su vida media no se modificaron. La nifedipina aumenta la absorción de metformina. Metformina tuvo efectos mínimos sobre la nifedipina.
Medicamentos que reducen la depuración de metformina: El uso concomitante de medicamentos que interfieren con los sistemas comunes de transporte tubular renal, involucrados en la eliminación renal de la metformina (p. ej. Transportador-2 de cationes orgánicos [OCT2], por las siglas en inglés para organic cationic transporter-2] / inhibidores de extrusión de múltiples fármacos y toxinas [MATE, por las siglas en inglés para multidrug and toxin extrusion] tales como ranolazina, vandetanib, dolutegravir y cimetidina), pueden incrementar la exposición sistémica a la metformina y puede aumentar el riesgo de acidosis láctica. Se debe considerar los beneficios y los riesgos de tratamientos concomitantes.
Otros: Ciertos medicamentos tienden a producir hiperglucemia y pueden impedir el control de la glucemia. Esos medicamentos incluyen las tiacidas y otros diuréticos, corticosteroides, fenotiacinas, productos tiroideos, estrógenos, anticonceptivos orales, fenitoína, ácido nicotínico, simpaticomiméticos, bloqueadores de canales de calcio y la isoniacida. Cuando se administra alguno de esos medicamentos a un paciente que está tomando JANUMET, se le debe vigilar estrechamente para controlar bien su glucemia.
En estudios de interacción con dosis únicas en voluntarios sanos, la administración concomitante de metformina y propranolol o de metformina e ibuprofeno no afectó la farmacocinética de esos medicamentos.
A diferencia de las sulfonilureas, que se unen en gran proporción a las proteínas plasmáticas, la metformina se une escasamente a ellas, por lo que es menos probable que interactúe con medicamentos que se unen altamente a las proteínas plasmáticas, como los salicilatos, las sulfonamidas, el cloranfenicol y el probenecid.
XI. ALTERACIONES EN LOS RESULTADOS DE PRUEBAS DE LABORATORIO
Fosfato de sitagliptina
La incidencia de reacciones adversas de laboratorio fue similar en los pacientes tratados con sitagliptina y metformina comparado con los pacientes tratados con placebo y metformina. A lo largo de esos estudios se observó un pequeño aumento del número de leucocitos (WBC, por las siglas en inglés para white blood cell) una diferencia de aproximadamente 200 células/μl en las WBC en comparación con el placebo; cuenta promedio basal de WBC de aproximadamente 6,600 células/μl), debido a un pequeño aumento de los neutrófilos. Esta observación se ha observado en la mayoría pero no en todos los estudios. Este cambio en los parámetros de laboratorio no se considera clínicamente importante.
Clorhidrato de metformina
En estudios clínicos controlados de metformina de 29 semanas de duración, se observó una disminución a valores subnormales de las concentraciones séricas previas normales de vitamina B12, sin manifestaciones clínicas, en aproximadamente 7% de los pacientes. Sin embargo, esa disminución debida posiblemente a la interferencia de la absorción de esa vitamina a partir del complejo B12-factor intrínseco muy rara vez se acompaña de anemia y parece ser rápidamente reversible al suspender la administración de metformina o al administrar vitamina B12 (ver PRECAUCIONES GENERALES, Clorhidrato de metformina).
XIII. DOSIS Y VÍA DE ADMINISTRACIÓN
Vía de administración: Oral
General
La dosificación del tratamiento hipoglucemiante con JANUMET se debe individualizar basándose en el tratamiento actual del paciente, la eficacia y la tolerabilidad, sin exceder las dosis diarias máximas recomendadas de 100 mg de sitagliptina.
Generalmente JANUMET se debe administrar dos veces al día con alimentos, aumentando gradualmente la dosis para disminuir los efectos colaterales gastrointestinales (GI) asociados a metformina.
Recomendaciones sobre la dosificación
La dosis inicial de JANUMET se debe basar en el tratamiento actual del paciente. JANUMET se debe administrar dos veces al día con alimentos. Los comprimidos de JANUMET están disponibles en:
• 50 mg de sitagliptina / 500 mg de clorhidrato de metformina
• 50 mg de sitagliptina / 850 mg de clorhidrato de metformina
• 50 mg de sitagliptina / 1,000 mg de clorhidrato de metformina
Tratamiento inicial:
En pacientes con diabetes mellitus tipo 2 con hiperglucemia inadecuadamente controlada solamente con dieta y ejercicio, la dosis inicial total diaria recomendada de JANUMET es de 100 mg de sitagliptina/1,000 mg de clorhidrato de metformina. En los pacientes con control glucémico inadecuado a esta dosis, se puede escalar gradualmente para reducir los efectos adversos gastrointestinales (GI) asociados con metformina, hasta la dosis máxima diaria recomendada de metformina de 2,000 mg.
Para pacientes inadecuadamente controlados con la monoterapia con metformina:
En los pacientes en los que metformina sola no controla suficientemente la glucemia, la dosis inicial total recomendada de JANUMET es de 100 mg de sitagliptina y la dosis previamente prescrita de metformina
Para pacientes inadecuadamente controlados con la monoterapia con sitagliptina:
En los pacientes en los que sitagliptina sola no controla suficientemente la glucemia, la dosificación inicial recomendada de JANUMET es de 100 mg de sitagliptina y 1,000 mg de clorhidrato de metformina. La dosis de metformina puede ser escalada gradualmente conforme sea necesario para lograr el control glucémico. Se debe considerar escalar gradualmente la dosis para reducir los efectos adversos gastrointestinales (GI) asociados con metformina. A los pacientes que están tomando sitagliptina sola a una dosificación ajustada por insuficiencia renal no se les debe cambiar a JANUMET (ver CONTRAINDICACIONES).
Para pacientes que están tomando sitagliptina coadministrada con metformina:
En los pacientes que están tomando sitagliptina y metformina por separado, se puede iniciar la administración de JANUMET a la dosis previamente prescrita de sitagliptina y metformina.
Para pacientes inadecuadamente controlados con la combinación de tratamiento dual con cualquiera de dos de los siguientes tres medicamentos hipoglucemiantes: sitagliptina, metformina o una sulfonilurea:
La dosificación inicial usual de JANUMET debe procurar 50 mg de sitagliptina dos veces al día (100 mg dosis total diaria de sitagliptina). Para determinar la dosis inicial del componente metformina se debe considerar el nivel de control glucémico del paciente y la dosis actual (si la hay) de metformina. Para reducir los efectos gastrointestinales (GI) asociados a metformina se debe considerar ajustar la dosis gradualmente. Los pacientes que inician o que actualmente toman una sulfonilurea pueden requerir una dosis menor de la sulfonilurea para reducir el riesgo de hipoglucemia inducida por sulfonilureas (ver PRECAUCIONES GENERALES).
Para pacientes inadecuadamente controlados con la combinación de tratamiento dual con cualquiera de dos de los siguientes tres medicamentos: sitagliptina, metformina o un agonista del PPARℽ (p. ej., tiazolidinedionas):
La dosificación inicial usual de JANUMET debe procurar 100 mg dosis total diaria de sitagliptina. Para determinar la dosis inicial del componente metformina se debe considerar el nivel de control glucémico del paciente y la dosis actual (si la hay) de metformina. Para reducir los efectos gastrointestinales (GI) asociados a metformina se debe considerar ajustar la dosis gradualmente.
Para pacientes inadecuadamente controlados con la combinación de tratamiento dual con cualquiera de dos de los siguientes tres medicamentos: sitagliptina, metformina o insulina:
La dosificación inicial usual de JANUMET debe procurar 100 mg dosis total diaria de sitagliptina. Para determinar la dosis inicial del componente metformina se debe considerar el nivel de control glucémico del paciente y la dosis actual (si la hay) de metformina. Para reducir los efectos gastrointestinales (GI) asociados a metformina se debe considerar ajustar la dosis gradualmente. Los pacientes con insulina o que la están iniciando pueden requerir dosis menores de ésta para reducir el riesgo de hipoglucemia (ver PRECAUCIONES GENERALES).
No se han hecho estudios examinando específicamente la seguridad y la eficacia de JANUMET en pacientes que estaban siendo tratados con otros agentes hipoglucemiantes y fueron cambiados a JANUMET. Cualquier cambio en el tratamiento de la diabetes tipo 2 se debe hacer con precaución y vigilancia adecuada, porque pueden ocurrir cambios en el control de la glucemia.
Recomendaciones de uso en pacientes con Insuficiencia Renal:
Se debe evaluar la función renal antes de iniciar el tratamiento con JANUMET y periódicamente después de iniciarlo.
JANUMET está contraindicado en pacientes con una eGFR < 30 mL/min/1.73 m2.
El uso de JANUMET no se recomienda en pacientes con una eGFR ≥ 30 mL/min/1.73 m2 y < 45 mL/min/1.73 m2 debido a que estos pacientes requieren una dosis inferior de sitagliptina, la cual, no está disponible para la presentación combinada de JANUMET.
Interrupción del tratamiento con JANUMET por procedimientos de imagenología con contraste yodado
Se debe descontinuar JANUMET al momento, o previo a un procedimiento de imagenología que involucre contraste yodado en pacientes con una eGFR de ≥ 30 a < 60 mL/min/1.73 m2, en pacientes con antecedente de enfermedad hepática, alcoholismo o insuficiencia cardiaca, o en pacientes que recibirán contraste yodado intraarterial. Se debe reevaluar la eGFR a las 48 horas después al procedimiento de imagenología, el tratamiento con JANUMET se puede restablecer si la función renal es aceptable (ver PRECAUCIONES GENERALES).
XIV. MANIFESTACIONES Y MANEJO DE LA SOBREDOSIFICACIÓN O INGESTA ACCIDENTAL
Fosfato de sitagliptina
Durante los estudios clínicos controlados en sujetos sanos, dosis únicas de hasta 800 mg de sitagliptina fueron generalmente bien toleradas. En un estudio se observaron aumentos mínimos del QTc, que no se consideraron clínicamente importantes, con la dosis de 800 mg (ver FARMACOCINÉTICA Y FARMACODINAMIA, Farmacodinamia, Electrofisiología cardiaca). No hay ninguna experiencia con dosis mayores de 800 mg en estudios clínicos. En estudios de Fase I de dosis múltiple, no se observaron reacciones adversas clínicas relacionadas con el medicamento con dosis de sitagliptina de hasta 600 mg por día durante periodos de hasta 10 días y 400 mg al día por periodos de hasta 28 días.
Si ocurre una sobredosis, es razonable emplear las medidas de soporte usuales, como retirar del tracto digestivo el medicamento no absorbido, aplicar monitoreo clínico (incluyendo electrocardiograma) y establecer tratamiento de sostén si es necesario.
La sitagliptina es poco dializable. En los estudios clínicos se extrajo aproximadamente 13.5% de la dosis durante una sesión de hemodiálisis de tres a cuatro horas. Se puede considerar hemodiálisis prolongada si es clínicamente apropiada. No se sabe si la sitagliptina es dializable por diálisis peritoneal.
Clorhidrato de metformina
Se han reportado sobredosis de clorhidrato de metformina, incluyendo la ingesta de más de 50 gramos. Se reportó hipoglucemia en aproximadamente 10% de los casos, pero no se ha determinado ninguna relación causal con el clorhidrato de metformina. Se ha reportado acidosis láctica en aproximadamente 32% de los casos de sobredosificación de metformina (ver PRECAUCIONES GENERALES, Clorhidrato de metformina). La metformina es dializable, con una depuración de hasta 170 mL/min en buenas condiciones hemodinámicas. Por lo tanto, la hemodiálisis puede ser útil para extraer el medicamento acumulado en los pacientes en los que se sospecha una sobredosificación de metformina.
XII. PRECAUCIONES EN RELACIÓN CON EFECTOS DE CARCINOGÉNESIS, MUTAGÉNESIS, TERATOGÉNESIS Y SOBRE LA FERTILIDAD
Carcinogenicidad
Fosfato de sitagliptina
Se hizo un estudio de dos años sobre la carcinogenicidad en ratas macho y hembra que recibieron dosis orales de sitagliptina de 50, 150 y 500 mg/kg/día. Con la dosificación mayor hubo un aumento de la incidencia de adenomas y carcinomas hepáticos en los machos y de carcinomas hepáticos en las hembras. Esta exposición en ratas resulta aproximadamente 58 veces mayor que en los seres humanos, basándose en la dosis diaria recomendada en adultos de 100 mg/día. Esa dosificación se asoció con hepatotoxicidad en las ratas. La dosificación con la que no se observó ninguna inducción de neoplasias hepáticas fue la de 150 mg/kg/día, aproximadamente 19 veces la exposición en humanos con la dosis recomendada de 100 mg. Como se ha mostrado que en las ratas la hepatotoxicidad está correlacionada con la inducción de neoplasias hepáticas, ese aumento de la incidencia de tumores hepáticos es probablemente secundario a toxicidad hepática crónica a esa alta dosificación. Se desconoce la importancia clínica de esos resultados para los humanos.
Se hizo un estudio de dos años sobre la carcinogenicidad en ratones macho y hembra, con dosis orales de sitagliptina de 50, 125, 250 y 500 mg/kg/día. La sitagliptina no aumentó la incidencia de tumores de ningún órgano en los ratones con dosis de hasta 500 mg/kg/día (exposición aproximadamente 68 veces mayor que la usada en humanos por la dosis recomendada de 100 mg/día).
Clorhidrato de metformina
Se han hecho estudios a largo plazo sobre la carcinogenicidad en ratas (dosificación durante 104 semanas) y en ratones (dosificación durante 91 semanas) con dosificaciones de hasta 900 mg/kg/día y 1,500 mg/kg/día respectivamente. Estas dosis son aproximadamente cuatro veces mayores que la dosis diaria máxima de 2,000 mg recomendada en seres humanos basándose en la comparación de las áreas de superficie corporal. No se encontró ningún indicio de carcinogenicidad de la metformina en los ratones macho o hembra. De forma similar, no se encontró ningún indicio de potencial teratogénico en las ratas macho. Sin embargo, sí aumentó la incidencia de pólipos benignos del estroma uterino en las ratas hembra tratadas con 900 mg/kg/día.
Mutagénesis
Fosfato de sitagliptina
La sitagliptina no fue mutagénica ni clastogénica en una serie de estudios de toxicología genética que incluyeron la prueba bacteriana de Ames (prueba de mutagénesis microbiana), la prueba de aberraciones cromosómicas en células de ovario de hámster Chino (células CHO, por las siglas en inglés para Chinese hamster ovary), una prueba citogenética in vitro con células CHO, un ensayo de dilución alcalina en ADN de hepatocitos de rata (que mide la capacidad del medicamento para inducir roturas de una cadena en el ADN), y una prueba de micronúcleos in vivo.
Clorhidrato de metformina
No hubo ningún indicio de potencial mutagénico de la metformina en las siguientes pruebas in vitro: Prueba de Ames (S. typhimurium), prueba de mutación genética (en células de linfoma de ratón) o prueba de aberraciones cromosómicas (en linfocitos humanos). Los resultados de la prueba de micronúcleos in vivo en ratones también fueron negativos.
Reproducción
Fosfato de sitagliptina
No se observó ningún efecto adverso sobre la fertilidad en ratas macho y hembra que recibieron dosis orales de hasta 1,000 mg/kg de sitagliptina (exposición hasta 100 veces la exposición en humanos, basándose en la dosis diaria recomendada en adultos de 100 mg/día) antes y durante el apareamiento.
Clorhidrato de metformina
La fertilidad de las ratas macho o hembra no fue afectada por la metformina administrada a dosificaciones tan altas como 600 mg/kg/día, que es aproximadamente tres veces la dosis diaria máxima recomendada en humanos basándose en la comparación de las áreas de superficie corporal.
Desarrollo fetal
Fosfato de sitagliptina
La sitagliptina no fue teratogénica en ratas a dosis orales de hasta 250 mg/kg ni en conejas que recibieron hasta 125 mg/kg durante la organogénesis (hasta 32 y 22 veces, respectivamente, la exposición en humanos por la dosis diaria recomendada en adultos de 100 mg diarios). En las ratas aumentó ligeramente la incidencia de malformaciones costales en los fetos (costillas ausentes, hipoplásicas u onduladas) con la dosificación de 1,000 mg/kg/día (aproximadamente 100 veces la exposición en humanos por la dosis diaria recomendada en adultos de 100 mg/día). El nivel de dosificación con el que no se observaron efectos sobre el desarrollo fetal fue de 250 mg/kg/día (32 veces la exposición en humanos por la dosis diaria recomendada en adultos de 100 mg/día). En las crías de las ratas que recibieron dosis orales de 1,000 mg/kg/día se observaron disminuciones relacionadas con el tratamiento del promedio de peso corporal antes del destete en ambos sexos y del promedio de aumento de peso después del destete en los machos.
XVIII. NOMBRE Y DOMICILIO DEL LABORATORIO
Representante legal en México:
Merck Sharp & Dohme Comercializadora, S. de R.L. de C.V.
Av. San Jerónimo No. 369, Piso 8, Col. La Otra Banda,
C.P. 01090, Álvaro Obregón, Ciudad de México, México.
XV. PRESENTACIÓN
Caja de cartón con 14, 28 o 56 comprimidos con 50 mg/500 mg o 50 mg/850 mg o 50 mg/1,000 mg.
Nota: No todas las presentaciones podrían estar disponibles en el mercado.
XVI. RECOMENDACIONES SOBRE ALMACENAMIENTO
Consérvese a no más de 25°C.
Consérvese la caja bien cerrada.
Protéjase de la luz.
XVII. LEYENDAS DE PROTECCIÓN
Literatura exclusiva para Profesionales de la Salud.
Su venta requiere receta médica.
Prohibida la venta fraccionada del producto.
No se deje al alcance de los niños.
No se use durante el embarazo ni lactancia.
Reporte las sospechas de reacción adversa al correo:
farmacovigilancia@cofepris.gob.mx y
dpoc.mexico@msd.com
