
LOWTIYEL
TESTOSTERONA
Gel
1 Caja,14 Sobres de aluminio,2.5 g,25 mg
1 Caja,30 Sobres de aluminio,2.5 g,25 mg
1 Caja,14 Sobres de aluminio,5 g,50 mg
1 Caja,30 Sobres de aluminio,5 g,50 mg
FORMA FARMACÉUTICA
Y FORMULACIÓN:
Cada sobre con 2.5 g contiene:
Testosterona 25 mg
Vehículo, c.b.p. 1 sobre.
Cada sobre con 5.0 g contiene:
Testosterona 50 mg
Vehículo, c.b.p. 1 sobre.
INDICACIONES TERAPÉUTICAS:
LOWTIYEL® 1% está indicado para el tratamiento de reemplazo en varones con padecimientos asociados a deficiencia o ausencia de testosterona endógena:
a. Hipogonadismo primario (congénito o adquirido).
b. Hipogonadismo hipogonadotrópico (congénito o adquirido): LOWTIYEL® 1% no ha sido evaluado clínicamente en varones menores a 18 años de edad.
FARMACOCINÉTICA Y FARMACODINAMIA:
Propiedades farmacocinéticas: LOWTIYEL® 1% aporta cantidades fisiológicas de testosterona, para producir concentraciones circulantes de testosterona que se aproximan a las concentraciones normales (298-1,043 ng/dL), observadas en hombres sanos.
LOWTIYEL® 1% libera testosterona, transdérmicamente, durante 24 horas después de una sola aplicación sobre la piel intacta, limpia y seca de los hombros, porción superior de los brazos y/o abdomen. Una aplicación diaria de LOWTIYEL® 5, 7.5 o 10 g, proporciona 50, 75 o 100 mg de testosterona respectivamente.
LOWTIYEL® 1% es una formulación hidroalcohólica que seca rápidamente cuando se aplica a la superficie de la piel. La piel sirve de reservorio para la liberación sostenida de testosterona hacia la circulación sistémica. Aproximadamente 10% de la dosis de testosterona administrada se absorbe a través de la piel a la circulación sistémica.
En un estudio con 10 g de LOWTIYEL® 1% a dosis de 100 mg, todos los pacientes mostraron incremento en la testosterona sérica a los 30 minutos y ocho de nueve pacientes tenían concentración sérica de testosterona en rangos normales a las 4 horas de la aplicación inicial. La absorción de testosterona a la sangre continúa durante todo el periodo de dosificación de 24 horas. Las concentraciones séricas se aproximan al estado estable al final de las primeras 24 horas de tratamiento y alcanzan el estado estable al segundo o tercer día.
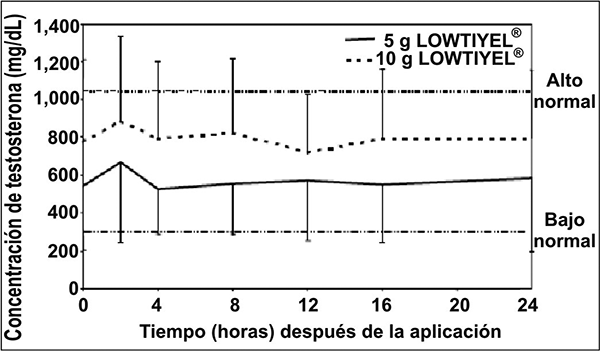
Con aplicaciones de una sola vez al día de LOWTIYEL® 1%, se ha confirmado que las concentraciones de testosterona sérica generalmente se mantienen dentro del rango eugonadal con determinaciones de seguimiento a los 30, 90 y 180 días después de haber iniciado el tratamiento. La figura 1 resume los perfiles farmacocinéticos de 24 horas de testosterona en hombres hipogonadales (menos de 300 ng/dL) tratados con LOWTIYEL® 1% 50 o 100 mg por 30 días. La concentración diaria promedio de testosterona (± SD) producida por LOWTIYEL® 1%, 100 mg al día 30 fue 792 (±294) ng/dL y por LOWTIYEL® 1% 50 mg 566 (±262) ng/mL.
Figura 1. Concentraciones séricas de testosterona promedio en estado estable al día 30 en pacientes que recibieron LOWTIYEL® 1% una vez al día
Distribución: La testosterona circulante en suero se fija principalmente a la globulina fijadora de hormonas sexuales (SHBG) y a la albúmina. La fracción unida a albúmina se libera fácilmente y es bioactiva. Aproximadamente 40% de la testosterona en plasma se fija a SHBG, 2% permanece sin unirse (libre) y el resto se une a albúmina y otras proteínas.
Metabolismo: La testosterona se metaboliza a varios 17-ceto esteroides a través de dos vías diferentes. Los principales metabolitos activos de testosterona son el estradiol y la dihidrotestosterona (DHT).
Las concentraciones de DHT aumentan en paralelo con las concentraciones de testosterona durante el tratamiento con LOWTIYEL® 1%. Los valores del cociente promedio en estado estable DHT/T durante 180 días de tratamiento con LOWTIYEL® 1% fluctuaron entre 0.23 a 0.29 (con 50 mg de testosterona por día) y de 0.27 a 0.33 (con 100 mg de testosterona por día).
Excreción: Existe considerable variación en la vida media de testosterona reportada en la literatura, desde 10 hasta 100 minutos. Aproximadamente 90% de la testosterona administrada intramuscularmente se elimina en la orina como testosterona y sus metabolitos conjugados con ácido glucurónico y sulfúrico. Aproximadamente 6% de la dosis se excreta en las heces, principalmente en forma no conjugada. La inactivación de la testosterona ocurre principalmente en el hígado.
Cuando se suspende el tratamiento con LOWTIYEL® 1%, después de alcanzar el estado estable, los niveles séricos de testosterona permanecen normales durante 24 a 48 horas pero regresan a los niveles previos al tratamiento alrededor del quinto día desde la última aplicación.
Propiedades farmacodinámicas: Los andrógenos endógenos, incluyendo a testosterona y a dihidrotestosterona (DHT), son responsables del crecimiento y desarrollo normal de los órganos sexuales masculinos y del mantenimiento de los caracteres sexuales secundarios. Estos efectos incluyen el crecimiento y maduración de la próstata, las vesículas seminales, el pene y el escroto; el desarrollo de la distribución del pelo en el hombre, tal como facial, púbico, pecho y axilas; el crecimiento laríngeo, el engrosamiento de las cuerdas vocales, alteraciones en la musculatura corporal y la distribución de la grasa. La testosterona y la DHT son necesarias para el desarrollo normal de las características sexuales secundarias.
El hipogonadismo masculino resulta de la secreción insuficiente de testosterona y se caracteriza por concentraciones séricas de testosterona bajas. Los síntomas asociados al hipogonadismo masculino incluyen disfunción eréctil, disminución del deseo sexual, fatiga y pérdida de energía, depresión emocional, regresión de los caracteres sexuales secundarios y osteoporosis.
El hipogonadismo en el hombre se puede presentar como hipogonadismo primario causado por defecto de las gónadas, tal como en el caso del síndrome de Klinefelter o la aplasia de células de Leydig, mientras que el hipogonadismo secundario es la insuficiencia del hipotálamo o la pituitaria para producir suficientes gonadotropinas (FSH, LH).
No se han conducido estudios farmacodinámicos específicos, utilizando LOWTIYEL® 1%.
CONTRAINDICACIONES:
• Diagnóstico o sospecha de cáncer de próstata o carcinoma de mama.
• Hipersensibilidad a la sustancia activa o a cualquiera de los excipientes.
• Mujeres embarazadas o lactando, la testosterona puede causar daño fetal.
• Menores de 18 años de edad.
RESTRICCIONES DE USO DURANTE EL EMBARAZO Y LA LACTANCIA: LOWTIYEL® 1% está contraindicado en mujeres embarazadas o en periodo de lactancia.
Las mujeres embarazadas deberán evitar cualquier contacto con los sitios de aplicación de LOWTIYEL® 1% (Ver Precauciones generales). La testosterona es teratogénica y puede causar daño fetal. Este medicamento puede tener efectos virilizantes sobre el feto.
Aunque se desconoce qué tanta testosterona se transfiere en la leche humana, LOWTIYEL® 1% está contraindicado en mujeres lactando, debido a la posibilidad de reacciones adversas en los lactantes.
En caso de contacto, lavar con jabón y agua lo más pronto posible (ver Precauciones generales).
Con dosis grandes de andrógenos exógenos, incluyendo LOWTIYEL® 1%, se puede suprimir la espermatogénesis a través de inhibición por retroalimentación de la hormona folículo estimulante (HFE) de la pituitaria.
REACCIONES SECUNDARIAS Y ADVERSAS: En un estudio clínico controlado, 154 pacientes fueron tratados con LOWTIYEL® 1% hasta por 6 meses. Las reacciones adversas más frecuentemente observadas fueron trastornos de la piel. Los eventos adversos posible, probable o definitivamente relacionados con el uso de LOWTIYEL® 1% y reportados por ³ 1% de los pacientes se presentan en la tabla 1.
Tabla 1. Incidencia de los eventos adversos posible, probable o definitivamente relacionados con el uso de LOWTIYEL® 1% en un ensayo clínico controlado de 180 días
|
Clase de sistema-órgano/término preferido |
Grupo de tratamiento |
||
|
Gel de 50 mg (n = 77) |
Gel de 75 mg (n = 40) |
Gel de 100 mg (n = 78) |
|
|
Trastornos de la piel y el tejido subcutáneo |
|||
|
Acné |
1 (1%) |
1 (3%) |
6 (8%) |
|
Alopecia |
1 (1%) |
0 (0%) |
1 (1%) |
|
Reacción en el sitio de aplicación |
4 (5%) |
1 (3%) |
3 (4%) |
|
Investigaciones |
|||
|
Pruebas de laboratorio anormales* |
5 (6%) |
2 (5%) |
2 (3%) |
|
Trastornos del sistema nervioso |
|||
|
Dolor de cabeza |
3 (4%) |
1 (3%) |
0 (0%) |
|
Trastornos psiquiátricos |
|||
|
Depresión |
1 (1%) |
0 (0%) |
1 (1%) |
|
Disminución de la libido |
0 (0%) |
1 (3%) |
1 (1%) |
|
Nerviosismo |
0 (0%) |
1 (3%) |
1 (1%) |
|
Labilidad emocional |
0 (0%) |
1 (3%) |
2 (3%) |
|
Trastornos generales y trastornos en el sitio de administración |
|||
|
Astenia |
0 (0%) |
1 (3%) |
1 (1%) |
|
Trastornos del sistema reproductor y de las mamas |
|||
|
Ginecomastia |
1 (1%) |
0 (0%) |
2 (3%) |
|
Dolor de las mamas |
1 (1%) |
1 (3%) |
1 (1%) |
|
Trastorno prostático** |
2 (3%) |
1 (3%) |
4 (5%) |
|
Trastorno en los testículos*** |
2 (3%) |
0 (0%) |
0 (0%) |
|
Trastornos vasculares |
|||
|
Hipertensión |
2 (3%) |
0 (0%) |
2 (3%) |
* Ocurrieron anormalidades en las pruebas de laboratorio en nueve pacientes con uno o más de los siguientes eventos: hemoglobina o hematócrito elevados, hiperlipidemia, triglicéridos elevados, hipopotasemia, reducción de HDL, glucosa elevada, creatinina elevada o bilirrubina total elevada.
** Los trastornos prostáticos incluyeron a cinco pacientes con próstata agrandada, un paciente con BPH y un paciente con resultados de antígeno prostático específico PSA elevados.
*** Los trastornos en los testículos fueron reportados por dos pacientes: un paciente con varicocele izquierdo y un paciente con ligera sensibilidad en el testículo izquierdo.
En este estudio clínico de LOWTIYEL® 1% se reportaron reacciones en la piel en el sitio de aplicación con LOWTIYEL®, 1% pero ninguna suficientemente severa como para requerir tratamiento o la interrupción del fármaco.
Tabla 2. Incidencia de eventos adversos surgidos durante el tratamiento, posible, probable o definitivamente relacionados con el uso de LOWTIYEL® 1% en un estudio clínico de extensión, abierto de 3 años
|
Clase de sistema-órgano/ |
Grupo de tratamiento n = 162 (%) |
|
Trastorno de la sangre y del sistema linfático |
|
|
Anemia |
4 (2.5) |
|
Investigaciones |
|
|
Pruebas de laboratorio anormales* |
15 (9.3) |
|
Neoplasias benignas, malignas y no especificadas |
|
|
Carcinoma de próstata |
2 (1.2) |
|
Trastornos renales y urinarios |
|
|
Síntomas urinarios** |
6 (3.7) |
|
Trastornos del sistema reproductor y de las mamas |
|
|
Ginecomastia |
4 (2.5) |
|
Trastorno de los testículos*** |
3 (1.9) |
|
Próstata agrandada |
19 (11.7) |
|
Trastornos de la piel y el tejido subcutáneo |
|
|
Acné |
5 (3.1) |
|
Reacción en el sitio de aplicación |
9 (5.6) |
|
Resequedad de la piel |
3 (1.9) |
|
Prurito |
3 (1.9) |
* Ocurrieron pruebas de laboratorio anormales en quince pacientes con uno o más de los siguientes eventos: AST elevada, ALT elevada, testosterona elevada, hemoglobina o hematócritos elevados, colesterol elevado, cociente colesterol/LDL elevado, triglicéridos elevados, HDL elevado o creatinina en suero elevada.
** Los síntomas urinarios incluyen nicturia, dificultad para iniciar la micción, incontinencia urinaria, retención urinaria, urgencia urinaria y chorro urinario débil.
*** El trastorno de los testículos incluyó a tres pacientes. Hubo dos pacientes con testículos no palpables y un paciente con leve sensibilidad dolorosa en el testículo derecho.
Experiencia poscomercialización: La tabla 3 incluye los eventos adversos reportados de manera espontánea en la experiencia posterior a la comercialización y los efectos generales de la testosterona. Debido a que las reacciones se reportan en forma voluntaria de una población de tamaño incierto, no es posible estimar de manera confiable su frecuencia ni establecer una relación causal con la exposición al fármaco.
Tabla 3. Reacciones adversas al fármaco a partir de la experiencia poscomercialización de LOWTIYEL® 1% y reacciones conocidas al tratamiento general con testosterona, ordenadas por clase de sistema-órgano de MedDRA
|
Sistema-órgano |
Reacción |
|
Trastornos de la sangre y del sistema linfático |
Hemoglobina elevada, hematócrito elevado (policitemia). |
|
Trastornos endocrinos |
Hirsutismo. |
|
Trastornos gastrointestinales |
Náuseas. |
|
Trastornos generales y reacciones en el sitio de administración |
Astenia, edema, malestar general. |
|
Trastornos genitourinarios |
Micción deteriorada. |
|
Trastornos hepatobiliares |
Pruebas de función hepática anormales (por ejemplo, transaminasas, gamma-glutamil transferasa GGTP elevada, bilirrubina). |
|
Investigaciones |
PSA elevado, cambios en los electrólitos (nitrógeno, calcio, potasio, fósforo, sodio), deterioro en la tolerancia a la glucosa, cambios en los lípidos en suero (hiperlipidemia, triglicéridos elevados, lipoproteína de alta densidad [HDL] disminuida), niveles de testosterona fluctuantes, aumento de peso. |
|
Neoplasias benignas, malignas y no especificadas (quistes y pólipos) |
Cáncer de próstata (ver Precauciones generales). |
|
Trastornos del sistema nervioso |
Mareo, dolor de cabeza, insomnio, apnea del sueño. |
|
Trastornos psiquiátricos |
Amnesia, ansiedad, depresión, hostilidad, labilidad emocional, disminución de la libido, nerviosismo. |
|
Trastornos del sistema reproductor y de mamas |
Ginecomastia, mastodinia, oligospermia, priapismo (erecciones frecuentes o prolongadas), agrandamiento de la próstata, atrofia de testículos. |
|
Trastornos respiratorios |
Disnea. |
|
Trastornos de la piel y del tejido subcutáneo |
Acné, alopecia, reacción en el sitio de aplicación (cabello descolorido, piel reseca, eritema, parestesia, prurito, comezón), sudoración. |
|
Trastornos vasculares |
Hipertensión, vasodilatación (bochornos), tromboembolismo venoso. |
Exposición secundaria a testosterona en niños: En vigilancia poscomercialización se han reportado casos de exposición secundaria a testosterona que ha producido virilización en niños. En estos casos reportados, los signos y síntomas han incluido agrandamiento del clítoris (con intervención quirúrgica) o del pene, desarrollo de vello púbico, incremento de las erecciones y de la libido, conducta agresiva y edad ósea avanzada. En la mayoría de los casos con desenlace conocido, se reportó que los signos y síntomas han regresado al eliminar la exposición al gel de testosterona. Sin embargo, en algunos casos, el agrandamiento de los genitales no regresó completamente al tamaño normal, apropiado para la edad y la edad ósea permaneció modestamente mayor que la edad cronológica. En algunos casos se reportó contacto directo con el sitio de aplicación en la piel de hombres que estaban utilizando el gel de testosterona. En al menos un caso reportado, el reportador consideró la posibilidad de exposición secundaria desde artículos tales como las camisetas del usuario del gel de testosterona y/u otras prendas tales como toallas o sábanas (ver Precauciones generales).
PRECAUCIONES EN RELACIÓN CON EFECTOS DE CARCINOGÉNESIS, MUTAGÉNESIS, TERATOGÉNESIS Y SOBRE LA FERTILIDAD: La testosterona ha sido probada por inyección subcutánea e implantación en ratones y ratas. En ratones, el implante de testosterona indujo la formación de tumores cervicouterinos, metastásicos en algunos casos. Existe evidencia sugestiva de que la inyección de testosterona en algunas cepas de ratones hembras incrementa su susceptibilidad a la formación de hepatomas; también se sabe que la testosterona incrementa el número de tumores y disminuye el grado de diferenciación de carcinomas hepáticos inducidos químicamente en ratas.
Testosterona fue negativa en los ensayos in vitro de Ames y en los ensayos in vivo de micronúcleo en ratón.
Se ha reportado que la administración exógena de testosterona suprime la espermatogénesis en la rata, perro y primates no humanos, la cual fue reversible al interrumpir el tratamiento.
Existen reportes escasos de carcinoma hepatocelular en hombres tratados con andrógenos a altas dosis por tiempos prolongados; sin embargo, la suspensión del fármaco no resultó en la regresión de los tumores en todos los casos. Los pacientes geriátricos tratados con andrógenos podrían estar en riesgo incrementado de desarrollar hiperplasia prostática y carcinoma prostático.
INTERACCIONES MEDICAMENTOSAS Y DE OTRO GÉNERO:
Anticoagulantes orales: Se pueden observar cambios en la actividad anticoagulante con el tratamiento con andrógenos, por lo tanto, se recomienda supervisión más frecuente del cociente normalizado internacional (INR) y del tiempo de protrombina en pacientes que están tomando anticoagulantes, sobre todo al iniciar y terminar el tratamiento con andrógenos.
Corticosteroides: La administración concomitante de testosterona y hormona adrenocorticotrópica (ACTH) o corticosteroides puede aumentar el riesgo de desarrollar edema. Como resultado de ello, estos medicamentos deberán administrarse con precaución, sobre todo en pacientes que sufren de enfermedad cardiaca, renal o hepática.
Control para diabéticos: En pacientes tratados con andrógenos, es probable que ocurran cambios en la sensibilidad a la insulina o el control glucémico. En pacientes diabéticos, quizá sea necesario modificar su tratamiento para el control de la diabetes.
Globulina fijadora de tiroxina: Los andrógenos pueden disminuir los niveles de globulina fijadora de tiroxina, dando como resultado una reducción de los niveles totales de T4 en suero y un incremento en la captación de T3 y T4 por resina. Sin embargo, los niveles hormonales libres de la tiroides permanecen sin cambios y no hay evidencias clínicas de insuficiencia tiroidea.
ALTERACIONES EN LOS RESULTADOS DE PRUEBAS DE LABORATORIO: Además de las pruebas de laboratorio de las concentraciones de testosterona y antígeno prostático específico (PSA) en pacientes en terapia con andrógenos a largo plazo, es necesario revisar los siguientes parámetros de laboratorio de manera periódica: hemoglobina, hematócrito (para detectar policitemia), pruebas de función hepática y pruebas de perfil de lípidos.
El ajuste de dosis o la discontinuación hasta la normalización de los parámetros puede ser necesaria.
Los productos a base de alcohol, incluyendo LOWTIYEL® 1%, son inflamables; por lo tanto, se deberá aconsejar a los pacientes evitar el fuego, flamas o fumar hasta que LOWTIYEL® 1% haya secado.
No ha habido un número suficiente de pacientes geriátricos involucrado en estudios clínicos utilizando LOWTIYEL® 1% para determinar si la eficacia en mayores de 65 años de edad difiere de la observada en sujetos más jóvenes. Adicionalmente, los datos de seguridad a largo plazo en pacientes geriátricos es insuficiente para evaluar los posibles riesgos de enfermedad cardiovascular y cáncer de próstata.
También es posible que los pacientes geriátricos tratados con andrógenos estén en riesgo de empeoramiento de los signos y síntomas de HPB.
PRECAUCIONES GENERALES: La testosterona se puede utilizar en hombres con un perfil apropiado con bajos niveles de testosterona confirmados, de acuerdo con muestras tomadas por la mañana, así como síntomas y signos clínicos.
Debido a la variabilidad en los valores de laboratorio, todas las mediciones de testosterona deben llevarse a cabo en el mismo laboratorio.
Antes del inicio del tratamiento con testosterona, es preciso identificar a los pacientes en riesgo (aquéllos con factores clínicos y familiares) y todos los pacientes deberán someterse a un examen detallado con el objeto de detectar cáncer prostático o de mama preexistente.
Los andrógenos pueden acelerar el avance del cáncer prostático subclínico y de la hiperplasia prostática benigna (HPB). En hombres que reciben tratamiento de reemplazo de testosterona, un monitoreo detallado y regular de la próstata deberá ser consistente con las prácticas actuales para hombres eugonadales.
En hombres que reciben tratamiento de reemplazo de testosterona, es necesario realizar un monitoreo detallado y regular de mama.
Las mujeres no deberán usar LOWTIYEL® 1%, debido a la falta de evaluaciones y los posibles efectos virilizantes.
El gel de testosterona no está indicado y no ha sido evaluado clínicamente en niñas ni en niños pre púberes.
Se ha reportado virilización en niños expuestos de manera secundaria al gel de testosterona.
La transferencia de testosterona a otras personas (incluidos mujeres y niños) puede ocurrir cuando se hace un contacto vigoroso piel con piel en el sitio de aplicación.
Se recomienda tomar las siguientes precauciones:
Para el paciente:
• Lavar las manos con jabón y agua inmediatamente después de aplicar el gel.
• Cubrir el área de aplicación con la ropa una vez que el gel haya secado, sobre todo durante el periodo de contacto con otras personas; en especial niños.
• Lavar el sitio de aplicación escrupulosamente con jabón antes de cualquier situación en la que se prevea un contacto cercano.
Para personas no tratadas con LOWTIYEL® 1%: Mujeres y niños deben evitar el contacto con cualquier sitio de aplicación sin lavar o descubierto en hombres que usan LOWTIYEL® 1%.
En caso de contacto con el área de aplicación sin lavar o descubierta:
• Lavar el área general de contacto con jabón y agua lo más pronto posible.
• Reportar el desarrollo de signos de exposición excesiva a andrógenos.
Por último, los profesionales del cuidado de la salud deberán aconsejar a sus pacientes que se apeguen en forma estricta a las indicaciones de uso recomendadas.
Las mujeres embarazadas deberán evitar cualquier contacto con los sitios de aplicación del gel de testosterona. Es preciso poner especial cuidado para prevenir la exposición de la pareja embarazada (ver Restricciones de uso durante el embarazo y la lactancia).
Los fármacos que pertenecen a la clase de andrógenos pueden promover la retención de sodio y agua, nitrógeno, potasio, fósforo y calcio, sobre todo durante una administración prolongada.
Los andrógenos deben usarse con precaución en pacientes con enfermedades cardiovasculares (por ejemplo, insuficiencia cardiaca congestiva, enfermedad cardiaca isquémica), renal o hepática.
Después de la comercialización se han reportado eventos de tromboembolismo venoso, incluyendo trombosis venosa profunda (DVT) y embolismo pulmonar (PE), en pacientes usando productos con testosterona tal como LOWTIYEL®. Los pacientes que reporten síntomas de dolor, edema, calor y eritema en una extremidad inferior para DVT y aquellos que presenten disnea aguda para PE deben ser evaluados. Si se sospecha un evento tromboembólico venoso, se debe suspender el tratamiento con LOWTIYEL® e iniciar el manejo apropiado.
Los andrógenos deberán utilizarse con precaución en pacientes con cáncer en riesgo de hipercalcemia (e hipercalciuria asociada). En estos pacientes, se recomienda un monitoreo regular de las concentraciones de calcio en suero.
Hay reportes publicados de un aumento en el riesgo de apnea del sueño en sujetos con hipogonadismo tratados con esteres de testosterona, sobre todo en aquéllos con factores de riesgo como obesidad y enfermedad respiratoria crónica.
Durante la administración exógena de andrógenos, la liberación de la testosterona endógena puede inhibirse a través de una inhibición por retroalimentación de la hormona luteinizante (LH) de la pituitaria. En dosis altas de andrógenos exógenos, también es posible suprimir la espermatogénesis a través de la inhibición por retroalimentación de la hormona estimulante del folículo (FSH) de la pituitaria.
Efectos sobre la habilidad para conducir y utilizar maquinaria: No se han realizado estudios con gel de testosterona a 1%; no se sabe que el gel de testosterona tenga alguna influencia sobre la habilidad para conducir o utilizar maquinaria.
DOSIS Y VÍA DE ADMINISTRACIÓN:
La vía de administración es cutánea.
La dosis de inicio recomendada de LOWTIYEL® 1% es de 50 mg (el contenido de un sobre de 5 g o de dos sobres de 2.5 g) aplicada una vez al día por la mañana (de preferencia a la misma hora cada día).
Para asegurar una dosificación apropiada, se deberán medir las concentraciones de testosterona sérica a intervalos. Si la concentración de testosterona sérica está por debajo del rango normal, se deberá de incrementar la dosis diaria de testosterona de 50 a 75 mg y de 75 a 100 mg en varones adultos como lo indique el médico. Si la concentración de testosterona sérica excede el rango normal, se deberá disminuir la dosis diaria de testosterona. Si la concentración sérica de testosterona excede el rango normal consistentemente con dosis de 50 mg de testosterona, se deberá discontinuar la terapia con LOWTIYEL® 1%. Adicionalmente, se deberán evaluar periódicamente las concentraciones séricas de testosterona.
Niños: LOWTIYEL® 1% no está indicado en niños. No se ha establecido la seguridad y eficacia en niños por debajo de 18 años de edad.
Método de administración: La aplicación deberá ser administrada por el paciente mismo, sobre piel limpia, seca, sana e intacta de la parte superior de los brazos/hombros derecho e izquierdo y/o lados derecho e izquierdo del abdomen. El área de aplicación se deberá limitar al área que será cubierta por la camiseta de manga corta del paciente. No aplique LOWTIYEL® 1% a ninguna otra parte del cuerpo, incluyendo los genitales, pecho o espalda. Se deberá distribuir el gel homogéneamente entre la parte superior de los brazos/hombros derecho e izquierdo o ambos lados del abdomen.
Se le deberá aconsejar al paciente que evite nadar o bañarse por lo menos 5 horas después de la aplicación de LOWTIYEL® 1%.
Estudios in vitro muestran que la testosterona residual es removida de la superficie de la piel por medio de lavado con jabón y agua. La eficacia es menos afectada cuando el lavado ocurre después de seis horas. El lavado ocasional después de 1-6 horas tiene un impacto mínimo en el tratamiento.
Después de aplicar el gel, se deberá permitir que seque el sitio de aplicación antes de vestirse. Se deberán lavar las manos escrupulosamente con jabón y agua después de la aplicación. Se deberán evitar el fuego, flamas o fumar, hasta que el gel haya secado, ya que los productos a base de alcohol, incluyendo LOWTIYEL® 1%, son inflamables.
Una vez abierto el sobre, se deberá extraer el contenido total del sobre y aplicarlo inmediatamente en la piel.
Para conocer las precauciones para minimizar la posibilidad de exposición secundaria a testosterona desde la piel tratada con LOWTIYEL® 1%, vea Precauciones generales.
MANIFESTACIONES Y MANEJO DE LA SOBREDOSIFICACIÓN O INGESTA ACCIDENTAL: En la literatura se ha reportado un caso de sobredosis de enantato de testosterona después de una inyección. Se trata de un caso de accidente cerebrovascular en un paciente con una concentración de testosterona en plasma alta de 11,400 ng/dL (395 nmol/L). Sería muy poco probable que estas concentraciones de testosterona en plasma se alcanzaran utilizando la vía transdérmica.
PRESENTACIONES:
Cajas con 14 o 30 sobres individuales de aluminio, conteniendo cada sobre 2.5 g o 5.0 g de gel, correspondientes a 25 mg o 50 mg de testosterona respectivamente.
RECOMENDACIONES SOBRE ALMACENAMIENTO:
Consérvese a temperatura ambiente a no más de 25°C.
LEYENDAS DE PROTECCIÓN:
Las mujeres embarazadas o en periodo de lactancia deberán evitar cualquier contacto con los sitios de aplicación del gel de testosterona. Este medicamento puede tener efectos virilizantes sobre el feto. Su venta requiere receta médica. No se deje al alcance de los niños. Literatura exclusiva para el médico.
Reporte las sospechas de reacción adversa al correo: farmacovigilancia@cofepris.gob.mx
ABBOTT LABORATORIES DE MÉXICO, S. A. de C. V.
Calz. de Tlalpan No. 3092
Col. Ex Hacienda Coapa, C.P. 04980
Deleg. Coyoacán, D.F., México
Bajo licencia de:
Unimed Pharmaceuticals LLC.
Reg. Núm. 330M2006, SSA IV
143300415D0287