MONTACLAR - Tabletas
Sustancia(s):
- Loratadina, Montelukast
Presentaciones:
- 1 Caja, 15 Tabletas,
- 1 Caja, 30 Tabletas,
III. FORMA FARMACÉUTICA Y FORMULACIÓN
Fórmula:
Cada TABLETA contiene:
Montelukast sódico equivalente a 10 mg de montelukast ácido libre
Loratadina 10 mg
Excipiente cbp 1 tableta
XIX. NÚMERO DE REGISTRO DEL MEDICAMENTO ANTE LA SECRETARÍA
Reg. Núm. 370M2014 SSA IV
Número de Tracer: MK0476A-MEX-2019-020444
IV. INDICACIONES TERAPÉUTICAS
MONTACLAR (montelukast/loratadina) está indicado como tratamiento de segunda línea para el alivio de los síntomas de la rinitis alérgica, en mayores de 15 años.
V. FARMACOCINÉTICA Y FARMACODINAMIA
Clase Terapéutica
MONTACLAR tableta oral es una formulación combinada que contiene montelukast sódico, un antagonista de los receptores de leucotrienos, y loratadina, un antagonista del receptor H1 de histamina.
Mecanismo de Acción
MONTACLAR: MONTACLAR proporciona los efectos como antagonista de los leucotrienos de montelukast y los efectos antihistamínicos de la loratadina.
Montelukast: Los cisteinil leucotrienos (LTC4, LTD4, LTE4), son eicosanoides inflamatorios potentes liberados de diversas células, incluidos los mastocitos y los eosinófilos. Estos importantes mediadores de la reacción asmática se unen a los receptores de cisteinil leucotrieno (CysLT). El receptor CysLT de tipo 1 (CysLT1) se encuentra en las vías respiratorias humanas (incluyendo las células del músculo liso de las vías respiratorias y los macrófagos de las vías respiratorias) y en otras células pro-inflamatorias (incluyendo eosinófilos y ciertas células madre mieloides). Los CysLT han sido correlacionados con la fisiopatología del asma y la rinitis alérgica. En el asma, los efectos mediados por los leucotrienos comprenden varias acciones en las vías respiratorias, tales como broncoconstricción, secreción mucosa, permeabilidad vascular y reclutamiento de eosinófilos. En la rinitis alérgica, los CysLTs se liberan en la mucosa nasal después de la exposición a los alérgenos, tanto durante la reacción de fase temprana como de fase tardía y están asociados con los síntomas de la rinitis alérgica. El reto intra-nasal con los CysLTs ha mostrado incrementar la resistencia de las vías aéreas nasales y los síntomas de obstrucción nasal.
Montelukast es un potente compuesto con actividad por vía oral que mejora significativamente los parámetros de la inflamación asmática. Basado en los bioensayos bioquímicos y farmacológicos, se une con gran afinidad y selectividad al receptor CysLT1 (mucho más que a otros receptores de las vías aéreas farmacológicamente importantes tales como los receptores prostanoides, colinérgicos o β-adrenérgicos). Montelukast inhibe potentemente las acciones fisiológicas de LTC4, LTD4, y LTE4 sobre el receptor CysLT1 sin ninguna actividad agonista.
Loratadina: Loratadina es un antihistamínico tricíclico de acción prolongada con actividad antagonista periférica selectiva sobre el receptor H1 de la histamina.
Farmacodinamia
Montelukast: Montelukast produce broncodilatación dentro de las 2 horas de la administración oral; estos efectos fueron aditivos a la broncodilatación causada por un β-agonista.
Los estudios clínicos en pacientes de 15 años de edad y mayores demostraron que no hay un beneficio clínico adicional para dosis de montelukast arriba de 10 mg una vez al día. Esto se mostró en dos estudios en asma crónica, usando dosis de hasta 200 mg una vez al día y en un estudio de reto con ejercicio, utilizando dosis de hasta 50 mg, evaluados al final del intervalo de dosificación una vez al día.
En pacientes con rinitis alérgica estacional en edades de 15 años y mayores que recibieron montelukast, se observó un incremento promedio de 0.2% en la cuenta de eosinófilos en sangre periférica, comparado con un incremento promedio de 12.5% en los pacientes tratados con placebo, en los periodos de tratamiento doble ciego; esto refleja una diferencia promedio de 12.3% a favor de montelukast. Se desconoce la relación entre estas observaciones y los beneficios clínicos de montelukast señalados en los estudios clínicos.
Loratadina: Los estudios de ronchas cutáneas causadas por histamina en humanos después de la administración de dosis orales únicas y repetidas de 10 mg de loratadina han demostrado que el fármaco exhibe un efecto antihistamínico que comienza en el curso de 1 a 3 horas, alcanzando un máximo entre 8 y 12 horas y una duración de más de 24 horas. No hubo indicios de tolerancia a dicho efecto después de 28 días de administración con loratadina.
Farmacocinética
Absorción
MONTACLAR: Montelukast y loratadina se absorbieron rápidamente después de la administración por vía oral de tabletas de MONTACLAR. Los parámetros farmacocinéticos en plasma después de la administración oral de dosis únicas y múltiples se muestran en la Tabla 1.
|
Tabla 1 |
ABC† (ng.h/mL) |
Cmáx. (ng/mL) |
||
|
Día 1 |
Día 17 |
Día 1 |
Día 17 |
|
|
Montelukast |
2,222 |
2,134 |
345 |
314 |
|
Loratadina |
10.2 |
14.3 |
1.67 |
1.98 |
|
Descarboetoxiloratadina |
34.2 |
37.3 |
1.53 |
3.29 |
ABC = área bajo la curva de concentración plasmática-tiempo; Cmáx. = concentración plasmática máxima observada.
† ABC(0-∞) en el Día 1 y ABC(0-24 hr) en el Día 17.
Las concentraciones plasmáticas máximas (Cmáx) de montelukast y loratadina se alcanzaron en un tiempo mediano máximo (Tmáx) de 2 horas después de la administración, y para el metabolito activo de la loratadina, la descarboetoxiloratadina en un promedio del Tmáx de 4 a 6 horas después de la administración.
En un estudio de dosis única, el alimento aumentó la biodisponibilidad sistémica (ABC) de la loratadina y de la descarboetoxiloratadina 102% y 16%, respectivamente, y no tuvo efecto en la biodisponibilidad del montelukast de MONTACLAR.
Distribución
Montelukast: Montelukast se une en más de 99% a las proteínas plasmáticas. El volumen de distribución de montelukast en equilibrio dinámico (estado estable) es de 8 a 11 litros. Los estudios en ratas con montelukast radiomarcado indican una distribución mínima a través de la barrera hematoencefálica. Además, las concentraciones del material radiomarcado 24 horas después de la administración fueron mínimas en todos los demás tejidos.
Loratadina: Los estudios autorradiográficos de cuerpo entero en ratas y monos, los estudios de distribución tisular del fármaco radiomarcado y los estudios de radioligandos in vivo en ratones han demostrado que ni la loratadina ni sus metabolitos atraviesan con facilidad la barrera hematoencefálica. Los estudios de unión de radioligandos con receptores H1 de pulmón y encéfalo de conejillos de Indias indican que hubo una unión preferencial a los receptores H1 periféricos respecto a la unión a receptores en el sistema nervioso central.
Metabolismo y Excreción
MONTACLAR: En un estudio para evaluar el potencial de interacción entre montelukast y loratadina administrados en forma concomitante, la co-administración con loratadina no afectó la farmacocinética de montelukast. La exposición (ABC) a loratadina y a la descarboetoxiloratadina no se modificó por la co-administración con montelukast. En otro estudio, las vidas medias terminales promedio de eliminación en los adultos normales de loratadina, descarboetoxiloratadina, y montelukast fueron 13.4 horas, 22.1 horas, y 6.5 horas, respectivamente, después de una dosis única. En el mismo estudio, la depuración corporal total aparente (CL/F; promedio geométrico) para montelukast y loratadina después de una dosis única, fue aproximadamente 984 L/hr y 4.50 L/hr, respectivamente. La CL/F y el ABC de montelukast y de loratadina y el ABC de descarboetoxiloratadina fueron similares después de la administración de múltiples dosis orales de la tableta combinada de montelukast y loratadina, en comparación con los de una dosis única.
Montelukast: Montelukast se metaboliza extensamente. En estudios con dosis terapéuticas, las concentraciones plasmáticas de los metabolitos de montelukast son indetectables en el estado estacionario en pacientes adultos y pediátricos. Estudios in vitro utilizando microsomas hepáticos humanos indican que los citocromos P450 3A4, 2C8 y 2C9 están implicados en el metabolismo de montelukast [ver INTERACCIONES MEDICAMENTOSAS Y DE OTRO GÉNERO).
La depuración plasmática de montelukast es en promedio de 45 mL/min en adultos sanos. Después de la administración de una dosis oral de montelukast radiomarcado, el 86% de la radiactividad se recuperó en la materia fecal de 5 días y < 0.2% se recuperó en la orina. En conjunto con las estimaciones de la biodisponibilidad oral de montelukast, esto indica que montelukast y sus metabolitos se excretan de manera casi exclusiva a través de la bilis [ver FARMACOCINÉTICA, Poblaciones Especiales].
En diversos estudios sobre montelukast, la vida media plasmática promedio de montelukast varió de 2.7 a 5.5 horas en adultos jóvenes sanos. La farmacocinética de montelukast es prácticamente lineal para las dosis orales de hasta 50 mg. Durante la dosificación de 10 mg una vez al día de montelukast, hubo poca acumulación del fármaco precursor en el plasma (14%).
Loratadina: Aproximadamente 80% de la dosis total de loratadina administrada se puede encontrar distribuida igualmente entre la orina y las heces en la forma de productos metabólicos en el curso de 10 días. En casi todos los pacientes, la exposición (ABC) al metabolito descarboetoxiloratadina es mayor que el fármaco precursor de la loratadina [ver FARMACOCINÉTICA, Poblaciones Especiales].
La loratadina y la descarboetoxiloratadina alcanzaron el estado estacionario en la mayoría de los pacientes en aproximadamente el quinto día de dosificación.
Estudios in vitro con microsomas hepáticos humanos indican que la loratadina es metabolizada a descarboetoxiloratadina predominantemente por el citocromo P450 3A4 (CYP3A4), y en un grado menor, por el citocromo P450 2D6 (CYP2D6). En presencia de ketoconazol, un inhibidor del CYP3A4, la loratadina es metabolizada a descarboetoxiloratadina principalmente por el CYP2D6. La administración concomitante de loratadina con ketoconazol, eritromicina (ambos inhibidores de CYP3A4), o cimetidina (inhibidor de CYP2D6 y CYP3A4) a voluntarios sanos, se asoció con concentraciones plasmáticas sustancialmente mayores de loratadina [ver INTERACCIONES MEDICAMENTOSAS Y DE OTRO GÉNERO].
Asma Bronquial: se puede utilizar en pacientes con rinitis alérgica que tengan asma bronquial.
Poblaciones Especiales:
Lactancia:
Montelukast: Los estudios en ratas lactantes a las que se les administraron 100 y 200 mg/kg/día de montelukast sódico han mostrado que se excreta en la leche materna. Las muestras de leche a las 4 horas posteriores a la dosificación contenían aproximadamente 31% a 33% de las concentraciones plasmáticas maternas. Sin embargo, no se han observado afectos adversos relacionados con el fármaco en los descendientes de las ratas hembras que recibieron el fármaco durante la lactancia. Dado que se desconoce la relevancia de estos hallazgos para los seres humanos, y que se desconoce si el montelukast se excreta en la leche humana, se debe tener precaución cuando se administre montelukast a las madres lactantes.
Loratadina: Loratadina y su metabolito, la descarboetoxiloratadina pasan con facilidad a la leche materna y alcanzan concentraciones que son equivalentes a los niveles plasmáticos con una relación ABCleche/ABCplasma de 1.17 y 0.85 para loratadina y descarboetoxiloratadina, respectivamente. Para una dosis oral única de 40 mg, se excretó una pequeña cantidad de loratadina y de descarboetoxiloratadina en la leche materna (aproximadamente 0.03% de 40 mg en el curso de 48 horas).
Insuficiencia Renal
Montelukast: Ya que el montelukast y sus metabolitos no se excretan en la orina, no se evaluó la farmacocinética de montelukast en pacientes con insuficiencia renal.
Loratadina: En un estudio que involucró a 12 sujetos con insuficiencia renal crónica (depuración de creatinina ≤ 30 mL/min) a los que se les dio loratadina sola, el ABC y la Cmáx incrementaron aproximadamente 73% para la loratadina y 120% para la descarboetoxiloratadina, comparado con 6 sujetos con función renal normal (depuración de creatinina ≥ 80 mL/min). Las vidas medias promedio de eliminación de loratadina (7.6 horas) y descarboetoxiloratadina (23.9 horas) no fueron substancialmente diferentes de las observadas en los sujetos normales. La hemodiálisis no tiene efecto alguno sobre la farmacocinética de la loratadina ni de la descarboetoxiloratadina en sujetos con insuficiencia renal crónica.
Insuficiencia Hepática
Montelukast: Los pacientes con insuficiencia hepática de leve a moderada y evidencia clínica de cirrosis, a los que se les administró montelukast solo, mostraron evidencia de un menor metabolismo de montelukast, resultando en un ABC 41% mayor (lC 90% = 7%, 85%) después de una dosis única de 10 mg. La eliminación del montelukast fue ligeramente prolongada comparada con la observada en los sujetos sanos (vida media promedio, 7.4 horas). La farmacocinética de montelukast en pacientes con insuficiencia hepática grave o con hepatitis no se ha evaluado.
Loratadina: En siete pacientes con hepatopatía alcohólica crónica, a los que se administró loratadina sola, el ABC y la Cmáx de la loratadina fueron el doble, en tanto que el perfil farmacocinético de la descarboetoxiloratadina no fue substancialmente diferente de los observados en otros estudios que reclutaron sujetos sanos. Las vidas medias de eliminación para la loratadina y la descarboetoxiloratadina fueron de 24 horas y 37 horas, respectivamente, y se acrecentaron con el incremento de la severidad de la enfermedad hepática.
Geriátricos
Montelukast: El perfil farmacocinético y la biodisponibilidad oral de una dosis oral única de 10 mg de montelukast son similares en los adultos mayores y en los jóvenes. La vida media plasmática de montelukast es ligeramente más prolongada en los adultos mayores.
Loratadina: En un estudio que involucró a 12 sujetos geriátricos sanos (66-78 años) administrados solo con loratadina, el ABC y los niveles plasmáticos máximos (Cmáx), tanto de loratadina como de descarboetoxiloratadina fueron aproximadamente 50% más altos que los observados en los estudios de los sujetos más jóvenes. Las vidas medias de eliminación promedio para los sujetos geriátricos fueron 18.2 horas (rango, 6.7-37 horas) para loratadina y 17.5 horas (rango, 11-38 horas) para la descarboetoxiloratadina.
Esta combinación ofrece el mismo beneficio sobre los componentes por separado.
ESTUDIOS CLÍNICOS
Rinitis Alérgica Estacional (SAR)
La eficacia clínica de MONTACLAR para el tratamiento de la rinitis alérgica estacional se investigó en cuatro estudios diseñados de forma similar, aleatorios, doble ciego, grupo paralelo, controlado con placebo y con activo (montelukast y loratadina). Los cuatro estudios reclutaron un total de 2,527 pacientes, de los cuales 775 fueron tratados con MONTACLAR. Los pacientes fueron de 15 a 82 años de edad con antecedentes de rinitis alérgica estacional, una prueba cutánea positiva para al menos un alergeno estacional relevante y síntomas activos de rinitis alérgica estacional al entrar al estudio. Los síntomas individuales registrados en las bitácoras de los pacientes durante un curso del tratamiento de 14 días fueron rinorrea, congestión nasal, estornudos y comezón; ojos llorosos, comezón, hinchazón y enrojecimiento valorados según el paciente en una escala de clasificación de 0 a 3.
La variable primaria de desenlace en dos estudios fue el cambio promedio respecto al inicio en las puntuaciones de los síntomas nasales diurnos (el promedio de puntuaciones individuales de congestión nasal, rinorrea, comezón nasal, estornudos) y en los otros dos estudios fue el cambio promedio respecto al inicio en las puntuaciones combinadas de los síntomas diurnos y nocturnos. Un punto de valoración final consistente, (TSS*, por sus siglas en inglés) también fue analizado para estos cuatro estudios en comparación con el placebo; las tabletas de MONTACLAR una vez al día disminuyeron significativamente las puntuaciones totales de los síntomas nocturnos (TSS) en los pacientes con rinitis alérgica estacional en los cuatro estudios (p≤0.045) (ver la Tabla 2).
Tabla 2: Efectos de MONTACLAR sobre la Puntuación de Síntomas Totales* en Cuatro estudios de Dosis Múltiple, Controlados con Placebo, Multi-céntricos en Pacientes con Rinitis Alérgica Estacional
|
MONTACLAR 10 mg/10 mg |
Placebo |
||
|
Estudio 1 |
Puntuación Promedio Inicial (N) |
14.06 (90) |
13.72 (89) |
|
Cambio Promedio desde el Inicio |
-4.12 |
-1.36 |
|
|
Diferencia Entre el Tratamiento y el Placebo (95% IC) |
-2.77 (-3.93, -1.61) |
NA |
|
|
Estudio 2 |
Puntuación Promedio Inicial (N) |
13.97 (174) |
14.20 (56) |
|
Cambio Promedio desde el Inicio |
-4.09 |
-1.90 |
|
|
Diferencia Entre el Tratamiento y el Placebo (95% IC) |
-2.19 (-3.49, -0.89) |
NA |
|
|
Estudio 3 |
Puntuación Promedio Inicial (N) |
13.40 (209) |
14.21(53) |
|
Cambio Promedio desde el Inicio |
-3.47 |
-2.27 |
|
|
Diferencia Entre el Tratamiento y el Placebo (95% IC) |
-1.21 (-2.39, -0.03) |
NA |
|
|
Estudio 4 |
Puntuación Promedio Inicial (N) |
13.56 (298) |
13.28 (148) |
|
Cambio Promedio desde el Inicio |
-4.00 |
-1.66 |
|
|
Diferencia Entre el Tratamiento y el Placebo (95% IC) |
-2.34 (-3.11, -1.58) |
NA |
* La puntuación total de síntomas es la suma de las 8 puntuaciones de síntomas individuales evaluados el día previo a la dosificación reflejando las últimas 12 horas del intervalo de dosificación. El rango de valores es de 0 a 24 (cada uno de los 8 síntomas clasificados como grave o 3).
La seguridad de MONTACLAR se investigó en dos estudios con un total de 542 pacientes con asma o con asma concurrente con rinitis alérgica. No se observó evidencia de un efecto nocivo en las mediciones de la función pulmonar o el control del asma, y los resultados de los dos estudios respaldan la seguridad de la administración de MONTACLAR a pacientes adultos con rinitis alérgica y asma de leve a moderada.
No hubo diferencias significativas en la efectividad de MONTACLAR tabletas entre los subgrupos de pacientes definidos por género, edad o raza.
Congestión Nasal en SAR: El alivio de la congestión nasal con MONTACLAR en sujetos con rinitis alérgica estacional fue evaluado en dos estudios. El primero, un estudio de dosis múltiple, controlado con placebo, doble ciego, reclutó un total de 1,095 pacientes (363 recibieron placebo, 363 recibieron MONTACLAR y 369 recibieron pseudoefedrina 240 mg una vez al día) quienes fueron tratados por 15 días. MONTACLAR fue significativamente más efectivo (P=0.009) que el placebo en disminuir la congestión nasal cuando se midió 12 horas y 24 horas (punto final primario) después de la dosificación. El efecto sobre la congestión nasal fue comparable con el observado con pseudoefedrina 240 mg, el fármaco activo de control empleado en el mismo estudio (vea la Tabla 3).
Tabla 3: Efectos de MONTACLAR en Congestión Nasal en un Estudio de Dosis Múltiple, Controlado con Placebo, Multi-centros en Pacientes con Rinitis Alérgica Estacional
|
Tiempo de Evaluación¥ Puntuación Inicial Media* |
MONTACLAR 10 mg/10 mg QD (362)† |
Placebo (360)† |
PSE 240 mg QD (368)†∞ |
|
|
Puntuación Inicial Promedio*± |
Mañana |
2.66 |
2.69 |
2.67 |
|
Noche |
2.64 |
2.65 |
2.63 |
|
|
Cambio Promedio*± desde nivel basal |
Mañana |
-0.56 |
-0.44 |
-0.57 |
|
Noche |
-0.67 |
-0.53 |
-0.72 |
|
|
Diferencia Entre el Tratamiento y el Placebo (95% IC) |
Mañana |
-0.12 ( -0.20,-0.03) |
NA |
-0.13 ( -0.21,-0.04) |
|
Noche |
-0.14 (-0.23,-0.05) |
NA |
-0.19 (-0.28,-0.10) |
* Ajustado basado en un ANOVA de dos vías con tratamiento y factores del sitio.
± Escala de 0 (sin síntomas) a 3 (grave).
¥ Medido en la Noche (12 horas después de la dosificación) y la siguiente Mañana (24 horas después de la dosificación).
† 1 paciente para MONTACLAR, 2 pacientes para placebo y 1 paciente para PSE no fueron evaluados post-nivel basal.
∞ 2 pacientes solamente tuvieron puntuaciones en la Noche.
El flujo nasal inspiratorio máximo (PNIF, por sus siglas en inglés), que medía el flujo de aire nasal por la mañana antes de la dosificación mostró aumentos promedio respecto al inicio hasta los Días 2 a 15 (el punto de tiempo primario) de 10.64 L/min para MONTACLAR, 10.06 L/min para pseudoefedrina y 5.05 L/min para el placebo. Los aumentos en PNIF fueron similares con la combinación loratadina/montelukast y pseudoefedrina, y ambos fueron mayores, en forma estadísticamente significativa, que los incrementos observados con el placebo (P≤0.001).
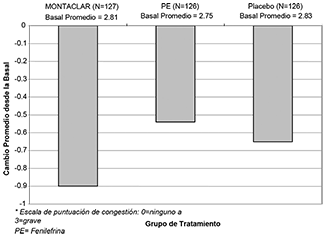
En el segundo estudio, síntomas de rinitis alérgica fueron inducidos en pacientes como respuesta a la exposición a polen de ambrosía, en una unidad de exposición ambiental. Una dosis única de MONTACLAR fue estadísticamente significativa superior al placebo (punto de evaluación final primario) y 10 mg de fenilefrina (punto de evaluación final secundario) en aliviar la congestión nasal (vea la Figura 1) y otros síntomas de la rinitis alérgica durante un periodo de 6 horas, medidos por una evaluación subjetiva y objetiva (PNIF) (todos los valores de P<0.03).
Figura 1: Cambio desde el nivel basal en la Congestión Nasal* 6 horas Post-tratamiento en un Estudio de Exposición Ambiental, de Dosis Única, Controlado con Placebo,
Cuestionario de Calidad de Vida en Rinoconjuntivitis (RQLQ, por sus siglas en inglés)
El RQLQ (una evaluación específica de alergia sobre la calidad de vida relacionada con la salud), fue evaluado en sujetos con rinitis alérgica estacional en cinco estudios controlados con placebo. Los estudios reclutaron un total de 3,622 pacientes (1,138 recibieron MONTACLAR 10/10 mg, 714 recibieron placebo, 369 recibieron pseudoefedrina 240 mg una vez al día, y 173 recibieron beclometasona 200 μg dos veces al día), quienes fueron tratados por lo menos 14 días. Evaluado por la puntuación total del RQLQ, MONTACLAR mejoró significativamente la calidad de vida de los pacientes comparado con placebo en cuatro de los cinco estudios.
Análisis acumulado de puntos finales de eficacia TSS, RQLQ y Congestión: Las dimensiones del efecto de MONTACLAR en los estudios pivotales de eficacia demostraron de manera consistente ser numéricamente mayores que con loratadina o montelukast en cuanto a TSS, RQLQ y congestión. En un análisis acumulado de 10 estudios de dosis múltiple (controlado con placebo y no controlado con placebo), MONTACLAR fue superior al placebo (p<0.001), loratadina (p<0.003), y montelukast (p<0.022) para todas las comparaciones entre los tres puntos de valoración final: TSS, RQLQ y congestión, proporcionando evidencias que respaldan el hecho de que el beneficio numérico observado para estos puntos de valoración final fue significativo.
Rinitis alérgica perenne (RAP): Aunque no hay estudios para MONTACLAR, la seguridad y la eficacia tanto de montelukast como de loratadina han sido bien establecidas para el tratamiento de rinitis alérgica perenne.
Inicio de la acción: En estudios controlados con placebo, el efecto del tratamiento de MONTACLAR, medido por la Puntuación Total de Síntomas (TSS), se alcanzó después de la primera dosis y se mantuvo a través de los intervalos de dosificación (24 horas). Los estudios realizados en entornos de provocación mediante exposición ambiental demostraron un inicio de acción para MONTACLAR, basado en los cambios en la TSS, que varió entre 75 minutos y 140 minutos.
VI. CONTRAINDICACIONES
MONTACLAR está contraindicado en pacientes con hipersensibilidad a montelukast, a la loratadina o a cualquier otro componente de este producto.
MONTACLAR está contraindicado en pacientes con insuficiencia hepática grave porque pueden tener una menor depuración de loratadina.
VII. PRECAUCIONES GENERALES
Se han reportado trastornos del sueño y cambio de comportamiento/humor en pacientes que toman montelukast. Los médicos deben discutir estas experiencias adversas con sus pacientes y/o cuidadores. Debe indicarse a los pacientes y/o cuidadores que notifiquen al médico si se presentan alteraciones de este tipo (ver IX. REACCIONES SECUNDARIAS Y ADVERSAS, Análisis acumulado de las Experiencias de los Estudios Clínicos y Experiencia Post-comercialización).
Las siguientes precauciones están asociadas con el uso de montelukast para el tratamiento del asma: La eficacia de montelukast oral para el tratamiento de ataques agudos de asma no se ha establecido. Por consiguiente, montelukast oral no debe ser usado para tratar ataques agudos de asma. Se debe aconsejar a los pacientes que tengan siempre disponible el medicamento de rescate apropiado.
Mientras que la dosis del corticosteroide inhalado concomitante puede ser reducida gradualmente bajo supervisión médica, el montelukast no debe ser substituido abruptamente por corticosteroides inhalados u orales.
En casos raros, pacientes que reciben fármacos antiasmáticos incluyendo antagonistas de receptores de leucotrienos han experimentado uno o más de los siguientes: eosinofilia, exantema vasculítico, empeoramiento de los síntomas pulmonares, complicaciones cardiacas, y/o neuropatía algunas veces diagnosticada como síndrome Churg-Strauss, una vasculitis eosinofílica sistémica. En algunas ocasiones, estos casos han sido asociados con la reducción o suspensión del tratamiento oral con corticosteroide. Aunque no se ha establecido una relación causal con el antagonismo de los receptores de leucotrienos, se recomienda precaución y supervisión clínica apropiadas en pacientes que estén recibiendo montelukast.
Uso Pediátrico
La seguridad y la eficacia de MONTACLAR 10 mg/10 mg no han sido evaluadas en pacientes menores de 15 años de edad.
VIII. RESTRICCIONES DE USO DURANTE EL EMBARAZO Y LA LACTANCIA
EMBARAZO
MONTACLAR: No existen estudios adecuados y bien controlados en mujeres embarazadas. Este fármaco debe ser usado durante el embarazo sólo si es claramente necesario.
Montelukast: La información disponible de estudios de cohortes prospectivos y retrospectivos publicados sobre el uso de montelukast en mujeres embarazadas, que evaluaron defectos congénitos mayores, no han establecido un riesgo asociado con el medicamento. Los estudios disponibles tienen limitaciones metodológicas, incluyendo un tamaño de muestra pequeño, en algunos casos recolección de información retrospectiva, e inconsistencia en los grupos comparativos.
Loratadina: La loratadina solamente se debe usar si el beneficio potencial justifica el riesgo potencial para el feto o el recién nacido.
LACTANCIA
Se debe tener precaución cuando se administre MONTACLAR a una madre lactante.
Montelukast: No se sabe si el montelukast se excreta en la leche materna. Debido a que muchos fármacos son excretados en la leche humana, se debe tener precaución cuando se administra montelukast a una madre lactante.
Loratadina: La loratadina solamente debe ser usada si el beneficio potencial justifica el riesgo potencial para el feto o el recién nacido.
IX. REACCIONES SECUNDARIAS Y ADVERSAS
Experiencia en Estudios Clínicos
MONTACLAR fue estudiado en más de 3,800 pacientes en 21 estudios clínicos. Las reacciones adversas comunes agrupadas, reportadas con una frecuencia de ≥ 1% para el placebo y MONTACLAR en 7 estudios clínicos de dosis múltiple, controlados con placebo se muestran en la Tabla 4.
Tabla 4. Reacciones Adversas Comunes (≥ 1%) Reportadas para Placebo y MONTACLAR Durante Estudios Clínicos de Dosis Múltiple, Controlados con Placebo en Pacientes con Rinitis Alérgica Estacional
|
Reacción Adversa |
Placebo (%) N = 1,111 |
MONTACLAR (%) N = 1,529 |
|
Trastornos del Sistema Nervioso |
||
|
Cefalea |
1.7 |
1.4 |
Otras reacciones adversas no comunes (≥ 0.1 y < 1%) reportadas para MONTACLAR durante los estudios clínicos en pacientes con rinitis alérgica estacional (SAR) fueron: somnolencia, sed, letargia, cefalea sinusal, tos, epistaxis, molestia nasal, sequedad nasal, diarrea, irritabilidad, dolor faringolaríngeo, dispepsia, vómito, mareo, boca seca, náusea, fatiga, anorexia e insomnio, todos ellos han reportado incidencias similares a las del placebo.
El perfil de seguridad de MONTACLAR en estudios clínicos fue similar al de montelukast y loratadina individualmente. Debido a que los estudios clínicos son conducidos bajo condiciones controladas y que varían ampliamente, las tasas de reacción adversa observadas en los estudios clínicos de un fármaco no pueden ser comparadas directamente con las tasas en los estudios clínicos de otro fármaco y no puede predecir las tasas observadas en una población de pacientes más amplia en la práctica clínica.
Análisis Agrupado de la Experiencia en Estudios Clínicos de Montelukast (monoterapia): En un análisis agrupado que empleó un método validado para evaluar las tendencias suicidas en 41 estudios clínicos controlados con placebo (35 estudios en pacientes de 15 años de edad y mayores; 6 estudios en pacientes pediátricos de 6 a 14 años de edad). Entre los 9,929 pacientes que recibieron montelukast y 7,780 pacientes que recibieron placebo en estos estudios, hubo un paciente con ideas suicidas en el grupo que tomaba montelukast. No hubo suicidios completados, intentos de suicidio o actos preparatorios hacia el comportamiento suicida en ninguno de los grupos de tratamiento.
Se realizó otro análisis agrupado de 46 estudios clínicos controlados con placebo (35 estudios en pacientes de 15 años de edad y mayores; 11 estudios en pacientes pediátricos de 3 meses a 14 años de edad) que evaluaron las reacciones adversas relacionadas con el comportamiento (BRAEs). Entre los 11,673 pacientes que recibieron montelukast y 8,827 pacientes que recibieron placebo en estos estudios, la frecuencia de pacientes con al menos una BRAE fue de 2.73% en pacientes que recibieron montelukast y 2.27% en pacientes que recibieron placebo; la razón de momios fue de 1.12 (IC 95% [0.93; 1.36]).
Los estudios clínicos incluidos en este análisis combinado no fueron diseñados específicamente para examinar las tendencias suicidas o BRAEs.
Experiencia Post-comercialización: Se han identificado las siguientes reacciones adversas durante el uso posterior a la aprobación de montelukast y loratadina. Debido a que estas reacciones son reportadas de manera voluntaria de una población de tamaño incierto, no siempre es posible estimar su frecuencia de manera confiable o establecer una relación causal por la exposición a MONTACLAR.
Montelukast (monoterapia):
Infecciones e infestaciones: infección de vías respiratorias altas.
Trastornos de la sangre y del sistema linfático: tendencia aumentada al sangrado, trombocitopenia.
Trastornos del sistema inmune: reacciones de hipersensibilidad incluyendo anafilaxia, muy raramente infiltración eosinofílica hepática.
Trastornos psiquiátricos: agitación, incluyendo comportamiento agresivo y hostilidad, ansiedad, depresión, desorientación, alteración de la atención, alteraciones del sueño, disfemia (tartamudeo), alucinaciones, insomnio, deterioro de la memoria, síntomas obsesivo-compulsivos, hiperactividad psicomotora (incluyendo irritabilidad, inquietud y temblores), sonambulismo, pensamientos y comportamiento suicida (tendencias suicidas), tic.
Trastornos del sistema nervioso: mareo, somnolencia, parestesia/hipoestesia, muy rara vez convulsiones.
Trastornos cardiacos: palpitaciones.
Trastornos respiratorios, torácicos y del mediastino: epistaxis, eosinofilia pulmonar.
Trastornos gastrointestinales: diarrea, dispepsia, náusea, vómito.
Trastornos hepatobiliares: aumento de ALT y AST, muy rara vez hepatitis (incluyendo lesión hepática de patrón mixto, colestático, y hepatocelular).
Trastornos del tejido subcutáneo y piel: angioedema, moretones, eritema multiforme, eritema nodoso, prurito, exantema, urticaria.
Trastornos del tejido osteomuscular y conectivo: artralgia, mialgia incluyendo calambres musculares.
Trastornos renales y urinarios: enuresis en niños.
Trastornos generales y condiciones del sitio de administración: astenia/fatiga, edema pirexia.
Loratadina (monoterapia):
Trastornos del sistema inmune: anafilaxia (incluyendo angioedema).
Trastornos del sistema nervioso: mareo, convulsión.
Trastornos cardiacos: palpitaciones, taquicardia.
Trastornos hepatobiliares: función hepática anormal.
Trastornos de la piel y del tejido subcutáneo: alopecia.
X. INTERACCIONES MEDICAMENTOSAS Y DE OTRO GÉNERO
No se han realizado estudios de interacción medicamentosa con MONTACLAR. Se espera que las interacciones medicamentosas de la combinación reflejen las de sus componentes por separado.
Interacciones de Montelukast
El montelukast, administrado en una dosis de 10 mg una vez al día hasta el equilibrio dinámico farmacocinético, no causó cambios clínicamente significativos en la farmacocinética de una dosis única intravenosa de teofilina (predominantemente un substrato del citocromo P450 1A2) y no modificó el perfil farmacocinético de la warfarina (predominantemente un sustrato del CYP2C9, 3A4 y 1A2) o influenció el efecto de una sola dosis oral de 30 mg de warfarina, sobre el tiempo de protrombina o el índice internacional normalizado (INR, por sus siglas en inglés). No hubo cambio en el perfil farmacocinético o en la excreción urinaria de digoxina inmunoreactiva o el perfil de concentración plasmática de la terfenadina (un substrato de CYP3A4) o fexofenadina, su metabolito carboxilado, y no prolongó el intervalo QTc después de la administración concomitante con terfenadina 60 mg dos veces al día.
El montelukast en dosis de ≥ 100 mg diarios, dosificado para un estado estacionario farmacocinético, no cambió significativamente las concentraciones plasmáticas de ninguno de los componentes de un anticonceptivo oral que contenía 1 mg noretrindona/35 μg de etinilestradiol o causó algún cambio clínicamente significativo en los perfiles plasmáticos de prednisona o prednisolona después de la administración de prednisona oral o prednisolona intravenosa.
El fenobarbital, el cual induce metabolismo hepático, disminuyó el ABC de montelukast aproximadamente 40% después de una dosis única de 10 mg de montelukast. No se recomienda ajuste de la dosificación de montelukast. Es razonable emplear el monitoreo clínico apropiado cuando se co-administran inductores potentes de las enzimas del citocromo P450,tales como fenobarbital o la rifampicina con montelukast.
Basado en los resultados in vitro en microsomas hepáticos humanos, las concentraciones plasmáticas terapéuticas de montelukast no inhiben los citocromos P450 3A4, 2C9, 1A2, 2A6, 2C19, o 2D6. El montelukast es un inhibidor de CYP2C8 in vitro. Sin embargo, los datos de un estudio de interacciones medicamentosas con montelukast y rosiglitazona (una sustancia de prueba representativa de fármacos principalmente metabolizados por el CYP2C8) demostraron que montelukast no inhibe el CYP2C8 in vivo. Por consiguiente, no se prevé que el montelukast altere el metabolismo de los fármacos metabolizados por esta enzima (por ejemplo, paclitaxel, rosiglitazona y repaglinida).
Estudios in vitro han demostrado que montelukast es un sustrato de CYP 2C8, 2C9 y 3A4. Los datos de un estudio de interacciones medicamentosas implicando montelukast y gemfibrozil (un inhibidor tanto de CYP 2C8 como de 2C9) demostró que el gemfibrozil aumentó la exposición sistémica de montelukast 4.4 veces. La co-administración de itraconazol, un inhibidor potente de CYP3A4, con gemfibrozil y montelukast no aumentó más la exposición sistémica del montelukast. El efecto de gemfibrozil sobre la exposición sistémica de montelukast no se consideró como clínicamente significativo basado en los datos de seguridad clínica con dosis mayores de 10 mg de la dosis aprobada en adultos (por ejemplo, 200 mg/día para pacientes adultos por 22 semanas, y hasta 900 mg/día para pacientes por aproximadamente una semana) donde las experiencias adversas clínicamente importantes no se observaron. Por lo tanto, no se requiere un ajuste de la dosis de montelukast con la co-administración con gemfibrozil. Basado en los datos in vitro, no se anticipan interacciones medicamentosas clínicamente importantes con otros inhibidores conocidos del CYP2C8 (por ejemplo, trimetoprima). Además, la co-administración de montelukast con itraconazol solo resultó en un aumento no significativo en la exposición sistémica del montelukast.
Interacciones de la loratadina: La loratadina a una dosis de 10 mg una vez al día, ha sido administrada concomitantemente con dosis terapéuticas de eritromicina, cimetidina y ketoconazol en estudios controlados de farmacología clínica en voluntarios adultos. Se observaron concentraciones plasmáticas elevadas (ABC[0-24 hr]) de loratadina (40%, 103% y 307%, respectivamente) y/o descarboetoxiloratadina (46%, 6% y 73%, respectivamente), después de la co-administración de loratadina con cada uno de estos fármacos en voluntarios normales (n = 24 en cada estudio).
En estos estudios de interacción, no hubo cambios clínicamente relevantes en el perfil de seguridad de la loratadina, evaluado mediante parámetros electrocardiográficos, pruebas de laboratorio clínico, signos vitales y reacciones adversas. Tampoco hubo efectos significativos sobre los intervalos QTc y no se reportaron sedación o síncope. No se observaron efectos sobre las concentraciones plasmáticas de cimetidina o ketoconazol. Las concentraciones plasmáticas (AUC[0-24 hr.]) de eritromicina disminuyeron 15% con la administración concomitante de loratadina respecto a las observadas con eritromicina sola; sin embargo, la relevancia clínica de estas diferencias se desconoce.
XI. ALTERACIONES EN LOS RESULTADOS DE PRUEBAS DE LABORATORIO
No hubo diferencias significativas entre los grupos tratados con la combinación de montelukast/loratadina y con placebo en la aparición de reacciones adversas de laboratorio relacionadas con el fármaco en los estudios clínicos en pacientes adultos.
INTERACCIONES DE LA PRUEBA DE LABORATORIO:
El tratamiento con MONTACLAR debe ser descontinuado aproximadamente 48 horas antes de realizar cualquier prueba cutánea, ya que los fármacos antihistamínicos pueden prevenir o disminuir las reacciones de hipersensibilidad cutánea.
XIII. DOSIS Y VÍA DE ADMINISTRACIÓN
Vía de administración: Oral.
General
MONTACLAR no debe usarse de manera concomitante con otros productos que contengan los mismos ingredientes activos, montelukast o loratadina.
Adultos
Adultos y adolescentes de 15 años de edad y mayores: La dosis recomendada de MONTACLAR es una tableta (montelukast 10 mg/loratadina 10 mg) una vez al día. El tiempo de administración puede ser individualizado en los pacientes con rinitis alérgica para ajustarse a las necesidades del paciente. Los pacientes con rinitis alérgica deben tomar solo una tableta diaria por la noche.
Recomendaciones Generales para los Pacientes con Rinitis Alérgica y Asma
El efecto terapéutico de MONTACLAR sobre los parámetros de control del asma aparece en el transcurso de un día. A los pacientes se les debe recomendar continuar tomando MONTACLAR mientras su asma esté controlada, así como también durante los periodos de empeoramiento del asma.
Tratamiento con MONTACLAR en Relación con Otros Tratamientos para Asma: MONTACLAR puede ser adicionado al régimen de tratamiento existente del paciente.
Reducción en la Terapia Concomitante:
Tratamiento con Broncodilatador: MONTACLAR puede adicionarse al régimen de tratamiento del paciente que no está adecuadamente controlado con un broncodilatador solo. Cuando la respuesta clínica es evidente (habitualmente después de la primera dosis), puede reducirse el tratamiento broncodilatador del paciente conforme éste lo tolere.
Corticosteroides Inhalados: El tratamiento con MONTACLAR proporciona un beneficio clínico adicional a los pacientes tratados con corticosteroides inhalados. Se puede hacer una reducción en la dosis del corticosteroide, según se tolere. La dosis debe ser reducida gradualmente bajo supervisión médica. En algunos pacientes, la dosis de los corticosteroides inhalados puede disminuirse completamente. MONTACLAR no debe ser substituido abruptamente por corticosteroides inhalados.
XIV. MANIFESTACIONES Y MANEJO DE LA SOBREDOSIFICACIÓN O INGESTA ACCIDENTAL
MONTACLAR: En el caso de sobredosis, las medidas generales sintomáticas y de apoyo deben instituirse rápidamente y mantenerse por tanto tiempo como sea necesario.
Montelukast: No se tiene disponible información específica sobre el tratamiento de la sobredosis con montelukast. En estudios de asma crónica, montelukast ha sido administrado en dosis de hasta 200 mg/día a pacientes adultos por 22 semanas y, en estudios de corto plazo, hasta 900 mg/día a pacientes por aproximadamente una semana sin experiencias adversas clínicamente importantes.
Ha habido reportes de sobredosis grave en la experiencia post-comercialización y en estudios clínicos con montelukast. Estos incluyen reportes en adultos y en niños con una dosis tan alta como 1,000 mg. Los hallazgos clínicos y de laboratorio observados fueron consistentes con el perfil de seguridad en pacientes adultos y pediátricos. No hubo experiencias adversas en la mayoría de los reportes de sobredosis. Las reacciones adversas más comunes fueron consistentes con el perfil de seguridad de montelukast e incluyeron dolor abdominal, somnolencia, sed, cefalea, vómito e hiperactividad psicomotora. No se sabe si el montelukast es removido por diálisis peritoneal o por hemodiálisis.
Loratadina: En adultos, se han reportado somnolencia, taquicardia y cefalea con sobredosis de loratadina mayores de 10 mg con la formulación de tableta (40-180 mg). Se han reportado signos extra-piramidales y palpitaciones en niños con sobredosis de más de 10 mg de loratadina. La loratadina no se elimina por hemodiálisis. No se sabe si la loratadina es eliminada por diálisis peritoneal.
Medidas generales sintomáticas y de soporte se deben instituir y mantener el tiempo que sean necesarias.
XII. PRECAUCIONES EN RELACIÓN CON EFECTOS DE CARCINOGÉNESIS, MUTAGÉNESIS, TERATOGÉNESIS Y SOBRE LA FERTILIDAD
Se realizaron estudios de mutagénesis y fertilidad con la combinación de montelukast y loratadina. Los estudios de carcinogenicidad se condujeron con montelukast o loratadina, pero no con la combinación de ambos fármacos.
Estudios de Carcinogenicidad
Montelukast: No se observaron evidencias de tumorigenicidad en un estudio de carcinogenicidad de 2 años en ratas Sprague Dawley, en dosis orales (por sonda gástrica) de hasta 200 mg/kg/día (la exposición estimada en ratas fue aproximadamente 120 veces el ABC en adultos y 75 veces el ABC en niños) o en un estudio de carcinogenicidad de 92 semanas en ratones en dosis orales hasta de 100 mg/kg/día (la exposición estimada en ratones fue aproximadamente 45 veces el ABC para adultos y 25 veces el ABC para niños, en las dosis orales diarias máximas recomendadas).
Loratadina: en un estudio de carcinogenicidad de 18 meses en ratones y un estudio de 2 años en ratas, la loratadina se administró en la dieta en dosis de hasta 40 mg/kg (ratones) y 25 mg/kg (ratas). En el estudio de carcinogenicidad en ratón, se llevaron a cabo evaluaciones farmacocinéticas para determinar la exposición de los animales al fármaco. Los datos sobre el ABC demostraron que la exposición de ratones que recibieron 40 mg/kg de loratadina fue 3.6 veces más alta (loratadina) y 18-veces más alta (descarboetoxiloratadina) que en los humanos a los que se les dio la dosis oral diaria máxima recomendada. La exposición de las ratas que recibieron 25 mg/kg de loratadina fue 28 veces más alta (loratadina) y 67-veces más alta (descarboetoxiloratadina) que en los humanos que recibieron la máxima dosis oral diaria recomendada. Los ratones machos que recibieron 40 mg/kg tuvieron una incidencia significativamente mayor de tumores hepatocelulares (adenomas y carcinomas combinados) que los controles concurrentes. En las ratas, se observó una incidencia significativamente mayor de tumores hepatocelulares (adenomas y carcinomas combinados) en los machos que recibieron 10 mg/kg y machos y hembras a los que se les dieron 25 mg/kg. La significancia clínica de estos hallazgos durante el uso a largo plazo de la loratadina se desconoce.
Estudios de mutagenicidad
MONTACLAR: En estudios de toxicología genética, incluyendo un ensayo de mutagenicidad bacteriana, un estudio de aberraciones cromosómicas en ovario de hámster Chino, y un estudio de micronúcleos de médula ósea en ratón, no hubo evidencia de potencial mutagénico ni clastogénico para la combinación de montelukast y loratadina.
Reproducción
MONTACLAR: Se han realizado estudios sobre la reproducción en ratas y conejos con dosis de hasta 18/18 mg/kg y 90/90 mg/kg (montelukast/loratadina) o 15 y 146 veces la dosis humana, respectivamente y no han mostrado evidencia alguna de alteración de la fertilidad ni daño fetal debido a MONTACLAR.
Estudios de Fertilidad
MONTACLAR: Efectos sobre la fertilidad en ratas macho con el producto de combinación se observaron con aproximadamente 23 veces la dosis diaria humana máxima recomendada con base en un ABC de loratadina. Esto es consistente con los hallazgos preclínicos previos en ratas macho con monoterapia de loratadina. No se observaron efectos sobre la fertilidad en ratas macho hasta con 158 veces de la dosis diaria humana máxima recomendada sobre una base de ABC con monoterapia con montelukast. Con base en la amplia experiencia con montelukast y loratadina, tanto clínica como posterior a la comercialización, lo anterior no tiene relevancia clínica para los humanos.
XVIII. NOMBRE Y DOMICILIO DEL LABORATORIO
SCHERING-PLOUGH, S.A. de C.V.
Av. 16 de Septiembre No. 301, Col. Xaltocan
C.P. 16090,
Xochimilco,
Ciudad de México, México.
XV. PRESENTACIÓN
Caja de cartón con 15 o 30 tabletas e instructivo anexo.
XVI. RECOMENDACIONES SOBRE ALMACENAMIENTO
Consérvese a no más de 25°C.
Consérvese la caja bien cerrada.
XVII. LEYENDAS DE PROTECCIÓN
Literatura exclusiva para médicos.
Su venta requiere receta médica.
No se deje al alcance de los niños.
MONTACLAR tabletas no está indicado para usarse en niños menores de 15 años de edad.
Su uso durante el embarazo o lactancia es responsabilidad del médico tratante.
Este medicamento contiene lactosa, que puede producir reacciones de hipersensibilidad.
Este medicamento puede producir somnolencia y afectar el estado de alerta, por lo que no deberá conducir vehículos automotores ni maquinaria pesada durante su uso.
Reporte las sospechas de reacción adversa al correo:
farmacovigilancia@cofepris.gob.mx
y dpocmx@merck.com
