VALCIDEM - Solución
Sustancia(s):
- Vancomicina
Presentaciones:
- 1 Charola, 10 Frasco(s) ámpula, 500 Miligramos
FORMA FARMACÉUTICA Y FORMULACIÓN:
Cada frasco ámpula con liofilizado contiene:
Clorhidrato de vancomicina equivalente a Vancomicina 500 mg
Excipiente cbp
INDICACIONES TERAPÉUTICAS: El clorhidrato de vancomicina está indicado para el tratamiento de las infecciones severas o graves causadas por cepas susceptibles de estafilococos resistentes a la meticilina (resistentes a betalactamasas). También está indicado en los pacientes alérgicos a la penicilina o en aquellos que no pueden recibir otros medicamentos o que han dejado de responder a los mismos, incluyendo penicilinas o cefalosporinas, así como en el tratamiento de las infecciones causadas por microorganismos susceptibles a la vancomicina que son resistentes a otros medicamentos antimicrobianos.
El clorhidrato de vancomicina es eficaz en el tratamiento de la endocarditis estafilocócica. Su eficacia ha sido documentada en otras infecciones causadas por estafilococos, incluyendo septicemia, infecciones óseas, infecciones de las vías respiratorias inferiores e infecciones cutáneas y de la estructura cutánea. Cuando las infecciones estafilocócicas son purulentas y están localizadas, los antibióticos se usan como coadyuvantes de las medidas quirúrgicas apropiadas.
Se ha reportado que el clorhidrato de vancomicina es eficaz solo o en combinación con un aminoglucósido en el tratamiento de la endocarditis causada por Streptococcus viridans o S. bovis. En la endocarditis causada por enterococos (por ejemplo E. faecalis) se ha reportado que el clorhidrato de vancomicina es eficaz únicamente en combinación con un aminoglucósido.
Se ha reportado que el clorhidrato de vancomicina es eficaz en el tratamiento de la endocarditis difteroide. El clorhidrato de vancomicina se ha utilizado exitosamente en combinación con rifampicina, un aminoglucósido, o ambos en la endocarditis de válvula protésica de comienzo precoz causada por S. epidermis o difteroides.
La forma parenteral del clorhidrato de vancomicina puede administrarse por vía oral en el tratamiento de la colitis pseudomembranosa relacionada con el uso de antibióticos producida por C. difficile y para la enterocolitis estafilocócica. No se ha comprobado que la administración parenteral de clorhidrato de vancomicina por sí mismo sea beneficiosa para estas indicaciones. El clorhidrato de vancomicina no es eficaz por vía oral contra otro tipo de infecciones.
Para reducir el desarrollo de bacterias resistentes a los medicamentos y para mantener la eficacia de la vancomicina y otros medicamentos antibacterianos, la vancomicina debe utilizarse solamente para tratar o prevenir infecciones de las que se esté seguro, o se tenga la firme sospecha, de que son causadas por bacterias susceptibles. Por tal motivo deben obtenerse muestras para cultivos bacteriológicos para aislar e identificar los microorganismos causantes y para determinar su susceptibilidad al clorhidrato de vancomicina.
FARMACOCINÉTICA Y FARMACODINAMIA:
Propiedades Farmacocinéticas: La vancomicina difícilmente se absorbe desde el tracto gastrointestinal normal y, por lo tanto, no es efectivo mediante la administración oral para el tratamiento de infecciones que no sean enterocolitis estafilocócica ni colitis pseudomembranosa por Clostridium difficile; se administra por vía intravenosa para el tratamiento de infecciones sistémicas. La inyección intramuscular es dolorosa.
En sujetos con función renal normal, la dosificación múltiple de 500 mg infundidos durante 30 minutos produce concentraciones plasmáticas promedio de alrededor de 49 mg/L al finalizar la infusión, concentraciones plasmáticas promedio de alrededor de 19 mg/L dos horas después de la infusión, y concentraciones plasmáticas promedio de alrededor de 10 mg/L seis horas después de la infusión. Las concentraciones plasmáticas durante la dosificación múltiple son similares a las concentraciones observadas después de una dosis única.
La vida media de eliminación promedio de vancomicina del plasma es de 4 a 6 horas en sujetos con función renal normal. En las primeras 24 horas, aproximadamente el 75% de una dosis administrada de vancomicina se excreta en la orina por filtración glomerular. La depuración plasmática promedio es de aproximadamente 0.058 L/kg/h, y la depuración renal promedio es de aproximadamente 0.048 L/kg/h. La disfunción renal hace que la excreción de la vancomicina sea más lenta. En pacientes anéfricos, la vida media de eliminación promedio es de 7.5 días. El volumen de distribución es de 0.39 a 0.97 L/kg. No hay aparente metabolismo del fármaco.
La vancomicina se une a las proteínas séricas aproximadamente en un 55%, de acuerdo a la medición por ultrafiltración con concentraciones séricas de vancomicina de 10 a 100 mg/L. Después de la administración I.V. de clorhidrato de vancomicina, se presentan concentraciones inhibitorias en los líquidos pleural, pericárdico, ascítico y sinovial, así como en la orina, en el líquido de diálisis peritoneal y en el tejido del apéndice auricular. El clorhidrato de vancomicina no difunde fácilmente al líquido cefalorraquídeo a través de las meninges normales, pero penetra al líquido cefalorraquídeo si las meninges están inflamadas.
La depuración sistémica y renal total de vancomicina puede ser menor en los sujetos de edad avanzada debido a la disminución natural de la filtración glomerular.
Por lo general, vancomicina administrada por vía oral no entra a la circulación sistémica incluso cuando hay lesiones inflamatorias presentes. Pueden presentarse concentraciones séricas medibles con poca frecuencia en pacientes con colitis pseudomembranosa activa inducida por C. difficile y, en la presencia de disfunción renal, existe la posibilidad de acumulación.
La administración de vancomicina solución oral 2 g diarios durante 16 días a pacientes anéfricos sin enfermedad inflamatoria intestinal, entregó niveles séricos de < 0.66 mg/l. Con dosis de 2 g diarios, se pueden encontrar concentraciones de 3100 mg/kg en las heces y se pueden encontrar niveles de < 1 μg/mL en el suero de pacientes con función renal normal que tienen colitis pseudomembranosa.
Propiedades Farmacodinámicas.
Código ATC: J01 XA01 para administración intravenosa.
Clorhidrato de Vancomicina Inyectable, grado USP, intravenoso, es un antibiótico glicopéptido tricíclico cromatográficamente purificado que se deriva de Amycolatopsis orientalis (anteriormente Nocardia orientalis).
La acción bactericida de la vancomicina se debe principalmente a la inhibición de la biosíntesis de la pared celular. Además la vancomicina afecta la permeabilidad de la membrana celular bacteriana y también la síntesis del ARN. No hay resistencia cruzada entre la vancomicina y otros antibióticos.
Se ha demostrado que la vancomicina es activa contra la mayoría de cepas de los siguientes microorganismos, tanto in vitro como en infecciones clínicas, tal como se describen en la sección Indicaciones terapéuticas.
Puntos de Quiebre de la CIM Clínica del EUCAST:
|
CIM Clínica del EUCAST (versión 6.0, válida desde el 2016-01-01) |
||
|
Microorganismo |
Puntos de Quiebre (mg/L) |
|
|
Susceptible |
Resistente |
|
|
Especies de Staphylococcus (S. aureus) |
≤ 21 |
> 2 |
|
Estafilococo coagulasa negativo |
≤ 41 |
> 4 |
|
Especie de Enterococcus |
≤ 4 |
> 4 |
|
Streptococcus ABCG |
≤ 21 |
> 2 |
|
Streptococcus pneumoniae |
≤ 21 |
> 2 |
|
Streptococcus viridans |
≤ 21 |
> 2 |
|
Anaerobios grampositivos |
≤ 2 |
> 2 |
|
Clostridium difficile |
≤ 22 |
> 22 |
|
Especies de Corynebacterium |
≤ 2 |
> 2 |
1 Los aislados no susceptibles son poco frecuentes o aún no se han informado. Se debe confirmar el resultado de la identificación y de la prueba de susceptibilidad antimicrobiana sobre tal aislado y se debe enviar el aislado a un laboratorio de referencia.
2 Los puntos de quiebre tienen base en los valores de corte epidemiológicos (ECOFF), que distinguen a los aislados en estado natural de aquellos con susceptibilidad reducida.
La prevalencia de la resistencia adquirida puede variar geográficamente y con el tiempo para las especies seleccionadas y es recomendable la información local sobre la resistencia, especialmente cuando se tratan infecciones severas. Según sea necesario, se deberá buscar una opinión experta cuando la prevalencia local de la resistencia sea tal que la utilidad del agente sea cuestionable, al menos en algunos tipos de infecciones.
Especies comúnmente susceptibles:
Aerobios Gram-positivos:
Difteroides.
Enterococos (por ejemplo, Enterococcus faecalis).
Estafilococos, incluyendo Staphylococcus aureus, Staphylococcus epidermidis y Estafilococos coagulasa negativos.
Listeria monocytogenes.
Streptococcus pyogenes.
Streptococcus pneumoniae.
Streptococcus B, C y G.
Streptococcus viridans.
Especies para las que la resistencia adquirida puede ser un problema:
Aerobios grampositivos:
Enterococcus faecium.
Clostridium difficile (es decir, cepas toxigénicas involucradas en la colitis pseudomembranosa) es una especie objetivo para administración oral donde se alcanzan las concentraciones intraluminales altas de vancomicina.
CONTRAINDICACIONES: El clorhidrato de vancomicina Inyectable, grado USP, está contraindicado en los pacientes que se sabe son hipersensibles a este antibiótico.
RESTRICCIONES DE USO DURANTE EL EMBARAZO Y LA LACTANCIA:
Uso en embarazo: Se han realizado estudios de teratología en 5 veces la dosis humana en ratas y 3 veces la dosis humana en conejos, y no se ha revelado evidencia de daño al feto por vancomicina. En un estudio clínico controlado, los posibles efectos ototóxicos y nefrotóxicos del clorhidrato de vancomicina en infantes fue evaluado cuando el medicamento se administró en mujeres embarazadas que tenían infecciones estafilocócicas graves que ocurrieron como complicación del abuso de los fármacos. Se encontró clorhidrato de vancomicina en la sangre umbilical. No se observó pérdida neurosensorial auditiva ni nefrotoxicidad atribuible a la vancomicina. Un infante cuya madre recibió vancomicina en el tercer trimestre experimentó pérdida auditiva que no se atribuyó a la administración de vancomicina. Debido a que el número de pacientes tratados en este estudio fue limitado y debido a que la vancomicina se administró únicamente en el segundo y tercer trimestre, no se sabe si vancomicina causa daño fetal. La vancomicina se administrará en mujeres embarazadas únicamente cuando sea estrictamente necesario y los niveles en sangre se deben monitorear cuidadosamente para minimizar el riesgo de toxicidad fetal. Sin embargo, se ha informado que las pacientes embarazadas pueden requerir dosis significativamente mayores de vancomicina para alcanzar concentraciones séricas terapéuticas.
Uso en lactancia: La vancomicina se excreta en la leche humana. Se debe proceder con cautela al administrar vancomicina en mujeres que estén lactando. No es probable que un lactante pueda absorber una cantidad significativa de vancomicina desde el tracto gastrointestinal.
REACCIONES SECUNDARIAS Y ADVERSAS:
Eventos relacionados con la infusión: Durante o poco después de la infusión rápida de clorhidrato de vancomicina, los pacientes pueden desarrollar reacciones anafilactoides, incluyendo hipotensión, sibilancias, disnea, urticaria o purito. La infusión rápida también puede causar rubefacción de la parte superior del cuerpo ("síndrome del cuello enrojecido") o dolor y espasmos musculares en el pecho y la espalda. Estas reacciones generalmente se resuelven en un lapso de 20 minutos, pero pueden persistir durante varias horas. En estudios en animales, se presentó hipotensión y bradicardia en animales a los que se les administraron mayores dosis de vancomicina en concentraciones y tasas altas. Tales eventos son poco frecuentes si VALCIDEM se administra mediante infusión lenta de 60 minutos. En estudios realizados con voluntarios sanos, no ocurrieron eventos relacionados con la infusión cuando la vancomicina se administró a una velocidad de 10 mg/min o menos.
La inyección en bolo rápida puede provocar hipotensión, bradicardia, choque cardiogénico y en pocas ocasiones, paro cardiaco.
Nefrotoxicidad: En raras ocasiones se ha reportado insuficiencia renal, manifestada principalmente mediante incremento de la creatinina sérica o en las concentraciones de nitrógeno ureico en sangre, especialmente en pacientes que reciben dosis elevadas de vancomicina. Se han reportado casos raros de nefritis intersticial. La mayoría de ellos han ocurrido en pacientes que recibieron aminoglucósidos en forma concomitante, o que tenían disfunción renal preexistente. Cuando se discontinuó la vancomicina se resolvió la azotemia en la mayoría de los pacientes.
Ototoxicidad: Se han reportado casos de pérdida de la audición asociada con el uso de vancomicina. La mayoría de estos pacientes tenía disfunción renal, pérdida de la audición preexistente, o habían recibido tratamiento concomitante con un medicamento ototóxico. Raramente se han reportado casos de vértigo, mareos y tinnitus.
Puede ocurrir tinnitus posiblemente antes del comienzo de la sordera, y se debe considerar como una indicación de que se debe interrumpir el tratamiento.
Reacciones Hematológicas: Se han reportado casos de pacientes que desarrollan neutropenia reversible, que generalmente comienza en un lapso de una semana o más después del comienzo del tratamiento con vancomicina o después de una dosis total de más de 25 g.
La neutropenia parece revertirse rápidamente cuando se suspende la administración de clorhidrato de vancomicina. Raramente se ha reportado trombocitopenia.
Aunque no se ha establecido una causalidad, en raras ocasiones se ha reportado agranulocitis reversible (recuento de granulocitos menor a 500/mm3). Se ha informado eosinofilia.
Flebitis: Se ha reportado inflamación en el sitio de inyección.
Misceláneos: Con poca frecuencia, los pacientes han reportado haber tenido anafilaxia, fiebre medicamentosa, náusea, escalofríos, erupciones cutáneas, incluyendo dermatitis exfoliativa, dermatosis ampollosa IgA lineal, síndrome de Stevens-Johnson, necrólisis epidérmica tóxica y casos poco frecuentes de vasculitis asociada con la administración de vancomicina.
Vancomicina se ha asociado con los trastornos de erupciones ampollosas. Si se sospecha un trastorno ampolloso, se debe suspender la administración del medicamento y un especialista debe realizar una evaluación dermatológica.
PRECAUCIONES EN RELACIÓN CON EFECTOS DE CARCINOGÉNESIS, MUTAGÉNESIS, TERATOGÉNESIS Y SOBRE LA FERTILIDAD: Se han realizado estudios de teratología con 5 veces la dosis humana en ratas y 3 veces la dosis humana en conejos, y no se ha revelado evidencia de daño al feto por vancomicina. Aunque no se han realizado estudios a largo plazo en animales para valorar el potencial carcinogénico, no se encontró potencial mutagénico con el clorhidrato de vancomicina Inyectable, USP, en las pruebas estándares de laboratorio. No se han llevado a cabo estudios de reproducción en animales, por lo que no se sabe si el clorhidrato de vancomicina puede afectar la capacidad reproductiva.
INTERACCIONES MEDICAMENTOSAS Y DE OTRO GÉNERO: La administración concomitante de vancomicina y agentes anestésicos se ha asociado con eritema, con rubefacción semejante al provocado por la histamina (consultar Uso Pediátrico en la sección de Precauciones generales) y con Reacciones anafilácticas (consultar Reacciones secundarias y adversas).
Ha habido informes que indican que la frecuencia de los eventos relacionados con la infusión aumenta con la administración concomitante de agentes anestésicos. Los eventos relacionados con la infusión se pueden minimizar mediante la administración de vancomicina como una infusión de 60 minutos antes de la inducción anestésica.
El uso sistémico o tópico, simultáneo y/o secuencial, de otros medicamentos potencialmente neurotóxicos y/o nefrotóxicos, tales como la anfotericina B, aminoglucósidos, bacitracina, polimixina B, colistina, viomicina o cisplatino, cuando están indicados, requieren un monitoreo cuidadoso del paciente.
ALTERACIONES EN LOS RESULTADOS DE PRUEBAS DE LABORATORIO: El clorhidrato de vancomicina puede elevar el nitrógeno ureico en sangre.
PRECAUCIONES GENERALES:
Precauciones: Se han reportado concentraciones séricas clínicamente significativas en algunos pacientes que han recibido dosis orales múltiples de vancomicina para tratar la colitis pseudomembranosa activa inducida por C. difficile. Por lo tanto, puede ser apropiado monitorear las concentraciones séricas en estos pacientes.
A los pacientes con función renal en el límite de la normalidad y a individuos mayores de 60 años de edad se les deben realizar pruebas de serie de la función auditiva y de los niveles de vancomicina en sangre. Todos los pacientes que reciben el medicamento deben realizarse estudios hematológicos periódicos, análisis de orina y pruebas de función renal. El clorhidrato de vancomicina es muy irritante para los tejidos y se debe administrar por una vía intravenosa segura. La inyección intramuscular o la extravasación accidental provoca dolor, sensibilidad y necrosis. Puede presentarse tromboflebitis y su frecuencia y severidad se puede minimizar administrando el medicamento lentamente como una solución diluida (2.5 a 5.0 g/L), alternando los lugares de la inyección.
La administración prolongada de VALCIDEM puede dar como resultado un desarrollo excesivo de microorganismos no susceptibles. Es esencial observar con cuidado al paciente. Si se desarrolla una sobreinfección durante el tratamiento, se deben tomar las medidas adecuadas. Ha habido informes poco frecuentes de colitis pseudomembranosa por C. difficile que se desarrollan en pacientes que recibieron vancomicina por vía intravenosa.
Con el fin de minimizar el riesgo de nefrotoxicidad en el tratamiento de pacientes con disfunción renal subyacente, se debe realizar un monitoreo serial de la función renal, y en particular, se debe poner especial cuidado en seguir los esquemas de dosificación apropiados (consultar Dosis y vía de administración).
En los pacientes que van a recibir tratamiento prolongado con clorhidrato de vancomicina, o en los que están recibiendo medicamentos concomitantes que podrían causar neutropenia, debe hacerse un monitoreo periódico del recuento de leucocitos.
Advertencias: La administración en bolo rápida (es decir, en unos pocos minutos) se puede asociar con hipotensión exagerada, incluidos choque y, no muy frecuentemente, paro cardiaco. VALCIDEM se debe administrar en una solución diluida en no menos de 60 minutos para evitar las reacciones relacionadas con la infusión rápida. Generalmente, detener la infusión provoca que estas reacciones desaparezcan rápidamente.
Algunos pacientes con trastornos inflamatorios de la mucosa intestinal pueden tener absorción sistémica significativa de vancomicina oral y, por lo tanto, pueden estar en riesgo de desarrollar reacciones adversas asociadas con la administración parenteral de vancomicina. El riesgo es mayor en pacientes con disfunción renal. Se debe aclarar que las eliminaciones renales y sistémicas totales de vancomicina se reducen en los adultos mayores.
Debido a su ototoxicidad y nefrotoxicidad potencial, vancomicina se debe administrar con cuidado en pacientes con insuficiencia renal, ya que el riesgo de toxicidad es mucho mayor con concentraciones en sangre prolongadas y altas. Se debe monitorear los niveles de sangre y se deben realizar pruebas de función renal de forma regular. Se debe ajustar la dosis del clorhidrato de vancomicina para inyección en los pacientes con disfunción renal (consulte Dosis y vía de administración).
Vancomicina también se debe evitar en pacientes con pérdida previa de la audición. Si se utiliza en dichos pacientes, se debe regular la dosis, si es posible, determinando de forma periódica el nivel del medicamento en la sangre. La sordera puede ser precedida por tinnitus.
Los adultos mayores son más susceptibles al daño auditivo. La experiencia con otros antibióticos sugiere que la sordera puede ser progresiva a pesar de la suspensión del tratamiento.
Vancomicina se debe administrar con precaución en pacientes alérgicos a teicoplanina, ya que se han informado reacciones alérgicas cruzadas entre vancomicina y teicoplanina.
Uso Pediátrico: En neonatos prematuros y lactantes, puede ser apropiado confirmar las concentraciones séricas de VALCIDEM deseadas. La administración concomitante de vancomicina y agentes anestésicos se ha asociado con eritema y con rubefacción semejante al provocado por la histamina en pacientes pediátricos (consultar Reacciones secundarias y adversas).
Uso geriátrico: La disminución natural de la filtración glomerular a medida que la edad avanza puede provocar concentraciones séricas elevadas de VALCIDEM si la dosis no se ajusta. Los regímenes de dosificación de VALCIDEM deben ajustarse en los pacientes de edad avanzada (consultar Dosis y vía de administración).
DOSIS Y VÍA DE ADMINISTRACIÓN: Una velocidad de infusión de 10 mg/min o menos se asocia con un menor número de eventos relacionados con la infusión (consultar Reacciones secundarias y adversas). Los eventos relacionados con la infusión dependen tanto con la concentración como de la velocidad de administración de VALCIDEM. Se recomiendan concentraciones de no más de 5 mg/mL y las velocidades de no más de 10 mg/min en adultos. En pacientes seleccionados que requieran restricción de líquidos, se puede usar una concentración de 10 mg/mL; el uso de concentraciones tan elevadas puede aumentar el riesgo de efectos relacionados con la infusión. Sin embargo, pueden presentarse efectos relacionados con la infusión a cualquier velocidad o concentración.
La administración en bolo rápida (por ejemplo, en un curso de varios minutos) puede estar asociada con hipotensión exagerada, incluyendo shock y, en raras ocasiones, paro cardiaco. VALCIDEM debe administrarse en una solución diluida en no menos de 60 minutos para evitar las reacciones relacionadas con la infusión rápida. La suspensión de la infusión generalmente provoca un pronto cese de dichas reacciones.
Pacientes con Función Renal Normal:
Adultos: La dosis intravenosa diaria usual es de 2 g, divididos en dosis de 500 mg cada 6 horas o 1 g cada 12 horas en cloruro de sodio infusión intravenosa o 5% Dextrosa Infusión Intravenosa. Cada dosis debe administrarse a no más de 10 mg/min, o por lo menos en el transcurso de 60 minutos, lo que sea más prolongado. Otros factores relacionados con el paciente tales como la edad u obesidad, pueden requerir la modificación de la dosis usual diaria.
Pacientes Pediátricos: La dosis intravenosa usual diaria de VALCIDEM es de 10 mg/kg por dosis, administrada cada 6 horas. Cada dosis debe administrarse por lo menos en un transcurso de 60 minutos. En estos pacientes se recomienda el monitoreo cuidadoso de las concentraciones séricas de vancomicina.
Neonatos: En los pacientes pediátricos de hasta 1 mes de edad, la dosis intravenosa diaria total puede ser menor. En neonatos, se sugiere una dosis inicial de 15 mg/kg seguida por 10 mg/kg cada 12 horas en la primera semana de vida y cada 8 horas de ahí en adelante hasta la edad de 1 mes. Cada dosis debe administrarse en el transcurso de 60 minutos. En recién nacidos prematuros, la depuración de vancomicina disminuye a medida que disminuye la edad postconcepcional. Por lo tanto, se podrían requerir intervalos de dosificación más largos en recién nacidos prematuros. En estos pacientes se recomienda el monitoreo cuidadoso de las concentraciones séricas de VALCIDEM.
Pacientes con Insuficiencia Renal y Pacientes de Edad Avanzada: Es necesario hacer ajustes en la dosis en los pacientes con insuficiencia renal. Se deben realizar ajustes de dosis para evitar niveles séricos tóxicos. En recién nacidos prematuros y en personas de edad avanzada, podría ser necesario reducir la dosis en mayor grado del que se esperaba debido a la disminución de la función renal. La medición de las concentraciones séricas de vancomicina puede ser útil para optimizar el tratamiento, especialmente en los pacientes gravemente enfermos, que presentan cambios en la función renal. Las determinaciones de las concentraciones séricas de vancomicina pueden llevarse a cabo por ensayo microbiológico, radioinmunoensayo, inmunoensayo de polarización de la fluorescencia, inmunoensayo de fluorescencia o por cromatografía líquida de alta presión.
Si la depuración de creatinina se puede medir o estimar con precisión, la dosis para la mayoría de los pacientes con insuficiencia renal se puede calcular con la siguiente tabla. La dosificación de VALCIDEM en mg por día es de aproximadamente 15 veces la tasa de filtración glomerular en mL/min:
Tabla de Dosificación para la Vancomicina en Pacientes con Insuficiencia Renal (Adaptado de Moellering et al)4
|
Depuración de Creatinina mL/min |
Dosis de Vancomicina mg/24 h |
|
100 |
1,545 |
|
90 |
1,390 |
|
80 |
1,235 |
|
70 |
1,080 |
|
60 |
925 |
|
50 |
770 |
|
40 |
620 |
|
30 |
465 |
|
20 |
310 |
|
10 |
155 |
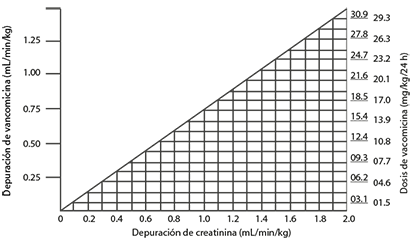
Nomograma de la dosis de vancomicina en pacientes con alteración de la función renal
La dosis inicial no debe ser inferior a 15 mg/kg, incluso en pacientes con insuficiencia renal leve a moderada.
La tabla no es válida para los pacientes funcionalmente anéfricos. Para tales pacientes, debe administrarse una dosis inicial de 15 mg/kg de peso corporal para alcanzar concentraciones terapéuticas en suero rápidas. La dosis necesaria para mantener concentraciones estables es 1.9 mg/kg/24 h. En pacientes con insuficiencia renal marcada, podría ser más conveniente dar dosis de mantenimiento de 250 a 1000 mg una vez cada varios días, en lugar de administrar el fármaco diariamente. En casos de anuria, se ha recomendado una dosis de 1000 mg cada 7 a 10 días.
Cuando sólo se conoce la concentración de creatinina en suero, se puede utilizar la siguiente fórmula (basada en el sexo, el peso y la edad del paciente) para el cálculo de la depuración de creatinina. Las depuraciones de creatinina calculadas (mL/min) son sólo estimaciones. La depuración de creatinina debe evaluarse rápidamente.
|
Hombres: |
Peso (kg) x (140-edad en años) |
|
72 x concentración de creatinina sérica (mg/dL) |
|
Mujeres: 0.85 x valor de arriba
La creatinina sérica debe representar un estado estable de función renal, o si no el valor estimado de depuración de creatinina no es válido. Tal depuración calculada es una estimación excesiva verdadera de la depuración renal en pacientes con condiciones: (1) caracterizados por función renal decreciente, tales como shock, insuficiencia cardiaca grave u oliguria; (2) en las cuales no hay una relación normal entre la masa muscular y el peso corporal total, tales como pacientes obesos o pacientes con enfermedad de hígado, edema o ascitis; y (3) acompañadas de debilitamiento, mal nutrición o inactividad.
Todavía no se ha determinado la seguridad y eficacia de la administración de vancomicina por vía intratecal (intralumbar o intraventricular).
La infusión intermitente es el método de administración recomendado.
Preparación y estabilidad:
Instrucciones para su reconstitución: En el momento de uso, reconstituir el vial añadiendo 10 mL de solución de dextrosa al 5% o de solución de cloruro de sodio 0.9% al vial de 500 mg. Se requiere dilución adicional para su administración (ver adelante).
Después de la reconstitución los frascos ámpula se pueden almacenar hasta por 48 horas a temperatura ambiente (15 a 30°C) o hasta por 14 días en refrigeración (2 a 8°C) sin que se presente una pérdida significativa de la potencia.
Las soluciones reconstituidas que contienen 500 mg de vancomicina deben diluirse más con al menos 100 mL de diluyente. La dosis deseada, diluida de esta manera, debe ser administrada por infusión intravenosa intermitente durante un periodo de al menos 60 minutos.
La solución de VALCIDEM tiene un pH bajo y puede causar inestabilidad química o física cuando se mezcla con otros compuestos.
Se ha demostrado que las mezclas de soluciones de vancomicina y de antibióticos betalactámicos son físicamente incompatibles. La probabilidad de formación de precipitados aumenta con concentraciones más altas de vancomicina. Se recomienda lavar adecuadamente las vías intravenosas entre la administración de estos antibióticos. También se recomienda diluir las soluciones de vancomicina hasta una concentración igual o inferior a 5 mg/mL.
Antes de la administración, los medicamentos parenterales deben ser inspeccionados visualmente para detectar partículas y decoloración antes de su administración, siempre que la solución o el envase lo permitan.
VALCIDEM oral se utiliza en el tratamiento de la colitis pseudomembranosa relacionada con el uso de antibióticos producida por C.difficile y para la enterocolitis estafilocócica. VALCIDEM no es eficaz por vía oral para otros tipos de infecciones. La dosificación diaria total habitual en adultos es de 500 mg a 2 g administrados en 3 o 4 dosis divididas durante 7 a 10 días. La dosis diaria total en pacientes pediátricos es de 40 mg/kg de peso corporal en 3 o 4 dosis divididas durante 7 a 10 días. La dosis total diaria no debe exceder de 2 g. La dosis apropiada puede ser diluida en 1 oz de agua (30 mL) y dar a beber al paciente. Se pueden añadir jarabes de sabores comunes a la solución para mejorar el sabor de la solución oral. El material diluido se puede administrar a través de sonda nasogástrica.
MANIFESTACIONES Y MANEJO DE LA SOBREDOSIFICACIÓN O INGESTA ACCIDENTAL: Se recomienda terapia de apoyo con mantenimiento de la filtración glomerular. La eliminación de VALCIDEM mediante diálisis es deficiente. Se ha reportado que la hemofiltración y la hemoperfusión con resina XAD-4 proporciona un beneficio limitado.
PRESENTACIÓN: VALCIDEM Solución, se suministra como liofilizado estéril en frascos ámpula fliptop unidosis que contienen el equivalente de vancomicina 500 mg.
Charola con 10 frascos ámpula.
RECOMENDACIONES SOBRE ALMACENAMIENTO: Consérvese a no más de 30°C. No requiere refrigeración.
LEYENDAS DE PROTECCIÓN:
ANTIBIÓTICO. El uso incorrecto de este producto puede causar resistencia bacteriana. Hecha la mezcla adminístrese de inmediato y deséchese el sobrante. No se administre si la solución no es transparente, si contiene partículas en suspensión o sedimentos, o si el cierre ha sido violado. No se use en el embarazo y lactancia. Su venta requiere receta médica. No se deje al alcance de los niños.
Reporte las sospechas de reacción adversa al correo:
farmacovigilancia@cofepris.gob.mx y
MEX.AEReporting@pfizer.com
PFIZER, S.A. de C. V.
Km. 63 Carretera México Toluca ,Zona Industrial,
C.P. 50140 Toluca, México, México.
Reg. Núm. 427M2015, SSA
173300415J0132
®Marca Registrada
