
NOVOMIX 30 FLEXPEN
INSULINA ASPARTA RECOMBINANTE
Suspensión para inyección
Estuche, 5 Pluma prellenada, 3 ml,
Estuche, 1 Pluma prellenada, 3 ml,
COMPOSICIÓN: Cada mL contiene:
|
Sustancia |
Cantidad |
Referencia de calidad |
|
Insulina asparta |
100 U= 600 nmol (aproximadamente 3.5 mg) |
NOVO NORDISK |
|
Sulfato de protamina |
Aprox. 0.32 mg |
F.Eur./FJ |
|
Zinc |
19.6 μg |
F.Eur./USP/FJ |
|
Glicerol |
16,00 mg |
F.Eur./USP/FJ |
|
Fenol |
1,50 mg |
F.Eur./USP/FJ |
|
Metacresol |
1,72 mg |
F.Eur./USP |
|
Cloruro de sodio |
0.877 mg |
F.Eur./USP/FJ |
|
Fosfato disódico dihidratado |
1,25 mg |
F.Eur./USP |
|
Hidróxido de sodio 2 N, csp para ajuste de pH |
F.Eur./USP/FJ |
|
|
Ácido clorhídrico 2N, csp para ajuste de pH |
F.Eur./USP/FJ |
|
|
Agua para inyección csp |
1,0 mL |
F.Eur./USP/FJ |
FORMA FARMACÉUTICA: Suspensión para inyección blanca en un dispositivo pre-llenado.
Fortaleza: 100 U/mL.
INDICACIONES: Tratamiento para diabetes mellitus en adultos, adolescentes y niños de 10 años o más.
PROPIEDADES FARMACODINÁMICAS:
Grupo farmacoterapéutico: Fármacos usados en la diabetes. Insulinas y análogos para inyección, de acción intermedia o prolongada combinados con de acción rápida. Código ATC A10AD05.
Mecanismo de acción: El efecto reductor de glucosa en la sangre de la insulina asparta se debe a la facilitación de absorción de la glucosa después de la unión de insulina a los receptores en las células musculares y de grasa y a la inhibición simultánea de producción de glucosa en el hígado.
NOVOMIX® 30 es una insulina bifásica que contiene insulina asparta soluble al 30%. Esto tiene un inicio de acción rápido, permitiendo así una administración más cercana a los alimentos (entre cero y 10 minutos después de los alimentos) en comparación con insulina humana soluble. La fase cristalina (70%) consiste de insulina asparta cristalizada con protamina que tiene un perfil de actividad similar al de la insulina humana NPH.
Cuando NOVOMIX® 30 se inyecta en forma subcutánea, el inicio de acción ocurrirá en los siguientes 10 a 20 minutos de la inyección. El efecto máximo se obtiene entre 1 y 4 horas después de la inyección. La duración de la acción es hasta 24 horas.
Velocidad de infusión de glucosa:
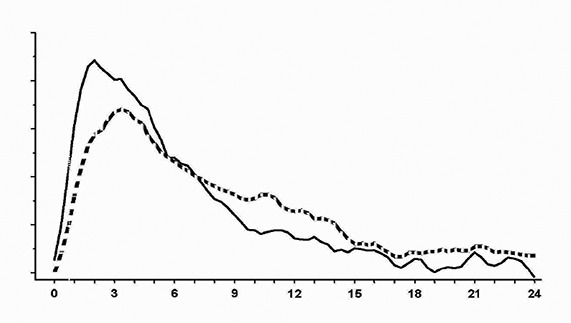
NOVOMIX® 30: Figura 1: Perfil de actividad de NOVOMIX® 30 (––) e insulina humana bifásica 30 (---) en sujetos sanos.
En un estudio de 3 meses que comparó NOVOMIX® 30 con administración de insulina humana bifásica 30 antes del desayuno y la cena en pacientes con diabetes tipo 1 y tipo 2, NOVOMIX® 30 resultó en un nivel significativamente menor de glucosa en sangre postprandial después de los alimentos (desayuno y cena).
Un meta-análisis que incluyó nueve estudios en pacientes con diabetes tipo 1 y tipo 2 demostró que en comparación con la administración de insulina humana bifásica 30, la administración de NOVOMIX® 30 antes del desayuno y la cena resultó en un control significativamente mejor de glucosa en sangre postprandial (incrementos promedio de glucosa postprandial en el desayuno, comida y cena). Si bien el nivel de glucosa en sangre en ayunas fue mayor en pacientes tratados con NOVOMIX® 30, el control glucémico total medido por hemoglobina glicosilada fue similar.
En un estudio, 341 pacientes con diabetes tipo 2 se distribuyeron aleatoriamente entre tratamiento con NOVOMIX® 30 solo o en combinación con metformina o con metformina y sulfonilurea. La variable de eficacia primaria - HbA1c después de 16 semanas de tratamiento no difirió entre pacientes con NOVOMIX® 30 combinado con metformina y pacientes con metformina más sulfonilurea. En este estudio, 57% de los pacientes tuvieron HbA1c basal por arriba de 9%; en estos pacientes, el tratamiento con NOVOMIX® 30 en combinación con metformina resultó en un nivel de HbA1c significativamente menor que con metformina en combinación con sulfonilurea.
En un estudio, pacientes con diabetes tipo 2, sin control suficiente solo con agentes hipoglucémicos, se distribuyeron aleatoriamente a tratamiento con NOVOMIX® 30 dos veces al día (117 pacientes) o insulina glargina una vez al día (116 pacientes). Después de 28 semanas de tratamiento siguiendo los lineamientos de dosificación, la reducción media en HbA1c fue 2.8% con NOVOMIX® 30 (media en la línea basal = 9.7%). Con NOVOMIX® 30, 66% y 42% de los pacientes alcanzaron niveles de HbA1c por debajo de 7% y 6.5%, respectivamente, y la glucosa en sangre en ayunas se redujo alrededor de 7 mmol/L (de 14.0 mmol/L en la línea basal a 7.1 mmol/L).
En pacientes con diabetes tipo 2, un meta-análisis demostró un riesgo reducido de episodios hipoglucémicos nocturnos totales e hipoglucemia importante con NOVOMIX® 30 en comparación con insulina humana bifásica 30. El riesgo de episodios hipoglucémicos diurnos totales fue mayor en pacientes tratados con NOVOMIX® 30.
Población pediátrica: Se llevó a cabo un estudio clínico de 16 semanas que comparó el control glucémico postprandial de NOVOMIX® 30 relacionado con alimentos con insulina humana/insulina humana bifásica 30 relacionada con alimentos e insulina NPH nocturna con 167 sujetos entre 10 y 18 años. El nivel medio de HbA1c permaneció similar a la línea basal en todo el estudio en ambos grupos de tratamiento y no hubo diferencia en la tasa de hipoglucemia con NOVOMIX® 30 o insulina humana bifásica 30.
En una población menor (54 sujetos) y más joven (rango de edad 6 a 12 años) tratada en un estudio abierto cruzado (12 semanas en cada tratamiento) la tasa de episodios hipoglucémicos y el aumento de glucosa postprandial fue significativamente menor con NOVOMIX® 30 en comparación con insulina humana bifásica 30. El nivel final de HbA1c fue menor en el grupo tratado con insulina humana bifásica 30 en comparación con NOVOMIX® 30.
Poblaciones especiales:
Ancianos: Las propiedades farmacodinámicas de NOVOMIX® 30 no se han investigado en ancianos. Sin embargo, se realizó un estudio aleatorio, doble-ciego, cruzado de farmacocinética/farmacodinamia que comparó insulina asparta con insulina humana soluble en pacientes mayores con diabetes tipo 2 (19 pacientes entre 65-83 años, edad promedio 70 años). Las diferencias relativas en las propiedades farmacodinámicas (GIRmáx, ABCGIR, 0-120 min) entre insulina asparta e insulina humana soluble en ancianos fue similar a aquellas observadas en sujetos sanos y en sujetos jóvenes con diabetes.
Embarazo: NOVOMIX® 30 no se ha investigado en mujeres embarazadas. Sin embargo, un estudio clínico que comparó la seguridad y eficacia de insulina asparta vs. insulina humana soluble en el tratamiento de mujeres embarazadas con diabetes tipo 1 (322 embarazos expuestos (insulina asparta: 157; insulina humana soluble: 165)) no indicó ningún efecto adverso de insulina asparta en el embarazo o en la salud del feto/neonato.
Además, los datos de un estudio clínico que incluyó a 27 mujeres con diabetes gestacional distribuidas aleatoriamente entre tratamiento con insulina asparta vs. insulina humana soluble (insulina asparta: 14; insulina humana soluble: 13) demostró perfiles de seguridad similares entre tratamientos.
Sección IO opcional: En un estudio observacional en el que participaron más de 17.000 pacientes con diabetes mellitus tipo 2, la HbAc1 se redujo en un 1,81% a partir de una línea basal de 9,36% a 7,67% después de 6 meses de tratamiento con NOVOMIX® 30 (p <0,001 en comparación con la línea basal).
Un estudio observacional de 66.726 pacientes investigó la seguridad clínica y eficacia de NOVOMIX® 30, la insulina asparta e insulina detemir en pacientes con diabetes tipo 1I tratados previamente con otro medicamento antidiabético. Un total de 40.917 pacientes fueron expuestos a NOVOMIX® 30, debido a la naturaleza observacional del estudio no todos los pacientes habían documentado sus valores glucémicos (cambio en la HbA1c desde la línea basal hasta la semana 24 en 27.033 pacientes que habían documentado HbAc1 fue de -2,1%, la tasa total de hipoglucemia basal fue de 2,4 y después de 24 semanas de tratamiento la tasa reportada fue de 1,5 por paciente al año). El número de pacientes a los que se cambió de otras terapias de insulina a NOVOMIX® 30 fue de 1.395, 1.423 y 6.323 de insulina glargina, insulina NPH o insulina humana bifásica, respectivamente. Después de 24 semanas, el 90% de los pacientes en cada uno de los grupos transferidos experimentó una reducción en la HbAc1. La HbAc1 se redujo en un 1,9%, 2% y 1,7% a partir de una línea basal de 9,7%, 9,5% y 9,1% a 7,8%, 7,6% y 7,5% (valores de p todos <0,001) para los pacientes trasladados desde glargina, insulina NPH o insulina humana bifásica, respectivamente. Se informó que las tasas de hipoglucemia totales en los grupos transferidos a NOVOMIX® 30 fue de 3,0; 2,8; 2,1 a partir de una línea basal de 3,1; 6,1 y 6,0, respectivamente. La calidad de vida se midió utilizando el cuestionario EQ-5D y las puntuaciones de las mejoras fueron de 10,3; 10,8 y 12,5 puntos en la Escala Analógica Visual (EAV), respectivamente, en comparación con los tratamientos de referencia (EVA basales fueron de 63,4; 63,0 y 64, respectivamente).
PROPIEDADES FARMACOCINÉTICAS:
Absorción, distribución y eliminación: En la insulina asparta, la sustitución del aminoácido prolina con ácido aspártico en la posición B28 reduce la tendencia de formar hexámeros como se observa en la insulina humana. La insulina asparta en la fase soluble de NOVOMIX® 30/ comprende 30% de la insulina total; ésta se absorbe más rápidamente de la capa subcutánea que el componente de insulina soluble de la insulina humana bifásica. El 70% restante está en forma cristalina como insulina asparta cristalizada con protamina; ésta tiene un perfil de absorción prolongado similar a la insulina NPH.
La concentración máxima de insulina en sangre es, en promedio, 50% mayor con NOVOMIX® 30 que con insulina humana bifásica 30. El tiempo para concentración máxima es, en promedio, la mitad que para insulina humana bifásica 30. En voluntarios sanos, se alcanzó una concentración máxima en sangre de 140 ± 32 pmol/L se alcanzó alrededor de 60 minutos después de una dosis subcutánea de 0.20 U/kg de peso corporal. La media de vida promedio (t½) de NOVOMIX® 30, que refleja la tasa de absorción de la fracción vinculada a protamina, fue alrededor de 8-9 horas. Los niveles de insulina en suero regresaron al nivel de línea basal 15-18 horas después de la dosis subcutánea. En pacientes con diabetes tipo 2, la concentración máxima se alcanzó alrededor de 95 minutos después de la dosificación, y se midieron concentraciones bien por sobre cero durante no menos de 14 horas después de la dosificación.
Poblaciones especiales:
Ancianos: Las propiedades farmacocinéticas de NOVOMIX® 30 no se han investigado en pacientes ancianos. Sin embargo, las diferencias relativas en las propiedades farmacocinéticas entre insulina asparta e insulina humana soluble en sujetos mayores (65-83 años, edad promedio 70 años) con diabetes tipo 2, fueron similares a las observadas en sujetos sanos y en sujetos más jóvenes con diabetes. Se observó una disminución en la tasa de absorción en sujetos mayores, resultando en una tmáx posterior (82 (rango intercuartil: 60-120) minutos), donde Cmáx fue similar a la observada en sujetos más jóvenes con diabetes tipo 2 y ligeramente menor que en sujetos con diabetes tipo 1.
Insuficiencia renal y hepática: Las propiedades farmacocinéticas de NOVOMIX® 30 no se han investigado en pacientes con insuficiencia renal o hepática.
Población pediátrica: Las propiedades farmacocinéticas de NOVOMIX® 30 no se han investigado en niños o adolescentes. Sin embargo, las propiedades farmacocinéticas y farmacodinámicas de insulina asparta soluble se investigó en niños (6-12 años) y en adolescentes (13-17 años) con diabetes tipo 1. La insulina asparta se absorbió rápidamente en ambos grupos de edad, con tmáx similares al valor en adultos. Sin embargo, Cmáx fue diferente entre los grupos de edad, enfatizando la importancia de la titulación individual de la insulina asparta.
CONTRAINDICACIONES: Hipersensibilidad a la sustancia activa (insulina asparta) o a alguno de los excipientes.
ADVERTENCIAS Y PRECAUCIONES: Antes de viajar entre diferentes zonas horarias el paciente debe solicitar asesoría médica pues quizá tenga que comer y administrarse la insulina a diferentes horas.
Hiperglucemia: La dosificación inadecuada o la suspensión del tratamiento, en particular en diabetes tipo 1, puede conducir a hiperglucemia y cetoacidosis diabética. Por lo general, los primeros síntomas de hiperglucemia se desarrollan gradualmente en un periodo de horas o días. Estos incluyen sed, aumento en la frecuencia de micción, náusea, vómito, mareos, piel seca y enrojecida, boca seca, pérdida de apetito así como aliento olor cetona. En diabetes tipo 1, los eventos hiperglucémicos sin tratar pueden conducir a la larga a cetoacidosis diabética, que es potencialmente mortal.
Hipoglucemia: La omisión de una comida o ejercicio físico extenuante no planeado puede conducir a hipoglucemia.
La hipoglucemia puede ocurrir si la dosis de insulina es muy alta con relación al requerimiento de insulina.
En comparación con insulina humana bifásica, NOVOMIX® 30 puede tener un efecto reductor de glucosa más pronunciado hasta 6 horas después de la inyección. Esto debe compensarse en cada paciente, ajustando la dosis de insulina y/o la ingesta de alimentos.
Los pacientes cuyo control de glucosa en sangre mejora bastante, por ejemplo con terapia intensificada de insulina, pueden experimentar un cambio en los síntomas habituales de advertencia de hipoglucemia, y deberán recibir asesoría. Estos síntomas de advertencia habituales pueden desaparecer en pacientes con diabetes desde hace tiempo.
Un control más estrecho de los niveles de glucosa puede aumentar los episodios hipoglucémicos potenciales y por lo tanto requiere atención especial durante la intensificación de la dosis.
Puesto que NOVOMIX® 30 debe administrarse en relación inmediata con los alimentos, el inicio rápido de la acción debe considerarse en pacientes con enfermedades concomitantes o medicamentos con los que se pueda esperar un retraso en la absorción de los alimentos.
Las enfermedades concomitantes, en especial infecciones y condiciones febriles, por lo general aumentan los requerimientos de insulina del paciente. Las enfermedades concomitantes en riñones o hígado, o que afecten las glándulas suprarrenales, pituitarias o tiroides, quizá requieran cambios en la dosis de insulina.
Cuando se transfiere a los pacientes entre diferentes tipos de productos de insulina, los síntomas anteriores de advertencia de hipoglucemia pueden cambiar o volverse menos pronunciados que los experimentados con la insulina anterior.
USO EN EMBARAZO Y LACTANCIA: No se ha investigado el efecto de NOVOMIX® 30 en mujeres embarazadas. Sin embargo, datos de dos estudios clínicos aleatorios controlados (157 y 14 embarazos expuestos a insulina asparta, respectivamente, en un régimen basal-bolo) no indican ningún efecto adverso de la insulina asparta en el embarazo o en la salud del feto/neonato al compararse con insulina humana soluble.
Existe poca experiencia clínica con NOVOMIX® 30 en el embarazo.
En general, se recomienda control y monitoreo intensificado en mujeres embarazadas con diabetes a lo largo del embarazo y al planearlo. Los requerimientos de insulina por lo general disminuyen en el primer trimestre y aumentan posteriormente durante el segundo y tercer trimestres. Por lo general, los requerimientos de insulina regresan rápidamente a los valores previos al embarazo después de dar a luz.
Lactancia: No hay restricciones de tratamiento con NOVOMIX® 30 durante la lactancia. El tratamiento con insulina en madres que están lactando no representa riesgo para el bebé. Sin embargo, quizá sea necesario ajustar la dosis de NOVOMIX® 30.
EFECTOS EN LA CONDUCCIÓN DE VEHÍCULOS/MAQUINARIAS: La capacidad del paciente para concentrarse y reaccionar puede verse deteriorada como resultado de la hipoglucemia.
Esto puede constituir un riesgo en situaciones en las que estas capacidades sean de especial importancia (por ej. Al conducir un auto u operar maquinaria).
Se debe recomendar a los pacientes tomar precauciones para evitar la hipoglucemia mientras conducen u operan maquinaria. Esto es particularmente importante en aquellas personas que desconocen o tienen poco conocimiento de los signos de advertencia de la hipoglucemia o que tienen episodios frecuentes de hipoglucemia. Se debe evaluar la conveniencia de conducir u operar una máquina en estas circunstancias.
EFECTOS INDESEABLES: Las reacciones adversas observadas en pacientes que usan NOVOMIX® se deben principalmente al efecto farmacológico de la insulina.
La reacción adversa reportada con mayor frecuencia durante el tratamiento es hipoglucemia. La frecuencia de hipoglucemia puede variar con la población de pacientes, los regímenes de dosis y el nivel de control glucémico. Por favor consulte la sección c a continuación.
Al inicio del tratamiento con insulina, pueden ocurrir anomalías de refracción, edema y reacciones en el sitio de inyección (dolor, enrojecimiento, urticaria, inflamación, hematomas, hinchazón y comezón en el sitio de inyección). Por lo general estas reacciones son de naturaleza transitoria. Una mejoría rápida del control de glucosa en sangre puede asociarse con neuropatía dolorosa aguda, que por lo general es reversible. La intensificación de la terapia de insulina con una mejoría abrupta del control glucémico puede asociarse con un empeoramiento temporal de la retinopatía diabética, mientras que una mejoría del control glucémico a largo plazo disminuye el riesgo de progresión de retinopatía diabética.
Lista tabular de reacciones adversas: Las reacciones adversas enlistadas a continuación se basan en datos de estudios clínicos y se clasifican conforme a la clasificación de órganos del sistema MedDRA y la clasificación de órganos del sistema. Las categorías de frecuencia se definen conforme al siguiente acuerdo: Muy común (≥ 1/10); común (≥ 1/100 a < 1/10); poco común (≥ 1/1,000 a < 1/100); rara (≥ 1/10,000 a < 1/1,000); muy rara (< 1/10,000); desconocida (no puede calcularse con los datos disponibles).
|
Desórdenes del sistema inmune |
Poco comunes – Urticaria, sarpullido, erupciones |
|
Muy raras – Reacciones anafilácticas* |
|
|
Desórdenes de metabolismo y nutrición |
Muy comunes – Hipoglucemia* |
|
Desórdenes del sistema nervioso |
Raras – Neuropatía periférica (neuropatía dolorosa) |
|
Desórdenes oculares |
Poco comunes – Desórdenes de refracción |
|
Poco comunes – Retinopatía diabética |
|
|
Desórdenes de la piel y el tejido subcutáneo |
Poco comunes - Lipodistrofia* |
|
Desórdenes generales y condiciones del sitio de administración |
Poco comunes – Reacciones en el sitio de inyección |
|
Poco comunes – Edema |
|
|
* Ver la sección Descripción de las reacciones adversas seleccionadas. |
|
Descripción de las reacciones adversas seleccionadas:
Reacciones anafilácticas: La ocurrencia de reacciones de hipersensibilidad generalizada (incluyendo urticaria generalizada de la piel, comezón, sudoración, molestia gastrointestinal, edema angioneurótico, dificultad para respirar, palpitaciones y reducción de la presión sanguínea) es muy rara pero puede, potencialmente, poner en peligro la vida.
Hipoglucemia: La reacción adversa reportada con mayor frecuencia es la hipoglucemia. La hipoglucemia puede ocurrir si la dosis de insulina es demasiado alta en relación con el requerimiento de insulina. La hipoglucemia severa puede conducir a la pérdida de conciencia y/o a convulsiones y puede resultar en daño temporal o permanente de la función cerebral o incluso la muerte. Los síntomas de la hipoglucemia por lo general ocurren súbitamente. Pueden incluir sudores fríos, piel pálida y fría, fatiga, nerviosismo o temblor, ansiedad, cansancio o debilidad inusual, confusión, dificultad para concentrarse, mareos, hambre excesiva, cambios en la visión, dolor de cabeza, náusea y palpitaciones.
En estudios clínicos, la frecuencia de hipoglucemia varió con la población de pacientes, los regímenes de dosis y el nivel de control glucémico. Durante los estudios clínicos, las tasas generales de hipoglucemia no difirieron entre pacientes tratados con insulina asparta en comparación con insulina humana.
Lipodistrofia: La lipodistrofia se reporta como poco común, pudiendo ocurrir en el sitio de inyección.
INTERACCIONES MEDICAMENTOSAS: Se sabe que varios medicamentos interactúan con el metabolismo de la glucosa.
Las siguientes sustancias pueden reducir los requisitos de insulina del paciente: Productos antidiabéticos orales, inhibidores de la monoaminooxidasa (MAOIs), bloqueadores beta, inhibidores de la enzima convertidora de angiotensina (ACE), salicilatos, esteroides anabólicos y sulfonamidas.
Las siguientes sustancias pueden aumentar los requisitos de insulina del paciente: Anticonceptivos orales, tiazidas, glucocorticoides, hormonas tiroides, simpaticomiméticos, hormona del crecimiento y danazol.
Los agentes bloqueadores beta pueden enmascarar los síntomas de hipoglucemia.
El octreotide/lanreotide puede aumentar o disminuir el requerimiento de insulina.
El alcohol puede intensificar o reducir el efecto hipoglucémico de la insulina.
MODO DE ADMINISTRACIÓN: NOVOMIX® 30 es únicamente para administración subcutánea. NOVOMIX® 30 no debe administrarse en forma intravenosa, pues puede provocar una hipoglucemia severa. La administración intramuscular debe evitarse. NOVOMIX® 30 no debe usarse en bombas de infusión de insulina.
NOVOMIX® 30 se administra de forma subcutánea por inyección en el muslo o en la pared abdominal. De ser conveniente puede usarse la región del glúteo o deltoides. Los sitios de inyección siempre deben rotarse dentro de la misma región para reducir el riesgo de lipodistrofia. No se ha investigado la influencia de los diferentes sitios de inyección en la absorción de NOVOMIX® 30. Al igual que con todos los productos de insulina, la duración de la acción variará conforme a la dosis, el sitio de inyección, el flujo sanguíneo, la temperatura y el nivel de actividad física.
NOVOMIX® 30 tiene un inicio de acción más rápido que la insulina humana bifásica y por lo general debe administrarse inmediatamente antes de una comida. Cuando sea necesario NOVOMIX® 30 puede administrarse poco después de los alimentos.
POSOLOGÍA: La dosificación de NOVOMIX® 30 es individual y se determina conforme a las necesidades del paciente. Se monitorea la glucosa en sangre y se recomiendan ajustes a la dosis de insulina para lograr un control glucémico óptimo.
En pacientes con diabetes tipo 2, NOVOMIX® 30 puede administrarse como monoterapia. NOVOMIX® 30 también puede administrarse en combinación con fármacos antidiabéticos orales si la glucosa en sangre del paciente no se controla de manera adecuada solo con fármacos antidiabéticos. Para pacientes con diabetes tipo 2, la dosis de inicio recomendada de NOVOMIX® 30 es 6 U en el desayuno y 6 U en la cena (o comida nocturna). NOVOMIX® 30 también puede iniciarse una vez al día con 12 U en la cena (o comida nocturna). Si se usa NOVOMIX® 30 una vez al día, por lo general se recomienda migrar a dos veces al día al alcanzar 30 unidades dividiendo la dosis en dosis iguales para el desayuno y la cena. Si la dosificación dos veces al día con NOVOMIX® 30 resulta en episodios recurrentes de hipoglucemia durante el día, la dosis de la mañana puede dividirse en dosis de mañana y almuerzo (dosificación tres veces al día).
Quizá sea necesario ajustar la dosificación en caso de que los pacientes realicen mayores actividades físicas, cambien su dieta habitual o durante enfermedades concomitantes.
Se recomiendan los siguientes lineamientos de titulación para ajustes de dosis:
|
Nivel de glucosa en sangre antes de alimentos |
Ajuste de dosis NOVOMIX® 30 |
|
|
< 4.4 mmol/L |
< 80 mg/dL |
- 2 U |
|
4.4 – 6.1 mmol/L |
80 – 110 mg/dL |
0 |
|
6.2 – 7.8 mmol/L |
111 – 140 mg/dL |
+ 2 U |
|
7.9 – 10 mmol/L |
141 – 180 mg/dL |
+ 4 U |
|
> 10 mmol/L |
> 180 mg/dL |
+ 6U |
Se deben usar los niveles más bajos de glucosa en sangre antes de alimento de los tres días anteriores. La dosis no debe aumentarse en caso de que ocurra hipoglucemia en estos días. Los ajustes de dosis pueden realizarse una vez a la semana hasta alcanzar el objetivo de HbA1c. Se deben usar los niveles de glucosa en sangre antes de los alimentos para evaluar la conveniencia de la dosis anterior.
En pacientes con diabetes tipo 1, el requerimiento individual de insulina es por lo general entre 0.5 y 1.0 unidades/kg/día. NOVOMIX® 30 puede cumplir este requerimiento total o parcialmente. El requerimiento diario de insulina puede ser mayor en pacientes con resistencia a la insulina (p. ej. debido a obesidad) y menor en pacientes con producción endógena residual de insulina.
Poblaciones especiales:
Ancianos: NOVOMIX® 30 puede usarse en pacientes mayores; sin embargo, existe experiencia limitada con el uso de NOVOMIX® 30 en combinación con antidiabéticos orales en pacientes mayores de 75 años.
Al igual que con todos los productos de insulina, en pacientes mayores el monitoreo de glucosa debe intensificarse y la dosis de insulina asparta ajustarse sobre una base individual.
Insuficiencia renal y hepática: La insuficiencia renal y hepática puede reducir los requisitos de insulina del paciente.
Al igual que con todos los productos de insulina, en pacientes con insuficiencia renal o hepática, el monitoreo de glucosa debe intensificarse y la dosis de insulina asparta ajustarse sobre una base individual.
Población pediátrica: NOVOMIX® 30 puede usarse en niños y adolescentes de 10 años o más cuando se prefiera insulina premezclada. Existen datos clínicos limitados para niños de entre 6 y 9 años.
Transferencia de otros productos de insulina: Cuando se transfiera a un paciente de insulina humana bifásica a NOVOMIX® 30, iniciar con la misma dosis y régimen. Titular entonces conforme a necesidades individuales (ver los lineamientos de titulación en la Tabla anterior).
Al igual que con todos los productos de insulina, se recomienda un monitoreo estrecho durante la transferencia y las semanas iniciales posteriores.
TRANSFERENCIA DE OTROS PRODUCTOS DE INSULINA: La transferencia de un paciente a otro tipo o marca de insulina se debe realizar bajo estricta supervisión médica. Los cambios de potencia, marca (fabricante), tipo, origen (insulina humana, insulina análoga) y/o método de fabricación pueden resultar en una necesidad de cambio de dosificación. Los pacientes transferidos a NOVOMIX® 30 desde otro tipo de insulina pueden requerir un aumento en el número de inyecciones diarias o un cambio en la dosificación de aquella que usaban con sus productos de insulina habituales. En caso de necesitarse un ajuste, esto puede ocurrir con la primera dosis o durante las primeras semanas o meses.
Reacciones en el sitio de inyección: Al igual que con cualquier terapia de insulina, pueden ocurrir reacciones en el sitio de inyección incluyendo dolor, enrojecimiento, urticaria, inflamación, hematomas, hinchazón y comezón. Una rotación continua del sitio de inyección dentro de un área dada puede ayudar a reducir o prevenir estas reacciones. Por lo general las reacciones se resuelven en unos cuantos días o semanas. Las reacciones del sitio de inyección raramente pueden requerir de la suspensión de NOVOMIX® 30.
Combinación de tiazolidinedionas y medicamentos de insulina: Se han reportado casos de insuficiencia cardíaca congestiva al usar tiazolidinedionas en combinación con insulina, en particular en pacientes con factores de riesgo para el desarrollo de insuficiencia cardíaca congestiva. Esto se debe tener en mente si se considera el tratamiento con la combinación de tiazolidinedionas y medicamentos de insulina. Si se usa esta combinación, se debe observar a los pacientes en busca de signos y síntomas de insuficiencia cardíaca congestiva, aumento de peso y edema. Se deben suspender las tiazolidinedionas en caso de ocurrir cualquier deterioro de los síntomas cardíacos.
Anticuerpos contra la insulina: La administración de insulina puede provocar la formación de anticuerpos contra la insulina. En raras ocasiones, la presencia de estos anticuerpos contra la insulina puede necesitar de un ajuste de la dosis de insulina para corregir una tendencia a la hiper o a la hipoglucemia.
SOBREDOSIFICACIÓN: No se puede definir una sobredosis específica para insulina, sin embargo, se puede desarrollar hipoglucemia a lo largo de etapas secuenciales si se administran dosis muy altas con relación a los requerimientos del paciente:
• Los episodios moderados de hipoglucemia pueden tratarse con administración oral de glucosa o productos azucarados. Por lo tanto es recomendable que el paciente diabético siempre lleve consigo productos que contengan azúcar.
• Los episodios severos de hipoglucemia, en los que el paciente pierde la conciencia, pueden tratarse con glucagón (0.5 a 1 mg) administrado intramuscular o subcutáneamente por una persona capacitada, o con glucosa administrada en forma intravenosa por un profesional de la salud.
La glucosa debe administrarse de forma intravenosa si el paciente no responde al glucagón en los siguientes 10 a 15 minutos. Tras recuperar la conciencia, se recomienda la ingesta de carbohidratos orales al paciente para prevenir una recaída.
PRESENTACIÓN: Estuche con 5 plumas pre-llenadas de 3 mL y estuche con 1 pluma pre-llenada de 3 mL.
Nombre del producto: NOVOMIX® 30 FLEXPEN®.
Fabricante y país: NOVO NORDISK A/S, Dinamarca.
Titular de la autorización: NOVO NORDISK A/S, Dinamarca.
No todas las presentaciones mencionadas están disponibles en todos los países.
Última revisión local: Agosto 2019 basada en el ENDS V.1.0 de 24 Agosto 2016 (Costa Rica) y ENDS V.2.0 de 24 Octubre 2017 (República Dominicana, El Salvador, Honduras).
Pueden existir diferencias en cuanto a las indicaciones aprobadas para cada país. Siempre refiérase a la información prescriptiva completa local a disposición en el departamento médico de NOVO NORDISK.
NOVO NORDISK
® Marca registrada
CONDICIONES DE ALMACENAMIENTO: Almacenar en refrigeración (2 ºC - 8 ºC). Mantener alejado del elemento enfriador. No congelar.
Tras la primera apertura o al llevarse como repuesto: Un máximo de 4 semanas al almacenarse por debajo de 30 ºC.
INSTRUCCIONES DE USO, MANIPULACIÓN Y DESTRUCCIÓN DEL REMANENTE NO UTILIZABLE DEL PRODUCTO: Las agujas y NOVOMIX® 30 FLEXPEN® no deben compartirse. El cartucho no debe recargarse.
Una vez que saque NOVOMIX® 30 FLEXPEN® del refrigerador, se recomienda dejar que NOVOMIX® 30 FLEXPEN® alcancen temperatura ambiente antes de resuspender la insulina según se instruyó para el uso de la primera vez.
NOVOMIX® 30 no debe usarse si el líquido resuspendido no tiene aspecto uniformemente blanco y turbio. Debe recalcarse al paciente la necesidad de resuspender la suspensión de NOVOMIX® 30 FLEXPEN® inmediatamente antes de usarse. No se deben usar NOVOMIX® 30 que haya sido congelado.
Se debe recomendar al paciente a desechar la aguja después de cada inyección.
Plazo de validez: 24 meses.