
TRESIBA FLEXTOUCH
INSULINA DEGLUDEC
Solución inyectable
Estuche, 1 Pluma prellenada, 3 ml,
Estuche, 5 Pluma prellenada, 3 ml,
Estuche, 3 Pluma prellenada, 3 ml,
COMPOSICIÓN: Cada mL contiene:
|
100 U/ml |
||
|
Sustancia |
Cantidad por mL |
Referencia de Calidad |
|
Insulina degludec |
600 nmol |
NOVO NORDISK |
|
Fenol |
1.50 mg |
FE ,USP, FJ |
|
Metacresol |
1.72 mg |
FE, USP |
|
Glicerol |
19.6 mg |
FE ,USP, FJ |
|
Zinc |
32.7 µg |
FE ,USP, FJ |
|
Ácido clorhídrico (para ajuste de pH) |
c.s.p. |
FE ,USP, FJ |
|
Hidróxido de sodio (para ajuste de pH) |
c.s.p. |
FE ,USP, FJ |
|
Agua para inyectables |
c.s.p. 1.00 ml |
FE ,USP, FJ |
Plazo de validez: 30 meses.
Después del primer uso: 8 semanas.
CONCENTRACIÓN:
100 unidades/mL: 1 mL de solución contiene 100 unidades de insulina degludec* (equivalente a 3.66 mg de insulina degludec).
FlexTouch®: Una pluma pre-llenada contiene 300 unidades de insulina degludec en 3 mL de solución.
*Producida en Saccharomyces cerevisiae mediante tecnología de ADN recombinante.
FORMA FARMACÉUTICA: Solución inyectable en pluma pre-llenada.
PROPIEDADES FARMACODINÁMICAS:
Grupo farmacoterapéutico: Medicamentos utilizados en la diabetes. Insulinas y análogos inyectables de acción prolongada.
Código ATC: A10AE06.
Mecanismo de acción: La insulina degludec se une específicamente al receptor de la insulina humana y produce los mismos efectos farmacológicos que esta.
El efecto hipoglucemiante de la insulina se debe a que facilita la absorción de glucosa luego de que la insulina se une a los receptores en las células musculares y adiposas, y a que inhibe al mismo tiempo la producción hepática de glucosa.
PROPIEDADES FARMACOCINÉTICAS:
Absorción: Tras la inyección subcutánea, se forman multihexámeros solubles y estables que crean un depósito de insulina en el tejido subcutáneo. Los monómeros de insulina degludec se separan gradualmente de los multihexámeros, dando como resultado una entrada lento y continua de insulina degludec a la circulación.
La concentración en suero en estado estacionario se alcanza a los 2–3 días de la administración diaria de TRESIBA®.
Durante un periodo de 24 horas, con el tratamiento una vez al día, la exposición de la insulina degludec se distribuyó uniformemente entre el primer y segundo periodo de 12 horas. La proporción entre AUCGIR,0-12 h,SS y AUCGIR,τ,SS fue de 0.5.
Distribución: La afinidad de la insulina degludec con la albúmina en suero corresponde a una unión con proteínas plasmáticas > 99% en plasma humano.
Metabolismo: La degradación de la insulina degludec es similar a la de la insulina humana; todos los metabolitos formados son inactivos.
Eliminación: La semivida después de la administración subcutánea de TRESIBA® está determinada por la velocidad de absorción desde el tejido subcutáneo. La semivida de TRESIBA® es de aproximadamente 25 horas, independientemente de la dosis.
Linealidad: La proporcionalidad de la dosis en la exposición total se observa luego de la administración subcutánea dentro del intervalo de dosis terapéutico. En una comparación directa, se cumplen los requisitos de bioequivalencia para TRESIBA® 100 unidades/ mL y TRESIBA® 200 unidades/ mL (con base en AUCIDeg,τ,SS y Cmáx,IDeg,SS).
Sexo: No hay diferencias entre sexos en cuanto a las propiedades farmacocinéticas de TRESIBA®.
Pacientes de edad avanzada, raza, insuficiencia renal y hepática: No hay diferencias en la farmacocinética de la insulina degludec entre pacientes de edad avanzada y adultos de menor edad; tampoco entre razas ni entre sujetos sanos y pacientes con insuficiencia renal o hepática.
Población pediátrica: Las propiedades farmacocinéticas de la insulina degludec en niños (1–11 años) y adolescentes (12–18 años de edad), en estado estacionario, fueron comparables con las de los adultos con diabetes mellitus tipo 1. No obstante, la exposición total tras una sola dosis fue más alta en niños y adolescentes que en adultos con diabetes mellitus tipo 1.
CONTRAINDICACIONES: Hipersensibilidad a la insulina degludec o a alguno de los excipientes.
ADVERTENCIAS Y PRECAUCIONES:
Hipoglucemia: La omisión de una comida o el ejercicio físico intenso no previsto pueden conducir a hipoglucemia.
Puede presentarse hipoglucemia si la dosis de insulina es demasiado alta en comparación con el requerimiento de insulina.
En niños, se debe tener cuidado para ajustar las dosis de insulina (especialmente en esquemas de bolo-basal) con la ingesta de alimentos y la actividad física, con el fin de minimizar el riesgo de hipoglucemia.
Los pacientes cuyo control glucémico muestra una gran mejoría (por ejemplo, por medio de terapia insulínica intensiva) podrían experimentar un cambio en sus síntomas habituales de alerta de hipoglucemia y se les debe advertir sobre esta posibilidad. Los síntomas habituales de alerta pueden desaparecer en los pacientes con diabetes de larga duración.
Las enfermedades concomitantes, especialmente las infecciones y fiebre, generalmente aumentan el requerimiento de insulina del paciente. Las enfermedades concomitantes renales, hepáticas o que afecten a las glándulas suprarrenal, pituitaria o tiroidea podrían requerir de un cambio en la dosis de insulina.
Como ocurre con otras insulinas basales, el efecto prolongado de TRESIBA® podría retrasar la recuperación de una hipoglucemia.
Hiperglucemia: Se recomienda la administración de insulina de acción rápida en caso de hiperglucemia grave.
La administración inadecuada y/o la interrupción del tratamiento en pacientes con necesidades de insulina pueden ocasionar hiperglucemia y, potencialmente, cetoacidosis diabética. Además, las enfermedades concomitantes, especialmente las infecciones, pueden provocar hiperglucemia y, por tanto, aumentar el requerimiento de insulina.
Los primeros síntomas de hiperglucemia generalmente aparecen de forma gradual, durante un periodo de horas o días. Estos incluyen sed, aumento de la frecuencia de micción, náuseas, vómitos, somnolencia, piel reseca y enrojecida, boca seca y pérdida de apetito; así como aliento con olor a acetona.
En la diabetes mellitus tipo 1, los eventos hiperglucémicos no tratados pueden dar lugar en última instancia a cetoacidosis diabética, que es potencialmente mortal.
Cambio desde otras insulinas: El cambio de un paciente a otro tipo, marca o fabricante de insulina debe realizarse bajo supervisión médica y podría ser necesario un cambio en la dosis.
Combinación de pioglitazona e insulinas: Cuando se utilizó pioglitazona en combinación con insulina, se refirieron casos de insuficiencia cardiaca, especialmente en pacientes con factores de riesgo para el desarrollo de insuficiencia cardiaca. Esto debe tenerse en cuenta si se considera el tratamiento combinado de pioglitazona y TRESIBA®. Si se utiliza esta combinación, debe monitorearse a los pacientes para detectar la aparición de signos y síntomas de insuficiencia cardiaca, ganancia de peso y edema. Debe interrumpirse el tratamiento con pioglitazona si se presenta cualquier deterioro de los síntomas cardiacos.
Trastornos oculares: La intensificación del tratamiento insulínico, con una mejoría abrupta del control glucémico, podría asociarse a un empeoramiento temporal de la retinopatía diabética; mientras que un mejor control glucémico a largo plazo reduce el riesgo de avance de la retinopatía diabética.
Previsión de errores de medicación: Debe indicarse a los pacientes que revisen siempre la etiqueta de la insulina antes de cada inyección, para evitar confusiones entre las dos concentraciones de TRESIBA® y también con otras insulinas.
Los pacientes deben comprobar visualmente las unidades marcadas en el contador de dosis de la pluma. Por lo tanto, para que los pacientes puedan autoinyectarse es imprescindible que sean capaces de leer dicho contador. Los pacientes no videntes o con visión reducida siempre deben pedir ayuda a otra persona sin problemas de visión y capacitado en el uso del dispositivo de administración de insulina.
Anticuerpos anti-insulina: La administración de insulina puede provocar la formación de anticuerpos contra la insulina. En casos raros la presencia de estos anticuerpos antiinsulina puede provocar el ajuste de la dosis de insulina para corregir la tendencia a la hiper o hipoglucemia.
USO EN EMBARAZO Y LACTANCIA:
Embarazo: No hay experiencia clínica con el uso de TRESIBA® en mujeres embarazadas.
Los estudios sobre reproducción animal no han revelado diferencias entre la insulina degludec y la insulina humana con respecto a embriotoxicidad y teratogenicidad.
En general, se recomienda intensificar el control glucémico y el monitoreo de mujeres embarazadas con diabetes, durante todo el embarazo y cuando se planea embarazarse. La necesidad de insulina generalmente disminuye en el primer trimestre del embarazo y aumenta posteriormente durante el segundo y tercer trimestres. Después del parto, la necesidad de insulina vuelve rápidamente a los niveles previos al embarazo.
Lactancia: No hay experiencia clínica con el uso de TRESIBA® durante la lactancia. En ratas, la insulina degludec se excretó en la leche; la concentración en leche fue inferior a la concentración en plasma.
Se desconoce si la insulina degludec se excreta en la leche materna. No se prevén efectos metabólicos en niños/recién nacidos lactantes.
Fertilidad: Los estudios sobre reproducción animal con insulina degludec no han revelado efectos adversos sobre la fertilidad.
EFECTOS EN LA CONDUCCIÓN DE VEHÍCULOS/MAQUINARIAS: La capacidad de concentración y de reacción de los pacientes podría verse afectada por la hipoglucemia. Esto puede suponer un riesgo en situaciones en las que estas capacidades sean de especial importancia (por ejemplo, conducir o utilizar máquinas).
Debe advertirse a los pacientes que tomen precauciones para evitar una hipoglucemia mientras conducen. Esto es particularmente importante en aquellos pacientes con reducida o nula capacidad para percibir los síntomas de hipoglucemia, o que padecen episodios frecuentes de hipoglucemia. Se debe considerar la conveniencia de conducir o no en estas circunstancias.
EFECTOS FARMACODINÁMICOS: TRESIBA® es una insulina basal que forma multihexámeros solubles cuando se inyecta por vía subcutánea, dando lugar a la formación de un depósito desde el que se absorbe a la circulación de forma lenta y continua, produciendo el efecto hipoglucemiante plano y estable de TRESIBA® (vea la figura 1). Durante un periodo de 24 horas con el tratamiento de una vez por día, el efecto hipoglucemiante de TRESIBA®, a diferencia del de la insulina glargina, se distribuyó uniformemente entre el primer y segundo periodo de 12 horas (AUCGIR,0-12 h,SS/AUCGIR,total,SS = 0.5).
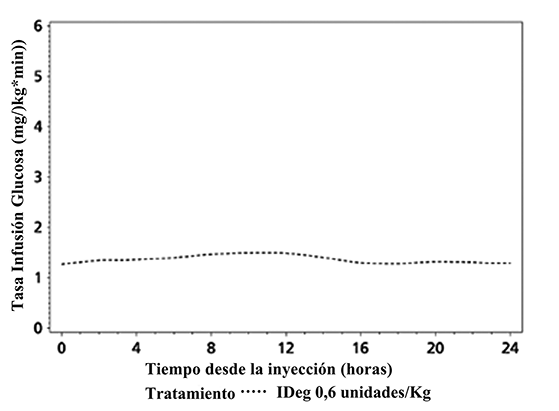
Perfil del índice de perfusión de glucosa, estado estacionario suavizado - Perfil medio 0-24 horas - IDeg 100 unidades/mL 0.6 unidades/kg - Estudio 1987.
La duración de la acción de TRESIBA® es superior a 42 horas dentro del intervalo de dosis terapéutico.
El estado estacionario se presenta 2–3 días después de la administración de la dosis.
La acción hipoglucemiante de la insulina degludec en estado estacionario muestra una variabilidad día a día cuatro veces más baja en términos del Coeficientes de Variación (CV) del efecto hipoglucemiante durante 0-24 horas (AUCGIR,τ,SS) y 2–24 horas (AUCGIR2-24 h,SS) en comparación con la insulina glargina; vea la tabla 1.
|
Tabla 1. Variabilidad día a día entre pacientes, en el efecto hipoglucemiante de TRESIBA® e insulina glargina en estado estacionario, en pacientes con diabetes mellitus tipo 1. |
||
|
Insulina degludec (N26) (CV%) |
Insulina glargina (N27) (CV%) |
|
|
Variabilidad día a día en el efecto hipoglucemiante durante un intervalo de dosificación (AUCGIR,τ,SS). |
20 |
82 |
|
Variabilidad día a día en el efecto hipoglucemiante de 2 a 24 horas (AUCGIR2-24 h,SS). |
22 |
92 |
|
CV: coeficiente de variación entre pacientes, en % SS: estado estacionario AUCGIR,2-24 h: efecto metabólico en las últimas 22 horas del intervalo de dosificación (es decir, no influido por la insulina I.V. durante el periodo de preinclusión de pinzamiento). |
||
El efecto hipoglucemiante total de TRESIBA® aumenta de forma lineal con el aumento de la dosis.
El efecto hipoglucemiante total es comparable para TRESIBA® 100 unidades/ mL y 200 unidades/ mL tras la administración de la misma dosis de los dos productos.
No hay diferencia clínicamente significativa en las propiedades farmacodinámicas de TRESIBA® entre los pacientes de edad avanzada y los pacientes adultos de menor edad.
Eficacia clínica: Se realizaron once estudios clínicos, multinacionales, de 26 o 52 semanas de duración, de tratamiento hasta la meta (treat-to-target), controlados, abiertos, con distribución al azar y paralelos en los que se administró TRESIBA® a 4,275 pacientes (1,102 con diabetes mellitus tipo 1 y 3,173 con diabetes mellitus tipo 2).
Se analizó el efecto de TRESIBA® en pacientes con diabetes mellitus tipo 1 (tabla 3), en pacientes sin tratamiento previo con insulina (inicio de insulina en pacientes con diabetes mellitus tipo 2, tabla 4) y en pacientes que recibieron insulina previamente (intensificación de insulina en los pacientes con diabetes mellitus tipo 2, tabla 5) con un horario de administración tanto fijo como flexible (tabla 6). Se confirmó la no inferioridad de la reducción de la HbA1c, desde el valor inicial hasta el final del estudio, para todos los estudios, con respecto a todos los comparadores (insulina detemir e insulina glargina). Al tiempo que las mejoras en la HbA1c no fueron inferiores en comparación con otras insulinas, respecto a la sitagliptina, TRESIBA® fue estadística y significativamente superior en la reducción de la HbA1c (tabla 5).
En un metaanálisis planificado de forma prospectiva en siete estudios confirmatorios, de tratamiento hasta la meta, en pacientes con diabetes mellitus tipos 1 y 2, TRESIBA® fue superior en términos de un menor número de episodios de hipoglucemia confirmada surgidos durante el tratamiento (motivado por un beneficio en la diabetes mellitus tipo 2; consulte la tabla 2) y de episodios de hipoglucemia nocturna confirmada, en comparación con la insulina glargina (administrada según la etiqueta). La reducción de hipoglucemia se logró con un nivel de glucosa plasmática en ayuno (GPA) medio inferior con TRESIBA®, en comparación con insulina glargina.
|
Tabla 2. Resultados del metaanálisis de hipoglucemia |
||
|
Hipoglucemia confirmadaa |
||
|
Índice de riesgo estimado (insulina degludec/insulina glargina) |
Total |
Nocturna |
|
Diabetes mellitus tipo 1 + tipo 2 (combinadas). |
0.91* |
0.74* |
|
Periodo de mantenimientob. |
0.84* |
0.68* |
|
Pacientes geriátricos ≥ 65 años. |
0.82 |
0.65* |
|
Diabetes mellitus tipo 1. |
1.10 |
0.83 |
|
Periodo de mantenimientob. |
1.02 |
0.75* |
|
Diabetes mellitus tipo 2. |
0.83* |
0.68* |
|
Periodo de mantenimientob. |
0.75* |
0.62* |
|
Terapia sólo basal en pacientes sin tratamiento previo de insulina. |
0.83* |
0.64* |
|
*Estadísticamente significativoa. La hipoglucemia confirmada se definió como los episodios confirmados mediante glucosa en plasma < 3.1 mmol/L o por la necesidad del paciente de asistencia de terceras personas. La hipoglucemia nocturna confirmada se definió como los episodios ocurridos entre la medianoche y las 6 a.m. b Episodios desde la semana 16. |
||
Sin desarrollo clínicamente significativo de anticuerpos antiinsulina después del tratamiento de largo plazo con TRESIBA®.
|
Tabla 3. Resultados de estudios clínicos en pacientes con diabetes mellitus tipo 1 |
||||
|
52 semanas de tratamiento |
26 semanas de tratamiento |
|||
|
TRESIBA®1 |
Insulina glargina1 |
TRESIBA®1 |
Insulina detemir1 |
|
|
N |
472 |
157 |
302 |
153 |
|
HbA1c (%) |
||||
|
Final del estudio |
7.3 |
7.3 |
7.3 |
7.3 |
|
Cambio medio |
- 0.40 |
- 0.39 |
- 0.73 |
- 0.65 |
|
Diferencia: - 0.01 [- 0.14; 0.11] |
Diferencia: - 0.09[- 0.23; 0.05] |
|||
|
GPA (mmol/L) |
||||
|
Final del estudio |
7.8 |
8.3 |
7.3 |
8.9 |
|
Cambio medio |
- 1.27 |
- 1.39 |
- 2.60 |
- 0.62 |
|
Diferencia: - 0.33 [- 1.03; 0.36] |
Diferencia: - 1.66 [- 2.37; - 0.95] |
|||
|
Índice de hipoglucemia (por año de exposición de paciente). |
||||
|
Grave |
0.21 |
0.16 |
0.31 |
0.39 |
|
Confirmada2 |
42.54 |
40.18 |
45.83 |
45.69 |
|
Índice: 1.07 [0.89; 1.28] |
Índice: 0.98 [0.80; 1.20] |
|||
|
Nocturna confirmada2 |
4.41 |
5.86 |
4.14 |
5.93 |
|
Índice: 0.75 [0.59; 0.96] |
Índice: 0.66 [0.49; 0.88] |
|||
|
1 En un esquema de una dosis diaria + insulina aspart para cubrir las necesidades de insulina durante las comidas 2 La hipoglucemia confirmada se definió como los episodios confirmados mediante glucosa en plasma < 3.1 mmol/L o por la necesidad del paciente de asistencia de terceras personas. La hipoglucemia nocturna confirmada se definió como los episodios ocurridos entre la medianoche y las 6 a.m. |
||||
|
Tabla 4. Resultados de estudios clínicos en pacientes con diabetes mellitus tipo 2 sin tratamiento previo con insulina (inicio de insulina) |
||||
|
52 semanas de tratamiento |
26 semanas de tratamiento |
|||
|
TRESIBA®1 |
Insulina glargina1 |
TRESIBA®1 |
Insulina glargina1 |
|
|
N |
773 |
257 |
228 |
229 |
|
HbA1c (%) |
||||
|
Final del estudio |
7.1 |
7.0 |
7.0 |
6.9 |
|
Cambio medio |
- 1.06 |
- 1.19 |
- 1.30 |
- 1.32 |
|
Diferencia: 0.09 [- 0.04; 0.22] |
Diferencia: 0.04[- 0.11; 0.19] |
|||
|
GPA (mmol/L) |
||||
|
Final del estudio |
5.9 |
6.4 |
5.9 |
6.3 |
|
Cambio medio |
- 3.76 |
- 3.30 |
- 3.70 |
- 3.38 |
|
Diferencia: - 0.43 [- 0.74; - 0.13] |
Diferencia: - 0.42 [- 0.78; - 0.06] |
|||
|
Índice de hipoglucemia (por año de exposición de paciente) |
||||
|
Grave |
0 |
0.02 |
0 |
0 |
|
Confirmada2 |
1.52 |
1.85 |
1.22 |
1.42 |
|
Índice: 0.82 [0.64; 1.04] |
Índice: 0.86 [0.58; 1.28] |
|||
|
Nocturna confirmada2 |
0.25 |
0.39 |
0.18 |
0.28 |
|
Índice: 0.64 [0.42; 0.98] |
Índice: 0.64 [0.30; 1.37] |
|||
|
1 Esquema de una dosis diaria + metformina ± inhibidor de DPP-4 2 La hipoglucemia confirmada se definió como los episodios confirmados mediante glucosa en plasma < 3.1 mmol/L o por la necesidad del paciente de asistencia de terceras personas. La hipoglucemia nocturna confirmada se definió como los episodios ocurridos entre la medianoche y las 6 a.m. |
||||
|
Tabla 5. Resultados de estudios clínicos en pacientes con diabetes mellitus tipo 2: izquierda – pacientes previamente tratados con insulina, derecha – pacientes sin tratamiento previo con insulina |
||||
|
52 semanas de tratamiento |
26 semanas de tratamiento |
|||
|
TRESIBA®1 |
Insulina glargina1 |
TRESIBA®1 |
Sitagliptina2 |
|
|
N |
774 |
248 |
225 |
222 |
|
HbA1c (%) |
||||
|
Final del estudio |
7.1 |
7.1 |
7.2 |
7.7 |
|
Cambio medio |
- 1.17 |
- 1.29 |
- 1.56 |
- 1.22 |
|
Diferencia: 0.08 [- 0.05; 0.21] |
Diferencia: - 0.43[- 0.61; - 0.24] |
|||
|
GPA (mmol/L) |
||||
|
Final del estudio |
6.8 |
7.1 |
6.2 |
8.5 |
|
Cambio medio |
- 2.44 |
- 2.14 |
- 3.22 |
- 1.39 |
|
Diferencia: - 0.29 [- 0.65; 0.06] |
Diferencia: - 2.17 [- 2.59; - 1.74] |
|||
|
Índice de hipoglucemia (por año de exposición de paciente) |
||||
|
Grave |
0.06 |
0.05 |
0.01 |
0 |
|
Confirmada2 |
11.09 |
13.63 |
3.07 |
1.26 |
|
Índice: 0.82 [0.69; 0.99] |
Índice: 3.81 [2.40; 6.05] |
|||
|
Nocturna confirmada2 |
1.39 |
1.84 |
0.52 |
0.30 |
|
Índice: 0.75 [0.58; 0.99] |
Índice: 1.93 [0.90; 4.10] |
|||
|
1 Esquema de una dosis diaria + insulina aspart para cubrir las necesidades de insulina durante las comidas ± metformina ± pioglitazona 2 Esquema de una dosis diaria ± metformina SU/glinida ± pioglitazona 3 La hipoglucemia confirmada se definió como los episodios confirmados mediante glucosa en plasma < 3.1 mmol/L o por la necesidad del paciente de asistencia de terceras personas. La hipoglucemia nocturna confirmada se definió como los episodios ocurridos entre la medianoche y las 6 a.m. |
||||
|
Tabla 6. Resultados de un estudio clínico con administración flexible de TRESIBA® en pacientes con diabetes mellitus tipo 2 |
|||
|
26 semanas de tratamiento |
|||
|
TRESIBA®1 |
TRESIBA® Flex2 |
Insulin glargina3 |
|
|
N |
228 |
229 |
230 |
|
HbA1c (%) |
|||
|
Final del estudio |
7.3 |
7.2 |
7.1 |
|
11 Cambio medio |
- 1.07 |
- 1.28 |
- 1.26 |
|
Diferencia: -0.13 [-0.29; 0.03]5 |
Diferencia: 0.04 [- 0.12; 0.20] |
||
|
GPA (mmol/L) |
|||
|
Final del estudio |
5.8 |
5.8 |
6.2 |
|
11 Cambio medio con respecto al inicio |
- 2.91 |
- 3.15 |
- 2.78 |
|
Diferencia: - 0.05 [- 0.45; 0.35]5 |
Diferencia: - 0.42 [- 0.82; - 0.02] |
||
|
Índice de hipoglucemia (por año de exposición de paciente) |
|||
|
Grave |
0.02 |
0.02 |
0.02 |
|
Confirmada4 |
3.63 |
3.64 |
3.48 |
|
Índice: 1.10 [0.79; 1.52]6 |
Índice: 1.03 [0.75; 1.40] |
||
|
Nocturna confirmada4 |
0.56 |
0.63 |
0.75 |
|
Índice: 1.18 [0.66; 2.12]6 |
Índice: 0.77 [0.44; 1.35] |
||
|
1 Esquema de una dosis diaria (con la comida vespertina principal) + uno o dos de los siguientes agentes antidiabéticos orales: SU, metformina o inhibidor de DPP-4 2 Esquema de una dosis diaria flexible (intervalos de aproximadamente 8-40 horas entre dosis) + uno o dos de los siguientes agentes antidiabéticos orales: SU, metformina o inhibidor de DPP-4 3 Esquema de una dosis diaria + uno o dos de los siguientes agentes antidiabéticos orales: SU, metformina o inhibidor de DPP-4 4 La hipoglucemia confirmada se definió como los episodios confirmados mediante glucosa en plasma < 3.1 mmol/L o por la necesidad del paciente de asistencia de terceras personas. La hipoglucemia nocturna confirmada se definió como los episodios ocurridos entre la medianoche y las 6 a.m. 5 La diferencia es para TRESIBA® Flex/TRESIBA®. 6 El índice es para TRESIBA® Flex/TRESIBA®. |
|||
En un estudio clínico de 104 semanas, 57% de los pacientes con diabetes tipo 2 tratados con TRESIBA® (insulina degludec) en combinación con metformina alcanzaron el objetivo de HbA1c < 7.0%. El resto de pacientes continuaron en un estudio abierto de 26 semanas y fueron distribuidos al azar para añadir a su tratamiento liraglutida o una dosis única de insulina aspart (con la comida principal). En el grupo de insulina degludec + liraglutida, la dosis de insulina se redujo un 20% para minimizar el riesgo de hipoglucemia. La adición de liraglutida dio como resultado una mayor reducción, estadísticamente significativa, de la HbA1c (- 0.73% para liraglutida frente a – 0.40% para el comparador, medias estimados) y del peso corporal (- 3.03 frente a 0.72 kg, medias estimados). El índice de episodios de hipoglucemia (por año de exposición de paciente) fue estadística y significativamente menor cuando se añadió liraglutida en comparación con la adición de una dosis única de insulina aspart (1.0 frente a 8.15; proporción: 0.13; IC del 95%: 0.08 a 0.21).
Población pediátrica: La Agencia Europea de Medicamentos ha condonado la obligación de presentar los resultados de los estudios con TRESIBA® en:
• Neonatos y bebés desde el nacimiento hasta menos de 12 meses de edad con diabetes mellitus tipo 1 y niños desde el nacimiento hasta menos de 10 años de edad con diabetes mellitus tipo 2, con el fundamento de que la enfermedad o padecimiento para el que está previsto el medicamento específico no se presenta en el subconjunto pediátrico especificado (consulte la sección 4.2 para ver la información sobre el uso en la población pediátrica).
Se ha estudiado la eficacia y seguridad de TRESIBA® en un estudio clínico con distribución al azar 1:1, controlado, en niños y adolescentes con diabetes mellitus tipo 1, durante un periodo de 26 semanas (n=350), seguido de un periodo de extensión de 26 semanas (n=280). Los pacientes en el grupo de TRESIBA® incluyeron a 43 niños de 1 a 5 años, 70 niños de 6 a 11 años y 61 adolescentes de 12 a 17 años. La administración de TRESIBA® una vez al día mostró una reducción similar en la HbA1c en la semana 52 y una mayor reducción de la GPA, con respecto a los valores iniciales, frente al comparador, insulina detemir, administrado una o dos veces al día. Esto se logró con dosis diarias de TRESIBA® 30% menores en comparación con insulina detemir. Los índices (acontecimientos por año de exposición de paciente) de hipoglucemia grave (definición ISPAD; 0.51 vs. 0.33), hipoglucemia confirmada (57.71 vs. a 54.05) e hipoglucemia nocturna confirmada (6.03 vs. 7.60), fueron comparables entre TRESIBA® e insulina detemir. En ambos grupos de tratamiento, los niños de 6 a 11 años tuvieron un índice numéricamente mayor de hipoglucemia confirmada, en comparación con los otros grupos de edad. En el grupo de TRESIBA®, se observó un índice numéricamente mayor de hipoglucemia grave en niños de 6 a 11 años. El índice de episodios de hiperglucemia con cetosis fue significativamente menor para TRESIBA® en comparación con insulina detemir, 0.68 y 1.09, respectivamente. No se identificaron problemas de seguridad con TRESIBA® con respecto a los eventos adversos y los parámetros de seguridad convencionales. El desarrollo de anticuerpos fue escaso y no tuvo impacto clínico. Los datos de eficacia y seguridad para pacientes adolescentes con diabetes mellitus tipo 2 se extrapolaron a partir de los datos de pacientes adolescentes y adultos con diabetes mellitus tipo 1 y pacientes adultos con diabetes mellitus tipo 2. Los resultados apoyan el uso de TRESIBA® en pacientes adolescentes con diabetes mellitus tipo 2.
EFECTOS INDESEABLES:
Resumen del perfil de seguridad: La hipoglucemia fue la reacción adversa informada más frecuentemente durante el tratamiento (véase la sección Descripción de las reacciones adversas seleccionadas más adelante).
Tabla de reacciones adversas: Las reacciones adversas presentadas a continuación se basan en los datos de los estudios clínicos y se clasifican de acuerdo con la clasificación por órganos o sistemas de MedDRA. Las categorías de frecuencias se definen según la siguiente convención: muy frecuentes (≥ 1/10); frecuentes (≥ 1/100 a < 1/10); poco frecuentes (≥ 1/1,000 a < 1/100); raras (≥ 1/10,000 a < 1/1,000); muy raras (< 1/10,000) y frecuencia desconocida (no puede estimarse a partir de los datos disponibles).
|
Clasificación por órganos o sistemas |
Frecuencia |
|
Trastornos del sistema inmunitario |
Rara – Hipersensibilidad |
|
Rara – Urticaria |
|
|
Trastornos del metabolismo y de la nutrición |
Muy frecuente - Hipoglucemia |
|
Trastornos de la piel y del tejido subcutáneo |
Poco frecuente - Lipodistrofia |
|
Trastornos generales y alteraciones en el lugar de administración |
Frecuente - Reacciones en la zona de inyección |
|
Poco frecuente - Edema periférico |
Descripción de las reacciones adversas seleccionadas:
Trastornos del sistema inmunitario: Pueden presentarse reacciones alérgicas con las insulinas. Las reacciones alérgicas inmediatas a la propia insulina o a los excipientes pueden poner en peligro la vida de los pacientes.
Se han referido casos raros de hipersensibilidad (manifestada por hinchazón de la lengua y los labios, diarrea, náuseas, cansancio y prurito) y urticaria derivados del uso de TRESIBA®.
Hipoglucemia: Puede ocurrir hipoglucemia si la dosis de insulina es demasiado alta en relación con la necesidad de insulina. Una hipoglucemia grave puede producir pérdida del conocimiento y/o convulsiones y podría dar lugar a una alteración neurológica temporal o permanente o incluso la muerte. Los síntomas de hipoglucemia aparecen generalmente de forma repentina. Pueden incluir sudoración fría, piel fría y pálida, fatiga, nerviosismo o temblor, ansiedad, cansancio o debilidad no habituales, confusión, dificultad para concentrarse, somnolencia, apetito excesivo, cambios en la visión, cefalea, náuseas y palpitaciones.
Lipodistrofia: Puede presentarse lipodistrofia (incluidas lipohipertrofia y lipoatrofia) en el lugar de la inyección. La rotación continua de la zona de inyección dentro de un área concreta puede ayudar a reducir el riesgo de desarrollar estas reacciones.
Reacciones en el sitio de inyección: Se han observado reacciones en la zona de inyección (como hematoma, dolor, hemorragia, eritema, nódulos, hinchazón, cambio de color, prurito, calor y abultamiento en el lugar de inyección) en pacientes tratados con TRESIBA®. Estas reacciones suelen ser leves y transitorias y normalmente desaparecen durante la continuación del tratamiento.
Población pediátrica: Se ha investigado las propiedades farmacocinéticas de TRESIBA® en niños y adolescentes menores de 18 años. Se ha demostrado la seguridad y eficacia en un estudio a largo plazo en niños de 1 a 18 años de edad. La frecuencia, tipo y gravedad de las reacciones adversas en la población pediátrica no muestran diferencias con respecto a la experiencia en la población diabética general.
Otras poblaciones especiales: Con base en los resultados de los estudios clínicos, la frecuencia, tipo y gravedad de las reacciones adversas observadas en los pacientes de edad avanzada y en los pacientes con insuficiencia renal o hepática no muestran diferencia alguna con la población general, en la que se tiene una mayor experiencia.
INTERACCIONES CON OTROS MEDICAMENTOS Y OTRAS FORMAS DE INTERACCIÓN: Se sabe que algunos medicamentos interaccionan con el metabolismo de la glucosa.
Las siguientes sustancias pueden reducir la necesidad de insulina: Antidiabéticos orales, agonistas del receptor de GLP-1, inhibidores de la monoamino oxidasa (IMAO), betabloqueantes, inhibidores de la enzima convertidora de angiotensina (ECA), salicilatos, esteroides anabólicos y sulfonamidas.
Las siguientes sustancias pueden aumentar la necesidad de insulina: Anticonceptivos orales, tiazidas, glucocorticoides, hormonas tiroideas, simpaticomiméticos, hormona de crecimiento y danazol.
Los betabloqueantes pueden enmascarar los síntomas de hipoglucemia.
El octreotide y lanreotide pueden aumentar o reducir la necesidad de insulina.
El alcohol podría intensificar o reducir el efecto hipoglucemiante de la insulina.
POSOLOGÍA Y MODO DE ADMINISTRACIÓN:
Posología: TRESIBA® es una insulina basal para administración subcutánea una vez al día, en cualquier momento del día, preferiblemente a la misma hora cada día.
La potencia de los análogos de la insulina, incluida la insulina degludec, se expresa en unidades (U). Una (1) unidad (U) de insulina degludec corresponde a 1 unidad internacional (UI) de insulina humana, 1 unidad de insulina glargina o 1 unidad de insulina Detemir.
En pacientes con diabetes mellitus tipo 2, TRESIBA® puede administrarse sola o en cualquier combinación con antidiabéticos orales, agonistas del receptor del GLP-1 y bolo de insulina.
En pacientes con diabetes mellitus tipo 1, TRESIBA® debe combinarse con insulina de acción corta/rápida para cubrir las necesidades de insulina durante las comidas.
TRESIBA® debe administrarse de acuerdo con las necesidades individuales de cada paciente. Se recomienda optimizar el control glucémico a través de un ajuste de dosis basado en el nivel de glucosa plasmática en ayunas.
Como ocurre con todas las insulinas, podría ser necesario ajustar la dosis si el paciente aumenta su actividad física, cambia su dieta habitual o sufre una enfermedad concomitante.
FlexTouch®: TRESIBA® 100 unidades/ mL y TRESIBA® 200 unidades/ mL:
TRESIBA® está disponible en dos concentraciones; en ambas, la dosis necesaria se selecciona en unidades. Sin embargo, los incrementos de dosis varían entre las dos concentraciones de TRESIBA®.
• Con TRESIBA® 100 unidades/ mL, se puede administrar una dosis de 1-80 unidades por inyección, en incrementos de 1 unidad.
• Con TRESIBA® 200 unidades/ mL, se puede administrar una dosis de 2-160 unidades por inyección, en incrementos de 2 unidades. La dosis se proporciona en la mitad del volumen de las insulinas basales de 100 unidades/mL.
El contador de dosis muestra el número de unidades, independientemente de la concentración, y no deben hacerse conversiones de dosis cuando se cambia a un paciente a una nueva concentración.
Flexibilidad en el horario de administración: Cuando no es posible la administración a la misma hora del día, TRESIBA® ofrece flexibilidad respecto al horario de administración de la insulina. Se debe asegurar que transcurran un mínimo de 8 horas entre las inyecciones.
Para los pacientes que olvidan administrarse una dosis es aconsejable que, cuando se percaten de ello, se la administren y reanuden a continuación su esquema de dosificación habitual de una vez al día.
Inicio
Pacientes con diabetes mellitus tipo 2: La dosis inicial diaria recomendada es de 10 unidades, seguida de ajustes individuales en la dosis.
Pacientes con diabetes mellitus tipo 1: TRESIBA® debe administrarse una vez al día en combinación con una insulina de acción rápida y requiere de posteriores ajustes individuales en la dosis.
Cambio desde otras insulinas: Se recomienda un estricto control glucémico durante el cambio y en las primeras semanas después de este. Podría ser necesario ajustar la dosis y el horario de administración de las insulinas de acción rápida o de acción corta administradas de forma simultánea, o del tratamiento concomitante con otros antidiabéticos.
Pacientes con diabetes mellitus tipo 2: En pacientes con diabetes mellitus tipo 2 que reciben tratamiento con insulina basal, bolo-basal, premezclas o mezclada por el paciente, el cambio de insulina basal a TRESIBA® puede realizarse unidad a unidad con base en la dosis previa de insulina basal y ajustando posteriormente la dosis de forma individual.
Pacientes con diabetes mellitus tipo 1: En la mayoría de los pacientes con diabetes mellitus tipo 1, el cambio de insulina basal a TRESIBA® puede realizarse unidad a unidad con base en la dosis previa de insulina basal y ajustando posteriormente la dosis de forma individual. En los pacientes con diabetes mellitus tipo 1 que cambian de insulina basal dos veces al día o que tienen una HbA1c < 8,0% al momento del cambio, la dosis de TRESIBA® debe determinarse de forma individual. Después de un ajuste individual, debe considerarse una reducción de la dosis, en función de la respuesta glucémica.
Uso de TRESIBA® en combinación con agonistas del receptor del GLP-1 en pacientes con diabetes mellitus tipo 2: Cuando se agrega TRESIBA® a agonistas del receptor del GLP-1, la dosis inicial diaria recomendada es de 10 unidades, seguida de ajustes individuales en la dosis.
Cuando se agregan agonistas del receptor de GLP-1 a TRESIBA®, se recomienda reducir la dosis de TRESIBA® un 20% para minimizar el riesgo de hipoglucemia. Posteriormente, la dosis se debe ajustar individualmente.
Poblaciones especiales
Pacientes de edad avanzada (≥ 65 años): TRESIBA® puede utilizarse en pacientes de edad avanzada. Es necesario intensificar el control glucémico y debe ajustarse individualmente la dosis de insulina.
Insuficiencia renal y hepática: TRESIBA® puede utilizarse en pacientes con insuficiencia renal y hepática. Es necesario intensificar el control glucémico y debe ajustarse individualmente la dosis de insulina.
Población pediátrica: TRESIBA® puede utilizarse en adolescentes y niños a partir de 1 año de edad. Al cambiar de otra insulina basal a TRESIBA®, es necesario considerar una reducción de la dosis de insulina basal y bolo de insulina, de forma individual, para minimizar el riesgo de hipoglucemia.
Método de administración:
• TRESIBA® sólo debe administrarse por vía subcutánea.
• TRESIBA® no debe administrarse por vía intravenosa, ya que puede provocar una hipoglucemia grave.
• TRESIBA® no debe administrarse por vía intramuscular, ya que puede cambiar la absorción.
• TRESIBA® no debe utilizarse en bombas de perfusión de insulina.
• TRESIBA® se administra por vía subcutánea mediante inyección en el muslo, zona superior del brazo o pared abdominal. Siempre debe rotarse el punto de inyección dentro de la misma zona con el fin de reducir el riesgo de lipodistrofia.
FlexTouch®: TRESIBA® viene en una pluma pre-llenada (FlexTouch®) diseñada para utilizarse con las agujas NovoFine® o NovoTwist®.
FlexTouch® 100 unidades/ mL: TRESIBA® FlexTouch® 100 unidades/ mL administra 1–80 unidades en incrementos de 1 unidad.
VÍA DE ADMINISTRACIÓN: TRESIBA® sólo debe administrarse por vía subcutánea.
SOBREDOSIS: No es posible definir una sobredosificación específica para la insulina; sin embargo, puede desarrollarse hipoglucemia en etapas secuenciales si el paciente recibe una dosis de insulina superior a sus necesidades:
• Los episodios hipoglucémicos leves pueden ser tratados mediante la administración oral de glucosa u otros productos azucarados. Por consiguiente, se recomienda que los pacientes diabéticos lleven siempre consigo productos con glucosa.
• Los episodios hipoglucémicos graves en los que el paciente no puede autotratarse pueden ser tratados con inyección intramuscular o subcutánea de glucagón (0.5 a 1 mg), administrada por una persona entrenada, o bien con glucosa por vía intravenosa administrada por un profesional sanitario. La glucosa debe administrarse por vía intravenosa si el paciente no responde al glucagón en 10-15 minutos. A fin de prevenir una recaída, se recomienda la administración de carbohidratos orales al paciente una vez que este recupere el conocimiento.
PRESENTACIÓN: Estuche con 1 pluma pre-llenada de 3 mL, estuche con 5 plumas pre-llenadas de 3 ml y estuche con 3 plumas pre-llenadas de 3 ml.
Nombre del producto (comercial y genérico): TRESIBA® FlexTouch®, Insulina Degludec.
Nombre del fabricante y país: NOVO NORDISK A/S, Dinamarca.
Titular de la autorización: NOVO NORDISK A/S, Dinamarca.
No todas las presentaciones mencionadas están disponibles en todos los países.
Última revisión local: Agosto 2019 basada en el SmPC Octubre 2017.
Pueden existir diferencias en cuanto a las indicaciones aprobadas para cada país. Siempre refiérase a la información prescriptiva completa local a disposición en el departamento médico de NOVO NORDISK.
NOVO NORDISK
® Marca registrada
CONDICIONES DE ALMACENAMIENTO:
FlexTouch®:
Antes del primer uso: Conservar en refrigeración (entre 2 °C y 8 °C). No guardar cerca del congelador.
No congelar. Conservar la pluma con la tapa puesta para protegerla de la luz.
FlexTouch®:
Después de abrirlo por primera vez o si se lleva como repuesto: No conservar a temperatura superior a 30 °C. Puede conservarse en refrigeración (entre 2 °C y 8 °C). Conservar la pluma con la tapa puesta para protegerla de la luz.
Indicaciones terapéuticas: Tratamiento de la diabetes mellitus en adultos, adolescentes y niños a partir de 1 año de edad.