
ATACAND PLUS 32/12.5 MG Y 32/25 MG
CANDESARTÁN, HIDROCLOROTIAZIDA
Tabletas
1 Caja,10 y 30 Tabletas,
Caja , 14 Tabletas
Caja , 28 Tabletas
Para visualizar el contenido completo de la IPPA (información para prescribir amplia), deberá iniciar sesión.
COMPOSICIÓN: Un COMPRIMIDO ATACAND PLUS® de 32 mg/12.5 mg contiene 32 mg de candesartán cilexetilo y 12.5 mg de hidroclorotiazida. Cada COMPRIMIDO ATACAND PLUS® de 32 mg/12.5 mg contiene 148.5 mg de lactosa monohidratada.
Un COMPRIMIDO ATACAND PLUS® de 32 mg/25 mg contiene 32 mg de candesartán cilexetilo y 25 mg de hidroclorotiazida. Cada COMPRIMIDO ATACAND PLUS® de 32 mg/25 mg contiene 136 mg de lactosa monohidratada.
LISTA DE EXCIPIENTES: Carmelosa cálcica, hidroxipropilcelulosa, óxido de hierro rojo E 172 (comprimidos ATACAND PLUS® de 32 mg/25 mg), óxido de hierro amarillo E 172, lactosa monohidratada, estearato de magnesio, almidón de maíz, macrogol.
INDICACIONES TERAPÉUTICAS: Hipertensión idiopática en pacientes que no han conseguido un control óptimo de la presión arterial con una monoterapia con el candesartán cilexetilo o la hidroclorotiazida.
FORMA FARMACÉUTICA: Comprimidos.
Los comprimidos ATACAND PLUS® de 32 mg/12.5 mg son ovalados, biconvexos, de color amarillo, y llevan una ranura y la marca 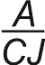 grabada en una cara, y una línea divisoria sensible a la presión en la otra cara.
grabada en una cara, y una línea divisoria sensible a la presión en la otra cara.
Los comprimidos ATACAND PLUS® de 32 mg/25 mg son ovalados, biconvexos, de color rosa, y llevan una ranura y la marca 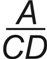 grabada en una cara, y una línea divisoria sensible a la presión en la otra cara.
grabada en una cara, y una línea divisoria sensible a la presión en la otra cara.
Los comprimidos pueden dividirse en dos partes iguales.
PROPIEDADES FARMACOCINÉTICAS: La coadministración del candesartán cilexetilo y de la hidroclorotiazida no tiene un efecto de importancia clínica en la farmacocinética de cada uno de los dos fármacos.
Absorción y distribución
Candesartán cilexetilo: Después de la administración oral, el candesartán cilexetilo se convierte en el principio activo, candesartán. Después de la administración de una solución oral de candesartán cilexetilo, la biodisponibilidad absoluta del candesartán es de aproximadamente un 40%. La biodisponibilidad relativa de una formulación de candesartán cilexetilo en comprimidos es de alrededor del 34% con respecto a la misma solución oral y muestra muy poca variabilidad. La concentración sérica máxima media (Cmáx) se alcanza de 3 a 4 horas después de la ingestión del comprimido. Las concentraciones séricas de candesartán aumentan de manera lineal en función de la dosis dentro del intervalo terapéutico. No se han observado diferencias relacionadas con el sexo en la farmacocinética del candesartán. La ingestión de alimentos no afecta de manera significativa el área bajo la curva de las concentraciones séricas en función del tiempo (ABC) del candesartán.
El candesartán se une considerablemente a las proteínas plasmáticas (más de un 99%) y su volumen de distribución aparente es de 0.1 l/kg.
Hidroclorotiazida: La hidroclorotiazida se absorbe rápidamente en el aparato digestivo, con una biodisponibilidad absoluta de alrededor del 70%. La ingestión concomitante de alimentos aumenta la absorción aproximadamente un 15%. La biodisponibilidad puede disminuir en los pacientes con insuficiencia cardiaca y edema pronunciado.
La unión de la hidroclorotiazida a las proteínas plasmáticas es de alrededor del 60% y su volumen aparente de distribución de aproximadamente 0.8 l/kg.
Metabolismo y eliminación
Candesartán cilexetilo: El candesartán se elimina principalmente en forma intacta en la orina y la bilis, y solo en un menor grado por metabolismo hepático (CYP2C9). Los estudios existentes sobre interacciones no revelan efecto alguno en las formas CYP2C9 y CYP3A4. En vista de los resultados in vitro, no se prevén interacciones in vivo con medicamentos cuyo metabolismo depende de las formas CYP1A2, CYP2A6, CYP2C9, CYP2C19, CYP2D6, CYP2E1 o CYP3A4 del citocromo P450. La vida media terminal (t½) del candesartán es de aproximadamente 9 horas. No se observa acumulación alguna después de la administración de dosis múltiples. La vida media terminal del candesartán prácticamente no cambia (aproximadamente 9 horas) después de la coadministración del candesartán cilexetilo con la hidroclorotiazida. Con respecto a la monoterapia, no se produce una acumulación adicional del candesartán después de la administración de dosis repetidas de la asociación farmacéutica.
La depuración plasmática total del candesartán es de aproximadamente 0.37 ml/min/kg y su depuración renal de aproximadamente 0.19 ml/min/kg. La eliminación renal del candesartán se realiza tanto por filtración glomerular como por secreción tubular activa. Tras una dosis oral de candesartán cilexetilo marcado con C14, alrededor del 26% de la dosis se excreta en forma de candesartán y el 7% en forma de un metabolito inactivo en la orina, mientras que el 56% de la dosis se recupera en forma de candesartán y el 10% en forma del metabolito inactivo en las heces.
Hidroclorotiazida: La hidroclorotiazida no se metaboliza y se excreta casi por completo en forma del medicamento intacto por filtración glomerular y secreción tubular activa. La vida media terminal de la hidroclorotiazida es de aproximadamente 8 horas. Alrededor del 70% de una dosis oral se elimina en la orina en 48 horas. La vida media de la hidroclorotiazida no cambia (aproximadamente 8 horas) tras la coadministración con el candesartán cilexetilo. Con respecto a la monoterapia, no se observa una acumulación adicional de la hidroclorotiazida después de la administración de dosis repetidas de la asociación farmacéutica.
Farmacocinética en grupos especiales de pacientes
Candesartán cilexetilo: En las personas de edad avanzada (mayores de 65 años), la Cmáx y el ABC del candesartán aumentan aproximadamente un 50% y un 80%, respectivamente, con respecto a sujetos jóvenes. Sin embargo, la respuesta de la presión arterial y la incidencia de reacciones adversas son similares entre sujetos jóvenes y de edad avanzada después de la administración de una dosis dada de ATACAND PLUS® (véase Posología y forma de administración).
En los pacientes con insuficiencia renal leve a moderada, durante la administración repetida se observaron aumentos de aproximadamente el 50% y el 70% de la Cmáx y el ABC del candesartán, respectivamente, mientras que la vida media terminal no cambió con respecto a pacientes con una función renal normal. Las variaciones correspondientes en pacientes con insuficiencia renal grave fueron de alrededor del 50% y el 110%, respectivamente. La vida media terminal del candesartán casi se duplicó en los pacientes con insuficiencia renal grave. En los pacientes sometidos a hemodiálisis, la farmacocinética fue similar a la observada en pacientes con insuficiencia renal grave.
En los pacientes con insuficiencia hepática leve a moderada se observó un aumento del 23% del ABC del candesartán.
Hidroclorotiazida: La vida media terminal de la hidroclorotiazida se prolonga en los pacientes con insuficiencia renal.
PROPIEDADES FARMACODINÁMICAS
Grupo farmacoterapéutico: Antagonistas de la angiotensina II + diuréticos.
Código ATC: C09D A06.
La angiotensina II es la principal hormona vasoactiva del sistema de renina-angiotensina-aldosterona, que interviene en la fisiopatología de la hipertensión y de otros trastornos cardiovasculares. También desempeña un papel en la patogenia de la hipertrofia y de los daños a los órganos afectados. Los principales efectos fisiológicos de la angiotensina II, tales como vasoconstricción, estimulación de la aldosterona, regulación de la homeostasis hidrosalina y estimulación del crecimiento celular, son mediados por el receptor de tipo 1 (AT1).
El candesartán cilexetilo es un promedicamento que se convierte rápidamente en el medicamento activo (candesartán) mediante hidrólisis del éster durante su absorción en el aparato digestivo. El candesartán es un antagonista de los receptores de angiotensina II que ejerce una acción selectiva en los receptores AT1, uniéndose estrechamente al receptor y disociándose lentamente del mismo. El candesartán carece de actividad agonista.
El candesartán no tiene efecto alguno en la ECA u otros sistemas enzimáticos que se asocian generalmente con el uso de inhibidores de la ECA. Como los antagonistas de los receptores de angiotensina II carecen de efectos en la degradación de cininas y en el metabolismo de otras sustancias como la sustancia P, es improbable que provoquen tos. En estudios clínicos controlados que compararon el candesartán cilexetilo con inhibidores de la ECA, la incidencia de tos fue menor en los pacientes tratados con el candesartán cilexetilo. El candesartán no bloquea ni se une a otros receptores hormonales o canales iónicos que desempeñan una función importante en la regulación cardiovascular. El antagonismo de los receptores AT1 provoca aumentos de las concentraciones plasmáticas de renina y de las concentraciones de angiotensina I y angiotensina II, así como una disminución de la concentración plasmática de aldosterona en función de la dosis.
Los efectos de 8 a 16 mg de candesartán cilexetilo una vez al día (dosis media: 12 mg) en la morbilidad y la mortalidad cardiovasculares se evaluaron en un estudio clínico aleatorizado en el que participaron 4937 pacientes de edad avanzada (de 70 a 89 años; 21% mayores de 80 años) con hipertensión leve a moderada, y cuya observación duró en promedio 3.7 años (Study on Cognition and Prognosis in the Elderly-Estudio sobre la función cognoscitiva y el pronóstico en los ancianos). Los pacientes recibieron el candesartán o un placebo, y se podía añadir otro tratamiento antihipertensivo si era necesario. La presión arterial disminuyó de 166/90 a 145/80 mmHg en el grupo del candesartán y de 167/90 a 149/82 mmHg en el grupo de control. No se observó una diferencia estadísticamente significativa en la variable principal, es decir, la frecuencia de acontecimientos cardiovasculares importantes (mortalidad cardiovascular, accidente vascular cerebral no mortal e infarto de miocardio no mortal). Ocurrieron 26.7 acontecimientos por 1000 años-paciente en el grupo del candesartán, frente a 30.0 acontecimientos por 1000 años-paciente en el grupo de control (riesgo relativo de 0.89, IC del 95%: 0.75-1.06, p=0.19).
La hidroclorotiazida inhibe la reabsorción activa de sodio, principalmente en los túbulos renales distales, y favorece la excreción de sodio, cloruro y agua. La excreción renal de potasio y magnesio aumenta en función de la dosis, mientras que se incrementa la reabsorción de calcio. La hidroclorotiazida disminuye el volumen de plasma y la cantidad de líquido extracelular, así como el gasto cardiaco y la presión arterial. Durante el tratamiento a largo plazo, la disminución de la resistencia periférica contribuye a reducir la presión arterial.
Los estudios clínicos a gran escala demostraron que el tratamiento a largo plazo con la hidroclorotiazida reduce el riesgo de morbimortalidad cardiovascular.
El candesartán y la hidroclorotiazida ejercen efectos antihipertensivos aditivos.
En los pacientes hipertensos, ATACAND PLUS® provoca una disminución prolongada de la presión arterial en función de la dosis, sin causar un aumento reflejo de la frecuencia cardiaca. No hay indicios de hipotensión grave o exagerada después de la primera dosis ni de un efecto de rebote después de la suspensión del tratamiento. Tras la administración de una sola dosis de ATACAND PLUS®, el efecto antihipertensivo empieza generalmente a manifestarse después de 2 horas. Al continuar el tratamiento, la mayor parte de la reducción de la presión arterial se consigue en un plazo de cuatro semanas y se mantiene durante el tratamiento a largo plazo. ATACAND PLUS® una vez al día produce una reducción eficaz y constante de la presión arterial durante las 24 horas, con poca diferencia entre los efectos máximos y mínimos durante el intervalo de administración. En un estudio aleatorizado con un diseño doble ciego, la disminución de la presión arterial y el número de pacientes con una presión controlada fueron significativamente mayores con ATACAND PLUS® una vez al día que con una asociación aprobada de dosis fijas similar que contenía un antagonista de los receptores de angiotensina II e hidroclorotiazida. En estudios aleatorizados con un diseño doble ciego, la incidencia de reacciones adversas, y en particular de tos, fue menor durante el tratamiento con la asociación de candesartán cilexetilo/hidroclorotiazida que durante el tratamiento con asociaciones de inhibidores de la ECA e hidroclorotiazida.
En dos estudios clínicos (aleatorizados, con un diseño doble ciego, controlados con placebo y con grupos paralelos) en los que participaron 275 y 1524 pacientes aleatorizados, respectivamente, las asociaciones de 32 mg/12.5 mg y 32 mg/25 mg de candesartán cilexetilo/hidroclorotiazida produjeron reducciones de la presión arterial de 21/14 mmHg (con la dosis más alta) y mostraron una eficacia significativamente mayor que cada uno de los dos componentes administrados individualmente.
En un estudio aleatorizado, con un diseño doble ciego y con grupos paralelos en el que participaron 1975 pacientes aleatorizados que no habían conseguido un control óptimo con 32 mg de candesartán cilexetilo una vez al día, la adición de 12.5 mg o 25 mg de hidroclorotiazida produjo reducciones adicionales de la presión arterial. La asociación de 32 mg/25 mg de candesartán cilexetilo/hidroclorotiazida fue significativamente más eficaz que la de 32 mg/12.5 mg, y las medias de las reducciones totales de la presión arterial fueron de 16/10 mmHg y 13/9 mmHg, respectivamente.
La asociación de candesartán cilexetilo/hidroclorotiazida muestra una eficacia similar en todos los pacientes, independientemente de su edad y sexo.
Por el momento se carece de información sobre el uso de la asociación de candesartán cilexetilo/hidroclorotiazida en pacientes con enfermedad renal/nefropatía, disfunción ventricular izquierda/insuficiencia cardiaca congestiva, y después de un infarto de miocardio.
CONTRAINDICACIONES: Hipersensibilidad a los principios activos de ATACAND PLUS®, a cualquiera de los excipientes o a los derivados de la sulfonamida (la hidroclorotiazida es un derivado de la sulfonamida).
Embarazo y lactancia.
Insuficiencia renal grave (depuración de creatinina <30 ml/min/1.73 m2 de superficie corporal).
Insuficiencia hepática grave y/o colestasis.
Hipopotasemia e hipercalcemia refractarias.
Gota.
EMBARAZO Y LACTANCIA:
Uso durante el embarazo: El uso de ATACAND PLUS® está contraindicado durante el embarazo (véase Contraindicaciones). Las pacientes tratadas con ATACAND PLUS® deben ser conscientes de esto antes de contemplar la posibilidad de un embarazo, de manera que puedan comentar con su médico las distintas opciones apropiadas. Si se detecta un embarazo, el tratamiento con ATACAND PLUS® debe suspenderse inmediatamente e iniciar un tratamiento alternativo, si procede.
Al utilizarse durante el embarazo, los medicamentos que actúan directamente en el sistema de renina-angiotensina pueden provocar lesiones fetales y neonatales e incluso la muerte. Se sabe que la exposición a antagonistas de los receptores de angiotensina II provoca fetotoxicidad en el ser humano (disfunción renal, oligohidramnios, retraso de la osificación craneana) así como toxicidad neonatal (insuficiencia renal, hipotensión, hiperpotasemia).
La experiencia con la hidroclorotiazida durante el embarazo es limitada, sobre todo durante el primer trimestre. Los estudios en animales son insuficientes. La hidroclorotiazida atraviesa la barrera placentaria. Dado su modo de acción farmacológico, el uso de la hidroclorotiazida durante el embarazo puede comprometer la perfusión fetal y placentaria provocando efectos en el feto y en el recién nacido tales como ictericia, trastornos del equilibrio electrolítico y trombocitopenia.
Uso durante la lactancia: El candesartán se excreta en la leche de la rata, pero no se sabe si se excreta en la leche materna humana. Por su parte, la hidroclorotiazida se detecta en la leche materna. Debido a los posibles efectos adversos en el lactante, ATACAND PLUS® no debe administrarse durante la lactancia (véase Contraindicaciones).
EFECTOS SOBRE LA CAPACIDAD PARA CONDUCIR Y UTILIZAR MÁQUINAS: Si bien no se ha estudiado el efecto de ATACAND PLUS® en la capacidad para conducir y utilizar máquinas, en vista de sus propiedades farmacodinámicas es improbable que afecte dicha capacidad. Durante el tratamiento de la hipertensión, debe tenerse en mente que al conducir vehículos u operar máquinas pueden presentarse ocasionalmente mareos o cansancio.
REACCIONES ADVERSAS: En los estudios clínicos controlados con la asociación de candesartán cilexetilo/hidroclorotiazida, las reacciones adversas fueron leves y transitorias. La frecuencia de las suspensiones del tratamiento debido a reacciones adversas fue similar con la asociación de candesartán cilexetilo/hidroclorotiazida (2.3%-3.3%) y con el placebo (2.7%-4.3%).
El análisis de los datos de estudios clínicos sobre la asociación de candesartán cilexetilo/hidroclorotiazida se limitó a las reacciones adversas que se habían notificado anteriormente con el candesartán cilexetilo y/o con la hidroclorotiazida.
Se aplicó la siguiente terminología para clasificar las reacciones adversas por frecuencia
Muy frecuentes (=1/10)
Frecuentes (=1/100 y <1/10)
Poco frecuentes (=1/1000 y <1/100)
Raras (=1/10000 y <1/1000)
Muy raras (<1/10000)
Frecuencia desconocida (imposible de estimar a partir de los datos disponibles).
Durante la farmacovigilancia se han notificado las siguientes reacciones adversas con el candesartán cilexetilo:
|
Sistema/Órgano |
Frecuencia |
Reacción adversa |
|
Trastornos de la sangre y del sistema linfático |
Muy raros |
Leucopenia, neutropenia y agranulocitosis |
|
Trastornos del sistema nervioso |
Muy raros |
Mareo, cefalea |
|
Trastornos respiratorios, torácicos y mediastínicos |
Muy raros |
Tos |
|
Trastornos gastrointestinales |
Muy raros |
Náuseas |
|
Trastornos renales y urinarios |
Muy raros |
Disfunción renal, que puede incluir insuficiencia renal en pacientes predispuestos |
|
Trastornos de la piel y del tejido subcutáneo |
Muy raros |
Edema angioneurótico, exantema, urticaria, prurito |
|
Trastornos osteomusculares, del tejido conjuntivo y óseos |
Muy raros |
Lumbalgia, artralgia, mialgia |
|
Trastornos hepatobiliares |
Muy raros |
Elevación de las enzimas hepáticas, disfunción hepática o hepatitis |
|
Trastornos del metabolismo y la nutrición |
Muy raros |
Hiperpotasemia, hiponatremia |
Se han notificado las siguientes reacciones adversas con la hidroclorotiazida en monoterapia, generalmente con dosis de 25 mg o más:
|
Sistema/Órgano |
Frecuencia |
Reacción adversa |
|
Exploraciones complementarias |
Frecuentes |
Elevaciones del colesterol y de los triglicéridos |
|
Raras |
Elevaciones del nitrógeno ureico en sangre y de la creatininemia |
|
|
Trastornos cardiacos |
Raros |
Arritmias cardiacas |
|
Trastornos de la sangre y del sistema linfático |
Raros |
Leucopenia, neutropenia/agranulocitosis, trombocitopenia, anemia aplásica, depresión medular, anemia hemolítica |
|
Trastornos del sistema nervioso |
Frecuentes |
Aturdimiento, vértigo |
|
Raros |
Parestesia |
|
|
Trastornos oculares |
Raros |
Vista borrosa transitoria |
|
Frecuencia desconocida |
Miopía aguda, glaucoma de ángulo cerrado agudo |
|
|
Trastornos respiratorios, torácicos y mediastínicos |
Raros |
Disnea (que puede acompañarse de neumonitis y edema pulmonar) |
|
Trastornos gastrointestinales |
Poco frecuentes |
Anorexia, pérdida del apetito, irritación gástrica, diarrea, estreñimiento |
|
Raros |
Pancreatitis |
|
|
Trastornos renales y urinarios |
Frecuentes |
Glucosuria |
|
Raros |
Disfunción renal y nefritis intersticial |
|
|
Trastornos de la piel y del tejido subcutáneo |
Poco frecuentes |
Exantema, urticaria, reacciones de fotosensibilidad |
|
Raros |
Necrólisis epidérmica tóxica, reacciones de tipo lupus eritematoso cutáneo, reactivación del lupus eritematoso cutáneo |
|
|
Trastornos osteomusculares, del tejido conjuntivo y óseos |
Raros |
Espasmo muscular |
|
Trastornos del metabolismo y la nutrición |
Frecuentes |
Hiperglucemia, hiperuricemia, desequilibrio electrolítico (que puede incluir hiponatremia e hipopotasemia) |
|
Trastornos vasculares |
Poco frecuentes |
Hipotensión ortostática |
|
Raros |
Angitis necrosante (vasculitis, vasculitis cutánea) |
|
|
Trastornos generales y reacciones en el lugar de la administración |
Frecuentes |
Debilidad |
|
Raros |
Fiebre |
|
|
Trastornos del sistema inmunitario |
Raros |
Reacciones anafilácticas |
|
Trastornos hepatobiliares |
Raros |
Ictericia (ictericia colestásica intrahepática) |
|
Trastornos psiquiátricos |
Raros |
Trastornos del sueño, depresión, agitación |
Hallazgos de laboratorio: Se han observado elevaciones de creatinina, urea, potasio, ácido úrico, glucosa y ALAT (TGP), y disminuciones del sodio. Se han observado asimismo pequeñas disminuciones de la hemoglobina y pequeñas elevaciones de ASAT (TGO) en pacientes aislados.
INTERACCIÓN CON OTROS MEDICAMENTOS Y OTRAS FORMAS DE INTERACCIÓN: Los compuestos que se han investigado en estudios clínicos de farmacocinética con el candesartán cilexetilo son la hidroclorotiazida, la warfarina, la digoxina, anticonceptivos orales (etinilestradiol/levonorgestrel), la glibenclamida y el nifedipino. No se han identificado interacciones farmacocinéticas de importancia clínica en estos estudios.
La ingestión de alimentos no afecta la biodisponibilidad del candesartán.
La administración de otros antihipertensivos puede potenciar el efecto antihipertensivo de ATACAND PLUS®.
Se prevé que el efecto de agotamiento del potasio de la hidroclorotiazida será potenciado por otros medicamentos que provocan pérdida de potasio e hipopotasemia (por ejemplo, otros diuréticos caliuréticos, laxantes, anfotericina, carbenoxolona, penicilina G sódica, derivados del ácido salicílico).
Según la experiencia adquirida con otros medicamentos que afectan el sistema de renina-angiotensina-aldosterona, pueden ocurrir elevaciones del potasio sérico con la coadministración de ATACAND PLUS® y diuréticos ahorradores de potasio, suplementos de potasio, sustitutos de sal u otros medicamentos que pueden aumentar las concentraciones séricas de potasio (por ejemplo, heparina sódica).
La hipopotasemia y la hipomagnesemia provocadas por los diuréticos predisponen a los efectos cardiotóxicos potenciales de los glucósidos digitálicos y antiarrítmicos. Cuando se administra ATACAND PLUS® junto con tales medicamentos, se recomienda vigilar periódicamente el potasio sérico.
Durante la coadministración de litio con inhibidores de la ECA o la hidroclorotiazida, se han observado aumentos reversibles de las concentraciones séricas de litio, así como toxicidad. Podría presentarse un efecto similar con antagonistas de los receptores de angiotensina II (ARAII), por lo que se recomienda vigilar cuidadosamente las concentraciones séricas de litio durante el tratamiento concomitante.
Si se coadministran antagonistas de los receptores de angiotensina II con antiinflamatorios no esteroides (es decir, inhibidores selectivos de la COX-2, ácido acetilsalicílico [>3 g al día] y AINE no selectivos), puede producirse una atenuación del efecto antihipertensivo.
Como sucede con los inhibidores de la ECA, la coadministración de antagonistas de los receptores de angiotensina II y AINE puede aumentar el riesgo de deterioro de la función renal, que puede evolucionar a insuficiencia renal aguda, y elevar la concentración sérica de potasio, sobre todo en pacientes con disfunción renal preexistente. Esta asociación farmacéutica debe administrarse con precaución, sobre todo en los pacientes de edad avanzada. Los pacientes deben presentar una hidratación adecuada y debe considerarse la supervisión de la función renal después de iniciar el tratamiento concomitante y luego periódicamente.
Los AINE atenúan el efecto diurético, natriurético y antihipertensivo de la hidroclorotiazida.
El colestipol y la colestiramina reducen la absorción de la hidroclorotiazida.
La hidroclorotiazida puede potenciar el efecto de los relajantes del músculo esquelético no despolarizantes (por ejemplo, el de la tubocurarina).
Los diuréticos tiazídicos pueden aumentar las concentraciones séricas de calcio debido a una disminución de su excreción. Al prescribir suplementos de calcio o vitamina D, deben vigilarse las concentraciones séricas de calcio y ajustarse la dosis en consecuencia.
Las tiazidas pueden potenciar el efecto hiperglucemiante de los betabloqueadores y del diazóxido.
Los anticolinérgicos (por ejemplo, atropina y biperideno) pueden aumentar la biodisponibilidad de los diuréticos tiazídicos mediante una disminución de la motilidad gastrointestinal y de la velocidad de vaciado gástrico.
Las tiazidas pueden aumentar el riesgo de presentar efectos adversos provocados por la amantadina.
Las tiazidas pueden reducir la excreción renal de medicamentos citotóxicos (por ejemplo, ciclofosfamida, metotrexato) y potenciar sus efectos mielosupresores.
El riesgo de hipopotasemia puede aumentar durante la coadministración de esteroides o corticotropina (ACTH).
La ingestión simultánea de alcohol, barbitúricos o anestésicos puede agravar la hipotensión postural.
El tratamiento con un diurético tiazídico puede alterar la tolerancia a la glucosa. Puede ser necesario ajustar la dosis de los medicamentos antidiabéticos, incluida la insulina.
La hidroclorotiazida puede provocar una disminución de la respuesta arterial a las aminas presoras (como la adrenalina) pero no suficientemente como para descartar un efecto presor.
La hidroclorotiazida puede aumentar el riesgo de insuficiencia renal aguda, sobre todo con dosis elevadas de medios de contraste yodados.
No se conoce ninguna interacción de importancia clínica entre la hidroclorotiazida y los alimentos.
ADVERTENCIAS Y PRECAUCIONES ESPECIALES DE USO
Insuficiencia renal/trasplante renal: En este grupo de pacientes se prefieren los diuréticos de ASA a las tiazidas. Si se utiliza ATACAND PLUS® en pacientes con insuficiencia renal, se recomienda vigilar periódicamente las concentraciones de potasio, creatinina y ácido úrico.
Se carece de experiencia sobre la administración de ATACAND PLUS® en pacientes con un trasplante renal reciente.
Estenosis de la arteria renal: Otros medicamentos que afectan el sistema de renina-angiotensina-aldosterona, a saber los inhibidores de la enzima convertidora de la angiotensina (ECA), pueden elevar las concentraciones de urea en sangre y de creatinina en suero en los pacientes con estenosis bilateral de las arterias renales o con estenosis de la arteria que irriga el único riñón. Puede preverse un efecto similar con los antagonistas de los receptores de angiotensina II.
Depleción hidrosalina intravascular: En los pacientes que sufren de depleción salina y/o hidrosalina intravascular, puede presentarse hipotensión sintomática como la descrita con otros medicamentos que actúan en el sistema de renina-angiotensina-aldosterona. Por lo tanto, no se recomienda utilizar ATACAND PLUS® antes de haber corregido esta situación.
Anestesia y cirugía: En los pacientes tratados con antagonistas de la angiotensina II puede presentarse hipotensión durante la anestesia y la cirugía debido al bloqueo del sistema de renina-angiotensina. En casos muy raros, la hipotensión puede llegar a ser grave y requerir la administración de líquidos intravenosos y/o de vasopresores.
Insuficiencia hepática: En los pacientes con insuficiencia hepática o una afección hepática progresiva, las tiazidas deben emplearse con precaución ya que alteraciones incluso menores del equilibrio de líquidos y electrólitos pueden precipitar un coma hepático. Se carece de experiencia clínica sobre el uso de ATACAND PLUS® en pacientes con insuficiencia hepática.
Estenosis de las válvulas aórtica y mitral (miocardiopatía hipertrófica obstructiva): Al igual que con otros vasodilatadores, es preciso tomar precauciones especiales en los pacientes que padecen estenosis de las válvulas aórtica o mitral acompañada de alteraciones hemodinámicas importantes, o miocardiopatía hipertrófica obstructiva.
Hiperaldosteronismo primario: Generalmente, los pacientes con hiperaldosteronismo primario no responden a los antihipertensivos cuyo mecanismo de acción es la inhibición del sistema de renina-angiotensina-aldosterona. Por lo tanto, no se recomienda utilizar ATACAND PLUS® en estos pacientes.
Desequilibrio electrolítico: Como en cualquier paciente que recibe un tratamiento diurético, las concentraciones séricas de electrólitos deben determinarse periódicamente.
Las tiazidas (incluida la hidroclorotiazida) pueden provocar un desequilibrio de líquidos o electrólitos (hipercalcemia, hipopotasemia, hiponatremia, hipomagnesemia y alcalosis hipoclorémica).
Los diuréticos tiazídicos pueden reducir la excreción urinaria de calcio y provocar elevaciones ligeras e intermitentes de las concentraciones séricas de calcio.
La hipercalcemia pronunciada puede ser un signo de hiperparatiroidismo oculto. Antes de efectuar ensayos de la función paratiroidea debe suspenderse la administración de tiazidas.
La hidroclorotiazida aumenta la excreción urinaria de potasio en función de la dosis, lo cual puede conducir a hipopotasemia. Este efecto de la hidroclorotiazida parece ser menos evidente cuando se asocia con el candesartán cilexetilo. El riesgo de hipopotasemia puede aumentar en pacientes con cirrosis hepática, pacientes que presentan diuresis intensa, pacientes con una ingestión oral inadecuada de electrólitos y pacientes que reciben un tratamiento concomitante con corticoesteroides u corticotropina (ACTH).
Según la experiencia adquirida con otros medicamentos que afectan el sistema de renina-angiotensina-aldosterona, pueden ocurrir elevaciones del potasio sérico si se coadministra ATACAND PLUS® con diuréticos ahorradores de potasio, suplementos de potasio, sustitutos de sal u otros medicamentos que pueden de aumentar las concentraciones séricas de potasio (por ejemplo, heparina sódica).
Aunque no se ha confirmado con ATACAND PLUS®, el tratamiento con inhibidores de la enzima convertidora de la angiotensina o con antagonistas de los receptores de angiotensina II puede provocar hiperpotasemia, sobre todo en pacientes con insuficiencia cardiaca y/o renal.
Se ha demostrado que las tiazidas aumentan la excreción urinaria de magnesio, lo cual puede conducir a hipomagnesemia.
Efectos metabólicos y endocrinos: El tratamiento con un diurético tiazídico puede alterar la tolerancia a la glucosa, haciendo necesario un ajuste de la dosis de los medicamentos antidiabéticos, incluida la insulina. Durante el tratamiento con tiazidas puede manifestarse una diabetes hasta entonces latente. El tratamiento con diuréticos tiazídicos ha provocado elevaciones de las concentraciones de colesterol y triglicéridos, aunque con las dosis contenidas en ATACAND PLUS® solo se han observado efectos mínimos. Los diuréticos tiazídicos aumentan la concentración sérica de ácido úrico y pueden precipitar gota en pacientes predispuestos.
Pruebas antidopaje:La hidroclorotiazida puede dar lugar a resultados positivos en las pruebas antidopaje.
Generalidades: En pacientes cuyo tono vascular y función renal dependen principalmente de la actividad del sistema de renina-angiotensina-aldosterona (por ejemplo, pacientes con insuficiencia cardiaca congestiva grave o enfermedades renales subyacentes, entre ellas la estenosis de las arterias renales), el tratamiento con otros medicamentos que afectan este sistema ha provocado hipotensión aguda, azotemia, oliguria y, raramente, insuficiencia renal aguda. No puede descartarse la posibilidad de que ocurran efectos similares con los antagonistas de los receptores de angiotensina II. Al igual que con cualquier medicamento antihipertensivo, una disminución excesiva de la presión arterial en pacientes con cardiopatía isquémica o con enfermedad cerebrovascular aterosclerótica puede precipitar un infarto de miocardio o un accidente vascular cerebral.
Pueden observarse reacciones de hipersensibilidad a la hidroclorotiazida en pacientes con o sin antecedentes de alergia o asma bronquial, aunque son más probables en pacientes con tales antecedentes.
Se ha observado exacerbación o activación del lupus eritematoso sistémico con los diuréticos tiazídicos.
Este medicamento contiene lactosa como excipiente, por lo que no deben tomarlo los pacientes con problemas hereditarios raros de intolerancia a la galactosa, deficiencia de lactasa de los lapones o malabsorción de glucosa-galactosa.
PRECAUCIONES ESPECIALES DE CONSERVACIÓN: No conservar a más de 30 °C.
POSOLOGÍA Y FORMA DE ADMINISTRACIÓN
Uso por vía oral: ATACAND PLUS® debe tomarse una vez al día, con o sin alimentos.
Si el cuadro clínico lo justifica, puede considerarse un cambio directo de la monoterapia al tratamiento con ATACAND PLUS®. En los pacientes que estaban recibiendo una monoterapia con la hidroclorotiazida, se recomienda ajustar progresivamente la dosis de candesartán cilexetilo. ATACAND PLUS® 32 mg/
12.5 mg o 32 mg/25 mg puede administrarse a pacientes que no han conseguido un control óptimo de la presión arterial con 32 mg de candesartán cilexetilo o con dosis más bajas de ATACAND PLUS®.
En general, la mayor parte del efecto antihipertensivo se consigue en un plazo de 4 semanas después de iniciar el tratamiento.
Uso en personas de edad avanzada: No es necesario ajustar la dosis en pacientes de edad avanzada.
Uso en pacientes con insuficiencia renal: En este grupo de pacientes se prefieren los diuréticos de asa a las tiazidas. En los pacientes con insuficiencia renal cuya depuración de creatinina es ³30 ml/min/1.73 m2 de superficie corporal, se recomienda ajustar progresivamente la dosis de candesartán cilexetilo antes de empezar el tratamiento con ATACAND PLUS®.
ATACAND PLUS® no debe usarse en pacientes con insuficiencia renal grave (depuración de creatinina <30 ml/min/1.73 m2 de superficie corporal).
Uso en pacientes con insuficiencia hepática: En los pacientes con insuficiencia hepática leve a moderada se recomienda ajustar progresivamente la dosis de candesartán cilexetilo antes de empezar el tratamiento con ATACAND PLUS®.
ATACAND PLUS® no debe administrarse a pacientes con insuficiencia hepática grave y/o colestasis.
Uso en niños y adolescentes: No se han establecido la seguridad y la eficacia de ATACAND PLUS® en niños y adolescentes (menores de 18 años de edad).
SOBREDOSIS
Síntomas: Basándose en consideraciones farmacológicas, es probable que la principal manifestación de una sobredosis de candesartán cilexetilo consista en hipotensión sintomática y mareo. En casos individuales de sobredosis (de hasta 672 mg de candesartán cilexetilo), el paciente mostró una recuperación normal.
La principal manifestación de una sobredosis de hidroclorotiazida consiste en una pérdida aguda de líquidos y electrólitos. También pueden observarse síntomas tales como mareo, hipotensión, sed, taquicardia, arritmias ventriculares, sedación/alteración del estado de vigilia y calambres musculares.
Tratamiento: No se tiene información específica sobre el tratamiento de sobredosis de ATACAND PLUS®. No obstante, en caso de sobredosis se sugiere tomar las siguientes medidas.
Cuando esté indicado, debe considerarse la posibilidad de inducir el vómito o efectuar un lavado gástrico. En caso de hipotensión sintomática debe aplicarse un tratamiento sintomático y vigilarse las constantes vitales. El paciente debe colocarse en posición supina con las piernas elevadas. Si esto no basta, debe aumentarse el volumen de plasma mediante una infusión de solución fisiológica. Debe verificarse y, si es necesario, corregirse el equilibrio electrolítico y ácido en el suero. Si las medidas antes mencionadas no surten efectos suficientes, pueden administrarse medicamentos simpaticomiméticos.
El candesartán no puede eliminarse por hemodiálisis. No se sabe hasta qué grado se elimina la hidroclorotiazida por hemodiálisis.
PRESENTACIONES COMERCIALES: ATACAND PLUS® 32/12,5 mg, caja por 14 tabletas y caja por 28 tabletas (Reg. San. No. INVIMA 2010M-0010542).
Venta con fórmula médica. Mantener fuera del alcance de los niños.
Fecha de revisión del texto: Septiembre de 2011.
Fecha de preparación de la versión: Julio de 2012.
ATACAND PLUS® 32/12,5 mg y 32/25 mg
Clave 1-2012 (2).
Fuente CV.000-719-474.2.0. Traducción de: CV.000-495.776.5.0.
ATACAND PLUS® es una marca registrada del grupo AstraZeneca.
© AstraZeneca 2011.
AstraZeneca AB, Södertälje, Suecia
El candesartán cilexetilo se fabrica con licencia de Takeda Pharmaceutical Company Limited.
Mayor información Departamento Médico de
AstraZeneca Colombia, S. A. S.
Bogotá, D.C., Colombia
PLAZO DE CADUCIDAD: Véase la fecha de caducidad en la caja externa.
TAMAÑO DEL ENVASE: Véase el tamaño del envase en la caja externa.