
ENBREL 25 MG / ENBREL 50 MG
ETANERCEPT
Solución para inyección, jeringas prellenadas
Jeringa(s) prellenada(s) , Solución para inyección , 25 Miligramos
Para visualizar el contenido completo de la IPPA (información para prescribir amplia), deberá iniciar sesión.
COMPOSICIÓN Y CARACTERÍSTICAS FARMACÉUTICAS: Cada jeringa prellenada contiene 25 mg o 50 mg de etanercept (ingrediente activo). Cada autoinyector contiene 50 mg de etanercept.
Naturaleza y Contenido del Envase: Solución para inyección de Jeringa Prellenada.
Jeringa de vidrio claro (vidrio tipo I) con aguja de acero inoxidable, con tapa de caucho y émbolo plástico. La tapa de la aguja contiene caucho natural seco (látex) (ver sección Precauciones especiales).
Las cajas plegadizas contienen jeringas prellenadas de dosis única de ENBREL® (25 mg o 50 mg) y torundas de alcohol.
Solución para inyección en Autoinyector MYCLIC: El autoinyector contiene jeringa de vidrio claro (vidrio tipo I) con aguja de acero inoxidable calibre 27, con tapa de caucho y émbolo plástico. La tapa de la aguja del autoinyector contiene caucho natural seco (látex) (ver sección Precauciones especiales).
Las cajas plegadizas contienen autoinyector de dosis única de ENBREL® (50 mg) y torundas de alcohol.
cnicas de auto-inyección o en la aplicación de una inyección a un niño. No intente administrar una inyección hasta que usted esté seguro de que entendió cómo preparar y administrar la inyección.
Antes de su utilización, la solución de ENBREL® no debe ser mezclada con otro medicamento.
Paso 1. Preparación para una inyección
• Seleccione una superficie plana de trabajo, limpia y bien iluminada.
• Saque del refrigerador la caja que contiene las jeringas prellenadas de ENBREL® y colóquela en la superficie plana de trabajo. Saqué una jeringa prellenada y una torunda de alcohol y colóquelas en la superficie de trabajo. No agite la jeringa prellenada de ENBREL®. Devuelva al refrigerador (2° a 8° C) la caja que contiene las jeringas prellenadas sobrantes. Si usted tiene alguna duda acerca del almacenamiento, contacte a su médico, enfermera o farmacéutico para más instrucciones.
• Verifique la fecha de vencimiento en la jeringa prellenada. No utilice el producto, si éste se encuentra vencido y contacte al farmacéutico para mayor información.
• Espere 15 a 30 minutos para que la jeringa prellenada de ENBREL® alcance la temperatura ambiente. NO remueva la tapa que protege a la aguja mientras que la jeringa prellenada de ENBREL® alcanza la temperatura ambiente. Esperar hasta que la solución alcance la temperatura ambiente puede hacer más confortable la inyección. No caliente el ENBREL® por ningún medio diferente al que se menciona aquí (p. ej., no caliente el producto en un microondas ni en agua caliente).
• Reúna los elementos adicionales que necesitará para su inyección. Estos incluyen: la torunda de alcohol de la caja de ENBREL®, y un algodón o gasa.
• Lave sus manos con jabón y agua tibia.
• Inspeccione la solución en la jeringa prellenada. Ésta deberá ser clara o levemente opalescente, incolora o amarilla pálida, y puede contener partículas de proteína pequeñas blancas o casi transparentes. Esta apariencia es normal para ENBREL®. No utilice la solución si se observa decolorada, turbia o si están presentes partículas diferentes a las antes mencionadas. Si siente inquietud con relación a la apariencia de la solución contacte al farmacéutico para asistencia.
Paso 2. Elección del sitio de inyección
• Se recomiendan tres sitios de inyección para la administración de la jeringa prellenada de ENBREL®, en los que se incluyen: (1) En la parte anterior del muslo medio; (2) el abdomen, excepto en el área de 5 cm alrededor del ombligo; y (3) en el área posterior y superior de los brazos (ver diagrama 1).
Diagrama 1.
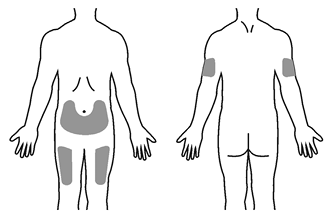
• Alterne los sitios de la inyección cada vez que aplique una nueva inyección. Deje un espacio de al menos 3 cm entre el nuevo sitio de inyección y el sitio anterior. No inyecte en áreas donde la piel este sensible, con hematoma, enrojecida o dura. Evite áreas con cicatrices o marcas de extensiones.
• Si usted o un niño tienen psoriasis, usted no debe tratar de inyectar directamente en capas levantadas de piel, o en piel gruesa, roja o parches de piel escamosa (“lesiones de piel psoriásicas“).
Paso 3: Inyección de la solución de ENBREL®
Limpie el sitio dónde va inyectar ENBREL® con una torunda de alcohol, realizando movimientos circulares. NO toque nuevamente esta área antes de administrar la inyección.
Recoja la jeringa prellenada de la superficie plana de trabajo. Retire la cubierta de la aguja jalándola firmemente y en forma recta de la jeringa (ver Diagrama 2). Tenga cuidado de no doblar o torcer la cubierta durante la remoción para evitar dañar la aguja.
Cuando usted retire la tapa que cubre la aguja, puede haber una gota de líquido al final de la aguja; lo cual es normal. No toque la aguja ni tampoco la toque con cualquier superficie. Ni golpee el tapón del émbolo. Si lo hace puede causar que el líquido se salga.
Diagrama 2.
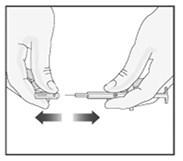
• Cuando el área limpia de la piel esté seca, forme un pellizco en la piel y manténgala firmemente con una mano. Con la otra mano, mantenga la jeringa inclinada como un lápiz.
• Con un movimiento rápido y corto, empuje la aguja hasta el final dentro de la piel en un ángulo entre 45º y 90º. A través de su experiencia, encontrará el ángulo más confortable para usted. Tenga cuidado de no empujar la aguja dentro de la piel demasiado lento, o con gran fuerza.
Diagrama 3.
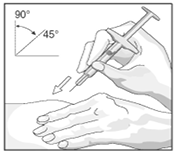
Cuando la aguja esté insertada completamente dentro de la piel, suelte la piel que está sosteniendo. Con la mano libre, sostenga la jeringa cerca de su base para estabilizarla. Posteriormente empuje el émbolo para inyectar toda la solución a una velocidad lenta, estable (ver Diagrama 4).
Diagrama 4.
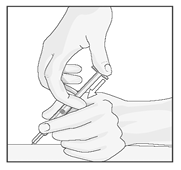
• Cuando la jeringa se desocupe, retire la aguja fuera de la piel, tratando de mantener cuidadosamente el mismo ángulo con que la inserto. Puede haber un pequeño sangrado en el sitio de la inyección. Usted puede presionar el sitio de inyección durante 10 segundos con un algodón o una gasa. No frote en el sitio de inyección. Si es necesario usted puede cubrir el sitio de inyección con una venda.
Paso 4: Descarte de desechos
• La jeringa prellenada es solamente para administrar en una única dosis. La jeringa ni la aguja NUNCA deben ser reutilizadas. NUNCA tape nuevamente la aguja. Deseche inmediatamente la aguja y la jeringa de acuerdo con las instrucciones de su médico, enfermera o farmacéutico.
Si usted tiene alguna pregunta sobre la aplicación por favor consulte a su médico, enfermera o farmacéutico quienes son las personas más familiarizadas con ENBREL®.
INDICACIONES
• ENBREL® está indicado para
Artritis reumatoide: ENBREL® está indicado para reducir los signos y síntomas e inhibir la progresión del daño estructural en pacientes con artritis reumatoide (AR) activa moderada a severa. ENBREL® puede iniciarse en combinación con metotrexato o ser utilizado solo.
ENBREL® puede utilizarse solo o en combinación con metotrexato para el tratamiento de la AR activa en adultos cuando la respuesta a uno o más medicamentos antirreumáticos modificadores de la enfermedad (DMARDs) ha sido inadecuada, incluyendo el metotrexato (a menos que esté contraindicado).
Artritis juvenil idiopática: Etanercept está indicado para el tratamiento de la artritis idiopática juvenil (AIJ) de curso poliarticular en niños y adolescentes a partir de los 2 años de edad cuando la respuesta a una o más DMARDs ha sido inadecuada.
Tratamiento de poliartritis (factor reumatoide positivo o negativo) y oligoartritis prolongada en niños y adolescentes a partir de los 2 años que han presentado una respuesta inadecuada o intolerancia al metotrexato.
Tratamiento de la artritis psoriásica en adolescentes a partir de los 12 años que han presentado una respuesta inadecuada o intolerancia al metotrexato.
Tratamiento de artritis relacionada con entesitis en adolescentes a partir de los 12 años que han presentado una respuesta inadecuada o intolerancia a la terapia convencional.
Artritis psoriásica: ENBREL® está indicado para reducir los signos y síntomas e inhibir la progresión del daño estructural de la artritis activa en pacientes con artritis psoriásica. ENBREL® puede ser usado en combinación con metotrexato en pacientes que no responden adecuadamente al metotrexato solo.
Espondiloartritis axial
Espondilitis anquilosante (EA): ENBREL® está indicado para reducir los signos y síntomas en pacientes con espondilitis anquilosante.
Psoriasis en placas: ENBREL® está indicado para el tratamiento de pacientes adultos (mayores de 18 años) con psoriasis en placas crónica de moderada a severa, que sean candidatos para la terapia sistémica o fototerapia.
Espondiloartritis axial no radiográfica: ENBREL® está indicado para el tratamiento de adultos con espondiloartritis axial no radiográfica grave con indicios objetivos de inflamación indicados por la PCR elevada y/o indicios en IRM, que hayan tenido una respuesta inadecuada a la terapia convencional o presenten intolerancia a ella.
Psoriasis en placas pediátrica: ENBREL® está indicado para el tratamiento de la psoriasis en placas severa en niños y adolescentes de 6 años en adelante que se han controlado inadecuadamente utilizando otras terapias sistémicas o fototerapias o que no toleran esta clase de terapias.
MECANISMO DE ACCIÓN: Etanercept es una forma soluble dimérica de receptor de FNT p75 (factor de necrosis tumoral) que puede unirse a cualquiera de las dos moléculas de FNT. Etanercept inhibe la unión tanto del FNT (FNTa) como de la linfotoxina alfa [LTa] (FNTb) a los receptores FNT de la superficie celular, de esta forma inactiva biológicamente el FNT y previene las respuestas celulares mediadas por el FNT. El FNT es una citoquina dominante en el proceso inflamatorio de la artritis reumatoide en pacientes adultos. El FNT y LTa son expresadas en pacientes con artritis juvenil crónica.1 Niveles elevados de FNT fueron encontrados en el líquido sinovial de pacientes con artritis reumatoide y artritis juvenil idiopática. En la placa de psoriasis, la infiltración por las células inflamatorias (incluyendo células T), causa un incremento en los niveles del FNT en las lesiones psoriásicas en comparación con los niveles en la piel no comprometida. Existen naturalmente dos receptores distintos para el FNT (RFNT), una proteína a 55 kilodalton (p55) y una a 75 kilodalton (p75) como moléculas monoméricas en la superficie celular y en formas insolubles. La actividad biológica del FNT es dependiente de la unión a cualquiera de los receptores de superficie celular. Etanercept puede también modular las respuestas biológicas controladas por moléculas adicionales (citoquinas, moléculas de adhesión o proteinasas) que son inducidas o reguladas por el factor de necrosis tumoral. Etanercept inhibe la actividad de FNT in vitro y ha mostrado que afecta modelos animales de inflamación, incluyendo la artritis inducida por colágeno en ratones.
USO EN PACIENTES GERIÁTRICOS: No se recomiendan ajustes específicos de la dosificación basados en la edad de los pacientes.
USO EN PACIENTES PEDIÁTRICOS: ENBREL® no ha sido estudiado en niños <2 años de edad (ver también las secciones Interacciones y Dosificación y administración). Para información de seguridad pediátrica específica relacionada con tumores malignos, vacunaciones y la enfermedad intestinal inflamatoria, ver la sección Precauciones.
FARMACOCINÉTICA
Absorción: ENBREL® se absorbe lentamente del sitio de inyección subcutánea alcanzando una concentración máxima aproximadamente 48 horas después de la única dosis. La biodisponibilidad absoluta es de 76%.
Distribución: Después de la dosis única subcutánea de 25 mg de ENBREL®, el promedio máximo de concentración sérica observada en voluntarios sanos fue de 1.65 ± 0.66 mg/mL, y el área bajo la curva fue de 235 ± 96.6 mg.hr/mL. No se ha evaluado formalmente la proporcionalidad de la dosis, pero no hay una aparente saturación de la depuración a través del rango de la dosis.
El volumen de distribución en estado estable luego de la administración subcutánea es 13.9 ± 9.4 L.
Luego de la dosis continuada con ENBREL® en pacientes con artritis reumatoide (n=25) por seis meses con 25 mg dos veces por semana, los niveles promedio observados fueron 3.0 mg/mL (rango 1.7 a 5.6 mg/mL). Basados en los datos disponibles, los pacientes en forma individual pueden sufrir de un incremento de dos a cinco veces en los niveles séricos con dosis repetidas.
Eliminación: ENBREL® se elimina lentamente del cuerpo. La vida media es de aproximadamente 80 horas.28
La depuración es aproximadamente 175 ± 116 mL/h en pacientes con artritis reumatoide, y de 131 ± 81 ml/h observado en voluntarios sanos.
La radioactividad es eliminada en la orina luego de la administración de etanercept radiomarcado en pacientes y voluntarios.
Deterioro hepático y renal: Aunque hay una eliminación de la radioactividad en la orina después de la administración de etanercept radiomarcado en pacientes y voluntarios, no se observaron incrementos en las concentraciones de etanercept en pacientes con falla hepática o renal aguda, por lo que la presencia del deterioro renal y hepático no requiere cambio de la dosis.
Género: No hay diferencia farmacocinética aparente entre hombre y mujer.
Relación concentración/ efecto: Las concentraciones séricas en estado estable de 1 a 2 mg/L de etanercept están asociadas con un efecto óptimo, y son obtenidas con dosis de 25 mg de ENBREL® dos veces por semana. En un estudio cruzado de etiqueta abierta, de una sola dosis, de dos grupos de tratamiento en 28 voluntarios sanos, se encontró que el ENBREL® administrado como una sola inyección de 50 mg/mL era bioequivalente a dos inyecciones simultáneas de 25 mg/mL.
COMPATIBILIDADES, INCOMPATIBILIDADES: En ausencia de estudios de incompatibilidad, ENBREL® no debe ser mezclado con otros medicamentos.
CONTRAINDICACIONES: Hipersensibilidad al etanercept o a cualquier componente del producto.
Sepsis o riesgo de sepsis. Ver secciones Advertencias especiales, Precauciones y Reacciones adversas.
El tratamiento con ENBREL® no debe ser iniciado en pacientes con infecciones activas serias, incluyendo infecciones crónicas o localizadas.
Embarazo, lactancia y niños menores de 2 años en artritis reumatoidea y niños menores de 6 años en psoriasis.
EMBARAZO: La seguridad de ENBREL® durante el embarazo no ha sido claramente establecida. El uso de ENBREL® durante el embarazo sólo debe realizarse si es claramente necesario. No se encuentran disponibles datos preclínicos sobre toxicidad perinatal y posnatal de ENBREL® y sus efectos en la fertilidad y el funcionamiento reproductivo general. Los estudios de toxicidad sobre el desarrollo se han realizado en ratas y conejos. Las exposiciones sistémicas a etanercept basadas en el AUC en ratas y conejos son 21 a 25 veces mayores que la exposición a la que se someten los humanos a dosis terapéuticas usuales de 50 mg semanales y son aproximadamente 10-13 veces mayores que la exposición a la que se someten los humanos a la dosis máxima recomendada de 50 mg dos veces a la semana (para psoriasis). En las ratas o conejos o ratas neonatas no se observó evidencia de peligro para el feto debido a ENBREL®. Los estudios de reproducción en animales no siempre predicen la respuesta en humanos.
ENBREL® atraviesa la placenta y se ha detectado en el suero de lactantes nacidos de pacientes de sexo femenino tratadas con ENBREL® durante el embarazo. Se desconoce el impacto de esto, sin embargo, los lactantes pueden tener un mayor riesgo de infección. Generalmente no se recomienda la administración de vacunas vivas a lactantes por 16 semanas después de la última dosis de ENBREL® de la madre.
LACTANCIA: La seguridad de ENBREL® durante la lactancia no ha sido claramente establecida. Se ha informado que ENBREL® se excreta en la leche humana luego de la administración subcutánea. En ratas lactantes, luego de la administración subcutánea, ENBREL® fue excretado en la leche y se detectó en el suero de las crías. Debido a que muchos medicamentos e inmunoglobulinas pueden ser excretados en la leche materna, se debe tomar una decisión si se debe descontinuar la lactancia o el uso de ENBREL® mientras se está lactando.
REACCIONES ADVERSAS
Pacientes adultos: La proporción de pacientes que descontinuaron el tratamiento debido a los eventos adversos en estudios clínicos controlados en pacientes con artritis reumatoide fue el mismo tanto en los grupos de ENBREL® como en los de placebo.
Reacciones en el sitio de inyección: Los pacientes en estudios clínicos controlados tratados con ENBREL® tuvieron una incidencia significativamente mayor de reacciones en el sitio de inyección (eritema y/o prurito, dolor o tumefacción) comparado con el grupo de pacientes tratado con placebo. La frecuencia de las reacciones en el sitio de inyección fue mayor durante el primer mes de tratamiento y subsecuentemente disminuyó en frecuencia. En los ensayos clínicos, estas reacciones fueron generalmente transitorias con una duración media de 4 días. Algunos pacientes que experimentaron reacciones en el sitio de inyección también experimentaron reacciones en sitios previos de inyección.
Durante la experiencia post-comercialización, el sangrado en el sitio de inyección y los hematomas también han sido observados durante la terapia con ENBREL®.
Infecciones: Se han reportado infecciones serias y fatales; los patógenos reportados incluyen bacterias, micobacterias (incluyendo tuberculosis), virus y hongos. Se han reportado también infecciones oportunistas, incluidas infecciones invasivas por hongos, parásitos (incluidos los protozoos), virus (incluido el herpes zoster), bacterianas (incluidas infecciones por Listeria y Legionella) e infecciones micobacterianas atípicas) (ver Advertencias especiales). Las infecciones fúngicas invasivas más comúnmente informadas incluían Candida, Pneumocystis, Aspergillus e Histoplasma.
En estudios clínicos controlados en pacientes con artritis reumatoide tratados con ENBREL®, las tasas de infecciones reportadas como serias (fatales, amenaza a la vida, que requieren hospitalización o antibióticos intravenosos) y no serias, fueron similares para ENBREL® y para el placebo cuando se ajustó para la duración de la exposición. De las infecciones del tracto respiratorio superior fueron las infecciones no serias las más frecuentemente reportadas.
Datos de un estudio clínico en pacientes con sepsis establecida sugirieron que el tratamiento con ENBREL® puede incrementar la mortalidad en estos pacientes.
Procesos malignos y desórdenes linfoproliferativos: En el periodo post-comercialización se han recibido reportes sobre procesos malignos que afectan varios sitios.
Se han reportado procesos malignos en un estudio clínico de pacientes en tratamiento por Granulomatosis de Wegener (ver Advertencias especiales).
Se han presentado informes postcomercialización de linfoma hepatoesplénico de células T asociado con inhibidores del factor de necrosis tumoral administrados solos o combinados con otros inmunosupresores. La mayoría de los casos reportados fueron en pacientes tratados por enfermedad de Crohn o colitis ulcerosa.
Autoanticuerpos: En estudios controlados, el porcentaje de pacientes que desarrollaron nuevos anticuerpos antinucleares positivos ANA (³1:40), anticuerpos nuevos positivos contra la doble hélice del ADN y anticuerpos nuevos anticardiolipina, fue mayor en pacientes tratados con ENBREL® que en los pacientes tratados con placebo. Es desconocido el impacto del tratamiento a largo plazo con ENBREL® en el desarrollo de enfermedades autoinmunes.
Han sido descritos en pacientes reportes de eventos raros, incluyendo aquellos con factor reumatoide (RA) positivo, que han desarrollado autoanticuerpos adicionales junto con un síndrome lúpico o erupción compatible con lupus cutáneo subagudo o lupus discoide por la presentación clínica y biopsia. (Ver la Tabla a continuación, Otras Reacciones Adversas).
Otras Reacciones adversas
Las reacciones adversas están enumeradas en la Tabla de acuerdo con las categorías de frecuencias de los CIOMS:
|
Muy común |
³ 10% |
|
Común |
³ 1% y <10% |
|
Poco común |
³ 0.1 y <1% |
|
Raro |
³0.01 y <0.1% |
|
Muy raro |
<0.01% |
|
No conocida |
La frecuencia no puede ser estimada con exactitud con los datos arrogados por los estudios clínicos. |
La siguiente tabla de efectos indeseables sospechados está basada en las tasas de reportes de estudios clínicos y/o reportes espontáneos post-comercialización
|
Sistema |
Reacciones adversas |
|
Infecciones e infestaciones |
|
|
Muy Común: |
Infecciones (incluidas infecciones del tracto respiratorio superior), bronquitis, cistitis, infecciones de la piel. |
|
Poco común: |
Infecciones serias (incluida neumonía, celulitis, artritis séptica, sepsis e infección parasitaria) |
|
Raro: |
Tuberculosis, infecciones oportunistas (incluidas infecciones invasivas por hongos, bacterianas, micobacterianas atípicas, infecciones virales y por Legionella) |
|
No conocida: |
Listeria. reactivación de la hepatitis B |
|
Neoplasmas benignos, tumores malignos y no especificados (incluidos quistes y pólipos) |
|
|
Poco común |
Cánceres de piel no melanocíticos (ver la sección Precauciones) |
|
Raro |
Melanoma (ver la sección Precauciones) |
|
No conocida |
Carcinoma de células de Merkel (ver la sección Precauciones) |
|
Trastornos en el sistema linfático y sanguíneo |
|
|
Poco común |
Trombocitopenia |
|
Raro |
Anemia, leucopenia, neutropenia, pancitopenia (ver la sección Precauciones) |
|
Muy raro |
Anemia aplásica (ver la sección Precauciones) |
|
Trastornos del sistema inmunitario |
|
|
Común |
Reacciones alérgicas, (ver Desórdenes en piel y tejido subcutáneo); formación de autoanticuerpos |
|
Poco común |
Vasculitis sistémica (incluida vasculitis positiva para ANCA). |
|
Raro |
Reacciones alérgicas/anafilácticas serias (incluyendo broncoespasmo) |
|
No conocida |
Activación de síndrome de macrófago |
|
Trastornos generales y condiciones en el sitio de administración |
|
|
Muy común |
Reacciones en el sitio de inyección (incluidos eritema, picazón, dolor e hinchazón) |
|
Común |
Fiebre |
|
Trastornos del sistema nervioso central |
|
|
Raro |
Convulsiones, eventos desmielinizantes del SNC, incluyendo esclerosis múltiple y condiciones desmielinizantes localizadas como neuritis óptica y mielitis transversa (ver la sección Precauciones) |
|
Trastornos Oculares |
|
|
Poco común |
Uveítis, escleritis |
|
Trastornos Respiratorios, Torácicos y Mediastínicos |
|
|
Poco común |
Enfermedad intersticial del pulmón (incluyendo fibrosis pulmonar y pneumonitis). |
|
Trastornos en la piel y tejidos subcutáneos |
|
|
Común |
Prurito |
|
Poco común |
Exantema, urticaria, angioedema, psoriasis (reaparición o exacerbación; incluidos todos los subtipos) y exantema psoriasiforme. |
|
Raro |
Vasculitis cutánea (incluyendo vasculitis leucocitoclástica), Síndrome de Stevens-Johnson, eritema multiforme. |
|
Muy raro |
Necrólisis tóxica epidérmica |
|
Trastornos musculoesqueléticos, de tejido conectivo y huesos |
|
|
Raro |
Lupus eritematoso cutáneo subagudo, lupus eritematoso discoide, síndrome lúpico |
|
Trastornos cardiacos |
|
|
Raro |
Empeoramiento de la insuficiencia cardiaca congestiva (ICC). |
|
Trastornos hepatobiliares |
|
|
Raro |
Aumento de enzimas hepáticas, hepatitis autoinmune. |
Población Pediátrica: En general los eventos adversos en pacientes pediátricos fueron similares en frecuencia y tipo a aquellos vistos en los pacientes adultos.
• Efecto no deseado en pacientes pediátricos con artritis idiopática juvenil
Los pacientes con artritis idiopática juvenil tratados con ENBREL® tuvieron una incidencia significativamente mayor de reacciones en el sitio de inyección (eritema y/o prurito, dolor o inflamación) comparados con los pacientes tratados con placebo en estudios clínicos controlados.
La infección fue el evento adverso más común reportado en pacientes pediátricos que reciben ENBREL® y ocurrió con una incidencia similar a la del placebo. Los tipos de infecciones reportadas en pacientes con artritis idiopática juvenil fueron generalmente leves y consistentes con aquellos comúnmente vistos en las poblaciones de pacientes pediátricos ambulatorios.
En los estudios clínicos realizados en pacientes con artritis idiopática juvenil tratados con ENBREL®, fueron reportados dos casos de infección por varicela con signos y síntomas indicativos de meningitis aséptica.
Se reportaron 4 eventos de síndrome de activación de macrófagos en los estudios clínicos de artritis idiopática juvenil.
• Efectos no deseados en pacientes pediátricos con psoriasis pediátrica en placas
En un estudio de 48 semanas con 211 niños de 4 a 17 años de edad con psoriasis pediátrica en placas, los eventos adversos reportados fueron similares a los observados en estudios previos en adultos con psoriasis en placas.
INTERACCIONES
Tratamiento concurrente con anakinra: Los pacientes tratados con ENBREL® y anakinra presentaron una tasa mayor de infecciones serias al compararlos con pacientes que fueron tratados únicamente con ENBREL® (datos históricos). Además, en un estudio doble enmascarado, controlado con placebo en pacientes recibiendo de base metrotexato, se observó una tasa más alta de infecciones serias y neutropenia en los pacientes tratados con ENBREL® y anakinra versus los pacientes tratados con ENBREL® únicamente (ver la sección Advertencias especiales).
Tratamiento concurrente con abatacept: En estudios clínicos, la administración concomitante de abatacept y ENBREL® ha mostrado un incremento en la incidencia de eventos adversos serios. Esta combinación no ha demostrado un incremento en los beneficios clínicos, por lo tanto no se recomienda su uso. (Ver sección Advertencias especiales).
Tratamiento concurrente con sulfasalazina: En un estudio clínico se adicionó ENBREL® a pacientes recibiendo dosis establecidas de sulfasalazina. Los pacientes del grupo de tratamiento combinado tuvieron una disminución estadísticamente significativa en el recuento de glóbulos blancos en comparación con el grupo tratado con ENBREL® solo o sulfasalazina sola. No se conoce la significancia clínica de este hallazgo.
No Interacciones: En las pruebas clínicas de pacientes adultos con artritis reumatoide no se observó ninguna interacción cuando ENBREL® fue administrado con glucocorticoides, salicilatos (excepto sulfasalazina), medicamentos antiinflamatorios no esteroideos (AINE), analgésicos o metotrexato.
El metotrexato no tiene efecto en la farmacocinética de ENBREL®. No se observaron interacciones farmacocinéticas medicamento - medicamento de importancia clínica en estudios con digoxina y warfarina.
DATOS DE SEGURIDAD PRECLÍNICA
Carcinogenicidad: No han sido conducidos estudios a largo plazo en animales para evaluar el potencial carcinogénico de ENBREL®. Estos estudios a largo plazo en animales no son factibles porque los animales pueden desarrollar anticuerpos al etanercept, pues es una proteína humana.
Mutagenicidad: Se realizaron estudios de mutagénesis f in vitro e in vivo, y no se observó evidencia de actividad mutagénica.
Estudios en la fertilidad: No han sido conducidos estudios a largo plazo en animales para evaluar el efecto en la fertilidad de ENBREL®.
EFICACIA CLÍNICA: Esta sección presenta datos de cuatro estudios clínicos llevados a cabo en adultos con artritis reumatoide, dos tres estudios en artritis idiopática juvenil, un estudio en adultos con artritis psoriásica, cuatro estudios en adultos con espondilitis anquilosante, un estudio en adultos con espondiloartritis axial no radiográfica, tres estudios en adultos con psoriasis en placas y dos estudios con pacientes pediátricos con psoriasis en placas.
• Pacientes adultos con artritis reumatoide
La eficacia de ENBREL® se evaluó en un estudio aleatorio, doble ciego, controlado con placebo. El estudio evaluó 234 pacientes adultos con artritis reumatoide activa, que tuvieron terapia fallida con al menos una pero no más de cuatro drogas antirreumáticas modificadoras de la enfermedad (DMARDs). Se administraron dos veces a la semana dosis subcutáneas de 10 mg o 25 mg de ENBREL® o placebo durante 6 meses consecutivos. Los resultados de este estudio controlado se expresaron en forma de porcentaje de mejoría de la artritis reumatoide utilizando los criterios de respuesta del Colegio Americano de Reumatología (ACR).
Las respuestas ACR 20 y 50 a los 3 y 6 meses fueron mayores en los pacientes tratados con ENBREL® que en los pacientes tratados con placebo (ACR 20: ENBREL® 62% y 59%, placebo 23% y 11% a los 3 y 6 meses, respectivamente; ACR 50: ENBREL® 41% y 40%, placebo 8% y 5% a los 3 y 6 meses, respectivamente; p<0,01 ENBREL® vs. placebo en todos los puntos de tiempo para las respuestas ACR 20 y ACR 50).
Aproximadamente el 15% de los pacientes que recibieron ENBREL® alcanzaron una respuesta ACR 70 en los meses 3 y 6, en comparación con menos del 5% de los pacientes tratados con placebo. Entre los pacientes que recibieron ENBREL®, las respuestas clínicas aparecieron, generalmente, entre la primera y segunda semana desde el inicio de la terapia y casi siempre ocurrió a los tres meses. Se observó una respuesta a la dosis; los resultados con 10 mg fueron intermedios entre el placebo y la dosis de 25 mg. ENBREL® fue significativamente mejor que el placebo en todos los componentes de los criterios del ACR, así como en otras medidas de actividad de la enfermedad de la artritis reumatoide no incluidas en los criterios de respuesta del ACR, como por ejemplo la rigidez matinal. Durante el estudio, cada 3 meses se aplicó un Cuestionario de Evaluación de la Salud (HAQ) que incluye parámetros de discapacidad, vitalidad, salud mental, estado general de salud y subdominios del estado de salud asociado con la artritis. Comparados con los pacientes del control, todos los subdominios del cuestionario HAQ mejoraron en los pacientes tratados con ENBREL® a los 3 y 6 meses.
Después de la interrupción de ENBREL®, los síntomas de la artritis generalmente reaparecieron en un mes. Según los resultados de estudios de etiqueta abierta, la reintroducción del tratamiento con ENBREL® después de interrupciones de hasta 24 meses produjo las mismas magnitudes de respuesta que la obtenida en pacientes que recibieron ENBREL® sin interrupción de la terapia. Se han observado respuestas duraderas continuas de hasta 10 años en los estudios de tratamiento de extensión de etiqueta abierta cuando los pacientes recibieron ENBREL® sin interrupción.
En un segundo estudio aleatorio, activo-controlado se comparó la eficacia de ENBREL® con metotrexato, con evaluaciones radiográficas ciegas como un punto de evaluación primario en 632 pacientes con artritis reumatoide activa (de duración menor de 3 años), que nunca habían recibido tratamiento con metotrexato. Se administraron subcutáneamente dos veces por semana durante 24 meses dosis de 10 ó 25 mg de ENBREL®. Las dosis de metotrexato se aumentaron desde 7,5 mg/semana hasta un máximo de 20 mg/semana durante las primeras 8 semanas del estudio, y se continuó hasta los 24 meses. La mejoría clínica, incluyendo el inicio de la acción dentro de las dos semanas, lograda con 25 mg de ENBREL® fue similar a la observada en los estudios previos, y se mantuvo hasta por 24 meses. Al inicio del estudio, los pacientes presentaron un grado moderado de discapacidad, con puntajes medios de Cuestionario de Evaluación de la Salud (HAQ) de 1,4 a 1,5. El tratamiento con ENBREL® 25 mg produjo una mejoría sustancial, aproximadamente el 44% de los pacientes alcanzaron puntajes normales de HAQ (menores de 0,5) a los 12 meses. Este beneficio se mantuvo en el segundo año de este estudio.
En este estudio, se evaluó radiográficamente el daño estructural en las articulaciones, expresándose como cambio en el Puntaje Total Sharp (PTS) y en sus componentes, el puntaje de erosión y el puntaje de estrechamiento del espacio articular (EEA). Las radiografías de manos/muñecas y pies se leyeron al inicio del estudio y a los 6, 12 y 24 meses. La dosis de ENBREL® de 10 mg presentó de forma consistente un efecto menor que la de 25 mg sobre el daño estructural. ENBREL® 25 mg fue significativamente superior a metotrexato en términos de puntajes de erosión a los 12 y a los 24 meses. Las diferencias en PTS y EEA no fueron estadísticamente significativas entre metotrexato y ENBREL® 25 mg. Los resultados se presentan en la siguiente figura.
Progresión radiográfica: Comparación de ENBREL® vs Metrotexato en pacientes con ar de < tres años de duración
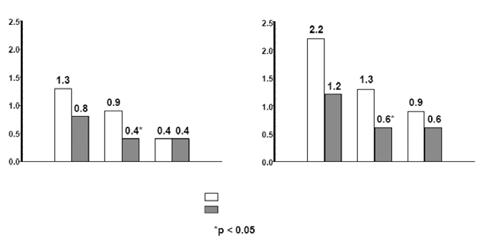
En otro estudio activo controlado, doble-ciego, aleatorio, en pacientes con Artritis Reumatoide (AR) tratados con ENBREL® solo (25 mg dos veces por semana), metotrexato solo (7,5 a 20 mg semanalmente, dosis media 20 mg), o la combinación de ENBREL® y metotrexato iniciados concomitantemente, se compararon la eficacia clínica, la seguridad y la progresión radiográfica en 682 pacientes adultos con artritis reumatoide activa de 6 meses a 20 años de duración (mediana 5 años) que tuvieron una respuesta menos que satisfactoria a al menos una droga antirreumática modificadora de la enfermedad (DMARD) diferente del metotrexato.
Los pacientes del grupo de ENBREL® en combinación con la terapia de metotrexato tuvieron respuestas ACR 20, ACR 50 y ACR 70 significativamente mayores y mejoría en los puntajes Puntaje de Actividad de la Enfermedad (Disease Activity Store -DAS-) y Cuestionario de Evaluación de la Salud (HAQ) a las 24 y a las 52 semanas comparados con los pacientes de cualquiera de los grupos de terapia individual (los resultados se muestran en la siguiente tabla). Después de 24 meses de tratamiento, se observaron también ventajas significativas con la administración de ENBREL® en combinación con metotrexato, cuando ésta se comparaba con ENBREL® en monoterapia y metrotexato en monoterapia.
|
Resultados de eficacia clínica a los 12 meses: Comparación de ENBREL® vs. Metotrexato vs. ENBREL® en combinación con metotrexato en pacientes con ar de 6 meses a 20 años de duración |
|||
|
Punto Final |
Metotrexato |
ENBREL® |
ENBREL® + |
|
Respuestas ACRa |
|||
|
ACR 20 |
58,8% |
65,5% |
74,5%†,f |
|
ACR 50 |
36,4% |
43,0% |
63,2%†,f |
|
ACR 70 |
16,7% |
22,0% |
39,8%†,f |
|
DAS |
|||
|
Puntaje inicialb |
5,5 |
5,7 |
5,5 |
|
Puntaje semana 52b |
3,0 |
3,0 |
2,3†,f |
|
Remisiónc |
14% |
18% |
37%†, f |
|
HAQ |
|||
|
Inicial |
1,7 |
1,7 |
1,8 |
|
Semana 52 |
1,1 |
1,0 |
0,8†,f |
|
a: Los pacientes que no completaron los 12 meses en el estudio fueron considerados como pacientes que no respondían al tratamiento. b: Los valores para el Puntaje de Actividad de la Enfermedad (DAS) son los valores medios c: La remisión se define como DAS < 1,6 Valores p de comparación de pares: † = p <0,05 para comparaciones de ENBREL® + metotrexato vs. metotrexato y f = p < 0,05 para comparaciones de ENBREL® + metotrexato vs. ENBREL® |
|||
El progreso radiográfico a los 12 meses fue significativamente menor en el grupo de ENBREL® que en el grupo de metotrexato, mientras que la combinación fue significativamente mejor que en cualquier grupo con monoterapia para progresión radiográfica lenta (ver la siguiente figura).
Progresión radiográfica: Comparación de ENBREL® vs. Metotrexato vs. ENBREL® en combinación con metotrexato en pacientes con ar de 6 meses a 20 años de duración (Resultados a los 12 meses)
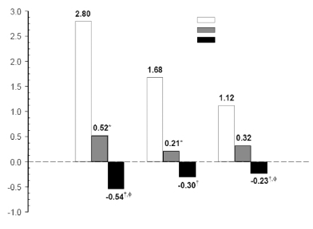
Valores p de comparación por pares: * = p <0,05 para comparaciones de ENBREL® vs. metotrexato, † = p < 0,05 para comparaciones de ENBREL® + metotrexato vs. metotrexato y f = p < 0,05 para comparaciones de ENBREL® + metotrexato vs. ENBREL®
Después de 24 meses de tratamiento, se observaron también ventajas significativas de ENBREL® en combinación con metotrexato, comparado con monoterapia de ENBREL® y monoterapia de metotrexato. De forma similar, también se observaron, después de 24 meses de tratamiento, ventajas significativas del tratamiento de ENBREL® como monoterapia, con respecto a la administración de metotrexato como monoterapia.
En un análisis, en el que se consideró que todos los pacientes que habían abandonado el estudio por cualquier motivo habían progresado, el porcentaje de pacientes sin progreso (cambio PTS = 0,5) a los 24 meses era mayor en los grupos de ENBREL® en combinación con metotrexato, comparado con los grupos de ENBREL® solo y de metotrexato solo (62%, 50% y 36%, respectivamente; p< 0,05). La diferencia entre los grupos de ENBREL® solo y de metotrexato solo también fue significativa (p< 0,05). Las tasas de no progreso, entre los pacientes del estudio que completaron el periodo total de 24 meses de tratamiento, fueron de 78%, 70% y 61%, respectivamente.
Se evaluó la seguridad y eficacia de 50 mg de ENBREL® (dos inyecciones subcutáneas de 25 mg) administrados una vez a la semana en un estudio doble ciego controlado con placebo con 420 pacientes con artritis reumatoide activa.2 En este estudio, 53 pacientes recibieron placebo, 214 pacientes recibieron 50 mg de ENBREL® una vez a la semana y 153 pacientes recibieron 25 mg de ENBREL® dos veces a la semana. Los perfiles de seguridad y eficacia de los dos regímenes de tratamiento de ENBREL® fueron comparables en la semana 8 en lo que se refiere a su efecto sobre los signos y síntomas de artritis reumatoide; los datos a las 16 semanas no mostraron comparabilidad (ni inferioridad) entre los dos regímenes.
• Población pediátrica con artritis idiopática Juvenil
Se evaluó la seguridad y eficacia de ENBREL® en un estudio dividido en dos fases con 69 niños con artritis idiopática juvenil de curso poliarticular que presentaban distintas formas de inicio de Artritis Idiopática Juvenil (poliartritis, pauciartritis, aparición sistémica). Se seleccionaron pacientes entre 4 y 17 años con artritis idiopática juvenil de curso poliarticular de intensidad moderada a severa, refractarios o con intolerancia al metotrexato. Se permitieron dosis estables de un solo antiinflamatorio no esteroide y/o prednisona (£0,2 mg/kg/día ó 10 mg máximo). En la primera fase del estudio, todos los pacientes recibieron dosis de 0,4 mg/kg (máximo 25 mg por dosis) de ENBREL® por vía subcutánea dos veces por semana. En la segunda fase, los pacientes con respuesta clínica al cabo de 90 días se asignaron de forma aleatoria para seguir recibiendo ENBREL® o para recibir placebo durante 4 meses y fueron evaluados para detectar la exacerbación de la enfermedad. Las respuestas se evaluaron utilizando la escala ACR Pedi 30, definida como mejoría ³30% en por lo menos 3 de los 6 criterios de evaluación para la ARJ y un deterioro ³30% en no más de 1 de los 6 criterios, que incluyen: El número de articulaciones activas, limitación de la movilidad, evaluación global del paciente/padre, evaluación global del médico, evaluación funcional y VSG. La exacerbación de la enfermedad se estableció como ³30% de deterioro en 3 de los 6 criterios de evaluación para la ARJ, ³30% de mejoría en no más de 1 de los 6 criterios y un mínimo de 2 articulaciones activas.
En la primera fase del estudio, 51 de los 69 pacientes (74%) mostraron una respuesta clínica favorable e ingresaron a la segunda fase. En esta segunda fase, 6 de 25 pacientes (24%) que recibían ENBREL® manifestaron una exacerbación de la enfermedad contra 20 de 26 pacientes (77%) del grupo de placebo (p=0.007). Desde el inicio de la segunda fase, el tiempo promedio hasta la exacerbación, fue ³116 días en los pacientes del grupo de ENBREL® y 28 días en los pacientes que recibieron placebo. Cada componente de los criterios de evaluación de la ARJ del brazo que recibió placebo empeoró, mientras que permaneció estable o mejoró el brazo que continuaba con ENBREL®. La información sugirió la posibilidad de una mayor incidencia de exacerbación entre aquellos pacientes con una mayor VSG basal. De los pacientes que mostraron una respuesta clínica a los 90 días y formaron parte de la segunda etapa del estudio, algunos permanecieron con ENBREL® continuando su mejoría desde el mes 3 hasta el mes 7, mientras aquellos que recibieron placebo no mejoraron.
En un estudio de extensión de seguridad abierto, 58 pacientes provenientes del estudio anteriormente descrito (de 4 años de edad en el momento de su inclusión en el estudio) continuaron recibiendo ENBREL® durante un periodo de hasta 10 años. La tasa de efectos adversos y de infecciones graves no aumentó con la exposición a largo plazo.122
En otro estudio de fase abierta y de un solo brazo, 60 pacientes con oligoartritis prolongada (15 pacientes de edades entre 2 y 4 años, 23 pacientes de edades entre 5 y 11 años y 22 pacientes de edades entre 12 y 17 años), 38 pacientes con artritis relacionada con entesitis (de edades entre 12 y 17 años), y 29 pacientes con artritis psoriásica (de edades entre 12 y 17 años) fueron tratados con ENBREL® en dosis de 0,8 mg/kg (hasta un máximo de 50 mg por dosis) una vez a la semana y durante un periodo de 12 semanas. En cada uno de los subtipos de AIJ, la mayoría de los pacientes cumplieron los criterios ACR Pedi 30 y demostraron una mejoraría clínica en las variables secundarias, tales como el número de articulaciones dolorosas y la evaluación global del médico. El perfil de seguridad fue consistente con el observado en otros estudios de AIJ.
No se han realizado estudios en pacientes con artritis idiopática juvenil que evalúen los efectos del tratamiento continuo con ENBREL® en pacientes que no responden dentro de los tres meses de iniciado el tratamiento con ENBREL®. Adicionalmente, no se han realizado estudios para evaluar los efectos de interrumpir o reducir la dosis recomendada de ENBREL® luego de su utilización prolongada en pacientes con AIJ.
La seguridad a largo plazo de la monoterapia con ENBREL® (n=103), ENBREL® más metotrexato (n=294), o la monoterapia con metotrexato (n=197) se evaluó por hasta 3 años en un registro de 594 niños de 2 a 18 años de edad con artritis idiopática juvenil, 39 de los cuales tenían de 2 a 3 años de edad. En general, las infecciones fueron reportadas más comúnmente en pacientes tratados con ENBREL® en comparación con los tratados con solo metotrexato (3,8 versus 2%) y las infecciones asociadas con la utilización de ENBREL® fueron de naturaleza más severa.
• Pacientes adultos con Artritis Psoriásica
Se evaluó la eficacia de ENBREL® en un estudio controlado con placebo, doble ciego, aleatorio con 205 pacientes con artritis psoriásica. Los pacientes tenían entre 18 y 70 años de edad y artritis psoriásica activa (3 o más articulaciones hinchadas y 3 o más articulaciones sensibles) en al menos una de las siguientes formas: (1) compromiso interfalángico distal (DIP), (2) artritis poliarticular (ausencia de nódulos reumatoides y presencia de psoriasis); (3) artritis mutilante; (4) artritis psoriásica asimétrica; o (5) espondilitis como anquilosis. Los pacientes también tenían placas psoriásicas con una lesión objetivo cualificada = a 2 cm de diámetro. Los pacientes se habían tratado previamente con AINES (86%), DMARDs (80%) y corticoesteroides (24%). Los pacientes que en ese momento se estaban tratando con metotrexato (estables durante 2 o más meses) pudieron continuar a una dosis estable igual o inferior a 25 mg/semana de metotrexato. Se administraron 2 veces a la semana dosis subcutáneas de 25 mg de ENBREL® (con base en los hallazgos relacionados con la dosis en estudios con pacientes con artritis reumatoide) o placebo durante 6 meses. Al final del estudio doble ciego, los pacientes podían ingresar a un estudio de extensión de etiqueta abierta de largo plazo de 2 años de duración total.
Las respuestas clínicas se expresaron como porcentajes de pacientes que alcanzaron las respuestas ACR 20, 50 y 70 y porcentajes de mejoría en los Criterios de Respuesta de Artritis Psoriásica (PsARC).
La siguiente tabla resume los resultados
|
Respuestas de pacientes con artritis psoriásica en el estudio controlado con placebo |
||
|
Porcentaje de Pacientes |
||
|
Respuesta de la artritis psoriásica |
Placebo |
ENBREL®a |
|
ACR 20 |
||
|
Mes 3 |
15 |
59b |
|
Mes 6 |
13 |
50b |
|
ACR 50 |
||
|
Mes 3 |
4 |
38b |
|
Mes 6 |
4 |
37b |
|
ACR 70 |
||
|
Mes 3 |
0 |
11b |
|
Mes 6 |
1 |
9c |
|
PsARC |
||
|
Mes 3 |
31 |
72b |
|
Mes 6 |
23 |
70b |
|
a: 25 mg ENBREL® subcutáneo dos veces a la semana. b: p < 0,001, ENBREL® vs. placebo c: p < 0,01, ENBREL® vs. placebo |
||
Las respuestas clínicas entre pacientes con artritis psoriásica que recibieron ENBREL® fueron visibles en la primera visita (4 semanas) y se mantuvieron a lo largo de 6 meses de tratamiento. ENBREL® resultó significativamente mejor que el placebo en todas las mediciones de actividad de la enfermedad (p < 0,001), y las respuestas fueron similares con y sin terapia concomitante de metotrexato. Se evaluó la calidad de vida de los pacientes con artritis psoriásica en cada punto del tiempo utilizando el índice de discapacidad del HAQ. El puntaje del índice de discapacidad fue significativamente mejor en todos los puntos del tiempo en los pacientes con artritis psoriásica tratados con ENBREL® en relación con los tratados con placebo (p< 0,001).
En el estudio de artritis psoriásica se evaluaron los cambios radiográficos. Se obtuvieron las radiografías de las manos y las muñecas al inicio del estudio y a los meses 6, 12 y 24. El PTS modificado a los 12 meses se presenta en la siguiente tabla. En un análisis en el que todos los pacientes que se retiraron del estudio por alguna razón se consideraron como que presentaron progreso, el porcentaje sin progreso (cambio de PTS <0,05) a los 12 meses era mayor en el grupo de ENBREL® que en el grupo de placebo (73% vs. 47%, respectivamente, p<0,001). El efecto de ENBREL® sobre el progreso radiográfico se mantuvo en pacientes que continuaron el tratamiento hasta el segundo año. Se observó un progreso más lento en el daño de las articulaciones periféricas en pacientes con articulaciones simétricas poliarticulares.
|
Cambio medio (ES) anual en el puntaje sharp total desde el inicio del estudio (TSS) |
||
|
Placebo |
ENBREL® |
|
|
Tiempo |
(n=104) |
(n=101) |
|
Mes 12 |
1,00 (0,29) |
-0,03 (0,09)a |
|
ES = error estándar |
||
El tratamiento de ENBREL® mejoró la función física durante el periodo doble ciego, y este beneficio se mantuvo durante la exposición de largo plazo de hasta 2 años.
No existe evidencia suficiente de la eficacia de ENBREL® en pacientes con artritis similar a espondilitis anquilosante y artropatías psoriásicas mutilantes debido al número pequeño de pacientes estudiados.
No se han realizado estudios en pacientes con artritis psoriásica utilizando un régimen de dosis de 50 mg una vez a la semana. La evidencia de eficacia para el régimen de dosis una vez a la semana para esta población de pacientes se basa en los datos de estudios en pacientes con espondilitis anquilosante.
• Pacientes adultos con espondilitis anquilosante.
La eficacia de ENBREL® en la espondilitis anquilosante se evaluó en 3 estudios doble ciego, aleatorizados que comparan la administración de 25 mg de ENBREL® dos veces a la semana con placebo. Un total de 401 pacientes fueron incluidos en el estudio, de los que 203 se trataron con ENBREL®. El mayor de estos estudios (n = 277) incluyó a pacientes de edades comprendidas entre 18 y 70 años y que tenían espondilitis anquilosante activa definida según los marcadores de la escala analógica visual (EAV) de = 30 para un promedio de duración e intensidad de rigidez matutina y marcadores de la escala analógica visual = 30 para al menos 2 de los siguientes 3 parámetros: evaluación global del paciente; la media de los valores de la EAV para dolor de espalda nocturno y dolor de espalda total; media de 10 preguntas sobre el índice funcional de espondilitis anquilosante (IFEA). Los pacientes que recibieron DMARDs, AINES o corticoesteroides pudieron continuar con ellos a dosis estables. No se incluyeron en el estudio pacientes con anquilosis completa de la columna. Se administraron subcutáneamente dosis de 25 mg de ENBREL® (con base en los hallazgos relacionados con la dosis en estudios con pacientes con artritis reumatoide) o placebo dos veces por semana durante 6 meses en 138 pacientes.
La medida primaria de eficacia (ASAS20) era una mejoría = 20% en al menos 3 de los 4 dominios de la evaluación de espondilitis anquilosante (ASAS) (evaluación global de paciente, dolor de espalda, IFEA e inflamación) y ausencia de deterioro en los dominios restantes. Las respuestas ASAS 50 y 70 utilizaron los mismos criterios con mejoría del 50% y del 70%, respectivamente. Comparado con placebo, el tratamiento con ENBREL® resultó en mejoras significativas en la respuesta ASAS 20, ASAS 50 y ASAS 70, a las 2 semanas después del inicio del tratamiento.
|
RESPUESTAS DE PACIENTES CON ESPONDILITIS ANQUILOSANTE EN UN ESTUDIO CONTROLADO CON PLACEBO |
||
|
Porcentaje de Pacientes |
||
|
Respuesta de la espondilitis anquilosante |
Placebo |
ENBREL® |
|
ASAS 20 |
||
|
2 semanas |
22 |
46ª |
|
3 meses |
27 |
60ª |
|
6 meses |
23 |
58ª |
|
ASAS 50 |
||
|
2 semanas |
7 |
24ª |
|
3 meses |
13 |
45ª |
|
6 meses |
10 |
42ª |
|
ASAS 70 |
||
|
2 semanas |
2 |
12b |
|
3 meses |
7 |
29b |
|
6 meses |
5 |
28b |
|
a: p < 0,001, ENBREL® vs. placebo b: p = 0,002, ENBREL® vs. placebo |
||
Entre los pacientes con espondilitis anquilosante que recibieron ENBREL®, las respuestas clínicas fueron evidentes en el momento de la primera visita (2 semanas) y se mantuvieron a lo largo de 6 meses de la terapia. Las respuestas fueron similares en pacientes que estaban recibiendo o no terapias concomitantes al inicio del estudio.
En los dos estudios más pequeños de espondilitis anquilosante se obtuvieron resultados similares.
En un cuarto estudio, la seguridad y eficacia de 50 mg de ENBREL® (dos inyecciones subcutáneas de 25 mg) administradas una vez a la semana vs. 25 mg de ENBREL® administrado dos veces a la semana se evaluaron en un estudio doble ciego, controlado por placebo que incluyó 356 pacientes con espondilitis anquilosante activa. Los perfiles de seguridad y eficacia de los regímenes de 50 mg una vez a la semana y 25 mg dos veces a la semana fueron similares.
Pacientes adultos con espondiloartritis axial no radiográfica: Se evaluó la eficacia de ENBREL® en pacientes con espondiloartritis axial no radiográfica (nr-AxSpa, por sus siglas en inglés) en un estudio aleatorizado de 12 semanas, doble ciego controlado con placebo.123 El estudio evaluó a 215 pacientes adultos (población con intención de tratar modificada) con nr-AxSpa activa (18 a 49 años de edad), definidos como los pacientes que cumplen con los criterios de clasificación ASAS de espondiloartritis axial pero que no cumplen con los criterios modificados de Nueva York para SpA. Los pacientes también debían tener una respuesta inadecuada a dos o más AINE. En el periodo a doble ciego, los pacientes recibieron ENBREL® 50 mg semanalmente o placebo durante 12 semanas. La medida primaria de eficacia (ASAS 40) fue un 40% de mejora en al menos tres de los cuatro dominios de ASAS y una ausencia de deterioro en el dominio restante. Se obtuvieron las IRM de la articulación sacroilíaca y la columna para evaluar la inflamación en el punto basal y en la semana 12. El periodo a doble ciego fue seguido por un periodo de etiqueta abierta durante el que todos los pacientes recibieron ENBREL® 50 mg semanalmente por hasta un adicional de 92 semanas.
En comparación con el placebo, el tratamiento con ENBREL® dio como resultado una mejora de importancia estadística en la ASAS 40, ASAS 20 y ASAS 5/6. También se observó una mejora importante para la remisión parcial de ASAS y BASDAI 50. Los resultados de la semana 12 se muestran en la tabla a continuación.
Respuesta de eficacia en el estudio de nr-AxSpa controlado con placebo: porcentaje de pacientes que alcanzaron criterios de valoración
|
Respuestas clínicas a doble ciego en la semana 12 |
Placebo |
ENBREL® |
|
ASAS** 40 |
15,7 |
32,4b |
|
ASAS 20 |
36,1 |
52,4c |
|
ASAS 5/6 |
10,4 |
33,0a |
|
ASAS remisión parcial |
11,9 |
24,8c |
|
BASDAI***50 |
23,9 |
43,8b |
|
*Algunos pacientes no proporcionaron datos completos para cada criterio de valoración **ASAS= Sociedad Internacional de Evaluación de la Espondiloatritis *** Índice de actividad de la espondilitis anquilosante de Bath a: p<0,001, b:<0,01 y c:<0,05, respectivamente entre ENBREL® y placebo |
||
En la semana 12, hubo una mejora de importancia estadística en el puntaje del SPARCC (Consorcio de investigación sobre la Espondiloartritis de Canadá) para la articulación sacroilíaca medida a través de la IRM para pacientes que recibían ENBREL®. El cambio medio ajustado desde el periodo basal fue de 3,8 para los pacientes (p<0,001) tratados con ENBREL® (n=95) en comparación con los tratados con placebo (n=105).
Se evaluó la calidad de vida relativa a la salud y la función física utilizando los cuestionarios de BASFI (índice funcional de la espondilitis anquilosante de Bath), de EuroQol 5D y SF-36. ENBREL® mostró una mejora de importancia estadística superior en el BASFI, el Indicador del estado de salud global EQ5D y el Puntaje del componente físico (PCS) SF-36 desde el punto basal a la semana 12 en comparación con el placebo.
Las respuestas clínicas entre los pacientes nr-AxSpa que recibieron ENBREL® fueron evidentes en la primera consulta (2 semanas) y se mantuvieron durante las 24 semanas del tratamiento.
• Pacientes adultos con psoriasis en placas
La seguridad y eficacia de ENBREL® en pacientes con psoriasis en placas, fueron evaluadas en tres estudios aleatorizados, doble enmascarados y controlados con placebo. En los tres estudios el punto final primario de eficacia fue la proporción de pacientes en cada grupo de tratamiento que alcanzaron el PASI 75 a las 12 semanas (ej. al menos 75% de mejoría en el índice del Área de Psoriasis y en la Severidad –PASI- desde la línea base).
El estudio 1 fue un estudio de Fase 2 en pacientes de 18 años de edad o mayores, con psoriasis en placas activa pero estable clínicamente, y con >10% del área de la superficie corporal involucrada. Ciento doce (112) pacientes fueron asignados de forma aleatoria para recibir una dosis de ENBREL® de 25 mg (n=57) o placebo (n=55) dos veces a la semana por 24 semanas.
El estudio 2 evaluó 652 pacientes con psoriasis crónica en placas y tuvo los mismos criterios de inclusión del estudio 1 con la adición de un PASI mínimo de 10 en la fase de selección. ENBREL® fue administrado a dosis de 25 mg una vez a la semana, 25 mg dos veces a la semana o 50 mg dos veces a la semana por 6 meses consecutivos. Durante las primeras 12 semanas del periodo del tratamiento doble enmascarado, los pacientes recibieron placebo o una de las tres dosis ya mencionadas de ENBREL®. Después de 12 semanas de tratamiento, los pacientes en el grupo placebo comenzaron el tratamiento enmascarado con ENBREL® (25 mg dos veces a la semana); los pacientes en los grupos del tratamiento activo continuaron hasta la semana 24 con la dosis a la que habían sido originalmente asignados de forma aleatoria.
El estudio 3 evaluó 583 pacientes y tuvo los mismos criterios de inclusión del estudio 2. Los pacientes en éste estudio recibieron una dosis de 25 mg o de 50 mg de ENBREL®, o placebo dos veces a la semana por 12 semanas posteriormente todos los pacientes continuaron recibiendo ENBREL® 25 mg con etiqueta abierta dos veces a la semana por 24 semanas adicionales.
En el estudio 1, el grupo tratado con ENBREL® tuvo una proporción significativamente mayor de pacientes con respuesta PASI 75 a la semana 12 (30%) comparado con el grupo tratado con placebo (2%) (p<0,0001). A las 24 semanas, el 56% de los pacientes en el grupo tratado con ENBREL® había alcanzado PASI 75 comparado con el 5% de los pacientes tratados con placebo. Los resultados relevantes de los estudios 2 y 3 son indicados a continuación:
|
RESPUESTAS DE LOS PACIENTES CON PSORIASIS EN LOS ESTUDIOS 2 Y 3 |
||||||||
|
ESTUDIO 2 |
ESTUDIO 3 |
|||||||
|
Placebo |
ENBREL® |
Placebo |
ENBREL® |
|||||
|
25 mg DPS |
50 mg DPS |
25 mg DPS |
50 mg DPS |
|||||
|
n=166 |
n=162 |
n=162 |
n=164 |
n=164 |
n=193 |
n=196 |
n=196 |
|
|
Respuesta |
Sem 12 |
Sem 12 |
Sem 24a |
Sem 12 |
Sem 24a |
Sem 12 |
Sem 12 |
Sem 12 |
|
PASI 50, % |
14 |
58* |
70 |
74* |
77 |
9 |
64* |
77* |
|
PASI 75 % |
4 |
34* |
44 |
49* |
59 |
3 |
34* |
49* |
|
DSGAb, claro o casi claro, % |
5 |
34* |
39 |
49* |
55 |
4 |
39* |
57* |
|
DPS: Dos Veces Por Semana *p < 0,0001 comparado con el placebo a. En la semana 24 del estudio 2, no se realizaron comparaciones estadísticas con el placebo porque el grupo original con placebo comenzó a recibir ENBREL®® DPS de la semana 13 a la 24 b. Dermatologist Static Global Assessment. Claro o casi claro: definido como 0 ó 1 sobre una escala de 0 a 5 |
||||||||
Entre los pacientes con psoriasis en placas que recibieron ENBREL®, se manifestaron respuestas significativas relacionadas con el placebo que se manifestaron en la primera visita (2 semanas), y que se mantuvieron durante las 24 semanas de la terapia.
El estudio 2 también tuvo un periodo de retiro de la medicación durante el cual los pacientes que alcanzaron una mejoría del PASI de al menos 50% a la semana 24, suspendieron el tratamiento. Los pacientes fueron observados fuera del tratamiento por la ocurrencia de rebote (PASI > 150 % de la línea base) y por el tiempo de recaída (definido como la pérdida de al menos la mitad de la mejoría alcanzada entre la línea base y la semana 24). Durante el periodo de retiro, los síntomas de psoriasis retornaron gradualmente con una mediana de tiempo de tres meses para recaída de la enfermedad. No se manifestaron rebotes de la enfermedad ni eventos adversos serios no relacionados con la psoriasis. Hubo alguna evidencia para apoyar el beneficio de re-tratamiento con ENBREL®, en pacientes que respondieron inicialmente al tratamiento.
En el estudio 3, la mayoría de los pacientes (77%) fueron inicialmente asignados de forma aleatoria para recibir 50 mg dos veces por semana y tuvieron la disminución de su dosis a la semana 12 y para recibir 25 mg dos veces por semana manteniendo su respuesta PASI 75 hasta la semana 36. Para los pacientes que recibieron 25 mg dos veces a la semana a través del estudio, la respuesta PASI 75 continuó mejorando entre las semanas 12 y 36.
En los estudios abiertos de larga duración (hasta 34 meses) en los que se administró ENBREL® sin interrupción, la respuesta clínica fue sostenida y la seguridad fue similar a la de los estudios de menor duración.
• Pacientes pediátricos con psoriasis en placas
La eficacia de ENBREL® fue evaluada en un estudio aleatorizado doble ciego controlado con placebo en 211 pacientes pediátricos de 4 a 17 años de edad con psoriasis en placas grave (como se estableció por el puntaje sPGA > 3, que involucra > 10% de BSA y PASI > 12). Los pacientes que eran elegibles para el estudio tenían antecedentes de haber recibido fototerapia o terapia sistémica o fueron controlados inadecuadamente durante la terapia tópica.
Los pacientes recibieron ENBREL® 0,8 mg/kg (hasta 50 mg) o placebo una vez a la semana durante 12 semanas. A la semana 12, más pacientes asignados aleatoriamente a ENBREL® presentaban respuestas positivas de eficacia (por ejemplo: PASI 75) que los pacientes asignados aleatoriamente a placebo.
|
Resultados para Psoriasis Pediátrica en Placas a las 12 Semanas |
||
|
ENBREL® |
Placebo |
|
|
PASI 75, n(%) |
60 (57%)a |
12 (11%) |
|
PASI 50, n(%) |
79 (75%)a |
24 (23%) |
|
sPGA “claro” o “mínimo”, n(%) |
56 (53%) |
14 (13%) |
|
Abreviaturas: sPGA: Evaluación Global por el Médico-estática a. p< 0,0001 comparada con placebo |
||
Después de un periodo de tratamiento doble ciego de 12 semanas, todos los pacientes que ingresaron al periodo de etiqueta abierta recibieron ENBREL® 0,8 mg/kg (hasta 50 mg) una vez a la semana durante 24 semanas adicionales. Las respuestas observadas durante el periodo de etiqueta abierta fueron similares a las observadas en el periodo doble ciego.
Durante un periodo de retiro aleatorizado, significativamente más pacientes que fueron aleatorizados nuevamente a placebo experimentaron recaídas en la enfermedad (pérdida de la respuesta PASI 75) comparados con los pacientes que fueron aleatorizados nuevamente a ENBREL®. Con la terapia continua, la respuesta se mantuvo por hasta 48 semanas.
La seguridad y la eficacia a largo plazo de ENBREL® 0,8 mg/kg (hasta 50 mg) una vez a la semana se evaluó en un estudio de extensión abierto con 181 pacientes pediátricos con psoriasis en placas por hasta 2 años, en el estudio de 48 semanas antes mencionado. La experiencia a largo plazo con ENBREL® fue similar al estudio de 48 semanas y no reveló ningún resultado nuevo con respecto a la seguridad.
INTERFERENCIA CON PRUEBAS DE LABORATORIO Y OTRAS PRUEBAS DE DIAGNÓSTICO:
Efectos en actividades que requieren concentración: No se han realizado estudios sobre los efectos en la habilidad de manejar o utilizar maquinaria o vehículos.
PRECAUCIONES
Reacciones alérgicas: Se han reportado reacciones alérgicas asociadas con la administración de ENBREL®. Si ocurre cualquier reacción alérgica o anafiláctica, la terapia con ENBREL® debe descontinuarse inmediatamente. Ver también la sección Reacciones adversas.
Inmunosupresión: Las terapias anti-FNT, incluyendo ENBREL®, pueden afectar las defensas huésped contra infecciones y los procesos malignos debido a que el FNT actúa como mediador en el proceso inflamatorio y en la modulación de la respuesta celular inmune.
Tumores malignos y desórdenes linfoproliferativos
Tumores malignos sólidos y hematopoyéticos (excluidos cánceres de piel): Se han recibido reportes durante el periodo post-comercialización sobre procesos malignos que afectan varios sitios. En las fases controladas de los estudios clínicos con antagonistas-FNT, se observaron más casos de linfoma en pacientes que recibieron un antagonista-FNT comparados con los pacientes de control. Sin embargo, la aparición de casos fue poco frecuente, y el periodo de investigación de los pacientes del grupo placebo fue menor que el de los pacientes que recibieron la terapia con el antagonista-FNT. Se informaron casos de leucemia en pacientes tratados con antagonistas FNT, existe un riesgo incrementado de eventos de linfoma y leucemia en pacientes con artritis reumatoide con enfermedad inflamatoria de alta actividad y de larga duración, la cual complica la estimación del riesgo. Análisis posteriores de los ensayos clínicos de artritis reumatoide con ENBREL® no han confirmado ni excluido aumento del riesgo de tumores malignos.
Los tumores malignos (en particular los linfomas de Hodgkin y no Hodgkin) algunos mortales, se han reportado en niños y adolescentes que recibieron tratamiento con antagonistas del FNT incluido ENBREL®. La mayoría de los pacientes estaban recibiendo simultáneamente inmunosupresores.
Con base en el conocimiento actual, no se puede descartar un posible riesgo para el desarrollo de linfomas u otro tipo de tumores malignos hematopoyéticos o sólidos en pacientes tratados con antagonistas del FNT.
Cánceres de piel: Se han reportado cánceres de piel melanocítico y no melanocítico (CPNM) en pacientes tratados con antagonistas del FNT que incluían a ENBREL®. Se han reportado muy infrecuentemente casos poscomercialización de carcinoma de células de Merkel en pacientes tratados con etanercept. Se recomiendan exámenes periódicos de la piel para todos los pacientes con mayor riesgo de cáncer de piel.
Al combinar los resultados de las partes controladas de los estudios clínicos con ENBREL®, comparados con el grupo de placebo, la mayoría de los casos de CPNM se observaron en pacientes que recibían ENBREL®, en particular los pacientes con psoriasis.
Reacciones hematológicas: Han sido reportados raros casos de pancitopenia y muy raros casos de anemia aplásica, algunos casos con desenlace fatal en pacientes tratados con ENBREL®. Se debe ejercer especial precaución en pacientes tratados con ENBREL® con historia previa de discrasias sanguíneas. Todos los pacientes deben ser alertados que si desarrollan síntomas o signos que sugieran discrasia sanguínea o infecciones (ejemplo: Fiebre persistente, dolor de garganta, hematomas, hemorragia, palidez) durante el tratamiento con ENBREL® deberán consultar al médico en forma inmediata. Se deberá investigar a estos pacientes en forma urgente incluyéndose un cuadro hemático completo entre las medidas diagnósticas. Si se confirmara la presencia de una discrasia sanguínea se deberá descontinuar la administración de ENBREL®.
Formación de autoanticuerpos: El tratamiento con ENBREL® puede estar asociado con la formación de anticuerpos autoinmunes. Ver también la sección Reacciones adversas.
Vacunas: En un estudio clínico aleatorio, doble enmascarado, controlado con placebo en pacientes con artritis psoriásica, 184 pacientes recibieron también una vacuna neumocócica polisacárida multivalente a la semana 4. En este estudio, mayoría de los pacientes con artritis psoriásica recibiendo ENBREL® tuvieron respuesta de células B luego de recibir la vacuna neumocócica polisacárida, pero los títulos en conjunto fueron moderadamente menores y menos pacientes aumentaron al doble los títulos en comparación con los que no recibían ENBREL®. Se desconoce la significancia clínica de este hallazgo. No se deben administrar vacunas con gérmenes vivos concomitantemente con ENBREL®. Si es posible, el paciente pediátrico debe actualizar sus inmunizaciones de acuerdo a las guías locales vigentes antes de comenzar la terapia con ENBREL®.
• Trastornos neurológicos
Aunque no se han realizado estudios clínicos evaluando la terapia de ENBREL® en pacientes con esclerosis múltiple, ensayos clínicos con otros antagonistas del FNT en pacientes con esta condición han mostrado aumentos en la actividad de la enfermedad. Se han presentado raros reportes de desórdenes desmielinizantes del sistema nervioso central (SNC) en pacientes tratados con ENBREL® (ver la sección Reacciones adversas). Adicionalmente, se han presentado reportes muy raros de polineuropatías periféricas desmielinizantes (incluido el síndrome de Guillain-Barré). Se recomienda una evaluación cuidadosa del riesgo/beneficio, incluyendo una evaluación neurológica, cuando se realiza una terapia con ENBREL® a pacientes con enfermedades desmielinizantes del SNC de reciente aparición o preexistente; o a aquellos que se considera se encuentran en un riesgo aumentado para desarrollar enfermedades desmielinizantes.
Falla cardiaca congestiva: Durante el periodo post-comercialización, se han recibido reportes sobre el empeoramiento de la insuficiencia cardiaca congestiva (ICC), con y sin factores precipitantes identificables en pacientes que están recibiendo ENBREL®. Dos estudios clínicos a gran escala que evaluaban el uso de ENBREL® en el tratamiento de ICC, fueron terminados anticipadamente debido a una falta de eficacia. Aunque no son concluyentes, los datos de uno de estos estudios sugieren una posible tendencia hacia el empeoramiento de la ICC en aquellos pacientes asignados al tratamiento con ENBREL®. Además, un estudio clínico que evalúa el uso del infliximab (un anticuerpo monoclonal que se une al FNT - alfa) en el tratamiento de ICC se terminó de manera temprana debido al incremento en la mortalidad de los pacientes tratados con infliximab. Los médicos deberían tener precaución cuando usen ENBREL® en pacientes que también presenten ICC.
Infecciones: Los pacientes deben ser evaluados en cuanto a infecciones antes, durante y después del tratamiento con ENBREL®, teniendo en cuenta que el promedio de la vida media de eliminación del ENBREL® es de 80 horas (desviación estándar de 28 horas; rango de 7 a 300 horas).
En pacientes que se encontraban recibiendo ENBREL® se han reportado infecciones oportunistas que incluyen infecciones fúngicas invasivas. En algunos casos las infecciones fúngicas y otras infecciones oportunistas no se han reconocido lo que ha conllevado a demoras en el tratamiento apropiado y, en algunas ocasiones, incluso a la muerte. En muchos de los reportes, los pacientes estaban recibiendo también medicamentos concomitantes que incluían inmunosupresores. Durante la evaluación de los pacientes para determinar si existe infección, los médicos deben considerar el riesgo del paciente para infecciones oportunistas relevantes (p. ej.: La exposición a micosis endémica).
Tuberculosis: En pacientes que recibieron agentes bloqueadores del FNT incluyendo ENBREL®, se ha observado tuberculosis (incluyendo la presentación diseminada o extrapulmonar). La tuberculosis se puede deber a la reactivación de la infección de una tuberculosis latente o a una nueva infección.
Antes del inicio de la terapia con ENBREL®, cualquier paciente con riesgo incrementado de tuberculosis debe ser evaluado para la infección activa o latente. La profilaxis de la tuberculosis latente debe ser iniciada antes a la terapia con ENBREL®. Algunos pacientes que eran negativos para TB latente antes de recibir ENBREL® han desarrollado TB activa. Los médicos deben monitorear a los pacientes que reciben ENBREL® para establecer la presencia de signos y síntomas de TB activa, incluyendo los pacientes que eran negativos para infección latente deTB. Las directrices locales que apliquen deben ser consultadas. Pacientes con artritis reumatoide parecen tener una tasa incrementada tuberculosis.
Reactivación de la hepatitis B: Se ha reportado la reactivación de la hepatitis B en pacientes que fueron infectados con el virus de hepatitis B (VHB) con anterioridad y que recibieron agentes anti-FNT incluyendo ENBREL® de manera concomitante. La mayoría de estos reportes han ocurrido en pacientes quienes se encontraban recibiendo concomitantemente otros medicamentos supresores del sistema inmune, los cuales pueden también contribuir a la reactivación de la hepatitis B. Los pacientes con riesgo de infección del VHB deben ser evaluados para evidencia previa de infección del VHB antes del inicio de la terapia anti-FNT.
Debe tenerse precaución cuando ENBREL® sea administrado en pacientes que presentaron infección del VHB con anterioridad. Estos pacientes deben ser monitoreados para detectar signos y síntomas de infección activa del VHB.
Empeoramiento de la hepatitis C: Se han presentado reportes de empeoramiento de la hepatitis C en pacientes que recibían ENBREL®, aunque una relación de causalidad con ENBREL® no ha sido establecida.
Hipoglicemia en pacientes tratados por diabetes: Se han presentado reportes de hipoglicemia después del inicio de ENBREL® en pacientes que están recibiendo medicamentos para la diabetes, en algunos de estos pacientes es necesaria la reducción del medicamento antidiabético.
• Enfermedad intestinal inflamatoria (EII) en pacientes con artritis idiopática juvenil (AIJ):
Se han presentado reportes de EII en pacientes con AIJ tratados con ENBREL®, el cual no es efectivo para el tratamiento de la EII. Una relación causal con ENBREL® no es clara debido a que las manifestaciones clínicas de inflamación intestinal se han observado también en pacientes con AIJ no tratados.
ADVERTENCIAS ESPECIALES
Infecciones: Durante la utilización de ENBREL® se han reportado infecciones serias, que incluyen sepsis y tuberculosis (TB) (ver Reacciones adversas). Algunas de estas infecciones han sido mortales. Estas infecciones se produjeron por bacterias, micobacterias, hongos, virus y parásitos (incluidos protozoos). También se han reportado infecciones oportunistas (incluidas listeriosis y legionelosis). Los pacientes que desarrollen una infección nueva mientras reciben tratamiento con ENBREL® deben ser monitorizados cuidadosamente. La administración de ENBREL® debe descontinuarse si el paciente desarrolla una infección seria. Debe tenerse especial cautela cuando se considere el uso de ENBREL® en pacientes con historia de infecciones crónicas, recurrentes o con condiciones subyacentes que puedan predisponer el paciente a infecciones. Ver secciones Contraindicaciones, Precauciones y Reacciones adversas.
Tratamiento concurrente con anakinra: La administración concomitante de ENBREL® y anakinra ha sido asociada con aumento del riesgo de infecciones serias y neutropenia. No se ha demostrado aumento de los beneficios clínicos de esta combinación, por lo que su uso no es recomendado. Ver sección Interacciones.
Tratamiento concurrente con abatacept: En estudios clínicos, la administración concomitante de abatacept y ENBREL® ha mostrado un incremento en la incidencia de eventos adversos serios. Esta combinación no ha demostrado un incremento en los beneficios clínicos, por lo tanto no se recomienda su uso. (Ver sección Interacciones).
Granulomatosis de Wegener: En un estudio placebo-controlado con 180 pacientes que padecían de Granulomatosis de Wegener, la adición de etanercept al tratamiento estándar (incluyendo ciclofosfamida y altas dosis de esteroides) no fue más efectiva que el tratamiento estándar solo. El grupo de pacientes que recibieron ENBREL® experimentaron más malignidades no cutáneas de varios tipos, que el grupo de pacientes que recibieron el tratamiento estándar solo. No está recomendado el uso de etanercept para el tratamiento de la Granulomatosis de Wegener.
Hepatitis alcohólica: En un estudio con 48 pacientes hospitalizados tratados con ENBREL® o placebo por hepatitis alcohólica moderada a grave [puntaje medio de acuerdo con el Modelo de Enfermedad Hepática Terminal (MELD) = 25], ENBREL® no fue eficaz y después de 6 meses la tasa de mortalidad en los pacientes tratados con ENBREL® fue significativamente más alta. Las infecciones fueron también mayores en el grupo de ENBREL®. No se recomienda la utilización de ENBREL® para el tratamiento de la hepatitis alcohólica. Los médicos deben tener precaución cuando utilizan ENBREL® en pacientes que presentan también hepatitis alcohólica severa a moderada.
La cubierta de la aguja de la jeringa prellenada contiene látex (caucho natural seco). Antes de utilizar ENBREL®, los pacientes, las personas a cargo de su cuidado quien va a suministrar ENBREL® deben contactar a su médico si la cubierta de la aguja va a ser manipulada por alguien con hipersensibilidad conocida o posible (alergia) al látex.
Los pacientes mayores de 65 años de edad y los que toman inmunosupresores concomitantes pueden estar en mayor riesgo de infección.
La terapia empírica antifúngica debe considerarse en pacientes con riesgo de infecciones fúngicas invasivas que desarrollan una enfermedad sistémica grave.
Existe un posible riesgo de aparición con el uso de los inhibidores de los factores de necrosis tumoral, solos o asociados a otros inmunosupresores de linfoma hepatoesplénico de células T y cáncer de piel diferentes a melanomas.
Información adicional para los pacientes
• Los Bloqueadores TNFa pueden disminuir la capacidad del sistema inmunológico para combatir infecciones.
• Los pacientes deben informar a su médico si está siendo tratados por una infección o si tienen infecciones que reaparecen.
• Los pacientes deben leer la Guía del Medicamento que acompaña a su receta para un bloqueador de TNFa.
• Los pacientes deben comunicarse con su profesional de la salud si tienen preguntas o inquietudes acerca de los bloqueadores de TNFa.
Información adicional para los profesionales de la salud
• Los pacientes tratados con bloqueadores de TNFa están en mayor riesgo de desarrollar infecciones graves que pueden afectar múltiples órganos produciendo así una hospitalización o incluso la muerte.
• El riesgo de infección con los patógenos bacterianos Legionella y Listeria se debe añadir a las advertencias para toda la clase de los bloqueadores del TNF.
• Los riesgos y los beneficios de los bloqueadores TNF se deben considerar antes de iniciar el tratamiento en pacientes con infección crónica o recurrente y en pacientes con condiciones subyacentes que puedan predisponer a la infección.
• Pacientes mayores de 65 años de edad y los pacientes que toman inmunosupresores concomitantes pueden estar en mayor riesgo de infección.
• Antes de iniciar los bloqueadores de TNFa y periódicamente durante el tratamiento, los pacientes deben ser evaluados para la tuberculosis activa y prueba de la infección latente.
• Los pacientes deben ser monitorizados para detectar signos y síntomas de las infecciones graves mientras está tomando bloqueadores TNFa.
• La terapia empírica anti fúngica debe ser considerada en pacientes con riesgo de infecciones fúngicas invasivas que desarrollan una enfermedad sistémica grave.
• Los profesionales sanitarios deben animar a los pacientes a leer la Guía del Medicamento que acompaña a su receta para un bloqueador de TNF.
DOSIFICACIÓN Y ADMINISTRACIÓN
• Uso en adultos
Artritis reumatoide, artritis psoriásica, espondilitis anquilosante y espondiloartritis axial no radiográfica: Pacientes de 18 años de edad ó mayores: 50 mg de ENBREL® administrados una vez a la semana, en dosis única como inyección subcutánea.
En adultos, el tratamiento con metotrexato, glucocorticoides, salicilatos, medicamentos antiinflamatorios no esteroides (AINES) o analgésicos puede continuar durante el tratamiento con ENBREL®.
Psoriasis en Placas: La dosis de ENBREL® es de 50 mg una vez a la semana. Se pueden alcanzar mayores respuestas si se inicia con una dosis de 50 mg suministrada dos veces a la semana por hasta 12 semanas, seguidas, por una dosis de 50 mg una vez a la semana.
Los pacientes adultos se pueden tratar intermitente o continuamente, con base en el criterio médico y las necesidades específicas del paciente (ver Farmacodinamia y eficacia clínica). El tratamiento se debe descontinuar en pacientes que no presentan ninguna respuesta después de 12 semanas. Durante la utilización intermitente, los ciclos del tratamiento posteriores al ciclo inicial deben utilizar una dosis de 50 mg una vez a la semana.
• Población pediátrica
La dosificación de ENBREL® en pacientes pediátricos se basa en el peso corporal. Los pacientes que pesan menos de 62,5 kg se deben dosificar de forma exacta por mg/kg (para información sobre dosificación en indicaciones específicas ver más adelante). Los pacientes que pesan 62,5 kg o más se pueden dosificar utilizando una jeringa prellenada de dosis fija o un autoinyector.
Artritis idiopática juvenil (2 años de edad y mayores): Niños (³2 a <18 años): 0,4 mg/Kg (hasta un máximo de 25 mg por dosis) dos veces por semana (con un intervalo de 72 a 96 horas entre las dosis), o 0.8 mg/kg (hasta un máximo de 50 mg por dosis) una vez por semana.
En niños, el tratamiento con glucocorticoides, medicamentos antiinflamatorios no esteroides (AINES) o analgésicos se puede continuar durante el tratamiento con ENBREL®.
ENBREL® no ha sido estudiado aún en niños <2 años de edad.
Psoriasis pediátrica en placas (6 años de edad y mayores): Niños (>6 a <18 años): 0,8 mg/kg (hasta un máximo de 50 mg por dosis) una vez a la semana hasta por 24 semanas. El tratamiento se debe descontinuar en los pacientes que no presentan respuesta al tratamiento después de 12 semanas.
Si está indicado el retratamiento con ENBREL®, se debe acatar la recomendación anterior relacionada con la duración del tratamiento. La dosis debe ser de 0,8 mg/kg (hasta un máximo de 50 mg por dosis) una vez a la semana.
• Ancianos (= 65 años de edad): No se requiere ajuste de la dosis.
• Deterioro renal: No se requiere ajuste de la dosis.
• Deterioro hepático: No se requiere ajuste de la dosis.
• Método de administración: Administrar ENBREL® como inyección subcutánea en el muslo, abdomen o en la parte superior del brazo. Dejar un espacio de al menos 3 cm entre el nuevo sitio de inyección y el sitio anterior. No inyecte en áreas donde la piel este sensible, con hematoma, enrojecida o dura.
Los pacientes o sus cuidadores que están administrando ENBREL® deben ser instruidos sobre las técnicas de inyección. La primera inyección debe ser aplicada bajo supervisión de un profesional de la salud calificado si es que ENBREL® es para ser administrado por el mismo paciente o su cuidador.
Solución para inyección de jeringa prellenada: Antes de la inyección, se debe permitir que la jeringa prellenada o autoinyector de único uso de ENBREL® alcance la temperatura ambiente (aproximadamente 15 a 30 minutos). La tapa de la jeringa no debe ser removida mientras la jeringa prellenada o autoinyector alcanza la temperatura ambiente. La solución debe ser clara a ligeramente opalescente, incolora o amarilla pálida y puede contener pequeñas partículas traslúcidas o blancas de proteína.
Solución para inyección en Autoinyector MYCLIC: Antes de la inyección, se debe permitir que la jeringa prellenada o autoinyector de único uso de ENBREL® alcance la temperatura ambiente (aproximadamente 15 a 30 minutos). La tapa de la jeringa no debe ser removida mientras la jeringa prellenada o autoinyector alcanza la temperatura ambiente. Observando a través de la ventana de inspección, la solución debe ser clara a ligeramente opalescente, incolora o amarilla pálida y puede contener pequeñas partículas traslúcidas o blancas de proteína.
Ver también Instrucciones para la preparación y administración de la inyección de ENBREL®.
SOBREDOSIS: La dosis máxima tolerada de ENBREL® no ha sido establecida en humanos. Dosis únicas intravenosas hasta de 60 mg/m2 han sido administradas a voluntarios sanos en un estudio de endotoxemia sin evidencia de toxicidad dosis-limitante. El nivel de dosis más alto evaluado en pacientes con artritis reumatoide ha sido una dosis intravenosa de 32 mg/m2 seguido por dosis subcutáneas de 16 mg/m2 (~ 25 mg) administrado dos veces a la semana.
El etanercept no indujo letalidad o signos notables de toxicidad en ratones y ratas luego de una dosis subcutánea única de 2000 mg/Kg o una dosis intravenosa única de 1000 mg/Kg. El etanercept no dio lugar a una dosis limitante o una toxicidad del órgano blanco buscado en simios cynomolgus luego de la administración de dos dosis subcutáneas por semana, durante 4 ó 26 semanas consecutivas a una dosis (15 mg/kg) que resultó en una concentración droga sérica basadas en el AUC, 27 veces mayor que la obtenida a la dosis recomendada de 25 mg en humanos.
No se observaron toxicidades limitadas por la dosis durante los estudios clínicos de pacientes con artritis reumatoide.
No se conoce ningún antídoto para ENBREL®.
DESCRIPCIÓN:
Ingrediente activo: Etanercept.
Etanercept es una proteína de fusión Fc p75 del receptor factor de necrosis tumoral humano producido por tecnología ADN recombinante en ovario de hámster chino (OHC) del sistema de expresión de células de mamíferos. Etanercept es una proteína dimérica de fusión producida genéticamente, consistente en un ligando extracelular unido a la porción del receptor del factor de necrosis tumoral humano-2 (RFNT2/p75) enlazado a la porción Fc de la IgG1 humana. El componente Fc contiene la unión CH2 y CH3 pero no el dominio CH1 de IgG1.
Solubilidad: Etanercept es soluble en agua.
Peso molecular: (Aparente) 150 kilodaltons.
Características físicas: La solución para inyección en la jeringa prellenada es clara a levemente opalescente, incolora o amarilla pálida y puede contener partículas de proteína pequeñas translúcidas o blancas, con un pH de 6.3 + 0.2.
Nombre Comercial: ENBREL®.
MYCLIC® es la marca comercial del dispositivo autoinyector que se encuentra disponible para ENBREL® 50 mg.
Clase farmacológica y terapéutica: Inhibidor del factor de necrosis tumoral alfa (FNT alfa).
Código ATC: L04AB01
Formas de dosificación y rutas propuestas de administración: Solución para inyección en jeringa prellenada y autoinyector.
La vía de administración es subcutánea.
PRESENTACIÓN DE AUTOINYECTOR MYCLIC DE ENBREL®
Esta sección se encuentra dividida dentro de las siguientes subsecciones
• Introducción.
• Paso 1: Preparación para una inyección.
• Paso 2. Elección del sitio de inyección.
• Paso 3: Inyección de la solución de ENBREL®.
• Paso 4: Disposición del autoinyector MYCLIC utilizado.
Introducción: Las siguientes instrucciones explican cómo utilizar el autoinyector MYCLIC para inyectar ENBREL®. Por favor léalas cuidadosamente y sígalas paso a paso. Su médico o enfermera le indicarán como inyectar ENBREL®. No intente aplicar la inyección hasta que esté seguro que comprende apropiadamente la utilización del autoinyector MYCLIC. Si tiene preguntas sobre la forma de realizar la inyección, pida ayuda a su médico o enfermera.
Diagrama 1
Autoinyector MYCLIC
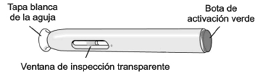
Paso 1. Preparación de la inyección de ENBREL®
• Seleccione una superficie plana, limpia y bien iluminada.
• Reúna los elementos que necesita para la inyección en la superficie seleccionada:
— Un autoinyector y una torunda de alcohol (tómelos de la caja de autoinyectores que tiene en su refrigerador). No agite el autoinyector.
— Un copo de algodón o una gasa.
• Inspeccione la solución en el autoinyector mirando a través de la ventana de inspección transparente. La solución debe ser clara o levemente opalescente, incolora o amarilla pálida y puede contener partículas de proteína pequeñas, blancas o casi transparentes. Esta apariencia es normal para el ENBREL®. No utilice la solución si la observa decolorada, turbia o si están presentes partículas diferentes a las antes mencionadas. Si le preocupa la apariencia de la solución, contacte a su médico, enfermera o farmacéutico para asistencia.
• Deje la tapa blanca de la aguja en su lugar y espere aproximadamente 15 a 30 minutos para permitir que la solución de ENBREL® en el autoinyector alcance la temperatura ambiente. Esperar hasta que la solución alcance la temperatura ambiente hará más confortable la inyección para usted. No caliente de ninguna otra forma. Deje siempre el autoinyector fuera de la vista y el alcance de los niños.
Mientras espera que la solución en el autoinyector alcance la temperatura ambiente, lea el Paso 2 y seleccione el sitio de inyección.
Paso 2. Selección del sitio de inyección
• El sitio de inyección recomendado es el centro de la parte frontal de los muslos. Si lo prefiere, puede utilizar el área del estómago, pero asegúrese de seleccionar un sitio a una distancia de al menos 5 cm del ombligo. Si otra persona le está aplicando la inyección, se puede utilizar el área externa de los brazos.
Diagrama 2

• Cada inyección se debe administrar al menos a 3 cm de donde se realizó la última inyección. No inyecte en áreas de la piel que presenten sensibilidad, enrojecimiento o rigidez. Evite áreas con cicatrices o estrías (podría ser útil mantener un registro sobre los lugares donde se realizaron las inyecciones anteriores).
• Si tiene psoriasis, trate de no inyectar directamente sobre piel levantada, gruesa, roja o escamosa.
Paso 3: Inyección de la solución de ENBREL®
• Después de esperar aproximadamente 15-30 minutos para que la solución del autoinyector se caliente a temperatura ambiente, lave sus manos con jabón y agua.
• Limpie el sitio de inyección con una torunda de alcohol, realizando movimientos circulares y deje secar. No toque nuevamente esta área antes de administrar la inyección.
Tome el autoinyector y retire la tapa blanca de la aguja halándola en dirección recta (ver Diagrama 3). Para evitar el daño de la aguja dentro del autoinyector, no doble la tapa blanca de la aguja cuando la esté retirando y no vuelva a colocarla después de haberla retirado. Después de retirar la tapa de la aguja, observará un protector de seguridad de la aguja morado que se extiende levemente desde el extremo del autoinyector. La aguja continuará estando protegida dentro del autoinyector hasta que se active el autoinyector.
Diagrama 3
Tapa blanca de la aguja
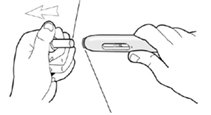
• Pellizcar suavemente la piel con el pulgar y el índice de la mano libre puede facilitar y hacer más confortable la inyección.
• Sin presionar el botón verde de activación de la parte superior del autoinyector, sostenga el autoinyector en ángulo recto (90º) con respecto al sitio de inyección y presione el extremo abierto del autoinyector firmemente contra la piel de modo que el protector de seguridad de la aguja se hunda completamente dentro del autoinyector. Observará una depresión leve sobre la piel (ver Diagrama 4). Observe que el botón verde de activación permanecerá asegurado y el autoinyector no se activará a menos que el protector de la aguja se hunda completamente dentro del autoinyector.
Diagrama 4
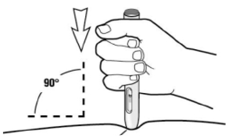
• Mientras empuja firmemente el autoinyector contra la piel para asegurarse de que el protector de seguridad de la aguja se hunda completamente dentro del autoinyector, presione y libere inmediatamente el botón verde sobre la parte superior del autoinyector con su dedo pulgar para iniciar la inyección (ver Diagrama 5). Al presionar el botón escuchará un clic. Continúe sosteniendo el autoinyector firmemente contra la piel hasta que escuche un segundo clic o hasta que hayan transcurrido 10 segundos después del primer clic (lo que ocurra primero).
Nota: Recuerde retirar su dedo pulgar del botón una vez escuche el primer clic o de lo contrario no se escuchará el segundo clic cuando se termine la inyección. No necesita mantener el dedo pulgar sobre el botón para inyectar ENBREL®.
Diagrama 5
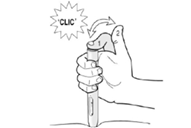
• Al escuchar el segundo “clic” (o, si no escucha el segundo “clic”, después de que hayan transcurrido 10 segundos), se habrá finalizado la inyección (ver Diagrama 6). Ahora puede levantar el autoinyector de la piel (ver Diagrama 7). Cuando levante el autoinyector, el protector de seguridad de la aguja morado se extenderá automáticamente cubriendo la aguja.
Diagrama 6 Diagrama 7
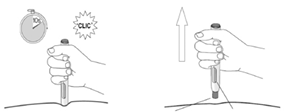
• La ventana de inspección del autoinyector ahora tendrá un color completamente morado, confirmando que la dosis se inyectó correctamente. Si la ventana no está completamente morada, comuníquese con su enfermera o farmacéutico para obtener ayuda, puesto que el autoinyector posiblemente no haya inyectado completamente la solución de ENBREL®. No trate de utilizar el autoinyector nuevamente y no trate de utilizar otro autoinyector sin aprobación de la enfermera o farmacéutico.
• Si observa una mancha de sangre en el sitio de inyección, presione con el copo de algodón o la gasa el sitio de inyección durante 10 segundos. No frote el sitio de inyección.
Paso 4: Disposición del autoinyector MYCLIC utilizado
• El autoinyector se debe utilizar solamente una vez – nunca se deberá reutilizar. Deseche el autoinyector utilizado en la forma indicada por el médico, la enfermera o el farmacéutico.
Si usted tiene alguna pregunta sobre la aplicación por favor consulte a su médico, enfermera o farmacéutico quienes son las personas más familiarizadas con ENBREL®.
Información adicional para el paciente
• Los profesionales sanitarios deben animar a los pacientes a leer el inserto que acompaña a su receta para un bloqueador de TNF.
• Los Bloqueadores TNFa puede disminuir la capacidad del sistema inmunológico para combatir infecciones.
• Los pacientes deben informar a su médico si están siendo tratados por una infección o si tienen infecciones que reaparecen.
• Los pacientes deben leer el inserto que acompaña a su receta para un bloqueador de TNFa.
• Los pacientes deben comunicarse con su profesional de la salud si tienen preguntas o inquietudes acerca de los bloqueadores de TNFa.
Es posible que la información de prescripción de este producto haya sido revisada y actualizada después de la fecha de impresión del PLM 2016. Para obtener información más actualizada comuníquese con la Dirección Médica de Pfizer S.A.S Teléfono: (1) 6002300 Ext. 2509 Bogotá – Colombia.
ENBREL® 25 mg Solución para inyección (Reg. San. INVIMA 2007M-0007384).
ENBREL® 50 mg Solución para inyección (Reg. San. INVIMA 2007M-0007375).
Título del Documento de Producto: ENBREL®
Fecha de CDS reemplazado: 04 de febrero de 2014
Fecha Efectiva: 25 de marzo de 2014
Versión CDS: 36.0
LPD_Etan_Col_25Apr2014_CDSv36.0_Draft.
PFIZER S.A.S.
ALMACENAMIENTO Y TIEMPO DE VIDA ÚTIL: ENBREL® debe ser almacenado refrigerado entre 2 °C a 8 °C (36 °F a 46 °F). No congelar.
Mantener las jeringas prellenadas y autoinyectores en la caja externa para proteger de la luz.
MANIPULACIÓN: La tapa que protege a la aguja de la Jeringa Prellenada y del Autoinyector MYCLIC contiene látex (caucho natural seco). Los pacientes o sus cuidadores deben contactar a su doctor antes de usar ENBREL®, si la tapa de la aguja será manipulada o si el producto será administrado a personas con hipersensibilidad (alergia) posible o conocida al látex.
Los pacientes o sus cuidadores quienes van a administrar ENBREL® deben ser instruidos acerca de cómo se desechan apropiadamente la jeringa y la aguja, y deben ser advertidos sobre la no reutilización de estos elementos.
Los materiales desechables, jeringas y droga no utilizadas deben eliminarse de acuerdo con los requisitos locales.
Ver también la sección Instrucciones para preparación y administración de la inyección de ENBREL® - Exclusivamente para uso subcutáneo”