
ERANZ 5 mg/ERANZ 10 mg
DONEPEZILO
Tabletas
Tabletas recubiertas, 5 y 10 mg
Para visualizar el contenido completo de la IPPA (información para prescribir amplia), deberá iniciar sesión.
INDICACIÓN TERAPÉUTICA: ERANZ® está indicado para el tratamiento sintomático de la demencia del tipo Alzheimer leve, modera y grave. El diagnóstico de demencia tipo Alzheimer se debe realizar teniendo en cuenta las directrices aceptadas (por ejemplo: DSM IV, ICD 10).1,2
PARTICULARIDADES FARMACÉUTICAS
Incompatibilidades: Ninguna.
PROPIEDADES FARMACOLÓGICAS: El clorhidrato de donepezilo es un inhibidor específico y reversible de la acetilcolinesterasa, la colinesterasa predominante en el cerebro. El Donepezilo es un inhibidor de esta enzima, con una potencia 1000 veces mayor que la enzima butirilcolinesterasa, presente principalmente fuera del sistema nervioso central.43
Enfermedad de Alzheimer leve a moderada: En pacientes con demencia de Alzheimer que participaron en ensayos clínicos, la administración de dosis diarias únicas de 5 mg o 10 mg de Clorhidrato de Donepezilo produjo inhibición estable de la actividad de la acetilcolinesterasa (medida en membranas eritrocíticas) de 63,6% y 77,3% respectivamente.4,5 La inhibición de la acetilcolinesterasa (AChE, por sus siglas en inglés) por el Clorhidrato de Donepezilo en los glóbulos rojos ha demostrado correlación con los cambios en ADAS-cog4,5, una escala de sensibilidad que examina algunos aspectos de la cognición.4444 No se ha estudiado el potencial del Clorhidrato de Donepezilo para alterar el curso de la neuropatología subyacente.
En los ensayos clínicos con pacientes con enfermedad de Alzheimer moderadamente grave, al finalizar el tratamiento de 6 meses con Clorhidrato de Donepezilo, se realizo un análisis utilizando una combinación de tres criterios de eficacia: el ADAS-Cog, la Entrevista del Clínico Basada en la Impresión de Cambio con Aportes del Cuidador CIBIC-Plus, por sus sigla en inglés - una medida de función global)45 y los Dominios Combinados de las Actividades de la Vida Diaria de la Escala de Valoración Clínica de la Demencia (CDRS por sus siglas en inglés, una medida de las capacidades en los aspectos comunitario, hogar y pasatiempos y cuidado personal)46.
Los pacientes que reunieron los criterios que se listan a continuación fueron considerados pacientes que respondieron al tratamiento:
Respuesta
• Mejoría en el ADAS-Cog de al menos 4 puntos.
• Ningún deterioro de los puntajes en el CIBIC-Plus.
• Ningún deterioro en los Dominios Combinados de Actividades de la Vida Diaria de la escala de valoración clínica de la demencia.
|
Grupo de |
% Respuesta |
|
|
Población con Intención de Tratamiento |
Población Evaluada |
|
|
Placebo |
10% |
10% |
|
Donepezilo 5 mg |
18%* |
18%* |
|
Donepezilo 10 mg |
21%* |
22%** |
|
*p<0,05; ** p<0,01 |
||
El clorhidrato de Donepezilo produjo un aumento estadísticamente significativo relacionado con la dosis en el porcentaje de pacientes que fueron considerados respondedores al tratamiento (Figura1). Los porcentajes de pacientes asignados aleatoriamente que completaron el estudio fueron: Placebo 80%; 5 mg/día 85% y 10 mg/día 68%.
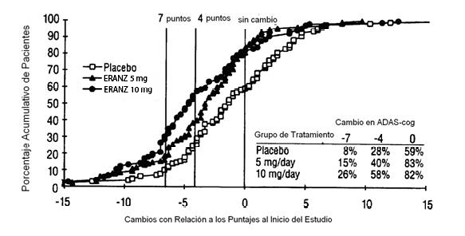
Figura 1. Porcentaje Acumulativo de Pacientes que Completaron 24 semanas de Tratamiento Doble Ciego con Cambios Específicos con Respecto a los Puntajes ADAS-Cog al Inicio del Estudio
Las curvas demuestran que los pacientes asignados a placebo o a Clorhidrato de Donepezilo tienen un rango amplio de respuestas, pero que los grupos con el tratamiento activo tienen mayor probabilidad de presentar mayor mejoría. Una curva correspondiente a un tratamiento efectivo debe desplazarse a la izquierda de la curva de placebo, mientras que una curva de un tratamiento no efectivo o nocivo debe sobreponerse o desplazarse a la derecha de la curva de placebo, respectivamente.
La Figura 2 es un histograma de la distribución de frecuencias de los Puntajes CIBIC-Plus obtenidos por los pacientes asignados a cada uno de los 3 grupos de tratamientos, que completaron 24 semanas de tratamiento. Las diferencias medias entre el medicamento y el placebo para estos grupos de pacientes fueron respectivamente 0,35 unidades y 0,39 unidades para 5 mg/día y 10 mg/día de Clorhidrato de Donepezilo, respectivamente. Las diferencias fueron estadísticamente significativas. No existió diferencia estadísticamente significativa entre los 2 tratamientos activos.
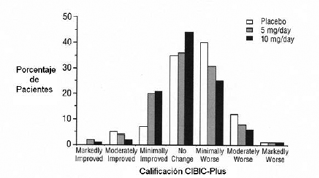
Figura 2. Distribución de Frecuencias de los Puntajes CIBIC-Plus en la Semana 24 para el tratamiento con Clorhidrato de Donepezilo.
Enfermedad de Alzheimer Grave
Estudio Sueco de 6 meses: La efectividad de Clorhidrato de Donepezilo como un tratamiento para la Enfermedad de Alzheimer grave se demostró mediante los resultados de un estudio clínico aleatorio doble ciego controlado con placebo realizado en Suecia (Estudio de 6meses) en pacientes con probable o posible Enfermedad de Alzheimer diagnosticada mediante los criterios NINCDS-ADRDA y DSM-IV, MMSE: Rango de 1 a 10 47. Doscientos cuarenta y ocho (248) pacientes con Enfermedad de Alzheimer grave fueron asignados aleatoriamente a Clorhidrato de Donepezilo o placebo. Para los pacientes asignados aleatoriamente a Clorhidrato de Donepezilo el tratamiento se inició con 5 mg una vez al día durante 28 días y posteriormente se incrementó a 10 mg una vez al día. Al final de periodo de 6 meses, 90,5% de los pacientes tratados con Clorhidrato de Donepezilo estaban recibiendo una dosis de 10 mg. La media de la edad de los pacientes fue 84,9 años con un rango de 59 a 99 años. Aproximadamente 77% de los pacientes eran mujeres y 23% eran hombres. Casi todos los pacientes eran caucásicos. A la mayoría de los pacientes se les diagnosticó probable enfermedad de Alzheimer (EA) (83,6% de los pacientes tratados con Clorhidrato de Donepezilo y 84,2% de los pacientes tratados con placebo).
Mediciones de los resultados del estudio: La efectividad del tratamiento con Clorhidrato de Donepezilo se determinó utilizando una estrategia dual de evaluación de resultados que evaluó la función cognitiva utilizando un instrumento diseñado para pacientes con mayor deterioro y el desempeño general a través la evaluación realizada por el cuidador. Este estudio demostró que los pacientes bajo tratamiento con Clorhidrato de Donepezilo experimentan mejora significativa en ambas medidas cuando se comparan con placebo.
La habilidad del Clorhidrato de Donepezilo para mejorar el desempeño cognitivo fue evaluada con la Batería de Deterioro Severo (SIB por sus siglas en inglés)48. La SIB, un instrumento de múltiples ítems, fue validada para la evaluación de la función cognitiva en pacientes con demencia moderadamente grave a grave. La SIB evalúa aspectos específicos del desempeño cognitivo, que incluyen elementos de la memoria, el lenguaje, la orientación, la atención, la praxis, la habilidad visuoespacial, construcción e interacción social. El rango de puntaje de la SIB va de 0 a 100, el menor puntaje indica mayor deterioro cognitivo.
El desempeño diario se evaluó utilizando el Inventario de Actividad de la Vida Diaria para la Enfermedad de Alzheimer Grave del Estudio Cooperativo Modificado de la Enfermedad de Alzheimer (ADCS-ADL-severe, por sus siglas en inglés)49. El ADCS-ADL-severe se derivó del Inventario de Actividades de la Vida Diaria del Estudio Cooperativo de la Enfermedad de Alzheimer, que es una batería completa de preguntas ADL utilizadas para medir las capacidades de desempeño de los pacientes. Cada ítem de las ADL se califica desde el nivel más alto de desempeño independiente hasta la pérdida completa. El ADCS-ADL-severe es un subconjunto de 19 ítems, que incluyen las calificaciones de las habilidades del paciente para comer, vestirse, bañarse, utilizar el teléfono, desplazarse (o viajar) y realizar otras actividades de la vida diaria; este se ha validado para la evaluación de pacientes con demencia moderada a grave. El ADCS-ADL-severe tiene un rango de puntaje de 0 a 54 y los puntajes menores indican mayor deterioro funcional. El investigador realiza el inventario entrevistando un cuidador, en este estudio un miembro del personal de enfermería familiarizado con el desempeño del paciente.
Efectos sobre la SIB: La Figura 3 presenta el cambio desde el puntaje SIB al inicio del estudio con el transcurso del tiempo para los dos grupos de tratamiento durante los 6 meses del estudio. A los 6 meses de tratamiento, la diferencia media en los cambios de puntaje de la SIB para los pacientes tratados con Clorhidrato de Donepezilo comparados con los pacientes tratados con placebo fue 5,9 unidades. El tratamiento con Clorhidrato de donepezilo fue estadísticamente superior que con el placebo.
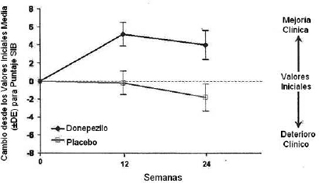
Figura 3. Curso en el tiempo del cambio desde los valores al inicio del estudio en el puntaje SIB para pacientes que completaron 6 meses de tratamiento
La Figura 4 presenta los porcentajes acumulativos de los pacientes de cada uno de los dos grupos de tratamiento quienes alcanzaron la medida de mejoría en el puntaje SIB que se muestra en el eje X. Aunque los pacientes asignados a Clorhidrato de Donepezilo y a placebo presentaron un amplio rango de respuestas, la curva muestra que el grupo de Clorhidrato de Donepezilo tiene mayor probabilidad para mostrar mayor mejoría en el desempeño cognitivo.
Figura 4. Porcentaje acumulativo de pacientes con cambios en los puntajes SIB después de ser tratados con Clorhidrato de Donepezilo
Efectos sobre el ADCS-ADL-severe: La Figura 5 ilustra el curso en el tiempo del cambio desde los valores iniciales para los puntajes ADCS-ADL-severe para los pacientes de los dos grupos de tratamiento durante 6 meses de estudio. Después de 6 meses de tratamiento, la diferencia media en el cambio de los puntajes ADCS-ADL-severe para los pacientes tratados con Clorhidrato de Donepezilo comparados con los del grupo de placebo fue 1,8 unidades. El tratamiento con Clorhidrato de Donepezilo fue estadísticamente significativamente superior a placebo.
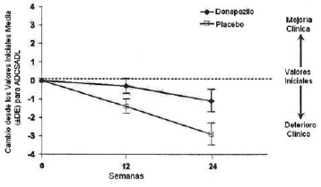
Figura 5. Curso en el tiempo del cambio desde los valores al inicio del estudio en el puntaje ADCS-ADL-severe para pacientes que completaron el tratamiento con Clorhidrato de Donepezilo
La Figura 6 muestra los porcentajes acumulativos de pacientes de cada grupo de tratamiento con cambios específicos de los puntajes ADCS-ADL-severe iniciales. Aunque los pacientes asignados a Clorhidrato de Donepezilo y placebo presentan un rango amplio de respuestas, las curvas demuestran que el grupo de Clorhidrato de Donepezilo tiene mayor probabilidad de demostrar un menor deterioro o una mejoría.
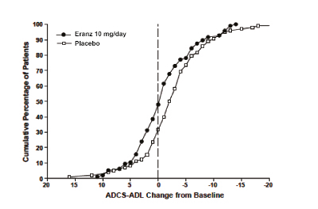
Figura 6. Porcentaje acumulativo de pacientes con cambios en los puntajes ADL después del tratamiento con Clorhidrato de Donepezilo
Estudio Japonés de 24 semanas: En un estudio de 24 semanas, realizado en Japón, 325 pacientes con Enfermedad de Alzheimer grave fueron asignados aleatoriamente a dosis de 5 mg/día o 10 mg/día de Clorhidrato de Donepezilo o placebo50. Los pacientes asignados aleatoriamente al tratamiento con Clorhidrato de Donepezilo alcanzaron sus dosis asignadas mediante titulación, iniciando con 3 mg/día que se extendió durante un máximo de 6 semanas. 248 pacientes completaron el estudio con proporciones similares de pacientes que completaron el estudio en cada grupo de tratamiento. Las mediciones de eficacia primaria para este estudio fueron SIB y CIBIC-Plus.
A las 24 semanas de tratamiento, se observaron diferencias estadísticamente significativas entre la dosis de 10 mg/día de Clorhidrato de Donepezilo y placebo tanto para SIB como para CIBIC-Plus. La dosis de 5 mg/día de Clorhidrato de Donepezilo mostró una superioridad estadísticamente significativa con respecto a placebo para SIB pero no para CIBIC-Plus.
Estudio Multinacional en Pacientes con EA Grave: También se realizó un estudio multinacional, multicéntrico, aleatorio, doble ciego, controlado con placebo, de grupo paralelo de 24 semanas en pacientes con Enfermedad de Alzheimer grave.51 Un total de 343 sujetos fueron asignados aleatoriamente, 176 a Clorhidrato de Donepezilo y 167 a placebo. Los sujetos recibieron 5 mg por día de Clorhidrato de Donepezilo durante las primeras 6 semanas, seguidos por 10 mg diarios de Clorhidrato de Donepezilo durante el tiempo restante de la fase doble ciega del estudio.
El Clorhidrato de Donepezilo fue superior a placebo con significancia estadística en el puntaje SIB en el punto final para la población ITT LOCF (diferencia media de LS 5,32 puntos; P=0,0001). En los pacientes, con relación a los puntajes CIBIC-Plus, la diferencia favoreció al tratamiento con Clorhidrato de Donepezilo pero no alcanzó significancia estadística (P=0,0905). Sin embargo, después de reducir la escala de 7 puntos a una escala de 3 puntos (mejoró, sin cambio o empeoró) se encontraron para ambas poblaciones ITT LOCF diferencias estadísticamente significativas que favorecen al grupo de Clorhidrato de Donepezilo en comparación con el grupo de placebo (P=0,0156).
PROPIEDADES FARMACOCINÉTICAS
Absorción: Los niveles plasmáticos máximos de Clorhidrato de Donepezilo se alcanzan aproximadamente 3 a 4 horas después de la administración oral de tabletas recubiertas de 5 mg y 10 mg. Las concentraciones plasmáticas y el área bajo la curva aumentan proporcionalmente con la dosis. La vida media de eliminación es aproximadamente 70 horas. Así la administración de múltiples dosis únicas diarias produce una aproximación gradual al estado estable. El estado estable se logra dentro de las 2 - 3 semanas después de iniciada la terapia. Una vez alcanzado el estado estable, las concentraciones plasmáticas de Clorhidrato de Donepezilo y la actividad farmacodinámica relacionada muestran poca variabilidad durante el transcurso del día.56,57,58
El alimento no afecta la absorción de Clorhidrato de Donepezilo.59
Distribución: El Clorhidrato de Donepezilo se une aproximadamente en un 95% a las proteínas plasmáticas humanas.60 En un estudio de balance de masa realizado en hombres voluntarios sanos, 240 horas después de la administración de una única dosis de 5 mg de Clorhidrato de Donepezilo, etiquetado con 14C, aproximadamente 28% del Clorhidrato de Donepezilo etiquetado no se recuperó. Esto sugiere que el Clorhidrato de Donepezilo y/o sus metabolitos pueden permanecer en el cuerpo por más de 10 días.60
Metabolismo y excreción: El Clorhidrato de Donepezilo es metabolizado por el hígado y la vía predominante para la eliminación del fármaco y sus metabolitos es la vía renal, un 79% de la dosis recuperada se encontró en la orina y el 21% restantes se encontró en las heces. Se elimina por orina principalmente como Clorhidrato de Donepezilo. Los metabolitos principales del Clorhidrato de Donepezilo incluyen M1 y M2 (vía O-dealquilación e hidroxilación), M11 y M12 (vía glucuronidación de M1 y M2 respectivamente), M4 (vía hidrólisis) y M6 (vía N-oxidación).60
Las concentraciones plasmáticas de Clorhidrato de Donepezilo disminuyen con una vida media de aproximadamente 70 horas.57,58
El sexo, la raza y los antecedentes de tabaquismo no tienen ninguna influencia clínicamente significativa sobre las concentraciones plasmáticas de Clorhidrato de Donepezilo.4,5 La farmacocinética del Clorhidrato de Donepezilo en los pacientes con Alzheimer es muy similar a la de voluntarios sanos32.
Existe una relación entre el peso corporal y la eliminación. Sobre un rango de peso corporal de 50 Kg a 110 Kg, se espera un incremento de la eliminación de 7.7 L/h a 14.04 L/h, siendo la eliminación de 10L/h para alguien con un peso corporal de 70 Kg. 32
CONTRAINDICACIONES: ERANZ® está contraindicado en pacientes con hipersensibilidad conocida al Clorhidrato de Donepezilo, a derivados de la piperidina o a cualquier otro excipiente utilizado en la fórmula.
EMBARAZO Y LACTANCIA
Embarazo: Estudios teratogénicos realizados en ratas preñadas tratadas con dosis de hasta 35 veces la dosis recomendada para humanos (con base en la masa corporal) y en conejas preñadas tratadas con dosis de hasta 22 veces la dosis recomendada por la FDA para humanos (23 mg/día) no demostraron ninguna evidencia de potencial teratogénico.33,34,35,36 Sin embargo, en un estudio en ratas preñadas a las que se les administró aproximadamente 22 veces la dosis recomendada para humanos desde el día 17 de la gestación hasta el día 20 postparto, se presentó un leve incremento de los nacidos muertos y un leve descenso de la supervivencia de las crías en el día 4 postparto. No se observó ningún efecto en la siguiente dosis más baja probada, que equivale a aproximadamente 6.5 veces la dosis para recomendada para humanos.37
No existen estudios clínicos adecuados ni bien controlados en mujeres embarazadas. El Clorhidrato de Donepezilo se debe utilizar durante el embarazo únicamente si el posible beneficio justifica el riesgo potencial para el feto.
Lactancia: Se desconoce si el Clorhidrato de Donepezilo se excreta en la leche materna humana y no existen estudios en mujeres en periodo de lactancia.
EFECTOS SOBRE LA HABILIDAD PARA CONDUCIR VEHÍCULOS Y OPERAR MAQUINARIA: La enfermedad de Alzheimer puede causar deterioro de la habilidad para conducir o comprometer la habilidad para utilizar maquinaria. Además, el Clorhidrato de Donepezilo puede producir fatiga, mareos, calambres musculares, principalmente cuando se inicia o aumenta la dosis.3
EFECTOS INDESEABLES
Estudios clínicos
Enfermedad de Alzheimer Leve a Moderada: Los eventos adversos más comunes (incidencia ³ 5% y dos veces la frecuencia de placebo en pacientes que reciben 10 mg/día) fueron diarrea, calambres musculares, fatiga, náusea, vómito e insomnio. (Tabla1)3
Otros eventos adversos comunes (incidencia ³ 5% y ³ placebo) fueron cefalea, dolor, accidentes, resfriado común, molestias abdominales y mareo.3
Se observaron casos de síncope, bradicardia, bloqueo sinoauricular y bloqueo auriculoventricular.
Se observaron anormalidades no relevantes en los valores del laboratorio asociados con el tratamiento, excepto leves incrementos en las concentraciones séricas de creatinin kinasa muscular.
|
Tabla 1. Eventos adversos reportados en Ensayos Clínicos Controlados de Enfermedad de Alzheimer Leve a Moderada en al menos 2% de los pacientes que recibían Clorhidrato de Donepezilo y en una frecuencia mayor que la de los Pacientes tratados con placebo |
||
|
SISTEMA CORPORAL/EVENTO ADVERSO |
Placebo |
Donepezilo |
|
Porcentaje de Pacientes con un evento adverso |
72% |
74% |
|
Cuerpo como un Todo |
||
|
Cefalea |
9% |
10% |
|
Dolor en varias localizaciones |
8% |
9% |
|
Accidentes |
6% |
7% |
|
Fatiga |
3% |
5% |
|
Cardiovascular |
||
|
Síncope |
1% |
2% |
|
Sistema digestivo |
||
|
Náusea |
6% |
11% |
|
Diarrea |
5% |
10% |
|
Vómito |
3% |
5% |
|
Anorexia |
2% |
4% |
|
Sistema Musculoesquelético |
||
|
Calambres musculares |
2% |
6% |
|
Sistema Nervioso |
||
|
Insomnio |
6% |
9% |
|
Mareo |
6% |
8% |
|
Sistema Psiquiátrico |
||
|
Sueños anormales |
0% |
3% |
|
Enfermedad de Alzheimer Grave Los eventos adversos más comunes (incidencia >5% y con una frecuencia dos veces la frecuencia de placebo) fueron la diarrea, las náuseas y la agresión (Tabla 2). |
||
|
Tabla 2. Eventos Adversos Reportados en Estudios Clínicos Controlados sobre la Enfermedad de Alzheimer grave en al menos 5% de los pacientes que recibieron Clorhidrato de Donepezilo y con una Frecuencia Mayor que la de los Pacientes Tratados con Placebo |
||
|
Sistema corporal/ |
Placebo (N=465) (%) |
Donepezilo (N=573, 477 asignados aleatoriamente a 10 mg, 96 asignados aleatoriamente a 5 mg) (%) |
|
Porcentaje de Pacientes con un evento adverso |
74,0% |
80,8% |
|
Diarrea |
4.1 |
10.3 |
|
Caídas |
8.8 |
10.1 |
|
Infección de las vías urinarias |
7.1 |
8.2 |
|
Nasofaringitis |
6.2 |
8.2 |
|
Vómito |
3,9% |
7,5% |
|
Agitación |
6,5% |
6,3% |
|
Náuseas |
2,6% |
5,6% |
|
Cefalea |
3,0% |
5,1% |
|
Agresión |
2,4% |
5,1% |
Experiencia Post- comercialización: Se han presentado reportes poscomercialización de alucinaciones, agitación, conducta agresiva, convulsiones, hepatitis, úlcera gástrica, úlcera duodenal y hemorragia gastrointestinal.38
INTERACCIONES CON OTROS MEDICAMENTOS Y OTRAS FORMAS DE INTERACCIÓN: Se debe evitar la administración concomitante de Clorhidrato de Donepezilo con otros inhibidores de la colinesterasa.
El Clorhidrato de Donepezilo y sus metabolitos no inhiben el metabolismo de la teofilina20, warfarina21, cimetidina22, digoxina23, tioridazina24, risperidona25,26, y sertralina27 en humanos. El metabolismo del Clorhidrato de Donepezilo no se afecta por la administración concurrente de digoxina, cimetidina, tioridazina, risperidona y sertralina.20.27 En un estudio en pacientes con enfermedad de Parkinson sobre el tratamiento óptimo con L-dopa/carbidopa, la administración de Clorhidrato de Donepezilo durante 21 días no tuvo ningún efecto sobre los niveles sanguíneos de L-dopa o carbidopa. En este estudio, no se observaron efectos sobre la actividad motora.28 Los estudios in vitro han demostrado que las isoenzimas 3A4 del citocromo P450 y en un menor nivel las 2D6 están involucradas en el metabolismo del Clorhidrato de Donepezilo.29,30 Los estudios de interacción medicamentosa realizados in vitro muestran que el ketoconazol y la quinidina, inhibidores del CYP3A4 y el CYP2D6 respectivamente, inhiben el metabolismo del Clorhidrato de Donepezilo. Por lo tanto, estos y otros inhibidores del CYP3A4, como por ejemplo itraconazol y eritromicina, y los inhibidores del CYP2D6, tales como la fluoxetina pueden inhibir el metabolismo del Clorhidrato de Donepezilo. En un estudio con voluntarios sanos, el ketoconazol aumentó las concentraciones medias de Clorhidrato de Donepezilo en aproximadamente 30%. Estos incrementos son menores que los producidos por ketoconazol a otros agentes que comparten la vía del CYP3A4. La administración del Clorhidrato de Donepezilo no tiene ningún efecto sobre la farmacocinética del ketoconazol.31
La influencia de CYP2D6 en la eliminación del donepezilo fue explorada más a fondo mediante un análisis farmacocinético en un estudio clínico controlado de Donepezilo 10 mg y dosis mayores en pacientes con demencia tipo Alzheimer moderadamente grave a grave.31 Según la base de datos para el estudio 326, había 31 pacientes clasificados como pobres metabolizadores, 508 clasificados como metabolizadores extensivos, 13 como metabolizadores ultrarápidos y 298 pacientes con su fenotipo CYP2D6 como no clasificado. El subtipo más grande correspondiente a de los metabolizadores extensivos fue usado como grupo de referencia. Pequeñas diferencias en cuanto a los valores de eliminación fueron observadas dentro de los subgrupos CYP2D6. Al comparar con los metabolizadores extensivos, el grupo de metabolizadores pobres mostró un 31.5% de eliminación menor y el grupo de los metabolizadores ultra rápidos un 24% de eliminación mayor. Mientras la diferencia entre los grupos fue relativamente pequeña, los resultados muestran que el Donepezilo es eliminado, en parte vía CYP2D6. En general, estos resultados sugieren que el CYP2D6 no contribuye en gran medida al metabolismo del Donepezilo.
Con base en estudios in vitro, donepezilo muestra poca o ninguna evidencia de inhibición directa de CYP2B6, CYP2C8 y CYP2C19 a concentraciones clínicamente relevantes.68
Los inductores de enzimas, como por ejemplo la rifampicina, la fenitoína, la carbamazepina y el alcohol pueden reducir los niveles de Clorhidrato de Donepezilo. Como la magnitud del efecto de inhibición o inducción se desconoce, dichas combinaciones de medicamentos se deben utilizar con cuidado. El Clorhidrato de Donepezilo tiene el potencial de interferir con medicamentos que tienen actividad anticolinérgica. Existe también el potencial para actividad sinérgica con el tratamiento concomitante que incluya medicamentos como succinilcolina y otros agentes bloqueadores neuromusculares. Asimismo existe un potencial de actividad sinérgica con los antagonistas colinérgicos o agentes betabloquedores que tienen efectos sobre la conducción cardiaca.
Donepezilo no fue un sustrato de la glicoproteína P en un estudio in vitro.69
INFORMACIÓN DE SEGURIDAD PRECLÍNICA
Generales: Pruebas de gran extensión en animales experimentales han demostrado que Clorhidrato de Donepezilo produce pocos efectos diferentes a los efectos farmacológicos relacionados con su acción como un inhibidor de la colinesterasa.
Mutagenicidad: Clorhidrato de Donepezilo no es genotóxico en los ensayos bacterianos de mutación inversa y en los ensayos con linfoma tk de ratón.61,62 Algunos efectos clastogénicos fueron observados en el ensayo in vitro de aberraciones cromosómicas a concentraciones excesivamente tóxicas para las células y a concentraciones más de 3000 veces las concentraciones plasmáticas en estado estable de 10 mg/día.63 Sin embargo, no se observó potencial clastogénico en el ensayo in vivo del modelo de micronúcleos de ratón y no se observó daño en el ADN en el ensayo in vivo/in vitro UDS.64,65 En resumen, Clorhidrato de Donepezilo resultó negativo en la batería de ensayos de genotoxicidad (ensayos in vitro bacterianos de mutación inversa, ensayos in vitro con linfoma tk de ratón, aberración cromosómica in vitro y micronúcleos de ratón in vivo).
Carcinogenicidad: En un estudio de carcinogenicidad de 88 semanas con Clorhidrato de Donepezilo realizado en ratones CD-1 a dosis de hasta de 180 mg/kg/día (aproximadamente 39 veces la dosis máxima recomendada para humanos por la FDA (23 mg/día) sobre una base de mg/m2, o en un estudio de carcinogenicidad de 104 semanas en ratas Sprague-Dawley a dosis hasta de 30 mg/kg/día (aproximadamente 13 veces la dosis máxima recomendada para humanos sobre una base de mg mg/m2), no se obtuvo evidencia de potencial carcinogénico.66,67
Fertilidad: Clorhidrato de Donepezilo no presentó efecto sobre la fertilidad a dosis de hasta 10 mg/kg/día (aproximadamente 4 veces la dosis máxima recomendada para humanos (23 mg/día) sobre una base de mg/m2) cuando se administró a machos y hembras antes y durante el apareamiento y continuando en hembras a través de la implantación. El Clorhidrato de Donepezilo no fue teratogénico en ratas ni en conejos. Clorhidrato de Donepezilo tuvo un efecto leve sobre las crías nacidas muertas y la sobrevivencia de las crías prematuras cuando se administró a ratas preñadas a dosis de hasta de 10 mg/kg/día (Sección Embarazo y Lactancia).33,34,35,36,37
ADVERTENCIAS Y PRECAUCIONES ESPECIALES PARA SU USO
Anestesia: Puede potenciar el efecto de los relajantes musculares tipo succinil colina.
Afecciones cardiovasculares: Se debe tener precaución en los pacientes que presentan trastornos de la conducción cardiaca “síndrome de seno enfermo, por la posibilidad que tiene el producto de disminuir la frecuencia cardiaca. Se han reportado episodios de síncope”.
Afecciones gastrointestinales: Por la posibilidad de aumentar la secreción de ácido gástrico, es necesario vigilar a los pacientes con enfermedad ácido péptica y sangrado gastrointestinal activo u oculto. El aumento de motilidad intestinal, si ocurre, aparece con mayor frecuencia con la dosis de 10 mg/día.
Urogenital: Los colinomiméticos pueden causar obstrucción del flujo de la vejiga.
Afecciones neurológicas: Convulsiones, se cree que los colinomimeticos poseen cierto potencial para causar convulsiones generalizadas. La actividad convulsiva también podría ser una manifestación de enfermedad de alzheimer.
Afecciones pulmonares: Dada su actividad colinomimetica se debe tener precaución con los pacientes con antecedentes de asma o enfermedad pulmonar obstructiva.
Anestesia: ERANZ® como inhibidor de la colinesterasa, puede acentuar la relajación muscular de tipo succinilcolinico durante la anestesia (ver Interacciones farmacológicas).11
Condiciones cardiovasculares: Debido a su acción farmacológica los inhibidores de la colinesterasa pueden causar efectos vagotónicos sobre la frecuencia cardiaca (por ejemplo: bradicardia).12,13 El potencial para esta acción puede ser particularmente importante en pacientes con el “síndrome del seno enfermo” u otras condiciones de conducción cardiaca supraventricular, como por ejemplo bloqueo sinoauricular o auriculoventricular.14
Condiciones gastrointestinales: Los colinomiméticos puede estimular la producción de ácido gástrico.15 Los pacientes con riesgo aumentado de desarrollar úlceras, por ejemplo, pacientes con antecedentes de enfermedad ulcerosa o aquellos que reciben concomitantemente medicamentos antiinflamatorios no esteroides (AINES), o con riesgo de desarrollar sangrado digestivo activo u oculto, deben ser monitorizados para evaluar su síntomas. Sin embargo, los estudios clínicos con Clorhidrato de Donepezilo no mostraron ningún aumento con relación a placebo, en la incidencia de úlcera péptica o hemorragia gastrointestinal.4,5
Resultados de estudios clínicos controlados a la dosis de 10 mg día vs otras dosis, demostraron una incidencia de 0.2 % de ulcera péptica y de 0.6% de sangrado gastrointestinal. 3
El clorhidrato de donepezilo, como una consecuencia predecible de sus propiedades farmacológicas, ha demostrado producir diarrea, náuseas y vómito. Estos efectos, cuando ocurrieron, aparecieron con mayor frecuencia con la dosis de 10 mg/día que con la dosis de 5 mg/día.
Aunque en la mayoría de los casos, estos efectos han sido leves y transitorios, a veces duran de una a tres semanas, y se han resuelto durante el uso continuado del clorhidrato de donepezilo, los pacientes deben ser observados de cerca en el inicio del tratamiento y tras el aumento de la dosis.
Condiciones neurológicas: Se considera que los colinomiméticos tienen algún potencial para causar convulsiones generalizadas.16,17 Sin embargo, la actividad convulsiva puede también ser una manifestación de la enfermedad de Alzheimer.18
Condiciones pulmonares: Debido a su acción colinomimética, los inhibidores de la colinesterasa se deben prescribir con cuidado a pacientes con antecedentes de asma o enfermedad pulmonar obstructiva.19
Pérdida de peso: En un estudio de pacientes con demencia tipo Alzheimer moderadamente grave a grave, los pacientes mantuvieron una dosis diaria de 10 mg/día que pudo haber sido escalado a dosis mayores. En éste estudio la pérdida de peso fue reportado como un evento adverso en el 2.5% de los pacientes que estuvieron bajo la dosis de 10 mg/día. En comparación con su peso inicial, 4.9% de los pacientes que tomaron 10 mg/día presentaron pérdida de peso = 7% al final del estudio. 7
POSOLOGÍA Y ADMINISTRACIÓN
Adultos/Ancianos: ERANZ® debe ser administrado por vía oral, una vez al día3. Las dosis efectivas clínicamente son de 5 y 10 mg en poblaciones de pacientes con demencia de tipo Alzheimer leve a moderada.4,5,6 En la población de pacientes con demencia de tipo Alzheimer moderadamente grave a grave la dosis clínicamente efectiva es de 10 mg.3,7 El tratamiento se inicia con 5 mg diarios y puede ser incrementado a 10 mg diarios después de 4 a 6 semanas de tratamiento.
En Japón, el tratamiento se inicia con 3 mg y se incrementa hasta 5 mg después de 1 a 2 semanas. En Japón, para los pacientes con la enfermedad de Alzheimer grave, la dosis se puede incrementar hasta 10 mg, después de mantener la dosis de 5 mg durante 4 semanas o más. La dosis diaria máxima recomendada es 10 mg.8
Tratamiento de mantenimiento: El tratamiento de mantenimiento puede mantenerse siempre y cuando exista beneficio terapéutico para el paciente.
Con la descontinuación del tratamiento se ha observado una disminución gradual de los efectos benéficos del ERANZ®. No hay evidencia de efectos de rebote después de una descontinuación abrupta de la terapia.4,5,6
Deterioro renal y hepático: En pacientes con deterioro renal o hepático leve a moderado, puede seguirse un plan de dosis similar ya que la eliminación de Clorhidrato de Donepezilo no se afecta significativamente por estas condiciones.9,10
Niños: No existen estudios adecuados y bien controlados que documenten la seguridad y eficacia del Clorhidrato de Donepezilo en enfermedades que se presentan en niños.
SOBREDOSIS
Datos de estudios con animales: La dosis letal estimada media o dosis letal de Clorhidrato de Donepezilo luego de la administración de una única dosis oral en ratones, ratas y perros es 45, 32 y 15 mg/kg respectivamente, o aproximadamente 98, 70 y 33 veces la dosis máxima recomendada para humanos. En modelos animales se observaron signos de estimulación colinérgica relacionados con la dosis e incluyeron reducción de movimientos espontáneos, postración, marcha vacilante, lagrimeo, convulsiones clónicas, respiración deprimida, salivación, miosis, fasciculación, temblores y disminución de la temperatura superficial corporal.39,40,41
Síntomas de sobredosis: La sobredosis con inhibidores de la colinesterasa pueden producir crisis colinérgicas caracterizadas por náuseas graves, vómito, salivación, sudoración, bradicardia, hipotensión, depresión en la respiración, colapso y convulsiones. Es posible un aumento en la debilidad muscular y puede producir la muerte si los músculos respiratorios están comprometidos.42
Tratamiento: Como en cualquier caso de sobredosis, se deben utilizar las medidas generales de apoyo. Los anticolinérgicos terciarios como la atropina pueden ser efectivos para la sobredosis de ERANZ®. Se desconoce si el Clorhidrato de Donepezilo y/o sus metabolitos se pueden remover mediante diálisis (hemodiálisis, diálisis peritoneal o hemofiltración).
DESCRIPCIÓN: ERANZ® (Clorhidrato de donepezilo) es un inhibidor de la enzima acetilcolinesterasa. Su fórmula empírica es C24H29N03HCl y su peso molecular es de 415.96. El Clorhidrato de dopenezilo es un polvo blanco cristalino. Se encuentra disponible para administración oral en tabletas recubiertas que contienen 5 y 10 mg de Clorhidrato de Donepezilo con 4.56 mg y 9.12 mg de Donepezilo libre respectivamente.
ALMACENAMIENTO: ERANZ® debe conservarse en su empaque original en un lugar seco y fresco, a temperatura ambiente por debajo de 30 ºC.
REFERENCIAS
l. Ametican Psyclúatric .Association. Diagnostic and statistical manual of mental disorders. 4th ed. American Psychianic .Association: 1994.
2. World Health Organisation. Intemational classification of diseases. 10th revision.
World Health Organisation; 1992.
3. Eisai. Inc. Presctibi.ng infonnation for .Aricept®
http://v;v.rw.aricept.com/pdflAliceptComboFullPIKovember201O.pdf .Accessed 14 Febmary 2011.
4. Rogers SL. Doody RS. Mohs RC. et al. Donepezil improves cognition and global function in .Alzheimer disease: a 15 week. double-blind. placebo-controlled study. Donepezil Study Group. .AJ·ch Intem Med 1998 May 11:158(9):1021-31. (Clinical Efficacy Smdy E2020-.A001-301)
5. Rogers SL. Farlow MR. Doody RS. et al. A 24 week. double-blind. placebo comrolled nial of donepezil in patients with .Alzheimer’s disease. Donepezil Study Group. Neurology 1998:50(1):136-45. (Clinical Efficacy Study E2020-.AOOI-302]
6. Bums A. Rossor M. Hecker J, Gauthier S. Petit H. Moller HJ et al. The effects of donepezil in Alzheimer’s disease - results from a multinational trial. Dement Geriatr Cogn Disord 1998:9(Suppl.3):29-42. (Clinical Efficacy Study E2020-E044-304]
7. Farlow MR, Salloway S. Tariot PN. Yardley J. Moline ML. Wang Q. Brand Schieber E. Zou H. Hsu T, Satlin A. Effectiveness and tolerability oflúgh-dose (23 mg/d) \·ersus standard-dose (10 mg/d) donepezil in moderate to severe .Alzhein1er’s disease: A 24-week. randomized, double-blind study. Clú1 Ther. 2010:32(7):1234-51. (Clinical Efficacy Study E2020-G000-326]
8. Honuna A. Takeda M Imai Y. Udaka F. Hasegawa K. Karneyama M et al. Clinical efficacy and safety of donepezil on cogrútive and global ftmction in patients with Alzheimer·s disease: a 24 week. multicenter. double-blind. placebo-conn·olled study in Japar1. Dement Getiatr Cog:n Disord 2000:11(6):299-313. [Cli.nical Efficacy Study E2020-J081-161]
9. Tiseo PJ, Foley K. Friedhoff LA Al1 evaluation of the pharmacokinetics of donepezil HCL in patients with moderately to severely impai.red renal ftmction. Br J Clin Phannacol 1998:46(Suppl.I):56-60. (Clinical Pharmacokinetic Study E2020-E044-001]
10. Tiseo PJ. Var·gas R. Perdomo C.A. Fiiedhoff LA. Al1 evaluation of the phannacoki.netics of donepezil HCL in patiems with impaired hepati.c ftmction. Br J Clin Phannacol 1998:46(SuppLI):51-S. (Clínica! Pharmacokinetic Study E2020-.AOOI -005]
11. Neuromuscular blocker and anesthetic dmg interactions. In: Stockley IH. Drug interactions. 4th ed. London: The Pharmaceutical Press: 1996. p. 722-56
12. Landsberg L. Yotmg JB. Physiology and phannacology of the autonomic nervous system. In: Fauci AS. Bratmwald E. Isselbacher KJ, Wilson .ID. Martin JB. Kasper DL et al, editors. Hanison’s Piinciples of lntemal Medicine. 14th ed.. New York: McGraw-Hill: 1998. p. 430-42.
13. Taylor P. Anticholinesterase agents. In: Hardman JG. Li.tnbi.rd LE. Moli.t10íi PB.
Ruddon RW, Goodman Gilinan A, editors. Goodman & Gilman’s The Phannacological Basis of T11erapeutics. 9th ed.. New York: McGraw-Hill; 1996. pp. 161-76.
14. Josephson ME, Zimetbamn P, March1i.tlski FE, BtLxton A.E. The bradyanythmias: disorders of sinus node function ancl AV conduction disturbances. In: Fauci AS, Braunwald E. Isselbacher KJ. Wilson ID. Martín JB. Kasper DL et al. eclitors. Hanison’s Ptinciples of Intemal Medicine. 14th ecl., New York: McGraw-Hill: 1998. pp. 1253-61.
15. Aihara T. Nakamura Y. Makoto M. et al. Choli.t1ergically stünulatecl gastric acicl secretion is 1necliatecl hy M3 ;me! M’i hnt not Ml mnsc;uinic ::cetylcholine receptors in mice. Am J Physiol Gastroi.t1test Liver Physiol2005:288:Gl199-G1207.
16. McNamara JO. Dmgs effective in the therapy of the epilepsies. In: Hardman JG.
Limbu·d LE, Molinoff PB, Ruddon RW, Gooclman Gilman A, eclitors. Goochnan & Gilman ‘s T11e Phannacological Basis of T11erapeutics. 9th ecl. New York: McGraw Hill: 1996. pp. 461-86.
17. Woocl AJJ. Adverse reactions to dmgs. In: Fauci AS, Brmmwalcl E. Isselbacher KJ, Wilson ID, Marti..t1 JB, Kasper DL et al, eclitors. Hauison ‘s Principies of Intemal
Medicine. 14th ecl.. New York: McGraw-Hill: 1998. pp. 422-30.
18. Hesclorffer DC, Hauser WA. Almegers JF, Kokmen E, Rocca ‘\VA, Gertmde H.
Dementia and aclult-onset provokecl seiztu·es. Nelll’ology 1996;46(3):727-30.
19. Belmonte KE. Cholinergic pathways in the lungs ancl anticholi..t1ergic therapy for chronic obstmctive pulmonmy clisease. Proc Am Thorac Soc 2005:2:297-304
20. Tiseo PJ, Foley K. F1ieclhoff LA. Conctm-ent administration of donepezil HC1 ancl theophyllllie: assessment of phmmacoki..t1etic changes followi..tlg single ancl multiple doses. Br J Cli..t1 Phannacol 1998;46(Suppl.I):35-9. [Cli..tlical Phannacokinetic Stucly E2020-E044-002]
21. Tiseo PJ. Foley K. F1ieclhoff LA. Concmrent aclmi..tlistration of donepezil HCl ancl w:rf:rin: : ssessment of phmm: cokinetic ch:nges following single m1d multip1e doses. Br J Cli..t1 Phmu1acol 1998;46(Suppl.I):45-50. [Clínica! Plmmacokinetic Stucly E2020-E044-003]
22. Tiseo PJ, Perdomo CA. F1iedhoff LA. Concmrent aclmi..ttistration of donepezil HCl and ci..tlleticli..tle: assessment of phannacokinetic changes followi..t1g si..t1gle ancl multiple doses. Br J Cli..t1 Phannacol 1998:46(Suppl.I):25-9. [Cli..tlical Phannacokinetic Stucly E2020-A001-006]
23. Tiseo PJ, Perdomo CA. Ftiedhoff LA. Concmrent adntinistration of donepezil HCl ancl cligoxin: assessment of phmmacoki..t1etic changes followi..t1g single and multiple doses. Br J Clin Phannaco11998;46(Suppl.I):40-4. [Cli..tlical Phannacokinetic Study E2020-AOO1-007]
24. Open label. nvo-way complete crossover study to investigate the effect of donepezil treatment on the safety and pha1macokinetics of single-dose thioridazine. [Clinical Phannacokinetic Stucly E2020-E044-006].
25. Zhao Q, Xie C.Pesco-Koplowitz L. et al. Phatmacokinetic and safety assessments of conctm·ent ach1tinistration of Iispetidone and donepezil. J Cli..t1 Phannacol.
2003;43:180-6.
26. Reyes JF, Preskom SH. Khan A, et al. Conctu1’ent administration of donepezíl HCl and rispeticlone in patients with schizoplu·enia: assessment of phannacokinetic changes ancl safety following multiple oral closes. Br J Clin Phannacol.
2004;58(Suppl 1):50-7.)
27. Nagy CF. Kmnar D. Perclomo CA, et al. Conctu1’ent aclministration of donepezil HCl ancl seJtraline HCl in healthy volunteers: assessment of pham1acokinetic changes and safety following single and multiple oral doses. Br J Clin Phannacol.
2004;58(Suppl 1):25-33. [Clínica!Phannacokinetic Stucly E2020-A001-014]
28. A safety ancl phannacokinetic study of Aticept and Sinemet in Parkinson’s disease (PD) patients compared to healthy volunteers adnúnistered At·icept alone. [Clínica! Phannacokinetic Study E2020-A001-105].
29. Interaction of E2020 with Htunan Cytoclu·ome P450. Non-clinical Phannacology Study. Rep01t No. 1995281 (D-23).
30. Iclentification of Cytoclu·ome P450 Involved in the Metabolism of E2020. Non clínica!Phmmacology Smdy No. 9411O l.Report No. 19952792 (D-22).
31. Tiseo PJ. Perdomo CA. F1iedhoff LA. Conctll1’ent aclnúnistration of donepezil HCl and ketoconazole: assessment of phannacokinetic changes following single ancl multiple doses. Br J Clín Phannacol 1998;46(Suppl.I):30-4. [Clínica! Phannacokinetic Stucly E2020-A001-012]
32. Eisaí subnússion to FDA, E2020 SR 23 mg fonnulation, September 24, 2009.
33. Fertílíty study in rats treatecl orally with E2020. Non-clínica!Reproductíve Toxicity StudyNo. 904313 (T-17).
34. E2020 teratology study in rats on oral administration dtuing the pe1iod of fetal organogenesis. Non-clinical Reproductive Toxícity Study No. R-248 (T-18).
35. E2020 teratology study in rabbits on oral aclnúnistratíon dtuing the pe1iod of fetal orgmwgenesis. Non-clinical Reprodnctive Toxicíty Stncly No. R-247 (T-19).
36. Adclítional teratology sn1dy of E2020 in rats. Non-clinical Reproductive Toxicíty Study No. S99007 (T-26).
37. E2020 reproduction study in rats on oral aclministration cluring the perinatal ancl lactation periods. Non-clínica!Reprocluctive Toxicíty Smcly No. S91512 (T-20).
38. Post Marketing Smveillance (PMS) cases in Intematíonal Pe1ioclic Safety Upclate Reports (PSUR) for Aticept®
39. E2020 toxicity sn1dy in núce receiving a single oral or intravenous aclnunístration.
Non-clüucal Acnte Toxicity Stucly No. 4088 (T-1).
40. E2020 toxicity stucly in rats receiving a single oral or intravenous aclministratíon.
Non-clinical Acute Toxicíty Stucly No. 4098 (T-2).
41. E2020 toxícíty stucly in beagle clogs on single oral aclnillústratíon. Non-clinical Acure Toxicity Stucly No. 881242 (T-3).
42. Hu H, Speizer FE. Specific envü·orunental ancl occupatíonal hazards. In: Faucí AS.
Brmmwalcl E, Isselbacher KJ. Wilson ID. MartÍll JB, Kasper DL et al. eclitors. Hanison’s Principies ofintemal MeclicÍ!le. 14th ecl. New York: McGraw-Hill: 1998. pp. 2521-44.
43. Inhibit01y effects of E2020 on cholínesterase actívitíes in vitro. Non-clülical
Phannacology Smcly. Report No. W-880700A (MP-1).
44. Rosen WG. Mohs RC. Davis KL. A new rating scale for Alzheimer’s disease.
Amer J Psychiatr 1984:141:1356-64.
45. Jofft·es C, Graham J, Rod.”wood K. Qnalitative analysis of the cli.nical intervi.ew based i.mpressi.on of change (Plus): methodological issues and implications for clinical research. Int Psychogeriatr. 2000;12:403-13.
46. Monis J. The cli.túcal dementia rating (CDR): Cunent version and scoring rules.
Neurology 1993;43:2412-14.
47. Winblad B, Kilander L. Eriksson S, et al. Donepezil in patients with severe Alzheimer ‘s disease: clouble-blind, parallel-group, placebo-controlled stucly. Lancet 2006:367:1057-65 [Clínica!Efficacy Stucly A2501017]
48. Schmitt FA. Ashforcl W, Emesto C. et al. The severe impairment battery: conctll1’ent validity ancl the assessment of longitudinal change in Alzheimer’s disease. The Alzhein1er’s Disease Cooperative Stucly. Alzheimer Dis Associ Disord 1997:1l(suppl2):S51-6.
49. Galasko D, Bennett D, Sano M. et al. A.n Í!lVentory to assess actívities of daily living for clirlical trials in Alzheirner’s dise.ase. Alzheirner Dis Assoc Disord 1997; 11(suppl2):S33-S39.
50. Homma A, Imai Y, Tago H, et al. Donepezil treatment of patients with severe Alzheirner ‘s disease in a Japanese population: results fi·om a 24-week, double-blind, placebo-controlled, randomized tlial. Dement Ge.Jiatr Cogn Disord 2008:25:399- 407. [Clínica!Efficacy Stucly E2020-J081-231]
51. Black SE, Doody R, Li H. et al. DonepezH preserves cogrlition and global function in patients with severe Alzheimer’s clisease. Nem·ology 2007:69:459-69. [Clínica! Efficacy Study E2020-A001-315]
52. Black S.Roman OC. Geldmacher DS. et al. Efficacy ancl tolerability of donepezil in vascular dementia: Positive results of a 24-week, multicenter, irltematíonal. randolllÍze.cl. placebo-controlled clirlical tria!. Str·oke 2003:34:2323-30. [Clinical Efficacy Study E2020-A001-307]
53. Wilkinson D. Doody R. Hehne R, et al. Donepezil 308 study group: Donepezil in vascular dementia: a randomizecl, placebo-controlled study. Nemology 2003;61:479-86. [Clirlical Efficacy Study E2020-AOO1-308]
54. Rornán OC. Salloway S. Black S et al. Randomizecl. placebo-controllecl. clínica! tria! of donepezil Íll vascular dementia. differential effects by hippocampal size Stroke 2010;41:1213. [Clinical Efficacy Stndy E2020-A001-319]
55. Roman GC, Wilkir1son D, Doody R, et al. Donepezil in vascular dementia: combir1ed analysis ofnvo large-scale clirucal trials. Dement Geriatr Cogn Disord 2005:20:338-344. [Clirlical Efficacy Study E2020-A001-307 and E2020-A001-308]
56. Rogers SL, Frieclhoff LA. Phannacokinetic and phannacodynamic profile of donepezil HCL following single oral doses. Br J Clin Phannacol1998:46(Suppl.I):1- 6. [Clínica!Efficacy Study E2020-AOO1-001]
57. Rogers SL, Frieclhoff LA Phannacokinetic and phannacodynamic profile of donepezil HCL following multiple oral doses. Br J Clir1 Phannacol 1998;46(Suppl.I):7-12. [Clirucal Efficacy Study E2020-A001-002]
68. In Vitro Evaluation of E2020 as a Direct Inhibitor of Cytochrome P450 (CYP) Enzymes in Human Liver Microsomes. Study Number XT105073.
69. Transcellular Transport of E2020 Using MDR1 Expressing Cells. Study Number GE-0787-G.
Es posible que la información de prescripción de este producto haya sido revisada y actualizada después de la fecha de impresión del PLM 2016. Para obtener información más actualizada comuníquese con la Dirección Médica de Pfizer S.A.S Teléfono: (1) 6002300 Ext. 2509 Bogotá – Colombia.
ERANZ® 5 mg Tabletas Recubiertas (Reg. San. INVIMA 2008 M-011314 R1).
ERANZ® 10 mg Tabletas Recubiertas (Reg. San. INVIMA 2008 M- 012620 R-1).
PFIZER S.A.S.