
LOPID
GEMFIBROZILO
Tabletas
Caja , 20 Tabletas , 600 y 900 Miligramos
Para visualizar el contenido completo de la IPPA (información para prescribir amplia), deberá iniciar sesión.
COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Ingrediente activo: Gemfibrozilo.
Cada TABLETA contiene 600 mg ó 900 mg de gemfibrozilo.
INDICACIONES TERAPÉUTICAS
Gemfibrozilo es un agente regulador de los lípidos que está indicado para lo siguiente
a. Trastornos primarios graves del metabolismo de los lípidos con aumento predominante de los triglicéridos (lípidos neutros) cuando no es posible rebajar adecuadamente la concentración de los lípidos en el suero mediante la dieta u otras modificaciones del estilo de vida).
b. Aumento secundario grave de triglicéridos que es imposible combatir con el tratamiento de la enfermedad primaria (como la diabetes mellitus y la gota) y si no responden a la dieta u otras modificaciones del estilo de vida.
PROPIEDADES FARMACOCINÉTICAS
Absorción: Gemfibrozilo es bien absorbido desde el tracto gastrointestinal después de su administración oral. Los niveles pico en plasma ocurren luego de una a dos horas con una vida media en plasma de 1,5 horas después de dosis múltiples. Los niveles en plasma son proporcionales a la dosis y no demuestran acumulación en el tiempo después de múltiples dosis. La farmacocinética de gemfibrozilo es afectada por el tiempo de las comidas con referencia al tiempo de la dosis. En un estudio, tanto la tasa como el grado de absorción de la droga aumentaron significativamente cuando se administró media hora antes de las comidas. El área bajo la curva (ABC) promedio se redujo en 14 - 44% cuando se administró gemfibrozilo después de las comidas, en comparación con media hora antes de las comidas. En un estudio posterior, la tasa de absorción de gemfibrozilo fue máxima cuando se administró media hora antes de las comidas con la Cmax 50 - 60% mayor que cuando se administró bien sea con las comidas o en ayunas. En este estudio, no hubo efectos significativos en el ABC del tiempo de la dosis con respecto a las comidas. (Ver sección Dosis y método de administración).
Distribución: Gemfibrozilo se une altamente a las proteínas plasmáticas y existe un potencial para interacciones de desplazamiento con otras drogas. (Ver sección Advertencias y precauciones especiales para su uso).
Metabolismo: Gemfibrozilo sufre oxidación de un grupo metilo del anillo para formar sucesivamente un metabolito hidroximetil y un metabolito carboxil.
Excreción: Aproximadamente 70% de la dosis humana administrada se excreta por la orina, en su mayoría como el conjugado glucurónido, con menos de 2% excretado como gemfibrozilo intacto. Seis por ciento de la dosis se excreta en las heces.
PROPIEDADES FARMACODINÁMICAS
Gemfibrozilo es un ácido fenoxipentanoico no halogenado con la siguiente fórmula estructural
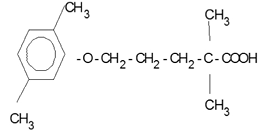
P.M. = 250,35
El nombre químico es ácido 5-(2,5-dimetilfenoxi)-2,2-dimetilpentanóico; la fórmula empírica es C15H22O3.
Gemfibrozilo es un compuesto blanco con un punto de fusión de 58° a 61 °C. Su solubilidad es 0,0019% en agua y en ácido y, aproximadamente 1% en base diluida. Gemfibrozilo es estable bajo condiciones ordinarias.
Mecanismo de acción: No se ha establecido definitivamente el mecanismo de acción de gemfibrozilo. En el ser humano, gemfibrozilo inhibe la lipólisis periférica y reduce la extracción hepática de ácidos grasos libres. Gemfibrozilo también inhibe la síntesis y aumenta la depuración de la apolipoproteína B que es un portador del VLDL provocando una disminución en la producción de VLDL. Gemfibrozilo aumenta el nivel de las subfracciones de la lipoproteína de alta densidad, HDL2 y HDL3, así como la apolipoproteína A-I y A-II. Los estudios en animales sugieren que el recambio y la remoción de colesterol del hígado aumenta con gemfibrozilo.
Gemfibrozilo es un agente regulador de los lípidos el cual reduce el colesterol total, el colesterol de las lipoproteínas de baja densidad (LDL), el colesterol de las lipoproteínas de muy baja densidad (VLDL) y los triglicéridos, y aumenta el colesterol de las lipoproteínas de alta densidad (HDL).
En el Estudio del Corazón de Helsinki, un estudio de prevención primaria a gran escala, aleatorizado, doble ciego, controlado con placebo, en el cual participaron sujetos con colesterol no HDL en suero de aproximadamente 200 mg/dl (5,2 mmol/l) y sin historia previa de cardiopatía, gemfibrozilo produjo una disminución significativa en los triglicéridos totales en plasma, disminuciones moderadas en el colesterol total y LDL, y un aumento significativo en el colesterol HDL. Durante el periodo de estudio de cinco años el grupo gemfibrozilo experimentó una disminución de 34% en la incidencia global de cardiopatía coronaria (en los años 4 y 5 del estudio la disminución de cardiopatía coronaria fue mayor que 50%). Hubo una disminución de 37% en el infarto del miocardio no fatal y una reducción de 26% en las muertes cardiacas. La diferencia global en la incidencia de enfermedad coronaria fue significativamente menor para los pacientes tratados con gemfibrozilo que para los que recibieron placebo (p < 0.02, dos colas).
CONTRAINDICACIONES: Hipersensibilidad a gemfibrozilo o cualquiera de los ingredientes inertes. Embarazo y lactancia, insuficiencia renal y/o hepática. Adminístrese con precaución en pacientes con antecedentes de litiasis biliar y/o que estén recibiendo anticoagulantes. Está contraindicado el uso concomitante de gemfibrozilo con repaglinida. La administración concomitante de gemfibrozilo con simvastatina está contraindicada.
(Ver sección Advertencias y precauciones especiales para su uso y sección Interacción con otros productos medicinales y otras formas de interacción).
FERTILIDAD, EMBARAZO Y LACTANCIA: No existen estudios adecuados y bien controlados en mujeres embarazadas. El uso de gemfibrozilo durante el embarazo se debe reservar para aquellos pacientes en los cuales los beneficios superen claramente los riesgos para la paciente o el feto.
No se ha establecido la seguridad en madres lactantes. Se desconoce si gemfibrozilo es excretado en la leche materna. Dado que muchas drogas se excretan en la leche materna, el paciente debe descontinuar la lactancia antes de iniciar la terapia con gemfibrozilo.
EFECTOS EN LA CAPACIDAD PARA MANEJAR Y UTILIZAR MÁQUINAS: Ninguno conocido.
EFECTOS INDESEABLES
En la fase controlada doble ciego del Estudio del corazón de Helsinki, 2.046 pacientes recibieron gemfibrozilo por hasta 5 años. En ese estudio, las siguientes reacciones adversas fueron estadísticamente más frecuentes en los sujetos en el grupo gemfibrozilo
|
Gemfibrozilo (n = 2.046) |
Placebo (N = 2035) |
|
|
Frecuencia en el porcentaje de sujetos (%) |
||
|
Reacciones gastrointestinales Dispepsia Dolor abdominal Apendicitis aguda Fibrilación auricular |
34,2 19,6 9,8 1,2 0,7 |
23,8 11,9 5,6 0,6 0,1 |
Eventos adversos reportados por más de 1% de los sujetos, pero sin una diferencia significativa entre los grupos
|
Gemfibrozilo (n = 2.046) |
Placebo (N = 2035) |
|
|
Frecuencia en el porcentaje de sujetos (%) |
||
|
Diarrea Cansancio Náusea/vómito Ecxema Erupción Vértigo Constipación Cefalea |
7,2 3,8 2,5 1,9 1,7 1,5 1,4 1,2 |
6,5 3,5 2,1 1,2 1,3 1,3 1,3 1,1 |
Las reacciones adversas adicionales que se han reportado en las cuales es probable una relación causal con el tratamiento con gemfibrozilo son
|
Sistema corporal |
Reacción adversa |
|
Trastornos hepatobiliares |
Ictericia colestática |
|
Trastornos gastrointestinales |
Pancreatitis |
|
Sistema Nervioso Central |
Vértigo, somnolencia, parestesia, neuritis periférica, cefalea |
|
Trastornos psiquiátricos |
Disminución de la líbido, depresión |
|
Ojo |
Visión borrosa |
|
Sistema reproductivo y trastornos de la mama |
Impotencia |
|
Trastornos musculoesqueléticos y de tejido conectivo |
Artralgia, sinovitis, mialgia, miopatía, miastenia, dolor en extremidades, rabdomiólisis |
|
Trastornos de piel y tejido subcutáneo |
Dermatitis exfoliativa, erupción, dermatitis, prurito, angioedema, urticaria |
|
Trastornos respiratorios, torácicos y mediastinales |
Edema laríngeo |
|
Trastornos de la sangre y el sistema linfático |
Anemia severa, leucopenia, trombocitopenia, eosinofilia, hipoplasia de médula ósea (ver sección Advertencias y precauciones especiales para su uso – Hematopoyético). |
Las reacciones adversas adicionales que se han reportado incluyeron fotosensibilidad, alopecia, colecistitis y colelitiasis (ver sección Advertencias y precauciones especiales para su uso).
INTERACCIÓN CON OTROS PRODUCTOS MEDICINALES Y OTRAS FORMAS DE INTERACCIÓN
Anticoagulantes: Se debe tener precaución al administrar anticoagulantes junto con gemfibrozilo. Se debe reducir la dosis de anticoagulante para mantener el tiempo de protrombina al nivel deseado para prevenir complicaciones de sangrado. Se aconseja realizar evaluaciones frecuentes del tiempo de protrombina hasta que se determine definitivamente que se haya estabilizado el tiempo de protrombina.
Inhibidores de la HMG-CoA Reductasa: La administración concomitante de gemfibrozilo con simvastatina está contraindicada. Ha habido reportes de miositis severa y mioglobinuria (rabdomiólisis) al utilizar en forma concomitante gemfibrozilo y los inhibidores de la HMG-CoA reductasa (ver sección Contraindicaciones y sección Advertencias y precauciones especiales para su uso).
Resinas de Unión al Ácido Biliar: Puede haber biodisponibilidad reducida de gemfibrozilo al administrarlo en forma simultánea con drogas de gránulos de resina como colestipol. Se recomienda la administración de las drogas dos horas o con mayor diferencia.
Repaglinida: En voluntarios sanos, la coadministración con gemfibrozilo incrementó la concentración plasmática de repaglinida y prolongó sus efectos hipoglicémiantes. La coadministración de gemfibrozilo y repaglinida incrementa el riesgo de hipoglicemia severa y está contraindicada. (Ver sección Contraindicaciones).
Colchicina: El riesgo de toxicidad neuromuscular y rabdomiólisis puede verse aumentado con la administración concomitante de gemfibrozilo y colchicina. Este riesgo puede aumentar en ancianos y pacientes con disfunción hepática o renal. Los síntomas usualmente duran entre 1 semana y varios meses después de retirar la colchicina. Se recomienda monitoreo clínico y biológico, especialmente al comienzo del tratamiento combinado.
DATOS DE SEGURIDAD PRECLÍNICA
Carcinogenesis, mutagenesis y deterioro de la fertilidad: No existen estudios adecuados, bien controlados en humanos. Se han efectuado estudios a largo plazo en ratas a 0,2 y 1,3 veces la exposición en humanos (basado en el ABC). La incidencia de ganglios hepáticos y carcinomas hepáticos benignos aumentó significativamente en las ratas machos que recibieron la dosis elevada. En las ratas hembras que recibieron la dosis alta, hubo un aumento significativo en la incidencia combinada de neoplasias hepáticas benignas y malignas.
También se efectuó un estudio comparativo de carcinogenecidad en ratas comparando tres medicamentos de esta clase: Fenofibrato (10 y 60 mg/kg; 0,3 y 1,6 veces la dosis humana), clofibrato (400 mg/kg; 1,6 veces la dosis humana), y gemfibrozilo (250 mg/kg; 1,7 veces la dosis en humanos). Los adenomas acinares pancreáticos aumentaron en los machos y las hembras que recibieron fenofibrato; los carcinomas hepatocelular y adenomas acinares pancreáticos aumentaron en los machos y los nódulos neoplásicos hepáticos aumentaron en las hembras tratadas con clofibrato; los nódulos neoplásicos hepáticos aumentaron en los machos y las hembras tratados con gemfibrozilo, mientras que los tumores de célula intersticial testicular aumentaron en los machos que recibieron los tres medicamentos.
Se han efectuado estudios a largo plazo en ratones a 0,1 y 0,7 veces la exposición en humanos (basada en el ABC). No hubo diferencias estadísticamente significativas de los controles en la incidencia de tumores hepáticos, pero las dosis analizadas fueron más bajas que las que se demostró que fueron carcinogénicas con otros fibratos. La administración de aproximadamente dos veces la dosis humana (basado en el área de superficie) a las ratas machos durante 10 semanas produjo una disminución en la fertilidad relacionada con la dosis. Los estudios subsiguientes demostraron que este efecto se revirtió después de un periodo sin medicamento de aproximadamente ocho semanas y que no se transmitió a la descendencia. Se evidenció fetotoxicidad leve mediante los pesos reducidos al nacer observados a los niveles de dosis más elevadas.
ADVERTENCIAS Y PRECAUCIONES ESPECIALES PARA SU USO
Colelitiasis: Gemfibrozilo puede aumentar la excreción de colesterol hacia la bilis elevando el potencial de formación de cálculos biliares. En caso de sospecha de colelitiasis, se indican estudios de vesícula. La terapia con gemfibrozilo debe ser descontinuada si se observan cálculos en la vesícula. Se han reportado casos de colelitiasis con la terapia con gemfibrozilo.
Inhibidores de la HMG-CoA reductasa: La administración concomitante de gemfibrozilo con simvastatina está contraindicada. Ha habido informes de miositis severa con niveles marcadamente elevados de creatinquinasa y mioglobinuria (rabdomiólisis) cuando se usaron en forma concomitante gemfibrozilo y los inhibidores de la HMG CoA reductasa. En la mayoría de los sujetos que han tenido una respuesta insatisfactoria en los niveles de los lípidos a cualquiera de las drogas sola, el posible beneficio de la terapia combinada con los inhibidores de la HMG-CoA reductasa y gemfibrozilo no supera los riesgos de miopatía severa, rabdomiólisis, e insuficiencia renal aguda. (Ver sección Contraindicaciones y sección Interacción con otros productos medicinales y otras formas de interacción).
Anticoagulantes: Se debe tener precaución con el uso concomitante de los anticoagulantes. La dosis del anticoagulante debe ser reducida para mantener los niveles deseados del tiempo de protrombina. Se aconseja el monitoreo frecuente de los niveles del tiempo de protrombina hasta que se estabilice el nivel de PT.
Pruebas de laboratorio: Rara vez se han reportado pruebas elevadas de función hepática como las transaminasas hepáticas (AST (SGOT) y ALT (SGPT)), niveles elevados de fosfatasa alcalina, creatinquinasa (CK), deshidrogenasa láctica (LDH, y bilirrubina con la administración de gemfibrozilo. Estas alteraciones suelen ser reversibles al descontinuar gemfibrozilo. Por lo tanto, se recomiendan estudios periódicos de la función hepática y se debe terminar la terapia con gemfibrozilo si persisten las anormalidades.
Hematopoyesis: Ocasionalmente se han observado disminuciones leves en los niveles de hemoglobina, hematocrito y glóbulos blancos al iniciar la terapia con gemfibrozilo. Sin embargo, estos niveles se estabilizan durante la administración a largo plazo. Rara vez se ha reportado anemia, leucopenia, trombocitopenia, esofinofilia e hipoplasia de médula ósea. Por lo tanto, se recomiendan las determinaciones de recuentos hematológicos periódicos durante los primeros 12 meses de administración de gemfibrozilo.
Información para el paciente: Se debe indicar a la’ paciente que le informe al médico si está embarazada, lactando, o si está planeando quedar embarazada.
Se debe indicar a los pacientes que toman gemfibrozilo sobre la importancia de tomar el medicamento bajo el régimen prescrito, sobre la importancia de las pruebas de laboratorio para monitorear los niveles de lípidos y reportar cualquier efecto secundario experimentado.
DOSIS Y MÉTODO DE ADMINISTRACIÓN
General: Se deben medir los niveles de lípidos en más de una ocasión para asegurarse que los niveles están consistentemente anormales. Antes de iniciar la terapia con gemfibrozilo, se deben hacer todos los intentos para controlar los niveles de lípidos en suero con dieta adecuada, limitando la ingesta de alcohol, el ejercicio y la baja de peso en pacientes obesos, así como controlando otros problemas médicos como la diabetes mellitus o el hipotiroidismo que pueden contribuir a los niveles lípidos anormales. El paciente debe continuar con una dieta estándar reductora del colesterol durante el tratamiento con gemfibrozilo. Se deben hacer evaluaciones periódicas de los niveles de lípidos. La droga debe ser retirada o iniciar terapia adicional si la respuesta de los lípidos resulta inadecuada después de tres meses.
La dosis diaria recomendada es 900 - 1200 mg. La dosis máxima diaria es 1.500 mg. La dosis de 900 mg se administra como una dosis única, media hora antes de la cena. La dosis de 1.200 mg se administra en dos dosis divididas media hora antes del desayuno y la cena. (Ver sección Propiedades farmacocinéticas).
Uso en Pacientes con disfunción hepática: (Ver sección Contraindicaciones y sección Advertencias y precauciones especiales para su uso).
Uso en pacientes con disfunción renal: (Ver sección Contraindicaciones y sección Advertencias y precauciones especiales para su uso).
Uso en niños: No se ha establecido la seguridad y eficacia en niños.
SOBREDOSIS: Se ha reportado sobredosis con gemfibrozilo. Los síntomas reportados con la sobredosis fueron dolor abdominal, anormalidades de las pruebas de función hepática (LFT), diarrea, elevación de la CPK, dolor en articulaciones y músculos, náuseas y vómito. Los pacientes se recuperaron totalmente.
Se deben tomar medidas de apoyo sintomático en caso de sobredosis.
PRESENTACIÓN: LOPID® 600 mg Tabletas (Reg. San. INVIMA 2005 M-08629-R2).
LOPID® 900 mg Tabletas recubiertas (Reg. San. INVIMA 2012 M-014067-R2).
Es posible que la información de prescripción de este producto haya sido revisada y actualizada después de la fecha de impresión del PLM 2016. Para obtener información más actualizada comuníquese con la Dirección Médica de Pfizer S.A.S Teléfono: (1) 6002300 Ext. 2509 Bogotá – Colombia.
Título del Documento de Producto: Gemfibrozilo
Número de Documento de Producto: CDS versión 5.0
Fecha: 22 de abril de 2013
Sustituye a: CDS de 2 de diciembre de 2008
LLD_Col_CDSv5.0_22Abr2013_v1_Aprobado por Resol. 2014032463, 2014008239_10Nov2014.
PFIZER S.A.S.