
TRAYENTA
LINAGLIPTINA
Tabletas recubiertas
1 Caja,30 Tabletas recubiertas,5 mg
Para visualizar el contenido completo de la IPPA (información para prescribir amplia), deberá iniciar sesión.
COMPOSICIÓN: Cada TABLETA Recubierta contiene 5mg de linagliptina 1H-purina-2,6-diona, 8-[(3R)-3-amino-1-piperidinil]-7-(-2-butin-1-il)-3,7-dihidro-3-metil-1- [(4-metil-2-quinazolinil)metil]-(= linagliptina)
USO EN POBLACIONES ESPECÍFICAS
• Fertilidad, embarazo y lactancia: Embarazo: Existen datos limitados sobre el uso de linagliptina en mujeres embarazadas. Los estudios realizados en animales no indican efectos nocivos directos ni indirectos en lo que respecta a la toxicidad reproductiva.
Como medida de precaución, es preferible evitar el uso de TRAYENTA® durante el embarazo.
Lactancia: Los datos disponibles sobre farmacodinamia/toxicología en animales mostraron excreción de linagliptina/sus metabolitos en la leche.
Se desconoce si este fármaco se excreta en la leche humana. Se deberá tener precaución cuando se administre TRAYENTA® a madres lactantes.
Fertilidad: No se han estudiado los efectos de TRAYENTA® sobre la fertilidad humana. No se observaron efectos adversos en la fertilidad en animales, con dosis máximas hasta 240 mg/kg/día (aproximadamente 943 veces superior a la exposición humana, sobre la base de las comparaciones del AUC).
• Capacidad de conducir vehículos u operar maquinarias:
No se han estudiado los efectos sobre la capacidad de conducir vehículos y de operar maquinarias.
• Pacientes pediátricos:
Puesto que no existen datos suficientes sobre la seguridad y efectividad de TRAYENTA® en niños y adolescentes menores de 18 años, no se recomienda su uso en estas poblaciones.
• Pacientes geriátricos:
No es necesario ajustar la dosis.
• Pacientes con insuficiencia renal: No es necesario hacer ningún ajuste de dosis para los pacientes con insuficiencia renal.
• Pacientes con insuficiencia hepática: No es necesario hacer ningún ajuste de dosis para los pacientes con insuficiencia hepática.
PROPIEDADES FARMACOLÓGICAS:
Grupo farmacoterapéutico: Inhibidor de la DPP-4. Código ATC: A10BH05
• Modo de acción: La linagliptina es un inhibidor de la enzima DPP-4 (Dipeptidil peptidasa 4, EC 3.4.14.5), enzima que interviene en la inactivación de las hormonas incretinas GLP-1 y GIP (péptido símil glucagón tipo 1, polipéptido insulinotrópico dependiente de la glucosa). Estas hormonas son rápidamente degradadas por la enzima DPP-4. Ambas hormonas incretinas intervienen en la regulación fisiológica de la homeostasis de la glucosa. Las incretinas se segregan en niveles basales bajos durante todo el día, y sus niveles aumentan inmediatamente después de la ingesta de comida. GLP-1 y el GIP aumentan la biosíntesis de insulina y la secreción de las células beta del páncreas en presencia de concentraciones normales y elevadas de glucosa sanguínea. Más aún la GLP-1 también reduce la excreción de glucagón en las células alfa del páncreas, lo cual conduce a una reducción de la producción hepática de glucosa. La linagliptina (TRAYENTA®) se une con alta afinidad a la DPP-4 de manera reversible y esto conduce a un incremento sostenido y a una prolongación de los niveles de incretinas activas. TRAYENTA® aumenta la secreción de insulina glucosa-dependiente y disminuye la secreción de glucagón, produciendo una mejora global de la homeostasis de la glucosa. La linagliptina se une selectivamente a la DPP-4 con una selectividad > 10000 veces superior comparada con la actividad a la DPP-8 o a la DPP-9 in vitro.
• Estudios clínicos: Linagliptina como monoterapia: La eficacia y seguridad de linagliptina como monoterapia se evaluó en un estudio a doble ciego controlado con placebo de 24 semanas de duración. El tratamiento con 5 mg diarios de linagliptina proporcionó una mejora significativa de la HbA1c (-0,69 % de cambio comparada con placebo), en pacientes con HbA1c basal de aproximadamente 8 %.
La linagliptina también mostró mejora significativa de la glucosa plasmática en ayunas (GPA), (-23,3 mg/dl/-1,3 mmol/l de cambio comparado con placebo), de la glucemia posprandial (GPP) a las 2 horas, y una mayor proporción de pacientes alcanzó la meta de HbA1c de < 7,0 %, comparado con el placebo.
La mejora de la HbA1c no fue afectada por el sexo, la edad, la raza, el índice de masa corporal basal, la existencia de síndrome metabólico, o un índice estándar de resistencia insulínica, HOMA-IR (Homeostatic Model Assessment Insulin Resistance). El tratamiento con 5 mg diarios de linagliptina mejoró significativamente los marcadores indirectos de la función de las células beta, incluyendo el HOMA (Homeostasis Model Assessment), el cociente proinsulina / insulina, y las mediciones de la respuesta de las células beta a partir del test de tolerancia a las comidas en una muestra seleccionada por frecuencia. La incidencia de hipoglucemia observada en los pacientes tratados con linagliptina fue similar a la del placebo. El peso corporal no mostró diferencias significativas entre los grupos.
Monoterapia con linagliptina para pacientes no aptos para recibir metformina: También se evaluó la eficacia y seguridad de la linagliptina como monoterapia en pacientes para quienes la metformina resulta inadecuada, debido a intolerancia o contraindicación, en un estudio doble ciego controlado con placebo de 18 semanas de duración, seguido por un período de extensión de seguridad de 34 semanas (en el cual los pacientes que habían recibido placebo fueron tratados con glimepirida). La linagliptina produjo mejoras significativas de la HbA1c, (-0,60% de cambio comparada con placebo), a partir de una HbA1c media basal de 8,09 %. El cambio medio de HbA1c desde el basal permaneció constante en el grupo tratado con linagliptina desde la semana 18 a la semana 52. La linagliptina también mostró mejoría significativa de la GPA, (-20,5 mg/dl/-1,1 mmol/l de cambio comparado con placebo), y una mayor proporción de pacientes alcanzó la meta de HbA1c < 7,0 %, comparada con placebo. La incidencia de hipoglucemia observada en los pacientes tratados con linagliptina fue similar a la del placebo, y menor que la observada con glimepirida durante el período de extensión de seguridad. El peso corporal no difirió significativamente entre los grupos durante el período de control con placebo de 18 semanas, y los pacientes que recibieron glimepirida aumentaron el peso corporal durante el período de extensión de seguridad.
Linagliptina como monoterapia durante 12 semanas en comparación con el placebo y datos de 26 semanas en comparación con un inhibidor de la α-glucosidasa (voglibosa): También se evaluó la eficacia y seguridad de linagliptina como monoterapia en pacientes japoneses en un estudio a doble ciego en comparación con placebo durante 12 semanas y voglibosa (un inhibidor de la α- glucosidasa) durante 26 semanas. La linagliptina (5 mg) produjo una mejora significativa de la HbA1c, (-0,87 % de cambio comparada con placebo) después de 12 semanas a partir de una HbA1c media basal de 8,0 %. Asimismo, la linagliptina (5 mg) produjo mejoras significativamente superiores de la HbA1c comparada con voglibosa, (-0,32 % de cambio comparada con voglibosa) después de 26 semanas, a partir de una HbA1c media basal de 8,0 %. La linagliptina también mostró mejora significativa de la GPA, (-19,7 mg/dl/-1,1 mmol/l de cambio comparado con placebo, y -6,9 mg/dl/-0,4 mmol/l de cambio comparado con voglibosa) y una mayor proporción de pacientes alcanzó la meta de HbA1c < 7,0 %, comparada con placebo y con voglibosa. La incidencia de hipoglucemia observada en los pacientes tratados con linagliptina fue similar a la del placebo y a la observada con voglibosa. El peso corporal no difirió significativamente entre linagliptina (5 mg) y placebo después de 12 semanas de tratamiento. Los pacientes tratados con linagliptina (5 mg), mostraron una pequeña disminución media del peso corporal en comparación con los valores basales (-0,16 kg) después de 26 semanas, comparada con una disminución media significativamente mayor del peso corporal en los pacientes tratados con voglibosa (-1,04 kg).
Linagliptina adicional al tratamiento con metformina: La eficacia y seguridad de linagliptina en combinación con metformina se evaluó en un estudio a doble ciego comparativo con placebo de 24 semanas de duración. La linagliptina produjo una mejora significativa de la HbA1c, (-0,64 % de cambio comparada con placebo) a partir de una HbA1c media basal de 8%.
La linagliptina también mostró mejoría significativa de la GPA, (-21,1 mg/dl/-1,2 mmol/l), la GPP a las 2 horas de -67,1 mg/dl (-3,7 mmol/l) en comparación con el placebo y una mayor proporción de pacientes alcanzó la meta de HbA1c < 7,0 %, (28,3% con linagliptin vs. 11,4% con placebo). La incidencia de hipoglucemia observada en los pacientes tratados con linagliptina fue similar a la del placebo. El peso corporal no difirió significativamente entre los grupos.
La eficacia y seguridad de linagliptina en combinación con metformina se evaluó en un estudio factorial de tratamiento inicial controlado con placebo de 24 semanas de duración. La linagliptina, 2,5 mg dos veces por día, en combinación con metformina (500 mg o 1000 mg dos veces por día) produjo mejoras significativas en los parámetros glicémicos en comparación con cualquiera de las dos monoterapias (HbA1c media basal 8,65 %).
La diferencia media de HbA1c entre el tratamiento combinado de linagliptina y metformina en comparación con la monoterapia con metformina desde el inicio hasta la semana 24 (extrapolación de la última observación [LOCF]) fue -0,51% (IC del 95 % -0,73, -0,30; p < 0,0001) para el tratamiento con 2,5 mg de linagliptina + 1000 mg de metformina dos veces por día en comparación con 1000 mg de metformina dos veces por día, -0,58 % % (IC del 95 % -0,79; -0,36; p < 0,0001) para el tratamiento con 2,5 mg de linagliptina + 500 mg de metformina dos veces por día en comparación con 500 mg de metformina dos veces por día. La media de cambio de HbA1c corregida por placebo desde el inicio para el tratamiento con 2,5 mg de linagliptina + 1000 mg de metformina dos veces por día fue 1,71 % lo que permitió el control de HbA1c (< 7,0 %) en 53,6 % de los pacientes (en comparación con 30,7 % de los pacientes en monoterapia con 1000 mg de metformina dos veces por día). La disminución media de HbA1c desde el inicio fue generalmente mayor en los pacientes con valores basales más elevados de HbA1c. El efecto sobre los lípidos plasmáticos generalmente fue neutro. La disminución del peso corporal con la combinación de linagliptina y metformina fue similar a la observada con metformina como monoterapia o con placebo; no hubo cambios desde el inicio para los pacientes que recibieron linagliptina como monoterapia. La incidencia de la hipoglucemia fue similar en todos los grupos de tratamiento (placebo 1,4 %; linagliptina 5 mg 0 %; metformina 2,1 %, y linagliptina 2,5 mg en combinación con metformina dos veces por día 1,4%).
Asimismo, este estudio incluyó pacientes (n = 66) con hiperglucemia más grave (HbA1c basal ≥11 %) tratados con linagliptina 2,5 mg y metformina 1000 mg dos veces por día, en un estudio abierto. En este grupo de pacientes, la HbA1c basal media fue 11,8 % y la GPA media fue 261,8 mg/dl/14,5 mmol/l. Se observó una disminución media desde los valores basales de -3,74 % en la HbA1c (n = 48) y de -81,2 mg/dl/- 4,5 mmol/l en la GPA (n = 41) en los pacientes que completaron el período de estudio de 24 semanas sin terapia de rescate. En el análisis LOCF que incluyó a todos los pacientes con mediciones del criterio de valoración primario (n = 65) en la última observación sin terapia de rescate los cambios desde los valores basales fueron -3,19 % para la HbA1c y de -73,6 mg/dl/-4,1 mmol/l para la GPA.
La eficacia y seguridad de linagliptina 2,5 mg dos veces por día en comparación con linagliptina 5 mg una vez por día en combinación con metformina en pacientes con control glicémico insuficiente con monoterapia con metformina se evaluó en un estudio a doble ciego controlado con placebo de 12 semanas de duración. La linagliptina (2,5 mg dos veces por día y 5 mg una vez por día) combinada con metformina produjo mejoras significativas en los parámetros glicémicos en comparación con placebo. La linagliptina 5 mg una vez por día y 2,5 mg dos veces por día produjo disminuciones significativas y comparables de la HbA1c (IC: -0,07; 0,19) de -0,80 % (a partir del valor basal de 7,98 %), y de -0,74 (a partir del valor basal de 7,96 %) en comparación con placebo. La incidencia de hipoglucemia observada en los pacientes tratados con linagliptina fue similar a la del placebo. El peso corporal no difirió significativamente entre los grupos.
Linagliptina en adición al tratamiento con sulfonilurea: La eficacia y seguridad de linagliptina en combinación con una sulfonilurea se evaluó en un estudio a doble ciego controlado con placebo de 18 semanas de duración. La linagliptina proporcionó una mejoría significativa de la HbA1c, (-0,47 % de cambio comparada con placebo) a partir de una HbA1c media basal de 8,6 %. La linagliptina también mostró mejorías significativas en pacientes que alcanzaron la meta de HbA1c de < 7,0 %. El peso corporal no difirió significativamente entre los grupos.
Linagliptina en adición al tratamiento con insulina: La eficacia y la seguridad de la administración concomitante de linagliptina 5 mg con el tratamiento con insulina sola o en combinación con metformina o pioglitazona se ha evaluado en un estudio a doble ciego en comparación con placebo de 24 semanas de duración.
La diferencia media entre los valores basales y los de la semana 24 (LOCF) de HbA1c para el tratamiento con linagliptina en comparación con placebo fue -0,65 % (IC de 95 % -0,74; -0,55; p < 0,0001) a partir de un valor basal de HbA1c de 8,3 %. Las reducciones promedio a partir de los valores basales de HbA1c en general fueron mayores en los pacientes con valores basales de HbA1c más elevados. Para la linagliptina, el cambio promedio de HbA1c a partir de los valores basales fue sostenido desde la semana 12 hasta la semana 24. La linagliptina también produjo mejoras significativas en los valores de GPA de -11,25 mg/dl/-0,62 mmol/l (IC del 95 % -16,14, -6,36; p<0,0001) en comparación con placebo, y un porcentaje más elevado de pacientes alcanzó el objetivo de HbA1c de < 7,0 % en comparación con placebo. Esto se logró con una dosis estable de insulina. Luego de 24 semanas de tratamiento, la dosis diaria promedio de insulina al inicio fue 42 unidades en los pacientes tratados con linagliptina y 40 unidades en los pacientes que recibieron placebo. El cambio promedio en la dosis diaria de insulina desde el inicio hasta la semana 24 fue 1,3 UI en el grupo placebo y 0,6 UI en el grupo linagliptina. No se observaron diferencias significativas entre los grupos en el peso corporal. El efecto sobre los lípidos plasmáticos fue neutral. La incidencia de hipoglucemia fue similar en ambos grupos de tratamiento (22,2 % para linagliptina y 21,2 % para placebo).
Linagliptina en adición a una combinación de metformina y sulfonilurea: Se realizó un estudio controlado con placebo de 24 semanas de duración para evaluar la eficacia y seguridad de 5 mg de linagliptina en comparación con placebo en pacientes insuficientemente tratados con una combinación de metformina y una sulfonilurea. La linagliptina proporcionó una mejoría significativa de la HbA1c, (-0,62 % de cambio comparada con placebo) a partir de una HbA1c media basal de 8,14 %. La linagliptina también mostró mejoras significativas en pacientes que alcanzaron la meta de HbA1c de < 7,0 % y también de glucosa plasmática en ayunas (GPA) (-12,7 mg/dl/-0,7 mmol/l), comparada con placebo. El peso corporal no difirió significativamente entre los grupos.
Linagliptina en adición a una combinación de metformina y empagliflozina: En pacientes que no estaban bien controlados con metformina y empagliflozina [10 mg (n = 247) o 25 mg (n = 217)], el tratamiento de adición de 5 mg de linagliptina durante 24 semanas se redujo la HbA1c media ajustada con respecto a los valores de referencia, respectivamente, en -0,53 % (diferencia significativa con respecto a la adición de placebo: -0,32 %; IC del 95 %: -0,25; -0,13) y -0,58 (diferencia significativa con la adición de placebo: -0,47 %; IC del 95 %: -0,66; -0,28). Una proporción mayor de pacientes con una HbA1c basal ≥ 7,0%, tratados con linagliptina 5mg, alcanzó la meta de ese parámetro (< 7 %) en comparación con placebo, lo cual fue estadísticamente significativo.
En subgrupos prespecificados de pacientes con HbA1c basal de 8,5 % o más (metformina más empagliflozina; 10 mg: n = 66; 25 mg: n = 42), la reducción media ajustada de ese valor desde el inicio hasta la semana 24, con la adición de linagliptina 5 mg fue, para ambas dosis de -0,97 % (p de la diferencia con la adición de placebo = 0,0875) y -1,16 % (p de la diferencia con la adición de placebo = 0,0046), respectivamente.
Linagliptina como tratamiento inicial combinado con pioglitazona: En un estudio controlado con placebo de 24 semanas en el cual se inició el tratamiento con 5 mg de linagliptina en combinación con 30 mg de pioglitazona, el tratamiento inicial con linagliptina y pioglitazona demostró una mejoría significativa de la HbA1c comparado con pioglitazona y placebo (-0,51 %), a partir de una HbA1c media basal de 8,6 %. La combinación inicial de linagliptina y pioglitazona también mostró mejorías significativas de la GPA (-14,2 mg/dl/-0,8 mmol/l de cambio comparado con placebo), y una mayor proporción de pacientes tendieron a alcanzar la meta de HbA1c (< 7 %), y una reducción de la HbA1c ≥ 0,5 %. El peso corporal aumentó significativamente más con el tratamiento inicial con linagliptina en combinación con pioglitazona, que con pioglitazona y placebo (1,1 kg).
Linagliptina como tratamiento adicional de una combinación de metformina y pioglitazona: Se realizó un estudio comparativo con placebo de 24 semanas de duración para evaluar la eficacia y seguridad de 5 mg de linagliptina en comparación con placebo en pacientes insuficientemente tratados con una combinación de metformina y pioglitazona. La linagliptina proporcionó una mejoría significativa de la HbA1c, (-0,57 % de cambio comparada con placebo) a partir de una HbA1c media basal de 8,42 %. La linagliptina también mostró mejorías significativas en pacientes que alcanzaron la meta de HbA1c de < 7,0 % y también de GPA (-10,4 mg/dl/-0,6 mmol/l), comparada con placebo. El peso corporal no difirió significativamente entre los grupos.
Datos de 24 meses con linagliptina en adición a metformina, en comparación con glimepirida: En un estudio que comparó la eficacia y seguridad de la adición de 5 mg de linagliptina o glimepirida (una sulfonilurea) en pacientes con control glicémico inadecuado, bajo tratamiento con metformina como monoterapia, la linagliptina fue similar a la glimepirida en reducir la HbA1c, con una diferencia media de la HbA1c entre tratamientos desde el nivel basal hasta las 104 semanas de +0,20 % para la linagliptina comparada con la glimepirida.
En este estudio, el cociente entre proinsulina e insulina, un marcador de la eficiencia de la síntesis y la liberación de insulina, mostró una mejoría estadísticamente significativa con linagliptina comparada con glimepirida. La incidencia de hipoglucemia en el grupo tratado con linagliptina (7,5 %) fue significativamente menor que en el grupo tratado con glimepirida (36,1 %). Los pacientes tratados con linagliptina mostraron una disminución media significativa a partir del peso corporal basal comparado con un aumento de peso significativo en los pacientes tratados con glimepirida (-1,39 vs. +1,29 kg).
Linagliptina como tratamiento adicional en pacientes con insuficiencia renal grave, datos comparativos con placebo de 12 semanas (tratamiento de base sin modificaciones) y período de extensión comparativo con placebo de 40 semanas (tratamiento de base con ajuste de la dosis): También se evaluó la eficacia y seguridad de la linagliptina en DM2 en pacientes con insuficiencia renal grave en un estudio a doble ciego comparativo con placebo de 12 semanas de duración, durante el cual los tratamientos de base de control glicémico se mantuvieron sin modificaciones. Los pacientes recibían una variedad de tratamientos de base que incluían insulina, sulfonilurea, glinidas y pioglitazona. El estudio incluyó un período de seguimiento de 40 semanas durante el cual se permitió el ajuste de las dosis de la terapia antidiabética de base.
La linagliptina produjo mejoras significativas de la HbA1c (-0,59% de cambio comparado con placebo) a partir de la HbA1c basal media de 8,2%. Una mayor proporción de pacientes alcanzó la meta de HbA1c de < 7,0%, comparado con placebo. La diferencia de HbA1c observada en comparación con placebo fue de -0,72% después de 52 semanas. El peso corporal no difirió significativamente entre los grupos. La incidencia de hipoglucemia observada en los pacientes tratados con linagliptina fue mayor que la observada con placebo debido a un aumento en los episodios hipoglucémicos asintomáticos, lo cual puede atribuirse a las terapias antidiabéticas de base (insulina y sulfonilurea o glinidas). No se observaron diferencias entre los grupos en los episodios hipoglucémicos graves.
Linagliptina como tratamiento adicional en pacientes de edad avanzada (edad ≥ 70 años) con diabetes tipo 2: La eficacia y la seguridad de la linagliptina en los pacientes de edad avanzada (edad ≥ 70 años) con diabetes tipo 2 han sido evaluadas en un estudio de diseño doble ciego comparado con placebo de 24 semanas de duración. Los pacientes recibieron metformina y/o sulfonilurea y/o insulina como tratamiento de base. Las dosis de medicación antidiabética de base se mantuvieron estables durante las primeras 12 semanas, luego de las cuales se permitieron ajustes. La linagliptina permitió lograr mejoras significativas en los valores de HbA1c, de -0,64 % (IC del 95 % -0,81, -0,48; p <0,0001) en comparación con el placebo al cabo de 24 semanas, respecto de un valor basal medio de HbA1c de 7,8 %. La linagliptina también evidenció mejorías significativas en los valores de GPA, de -20,7 mg/dl (IC del 95 % -30,2, -11,2; p <0,0001) en comparación con placebo (-1,1 mmol/l). El peso corporal no difirió significativamente entre los grupos. Las tasas de hipoglucemia también fueron comparables en una base de insulina con o sin metformina (13 de 35 pacientes, 37,1% tratados con linagliptina y 6 de 15 pacientes, 40 % tratados con placebo). Sin embargo, con una base de sulfonilurea con o sin metformina, se reportó hipoglucemia en una proporción más altas de pacientes tratados con linagliptina (24 de 82 pacientes, 29,3 %) comparado con placebo (7 de 42 pacientes, 16,7 %).
No hubo ninguna diferencia entre los grupos en lo que respecta a los eventos de hipoglucemia grave.
Linagliptina como tratamiento adicional de un tratamiento antidiabético oral preexistente, a lo largo de 52 semanas, en pacientes japoneses con diabetes tipo 2: La seguridad y la eficacia de la linagliptina fueron evaluadas en un estudio de diseño abierto, de grupos paralelos, en sujetos japoneses con DM2 insuficientemente tratados con un antidiabético oral (biguanida, glinida, glitazona, sulfonilurea [SU] o un inhibidor de la α-glucosidasa [A-GI]).
La linagliptina brindó mejorías estadísticamente significativas en la HbA1c y la GPA respecto del nivel basal en la semana 52 para todos los grupos de tratamiento de base), de un valor medio basal previo de HbA1c de 7,98 %. Las reducciones se ubicaron en el rango de -0,91 % a -0,70 %. La mejoría observada fue del -0,88 % en el grupo de biguanida y linagliptina; -0,73 % en el grupo de glinida y linagliptina, -0,79 % en el grupo de glitazona y linagliptina; -0,70 % en el grupo de sulfonilurea y linagliptina; y -0,91 % en el grupo de inhibidor de α-glucosidasa y linagliptina. Para la GPA, las reducciones se ubicaron en el rango entre -12,6 mg/dl/-0,7 mmol/l y -6,0 mg/dl/-0.3 mmol/l. La reducción observada fue -12,6 mg/dl/-0,7 mmol/l en el grupo de biguanida y linagliptina; -9,1 mg/dl/-0,5 mmol/l en el grupo de glinida y linagliptina, -9,8 mg/dl/- 0,5 mmol/l en el grupo de glitazona y linagliptina; -6,7 mg/dl/-0,4 mmol/l en el grupo de sulfonilurea y linagliptina; y -6,0 mg/dl/-0,3 mmol/l en el grupo de inhibidor de α-glucosidasa y linagliptina. En lo que respecta al peso corporal, los cambios entre el nivel basal y la semana 52 no difirieron significativamente para ninguno de los grupos de tratamiento de base.
La linagliptina fue similar a la metformina, sumada a un tratamiento de base con una sulfonilurea, en lo que respecta a la reducción de la HbA1c, con un valor medio de diferencia entre los tratamientos en términos de HbA1c entre el nivel basal y las 52 semanas para la linagliptina en comparación con metformina de + 0,18 %. La linagliptina fue similar a la metformina, sumada a un tratamiento de base con un inhibidor de la α- glucosidasa, en lo que respecta a la reducción de la HbA1c, con un valor medio de diferencia entre los tratamientos en términos de HbA1c entre el nivel basal y las 52 semanas para la linagliptina en comparación con la metformina de + 0,09 %.
Los eventos de hipoglucemia fueron informados infrecuentemente en todos los grupos (5,8 %) excepto en el caso de los pacientes que recibían tratamiento de base con una sulfonilurea, y en todos los casos fueron de intensidad leve. La incidencia observada de hipoglucemia se observó principalmente cuando la linagliptina se usó con una sulfonilurea (81 %); sin embargo, la frecuencia fue comparable a la observada para la metformina sumada a un régimen de base de una sulfonilurea.
Linagliptina y combinación inicial de linagliptina y metformina en pacientes con diagnóstico reciente, sin tratamiento previo, con hiperglucemia marcada: La eficacia y la seguridad de la combinación inicial de linagliptina 5 mg una vez al día y metformina dos veces al día (con ajuste ascendente de dosis durante las primeras 6 semanas a 1500 mg o 2000 mg/d) en comparación con linagliptina 5 mg una vez al día fue evaluada en un estudio de 24 semanas de duración en pacientes con diagnóstico reciente de diabetes mellitus tipo 2 y sin tratamiento previo que presentaban hiperglucemia marcada (valor basal de HbA1c de 8,5-12,0 %). Luego de 24 semanas, tanto la monoterapia con linagliptina como la combinación inicial de linagliptina y metformina redujeron de modo significativo los niveles de HbA1c a razón de -2,0 % y -2,8 % respectivamente, respecto de un valor inicial de HbA1c de 9,9% y 9,8 %, respectivamente. La diferencia entre los tratamientos observada, de -0,8 % (IC del 95 %: -1,1 a -0,5), indicó la superioridad de la combinación inicial frente a la monoterapia (p <0,0001). Es de destacar que el 40 % y el 61 % de los pacientes de los grupos de monoterapia y de la combinación, alcanzaron niveles de HbA1c <7,0 %.
Estudio de seguridad cardiovascular y renal con linagliptina (CARMELINA): CARMELINA fue un estudio aleatorizado realizado sobre 6979 pacientes con diabetes tipo 2, con riesgo cardiovascular elevado, evidenciado por la presencia de antecedentes de enfermedad renal o macrovascular establecida, que habían recibido 5 mg de linagliptina (3494) o placebo (3485) agregados al tratamiento protocolar regionalmente establecido para lograr los objetivos de HbA1c, para controlar los factores de riesgo cardiovascular y la enfermedad renal. La población del estudio incluyó 1211 (17,4 %) pacientes ≥ 75 años de edad y 4348 (62,3 %) pacientes con insuficiencia renal. Aproximadamente el 19 % de la población tenía una TFGe ≥ 45 y < 60 ml/min/1,73 m2, 28 % de la población tenía una TFGe ≥ 30 y < 45 ml/min/1,73 m2 y 15 % tenía una TFGe <30 ml/min/1,73 m2.
La HbA1c media al inicio del estudio fue del 8,0 %.
El estudio estuvo diseñado para demostrar la no inferioridad en función del criterio de valoración cardiovascular primario, que era un compuesto de la primera aparición de: o bien muerte cardiovascular, o un infarto de miocardio no mortal (IM), o un accidente cerebrovascular no mortal (3P-MACE). El criterio de valoración compuesto renal se definió como muerte renal o enfermedad renal en etapa terminal sostenida, o disminución sostenida del 40 % o más en la TFGe.
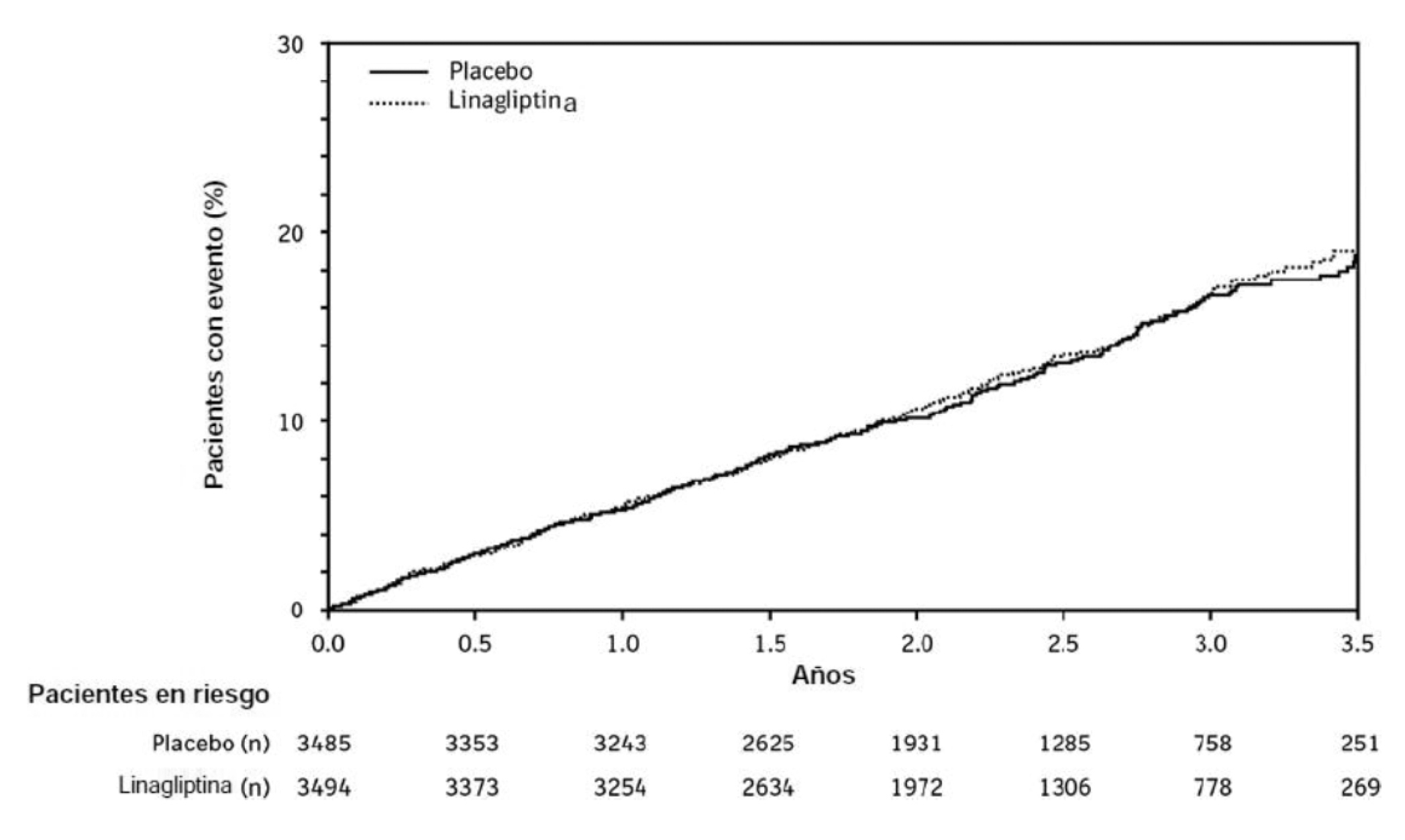
Después de un seguimiento de 2,2 años (mediana), la linagliptina, agregada al tratamiento estándar, no aumentó el riesgo de eventos cardiovasculares graves o eventos de desenlace renal (Tabla 1 y Figura 1). No hubo un aumento en el riesgo de hospitalización por insuficiencia cardíaca, que fue un criterio de valoración adjudicado adicional observado, en comparación con el tratamiento estándar sin linagliptina en pacientes con diabetes tipo 2 (Tabla 2).
|
Tabla 1. Eventos adversos graves cardiovaculares (MACE) y eventos de desenlace renal estratificados por grupo de tratamiento en el estudio CARMELINA |
|||||
|
Linagliptina 5 mg |
Placebo |
Razón de riesgos instantáneos |
|||
|
Cantidad de sujetos (%) |
Tasa de incidencia por cada 1000 PY* |
Cantidad de sujetos (%) |
Tasa de incidencia por cada 1000 PY* |
(IC del 95 %) |
|
|
Cantidad de pacientes |
3494 |
3485 |
|||
|
Compuesto CV (muerte por evento cardiovascular, IM no mortal, accidente cerebrovascular no mortal) |
434 (12,4) |
57,7 |
420 (12,1) |
56,3 |
1,02 (0,89 - 1,17)** |
|
Compuesto renal secundario (muerte renal, enfermedad renal terminal, disminución sostenida del 40 % de la TFGe) |
327 (9,4) |
48,9 |
306 (8,8) |
46,6 |
1,04 (0,89 - 1,22) |
|
* PY = años paciente ** Prueba de no inferioridad para demostrar que el límite superior del IC del 95 % para la razón de riesgos instantáneos es menor a 1,3 |
|||||
Figura 1. Tiempo transcurrido hasta la primera aparición de un componente el 3P- MACE en el estudio CARMELINA
|
Tabla 2. Hospitalización por insuficiencia cardíaca y mortalidad estratificados por grupo de tratamiento, en el estudio CARMELINA |
|||||
|
Linagliptina 5 mg |
Placebo |
Razón de riesgos instantáneos |
|||
|
Cantidad de sujetos (%) |
Tasa de incidencia por cada 1000 PY* |
Cantidad de sujetos (%) |
Tasa de incidencia por cada 1000 PY* |
(IC del 95%) |
|
|
Cantidad de pacientes |
3494 |
3485 |
|||
|
Mortalidad por todas las causas |
367 (10,5) |
46,9 |
373 (10,7) |
48,0 |
0,98 (0,84 - 1,13) |
|
Muerte por evento CV |
255 (7,3) |
32,6 |
264 (7,6) |
34 |
0,96 (0,81 - 1,14) |
|
Hospitalización por insuficiencia cardíaca |
209 (6,0) |
27,7 |
226 (6,5) |
30,4 |
0,90 (0,74 - 1,08) |
|
* PY = años-paciente |
|||||
En los análisis de progresión de la albuminuria (cambio de normoalbuminuria a micro o macroalbuminuria, o de microalbuminuria a macroalbuminuria), la razón de riesgos instantáneos estimada para la linagliptina, en comparación con placebo, fue 0,86 (IC del 95 %: 0,78 a 0,95). El criterio de valoración microvascular se definió como el compuesto de muerte renal, enfermedad renal crónica sostenida, reducción sostenida ≥ 50 % de la TFGe, progresión de la albuminuria, tratamiento de la retinopatía diabética con fotocoagulación retineana o inyecciones intravítreas de inhibidores del factor de crecimiento endotelial vascular, hemorragia vítrea o ceguera provocada por la diabetes. La razón de riesgos instantáneos estimada para el tiempo transcurrido hasta la primera aparición del criterio de valoración microvascular compuesto fue 0,86 (IC del 95 %: 0,78; 0,95) para la linagliptina, comparada con el placebo, y se debió principalmente a la progresión de la albuminuria.
Estudio de seguridad cardiovascular con linagliptina (CAROLINA): CAROLINA fue un estudio aleatorizado realizado con 6033 pacientes con diabetes tipo 2 incipiente y con riesgo cardiovascular elevado o complicaciones establecidas, que habían recibido 5 mg de linagliptina (3023) o glimepirida 1 - 4 mg (3010) agregados al tratamiento estándar (que incluyó un tratamiento de base con metformina en el 83 % de los pacientes) establecido regionalmente para lograr los objetivos de HbA1c y los factores de riesgo CV. La edad media de la población del estudio era 64 años e incluyó 2030 (34 %) pacientes ≥ 70 años de edad. La población del estudio incluyó 2089 (35 %) pacientes con enfermedad cardiovascular y 1130 (19 %) pacientes con insuficiencia renal con una TFGe basal < 60 ml/min/1,73 m2. La HbA1c media basal fue del 7,15 %.
El estudio se diseñó para demostrar la no inferioridad en función del criterio de valoración cardiovascular primario, que era un compuesto de la primera aparición de muerte por evento cardiovascular, un infarto de miocardio no mortal (IM), o un accidente cerebrovascular no mortal (3P-MACE).
Después de un seguimiento de 6,25 años (mediana), la linagliptina no aumentó el riesgo de eventos cardiovasculares graves (Tabla 3) en comparación con la glimepirida. Los resultados fueron concordantes para los pacientes tratados con o sin metformina.
|
Tabla 3. Eventos adversos cardiovasculares primarios (MACE) y mortalidad por grupo de tratamiento en el estudio CAROLINA |
|||||
|
Linagliptina 5 mg |
Glimepirida (1 - 4 mg) |
HR |
|||
|
Cantidad de sujetos (%) |
Tasa de incidencia por cada 1000 PY* |
Cantidad de sujetos (%) |
Tasa de incidencia por cada 1000 PY* |
(IC del 95%) |
|
|
Cantidad de pacientes |
3023 |
3010 |
|||
|
Compuesto CV primario (muerte por evento cardiovascular, IM no mortal, accidente cerebrovascular no mortal) |
356 (11,8) |
20,7 |
362 (12,0) |
21,2 |
0,98 (0,84 - 1,14)** |
|
* PY = años-paciente ** Prueba de no inferioridad para demostrar que el límite superior del IC del 95 % para la razón de riesgos instantáneos es menor a 1,3 |
|||||
El compuesto de sustentabilidad del tratamiento, un criterio de valoración secundaria clave, se definió como la proporción de pacientes sometidos al tratamiento del estudio luego del período de ajuste inicial (16 semanas) que mantienen el control glucémico (HbA1c ≤ 7,0 %) en la visita final sin necesidad de tratamiento adicional con fármacos antidiabéticos (medicación de rescate), sin ningún episodio de hipoglucemia moderado (sintomático con un valor de glucosa ≤ 70 mg/dl) o grave (que requiere asistencia) y sin un incremento de peso de > 2 %. Una cantidad más elevada de pacientes en tratamiento con linagliptina (481; 16 %) alcanzó este criterio de valoración secundaria clave en comparación con glimepirida (305; 10,2 %).
Para todo el período de tratamiento (mediana de tiempo en tratamiento de 5,9 años), la tasa de pacientes con hipoglucemia moderada o grave fue de 6,5 % con linagliptina frente al 30,9 % con glimepirida, el 0,3 % de los pacientes experimentó hipoglucemia grave con linagliptina frente al 2,2 % con glimepirida.
• Farmacocinética:
La farmacocinética de linagliptina ha sido caracterizada extensamente en individuos sanos y en pacientes con diabetes tipo 2. Después de la administración oral de una dosis de 5 mg a voluntarios sanos y pacientes, la linagliptina se absorbió rápidamente, con concentraciones plasmáticas máximas (Tmáx, mediana) de 1,5 horas después de la dosis.
Las concentraciones plasmáticas de linagliptina disminuyen de manera al menos bifásica, con una prolongada vida media terminal (más de 100 horas), que se relaciona principalmente con la unión estrecha y saturable de la linagliptina con la DPP-4, y que no contribuye a la acumulación del fármaco. La vida media eficaz para la acumulación de linagliptina, después de la administración oral de varias dosis de 5 mg, es aproximadamente de 12 horas. Después de la administración de 5 mg de linagliptina una vez por día, las concentraciones plasmáticas en estado de equilibrio se alcanzan con la tercera dosis. El AUC plasmática de linagliptina aumentó aproximadamente 33% después de administrar dosis de 5 mg en estado de equilibrio, en comparación con la primera dosis. Los coeficientes de variación intra e interindividual para el AUC de linagliptina fueron pequeños (12,6% y 28,5%, respectivamente). El AUC plasmática de la linagliptina aumentó en una proporción menor que la dosis. En general, la farmacocinética de la linagliptina fue similar en individuos sanos y en pacientes con diabetes tipo 2.
• Absorción:
La biodisponibilidad absoluta de la linagliptina es aproximadamente 30%. Debido a que la administración concomitante de comidas con alto contenido graso y linagliptina no causó efectos clínicos relevantes sobre su farmacocinética, esta puede administrarse con o sin alimentos. Estudios in vitro indican que la linagliptina es un sustrato de la glucoproteína P y del CYP3A4. El ritonavir, un inhibidor potente de la glucoproteína P y del CYP3A4, elevó al doble la exposición (AUC), y la coadministración múltiple de linagliptina con rifampicina, un inductor potente de la P-gp y del CYP3A dio lugar a una disminución aproximada del 40 % del AUC de linagliptina en estado de equilibrio, presumiblemente por aumento/disminución de la biodisponibilidad de la linagliptina por inhibición/inducción de la glucoproteína P.
• Distribución:
Como resultado de la unión a los tejidos, la media del volumen de distribución aparente en estado de equilibrio después de administrar una dosis intravenosa única de 5 mg de linagliptina a individuos sanos, es de aproximadamente 1110 litros, lo cual indica que la linagliptina se distribuye ampliamente en los tejidos. La unión de linagliptina a las proteínas plasmáticas depende de su concentración: disminuye desde alrededor del 99% a 1 nmol/l al 75 - 89% a ≥ 30 nmol/l, reflejando la saturación de la unión a la DPP-4 con concentraciones crecientes de linagliptina. En concentraciones elevadas, donde la DPP-4 está enteramente saturada, entre el 70-80 % de la linagliptina se unió a otras proteínas plasmáticas distintas de la DPP-4, de ahí que entre el 20-30 % no estuviera unida en el plasma.
• Biotransformación
Después de administrar una dosis oral de 10 mg de [14C] linagliptina, aproximadamente el 5 % de la radioactividad se excretó en la orina. El metabolismo desempeña una función subordinada en la eliminación de linagliptina. Se detectó un metabolito principal que resultó farmacológicamente inactivo, con una exposición relativa de la linagliptina del 13,3 % en estado de equilibrio, por lo cual no contribuye a la actividad inhibitoria de linagliptina sobre la DPP-4.
• Excreción
Después de la administración de una dosis oral de [14C] linagliptina a individuos sanos, aproximadamente el 85% de la radioactividad administrada se eliminó por las heces (80%) o la orina (5 %) en los 4 días posteriores a la administración de la dosis. La depuración renal en estado de equilibrio fue alrededor de 70 ml/min.
• Poblaciones especiales
Insuficiencia renal: Se llevó a cabo un estudio con dosis múltiples, abierto, para evaluar la farmacocinética de la linagliptina (dosis de 5 mg) en pacientes con distintos grados de insuficiencia renal crónica, comparados con individuos sanos como control. El estudio incluyó pacientes con insuficiencia renal clasificada según la depuración de creatinina como leve (50 a < 80 ml/min), moderada (30 a < 50 ml/min) y grave (< 30 ml/min), además de los pacientes con enfermedad renal terminal (ESRD) en hemodiálisis. Además, los pacientes con DM2 y disfunción renal grave (< 30 ml/min) fueron comparados con pacientes DM2 con función renal normal. Se determinó la depuración de creatinina en orina de 24 horas o se estimó a partir de la creatinina sérica sobre la base de la fórmula de Cockcroft-Gault:
CrCl = [140 - edad (años)] x peso (kg) (x 0,85 para pacientes mujeres) / [72 x creatinina sérica (mg/dl)]
En estado de equilibrio, la exposición a linagliptina fue comparable en los pacientes con insuficiencias renales leves y los individuos sanos. Se observó un moderado incremento de la exposición (alrededor de 1,7 veces) en los pacientes con insuficiencia renal moderada, en comparación con los controles. La exposición en los pacientes con DM2 e insuficiencia renal grave aumentó aproximadamente 1,4 veces comparados con los pacientes con DM2 con función renal normal. El AUC previsto de linagliptina en estado de equilibrio en pacientes con enfermedad renal terminal indicó una exposición comparable a la observada en pacientes con insuficiencias renales moderadas a graves. Además, no se prevé que la linagliptina sea eliminada en grado terapéuticamente significativo por hemodiálisis o diálisis peritoneal. Por lo tanto, no es necesario ajustar la dosis de linagliptina en pacientes con cualquier grado de insuficiencia renal. Además, la insuficiencia renal leve no tuvo efecto sobre la farmacocinética de la linagliptina en pacientes con diabetes tipo 2 como lo indican los análisis farmacocinéticos en la población.
Insuficiencia hepática: En los pacientes con insuficiencia hepática leve, moderada y grave (según la clasificación Child- Pugh), las AUC y la Cmáx medias de linagliptina fueron similares a las de los controles sanos comparables, después de la administración de dosis múltiples de 5 mg de linagliptina. No es necesario ajustar la dosis de linagliptina en los pacientes con insuficiencia hepática leve, moderada o grave.
Índice de masa corporal (IMC): No se requiere ajustar la dosis de acuerdo con el índice de masa corporal. El índice de masa corporal no tuvo efecto clínicamente relevante con respecto a la farmacocinética de linagliptina sobre la base de un análisis farmacocinético de la población de los estudios en Fase I y Fase II.
Sexo: No se requiere ajustar la dosis según el sexo. El sexo no tuvo efecto clínicamente relevante con respecto a la farmacocinética de linagliptina a partir de un análisis farmacocinético de los datos de la población de los estudios en Fase I y Fase II.
Población de edad avanzada: No se requiere ajuste de la dosis debido a la edad, dado que la edad no tiene un impacto de interés clínico respecto de la farmacocinética de linagliptina con base en un análisis de los datos farmacocinéticos en una población, de Fase I y Fase II. Las personas de edad avanzada (65 a 80 años) tuvieron concentraciones plasmáticas de linagliptina similares a las de las personas más jóvenes.
Población pediátrica: Aún no se han llevado a cabo estudios sobre farmacocinética con linagliptina en pacientes pediátricos.
Raza: No se requiere ajustar la dosis debido a la raza. La raza no tuvo efectos manifiestos sobre las concentraciones plasmáticas de linagliptina basado en análisis compuestos de los datos farmacocinéticos disponibles, que incluyeron pacientes de origen caucásico, hispano, afroamericano y asiático. Además, se observó que las características farmacocinéticas de la linagliptina fueron similares en estudios especiales de Fase I realizados en voluntarios sanos japoneses, chinos y caucásicos y en pacientes afroamericanos con diabetes tipo 2.
CONTRAINDICACIONES: Hipersensibilidad al principio activo o a alguno de los excipientes. Embarazo y lactancia, niños y adolescentes menores de 18 años.
REACCIONES ADVERSAS: Resumen del perfil de seguridad: La seguridad de TRAYENTA® se evaluó en pacientes con DM2, los cuales en la mayoría de los casos recibieron una dosis diana de 5 mg.
En el análisis combinado de los estudios comparativos con placebo, la incidencia general de eventos adversos (EA) en pacientes tratados con placebo fue similar a la observada con 5 mg de linagliptina (63,4 % vs. 59,1 %).
La discontinuación del tratamiento debida a EA fue más elevada en los pacientes que recibieron placebo que en los que recibieron 5 mg de linagliptina (4,3 % vs. 3,4 %).
Debido al impacto del tratamiento de base sobre los eventos adversos (por ejemplo, sobre la hipoglucemia), se analizaron los eventos adversos en relación a los respectivos esquemas de tratamiento (como monoterapia, adicional a metformina, adicional a tiazolidinediona [un fármaco agonista de los PPARg]), adicional a sulfonilurea, adicional a metformina más una sulfonilurea, adicional a insulina y adicional a la metformina e inhibidores del SGLT2.
Los estudios comparativos con placebo incluyen 28 estudios donde la linagliptina se administró como:
— Monoterapia a corto plazo, hasta 4 semanas
— Monoterapia con ≥ 12 semanas de duración
— Adicional a metformina
— Tratamiento combinado inicial con pioglitazona
— Adicional a una sulfonilurea
— Adicional a metformina + sulfonilurea
— Adicional a insulina (con o sin metformina y/o pioglitazona y/o sulfonilurea)
— Adicional a metformina y empagliflozina
El efecto adverso informado con mayor frecuencia fue la hipoglucemia observada con la combinación triple de linagliptina más metformina más sulfonilurea, 22,9 % vs. 14,8 % placebo.
En los estudios comparativos con placebo (10,9 %; N = 471), las hipoglucemias fueron de intensidad leve (80 %; N = 384), moderada (16,6 %; N = 78) o grave (1,9 %; N = 9).
Las reacciones adversas se clasificaron según los términos preferentes SOC y MedDRA, notificados en pacientes que recibieron 5 mg de TRAYENTA® en los estudios a doble ciego como monoterapia, como tratamiento inicial combinado o como tratamiento adicional en los estudios clínicos y las reacciones adversas identificadas a partir de la experiencia post-comercialización se presentan en la tabla que sigue (véase tabla 1).
• Resumen tabular de las reacciones adversas:
Reacciones adversas notificadas en pacientes tratados con 5 mg diarios de TRAYENTA®, como monoterapia o tratamiento adicional en estudios clínicos y reacciones adversas identificadas a partir de la experiencia post-comercialización
|
Terminología según la clasificación por sistema y órganos del MedDRA |
Reacciones adversas a la linagliptina |
|
Infecciones e infestaciones |
Nasofaringitis |
|
Trastornos del sistema inmunológico |
Hipersensibilidad |
|
Angioedema1 |
|
|
Urticaria1 |
|
|
Trastornos del metabolismo y la nutrición |
Hipoglucemia (cuando se usa en combinación con metformina más sulfonilurea) |
|
Hipertrigliceridemia (cuando se usa en combinación con sulfonilurea) |
|
|
Hiperlipidemia (cuando se usa en combinación con pioglitazona) |
|
|
Trastornos respiratorios, torácicos y del mediastino |
Tos |
|
Trastornos gastrointestinales |
Pancreatitis |
|
Estreñimiento (cuando se usa en combinación con insulina) |
|
|
Úlceras bucales1 |
|
|
Enfermedades de piel y tejido subcutáneo |
Exantema1 |
|
Penfigoide ampolloso1; 4 |
|
|
Otras exploraciones |
Aumento de peso (cuando se usa en combinación con pioglitazona) |
|
Aumento de la lipasa2 |
|
|
Aumento de la amilasa3 |
|
|
1 RAM identificada a partir de la experiencia post-comercialización 2 Basado en los aumentos de lipasa > 3 veces el ULN observado en estudios clínicos 3 En el estudio CAROLINA que comparó la linagliptina con el fármaco comparador del activo glimepirida (ver la sección Estudios Clínicos), el análisis de laboratorio de amilasa presentó aumentos de hasta > 3 veces el ULN en el 0,99 % de los pacientes tratados con linagliptina y en el 0,54 % de los pacientes tratados con glimepirida 4 Ver también el estudio de seguridad cardiovascular y renal de linagliptina (CARMELINA) más adelante. |
|
Estudio de seguridad cardiovascular y renal con linagliptina (CARMELINA): En el estudio CARMELINA, se evaluó la seguridad cardiovascular y renal de linagliptina comparada con un placebo en pacientes con diabetes tipo 2 y con un aumento del riesgo cardiovascular evidenciado por la presencia de antecedentes de enfermedad renal o macrovascular establecida (ver la sección Estudios clínicos). Se incluyeron en el estudio 3494 pacientes tratados con linagliptina (5 mg) y 3485 pacientes tratados con placebo. Ambos tratamientos se agregaron al tratamiento estándar empleado para alcanzar la meta de HbA1c, según los criterios regionales, y controlar los factores de riesgo cardiovascular. Al inicio del estudio, 57 % de los pacientes recibían insulina, 54 % metformina y 32 %, una sulfonilurea. La incidencia global de eventos adversos y eventos adversos serios en pacientes que recibieron linagliptina fue similar a la de los pacientes que recibieron placebo. Los datos de seguridad de este estudio estaban en línea con el perfil de seguridad conocido anterior de linagliptina.
En la población tratada, se informaron eventos hipoglucémicos graves (que requirieron asistencia) en 3,0 % de los pacientes tratados con linagliptina y en 3,1 % de los pacientes tratados con placebo. Entre los pacientes que estaban recibiendo una sulfonilurea al inicio del estudio, la incidencia de la hipoglucemia grave fue 2,0% con linagliptina y 1,7 % con placebo. Entre los pacientes que estaban recibiendo insulina al inicio del estudio, la incidencia de la hipoglucemia grave fue 4,4 % con linagliptina y 4,9 % con placebo.
En el período de observación total del estudio, se notificaron eventos adjudicados como pancreatitis aguda en 0,3 % de los pacientes tratados con linagliptina y en 0,1 % de los pacientes tratados con placebo.
En el estudio CARMELINA, se informó penfigoide ampolloso en 0,2 % de los pacientes tratados con linagliptina y en ningún paciente tratado con placebo.
INTERACCIONES
• Interacciones farmacocinéticas:
— Evaluación in vitro de las interacciones medicamentosas:
La linagliptina es un inhibidor competitivo débil y un inhibidor débil a moderado en el mecanismo de inhibición de la CYP, isoenzima CYP3A4, pero no inhibe otras isoenzimas CYP. No es inductor de las isoenzimas CYP.
La linagliptina es un sustrato de la glucoproteína P y un inhibidor del transporte de la digoxina mediado por la glucoproteína P, de baja potencia. Sobre la base de estos resultados y de los estudios de interacción farmacológica in vivo se considera improbable que la linagliptina cause interacciones con otros sustratos de la P-gp.
— Evaluación in vivo de las interacciones medicamentosas:
Los datos clínicos que se describen a continuación sugieren que el riesgo de interacciones de interés clínico por la coadministración de medicamentos es bajo. No se observaron interacciones clínicamente significativas que requirieran ajustes de la dosis. La linagliptina carece de efecto clínico relevante sobre la farmacocinética de la metformina, glibenclamida, simvastatina, pioglitazona, warfarina, digoxina o anticonceptivos orales; proporcionando evidencia in vivo de un bajo potencial de interacciones medicamentosas con los sustratos de CYP3A4, CYP2C9, CYP2C8, glucoproteína P y el transportador de cationes orgánicos (TCO).
— Metformina:
La coadministración de dosis múltiples de 850 mg de metformina tres veces por día con una dosis supraterapéutica de 10 mg de linagliptina una vez por día, no afectó de manera significativa la farmacocinética de la linagliptina ni de metformina en voluntarios sanos. Por lo tanto, la linagliptina no inhibe el transporte mediado por los TCO.
— Sulfonilureas:
La farmacocinética en estado de equilibrio de 5 mg de linagliptina no se modificó por la coadministración de una dosis única de 1,75 mg de glibenclamida (gliburida) y de múltiples dosis orales de 5 mg de linagliptina. Sin embargo, hubo una reducción clínicamente no relevante de 14 % tanto del AUC y de la Cmáx de glibenclamida. Debido a que la glibenclamida es metabolizada principalmente por el CYP2C9, estos datos también respaldan la conclusión de que linagliptina no es un inhibidor del CYP2C9. No se esperarían interacciones de interés clínico con otras sulfonilureas (por ejemplo, glipizida, tolbutamida y glimepirida) que, al igual que la glibenclamida, son eliminadas principalmente por el CYP2C9.
— Tiazolidinedionas:
La coadministración de múltiples dosis diarias de 10 mg de linagliptina (supraterapéuticas) con múltiples dosis diarias de 45 mg de pioglitazona, un sustrato de CYP2C8 y de CYP3A4, no tuvo efectos clínicamente relevantes sobre la farmacocinética, ya sea de linagliptina o de pioglitazona, ni sobre los metabolitos activos de la pioglitazona, lo cual indica que la linagliptina no inhibe el metabolismo mediado por CYP2C8 in vivo y respalda la conclusión de que la inhibición in vivo del CYP3A4 por parte de la linagliptina es insignificante.
— Ritonavir:
Se llevó a cabo un estudio para evaluar el efecto de ritonavir, un inhibidor potente de la glucoproteína P y del CYP3A4, sobre la farmacocinética de la linagliptina. La coadministración de una única dosis oral de 5 mg de linagliptina y de múltiples dosis orales de 200 mg de ritonavir aumentó el AUC y la Cmáx de la linagliptina alrededor de dos veces y tres veces, respectivamente. La simulación de concentraciones plasmáticas de linagliptina en estado de equilibrio, con y sin ritonavir, indicó que el aumento de la exposición no se asocia con aumento de la acumulación. Estos cambios en la farmacocinética de linagliptina no se consideraron clínicamente relevantes. Por lo tanto, no se anticipan interacciones clínicamente relevantes con otros inhibidores de la glucoproteína P/CYP3A4 y no se requieren ajustes de dosis.
— Rifampicina:
Se llevó a cabo un estudio para evaluar el efecto de rifampicina, un inductor potente de la glucoproteína P y de CYP3A4, sobre la farmacocinética de 5 mg de linagliptina. Coadministraciones múltiples de linagliptina con rifampicina, dieron lugar a una disminución de 39,6 % y 43,8 % del AUC y de la Cmáx de la linagliptina en estado de equilibrio y una disminución de alrededor del 30 % de la inhibición de la DPP-4, en concentraciones mínimas. Así, se prevé que la linagliptina en combinación con inductores potentes de la P-gp será clínicamente eficaz, si bien podría no alcanzarse la máxima eficacia.
— Digoxina:
La coadministración de múltiples dosis diarias de 5 mg de linagliptina con dosis múltiples de 0,25 mg de digoxina, no afectó la farmacocinética de la digoxina en voluntarios sanos. Por lo tanto, la linagliptina no es un inhibidor del transporte mediado por la glucoproteína P in vivo.
— Warfarina:
Múltiples dosis diarias de 5 mg de linagliptina no alteraron la farmacocinética de la S(-) o R(+) warfarina, un sustrato del CYP2C9, lo cual muestra que la linagliptina no es un inhibidor del CYP2C9.
— Simvastatina:
Múltiples dosis diarias de 10 mg de linagliptina (supraterapéuticas) tuvieron efectos mínimos sobre la farmacocinética en estado de equilibrio de la simvastatina, un sustrato sensible del CYP3A4, en voluntarios sanos. Después de administrar 10 mg de linagliptina en forma concomitante con 40 mg diarios de simvastatina durante 6 días, el AUC plasmática de la simvastatina aumentó el 34%, y la Cmáx, el 10%. Por lo tanto, la linagliptina se considera como un inhibidor débil del metabolismo mediado por el CYP3A4, y se considera que no requiere ajuste de la dosis cuando se administran en forma concomitante sustancias metabolizadas por el CYP3A4.
— Anticonceptivos orales:
La coadministración con 5 mg de linagliptina no alteró la farmacocinética en estado de equilibrio de levonorgestrel o etinilestradiol.
La biodisponibilidad absoluta de la linagliptina es de alrededor del 30 %. Debido a que la coadministración de comidas con alto contenido graso con linagliptina no causó efectos clínicos relevantes sobre su farmacocinética, linagliptina puede administrarse con o sin alimentos.
ADVERTENCIAS Y PRECAUCIONES ESPECIALES:
Generales: TRAYENTA® no debe utilizarse en pacientes con diabetes tipo 1 ni para el tratamiento de la cetoacidosis diabética.
Pancreatitis: Desde la comercialización del producto se ha notificado casos de pancreatitis aguda en pacientes tratados con este principio activo. Al empezar el tratamiento con este medicamento, se requiere una supervisión cuidadosa de los signos y síntomas de pancreatitis. Si se sospecha de pancreatitis el producto debe ser suspendido inmediatamente e iniciar el tratamiento adecuado. Los pacientes deben ser informados sobre los síntomas característicos de pancreatitis.
Hipoglicemia: La linagliptina como monoterapia mostró una incidencia de hipoglicemia comparable a la del placebo.
En los estudios clínicos con linagliptina como parte de un tratamiento combinado con fármacos con los cuales no se han informado episodios de hipoglicemia (metformina, tiazolidinedionas), las tasas de hipoglicemia reportadas con linagliptina fueron similares a las observadas en los pacientes que recibían placebo.
Se sabe que las sulfonilureas causan hipoglicemia. Por lo tanto, se recomienda precaución cuando se usa linagliptina en combinación con una sulfonilurea. Puede ser necesario considerar una reducción de la dosis de la sulfonilurea.
Penfigoide ampolloso: Se han observado casos de penfigoide ampolloso en pacientes que toman linagliptina. Si se sospecha de penfigoide ampolloso, el tratamiento con TRAYENTA® debe discontinuarse.
DOSIS Y ADMINISTRACIÓN:
Vía de administración: Oral.
• Dosis:
Adultos: La dosis recomendada es de 5 mg una vez al día. TRAYENTA® puede tomarse con o sin alimentos, en cualquier momento del día.
• Dosis olvidada:
Si se olvida una dosis, ésta debe ser tomada tan pronto como el paciente lo recuerde. No se debe tomar una dosis doble el mismo día.
SOBREDOSIS: Síntomas: Durante los estudios clínicos controlados que se realizaron en personas sanas, las dosis únicas hasta de 600 mg de linagliptina (equivalente a 120 veces la dosis recomendada) fueron bien toleradas. No existe experiencia con dosis superiores a 600 mg en humanos.
Tratamiento: En caso de sobredosis, es razonable emplear las medidas habituales de soporte, por ejemplo, eliminar del tracto gastrointestinal todo el material que no haya sido absorbido, monitoreo clínico e institución de medidas clínicas según necesidad.
TOXICOLOGÍA: Carcinogenicidad: Se realizó un estudio de dos años sobre carcinogenicidad en ratas machos y hembras tratadas con dosis orales de 6, 18 y 60 mg/kg/día de linagliptina. No hubo aumento en la incidencia de tumores en ninguno de los órganos hasta la dosis de 60 mg/kg/día. Esta dosis lleva a una exposición aproximadamente 418 veces mayor que la exposición humana alcanzada con la dosis diaria máxima recomendada para los seres humanos adultos (MRHD) de 5 mg/día, con base en las AUC comparativas. Se realizó también un estudio a dos años sobre carcinogenicidad en ratones machos y hembras tratados con dosis orales de 8, 25 y 80 mg/kg/día. No hubo evidencia de posible carcinogenicidad hasta con 80 mg/kg/día, aproximadamente 242 veces la exposición humana a la MRHD.
Genotoxicidad: La linagliptina no causó mutagénesis o clastogénesis con o sin activación metabólica con el método de mutagénesis bacteriana de Ames, en la prueba de aberración cromosómica en linfocitos humanos, ni tampoco en la prueba del micronúcleo in vivo.
Toxicidad reproductiva: En los estudios sobre fertilidad en ratas tratadas con dosis de 10, 30 y 240 mg/kg/día por sonda nasogástrica, los machos fueron tratados durante 4 semanas antes y durante el apareamiento; las hembras fueron tratadas desde 2 semanas antes del apareamiento hasta el día 6 de gestación. No se observaron efectos adversos sobre el desarrollo embrionario temprano, el apareamiento, ni la fertilidad y se obtuvieron crías vivas hasta con la dosis más elevada de 240 mg/kg/día (alrededor de 943 veces superior a la exposición humana, con base en la MRHD de 5 mg/día, según las AUC comparativas).
En los estudios sobre el desarrollo embrionario y fetal en ratas y conejos, la linagliptina no mostró ser teratogénica en dosis hasta de 240 mg/kg/día inclusive (943 x MRHD) en la rata y de 150 mg/kg/día (1943 x MRHD) en el conejo.
Se obtuvo un NOAEL(No Observed Adverse Effect Level) de 30 mg/kg/día (49 x MRHD) y de 25 mg/kg/día (78 x MRHD) para toxicidad embriofetal en ratas y conejos, respectivamente.
Condición de venta: Venta con fórmula facultativa.
Almacenar a: Temperatura inferior a 30ºC en su envase y empaque original.
• Anexo: frecuencia de las reacciones adversas TRAYENTA®
Categorías de frecuencia:
— Muy frecuentes: ≥ 1/10
— Frecuentes: ≥ 1/100 - < 1/10
— Poco frecuentes: ≥ 1/1000 - < 1/100
— Infrecuentes: ≥ 1/10000 - < 1/1000
— Muy infrecuentes: < 1/10000
— Desconocida: No puede estimarse en función de los datos disponibles
Nota: Las categorías de frecuencia mencionadas se basan en las directrices de la UE para la confección de resúmenes de características de productos (septiembre de 2009); por lo tanto, en los países no incluidos en la Unión Europea pueden regir otras definiciones.
Reacciones adversas incluidas en la información para prescribir e inserto y sus frecuencias* correspondientes de acuerdo con la directriz de la UE para la confección de resúmenes de características de productos
* Las categorías de frecuencia representan la frecuencia más elevada calculada por contexto.
|
Terminología según la clasificación por sistema y órganos del MedDRA |
Reacciones adversas a la linagliptina por término preferente del MedDRA (versión 18.1) usando literalmente en esta CCDS |
Categorías de frecuencia según directriz de la UE para elaborar SmPC |
|
Infecciones e infestaciones |
Nasofaringitis |
Poco frecuente |
|
Trastornos del sistema inmunológico |
Hipersensibilidad |
Poco frecuente |
|
Angioedema1 |
Infrecuente † |
|
|
Urticaria1 |
Infrecuente $ |
|
|
Trastornos del metabolismo y la nutrición |
Hipoglucemia (cuando se usa en combinación con metformina + SU) |
Muy frecuente |
|
Hipertrigliceridemia (cuando se usa en combinación con SU) |
Desconocida # |
|
|
Hiperlipidemia (cuando se usa en combinación con pioglitazona) |
Desconocida # |
|
|
Trastornos respiratorios, torácicos y del mediastino |
Tos |
Desconocida |
|
Trastornos gastrointestinales |
Pancreatitis |
Poco frecuente |
|
Estreñimiento (cuando se usa en combinación con insulina) |
Poco frecuente |
|
|
Úlceras bucales1 |
Infrecuente † |
|
|
Enfermedades de piel y tejido subcutáneo |
Exantema1 |
Poco frecuente † |
|
Penfigoide ampolloso1 |
Infrecuente $ |
|
|
Otras exploraciones |
Aumento de peso (cuando se usa en combinación con pioglitazona) |
Frecuente |
|
Aumento de la lipasa |
Frecuente 2 |
|
|
Aumento de la amilasa |
Poco frecuente 3 |
|
|
1. RAM identificada a partir de la experiencia post-comercialización. 2. Basado en el aumento de la lipasa > 3 veces el ULN en los pacientes tratados con linagliptina en el estudio MARLINA (1218.89). 3. RAM identificada a partir del análisis de laboratorio del aumento de la amilasa > 3 veces el ULN en el estudio CAROLINA (1218.74) que comparó la linagliptina con el fármaco comparador del activo, glimepirida. † RAM basada en la experiencia post-comercialización, para la que se notificaron EA relacionados con el fármaco en el conjunto de datos de referencia (SAF-2). $ RAM basada en la experiencia post-comercialización, para la que no se notificaron eventos adversos relacionados con el fármaco en el conjunto de datos de referencia (SAF-2). Como se indica en la Directriz de la UE para la confección del SmPC, “el límite superior del intervalo de confianza del 95 % no es superior a 3/X, donde X representa el tamaño de muestra total sumado de todos los estudios clínicos relevantes (SAF-2). Por ejemplo, si no se ha observado una reacción adversa particular entre 3600 sujetos expuestos al producto en ensayos y estudios clínicos, el límite superior del intervalo de confianza del 95 % para la estimación puntual es 1/1200 o menos y la categoría debe ser “infrecuente”, considerando el peor valor de la estimación puntual”. # RAM basada en la señal del o de los estudios clínicos, pero el evento no se notifica en los estudios clínicos como EA relacionado con el fármaco; por lo tanto, no se pudo calcular una frecuencia. De acuerdo con la Directriz de la UE para la confección del SmPC, se asignó la frecuencia “Desconocida” |
||
INDICACIONES/USO: La linagliptina está indicada en pacientes adultos con diabetes mellitus de tipo 2 (DM2) para mejorar el control glicémico, junto con la dieta y el ejercicio, como monoterapia cuando metformina no es tolerada o está contraindicada.
La linagliptina está indicada en pacientes adultos con diabetes mellitus tipo 2 (DM2) para mejorar el control glicémico, junto con la dieta y el ejercicio, sumada a metformina, sulfonilureas, tiazolidinedionas, insulina (con o sin metformina y/o pioglitazona y/o sulfonilurea), o metformina más sulfonilureas, o metformina más inhibidores del SGLT2.
PRESENTACIÓN: TRAYENTA®: Caja por 30 tabletas recubiertas en blíster (Reg. San. No. INVIMA 2017M-0012597-R1).
“¡Almacenar en un lugar seguro; fuera del alcance de los niños!
La información de seguridad del producto puede cambiar, consulte la información vigente en la Dirección Médica.
Teléfono: (601) 319 91 00
e-mail: medfora.co@boehringer-ingelheim.com
Carrera 11 No. 84A-09 Piso 5, Bogotá D.C. Colombia.
BOEHRINGER INGELHEIM S.A.
Versión-11 del 25 de abril de 2019