LINAZIC - Cápsula
Sustancia(s):
- Linaclotida
Presentaciones:
- 1 Caja, 1 Frasco(s), 30 Cápsulas, 145 µg
- 1 Caja, 1 Frasco(s), 30 Cápsulas, 290 µg
FORMA FARMACÉUTICA Y FORMULACIÓN:
Cada CÁPSULA contiene:
Linaclotida 145 μg o 290 μg
Excipiente cbp 1 cápsula
INDICACIONES TERAPÉUTICAS:
LINAZIC® es un agonista de la guanilato ciclasa-C indicado para el tratamiento sintomático delsíndrome del intestino irritable con constipación (SII-C) entre moderada y grave y laconstipación idiopática crónica (CIC) en adultos.
FARMACOCINÉTICA Y FARMACODINAMIA:
Propiedades farmacodinámicas:
Grupo farmacoterapéutico:
Agente contra la constipación (otro).
Mecanismo de acción:
Linaclotida es un péptido sintético de 14 aminoácidos que está relacionado estructuralmente con la familia de péptidos endógenos de la guanilina.
Linaclotida actúa como agonista del receptor de la enzima guanilato ciclasa C (GC-C).
Tanto linaclotida como su metabolito activo se unen al receptor de la GC-C en la superficie luminal del epitelio intestinal. Con la activación de la GC-C se produce un incremento de las concentraciones del monofosfato de guanosina cíclico (GMPc), tanto extracelular como intracelular.
El aumento intracelular del GMPc estimula la secreción de cloro y bicarbonato en la luz intestinal mediante la activación del canal iónico llamado regulador de la conductancia transmembrana de la fibrosis quística (RTFQ), lo que aumenta la cantidad de líquido luminal y acelera el tránsito intestinal.
En modelos animales, linaclotida demostró la capacidad de reducir el dolor visceral y acelerar el tránsito gastrointestinal. Dicha capacidad de reducir el dolor visceral es debida a que, a nivel extracelular, el aumento del GMPc disminuye la actividad de las fibras nociceptivas.
Farmacocinética:
Absorción:
Linaclotida es mínimamente absorbida y presenta baja biodisponibilidad sistémica luego de su administración oral.
En general, linaclotida es apenas detectable en el plasma tras la administración oral de las dosis terapéuticas y, por lo tanto, no pueden calcularse los parámetros farmacocinéticos típicos como el AUC, la Cmax y la t½.
Distribución: Debido a que linaclotida rara vez resulta detectable en el plasma tras su administración a las dosis terapéuticas, no se han llevado a cabo estudios sobre su distribución típica; con todo, se prevé que la distribución sistémica de linaclotida sea insignificante o nula.
Biotransformación:
Linaclotida se metaboliza localmente en el tubo digestivo y da lugar a su principal metabolito activo, destirosina. Tanto linaclotida como el metabolito activo destirosina son reducidos y proteolizados en el tubo digestivo por enzimas que los transforman en péptidos más pequeños y aminoácidos que pueden estar presentes de manera natural.
Eliminación:
Tras la administración por vía oral de una dosis única de 2897 microgramos de linaclotida en el día 8, después de un ciclo de 7 días de tratamiento con 290 microgramos diarios a 18 voluntarios sanos, en las heces se recuperó entre el 3 y el 5% de la dosis, en su práctica totalidad bajo la forma del metabolito activo.
Farmacodinamia:
Eficacia clínica:
La eficacia de linaclotida se demostró en dos estudios clínicos de fase III, aleatorizados, con doble enmascaramiento y controlados con placebo realizados en pacientes afectados de SII-E. En uno de estos estudios (estudio 1) se trató a 802 pacientes con linaclotida de 290 microgramos o placebo, tomados una vez al día durante 26 semanas; en el segundo estudio clínico (estudio 2) participaron 800 pacientes que recibieron tratamiento durante 12 semanas y fueron sometidos después a otro proceso de aleatorización para pasar a un periodo de tratamiento adicional de 4 semanas. En las dos semanas iniciales previas al tratamiento, los pacientes experimentaron un dolor abdominal cuya puntuación media fue de 5,6 (en una escala de 0 a 10), con un 2,2% de días sin dolor, una hinchazón de 6,6 de 7 media (en una escala de 0 a 10) y un promedio de 1,8 movimientos intestinales espontáneos (MIE) por semana.
Las características de los pacientes que tomaron parte en los ensayos clínicos de fase III fueron las siguientes: media de edad de 43,9 años (intervalo de 18-87 años, con un 5,3% ≥ 65 años), siendo mujeres el 90,1% del total. Todos los pacientes cumplían los criterios de Roma II para el SII-E y debieron referir una media de dolor abdominal ≥ 3 en una escala de puntuación numérica de 0 a 10 (criterios que corresponden a una población con SII de moderado a grave), < 3 movimientos intestinales espontáneos completos y ≤ 5 MIE por semana a lo largo de un periodo inicial de dos semanas.
En ambos estudios clínicos, los criterios de valoración principales (múltiples) fueron la existencia de una tasa de pacientes que presentasen alivio del SII durante 12 semanas y una tasa de pacientes que refiriesen dolor abdominal o incomodidad a lo largo del mismo periodo.
Por paciente que presentase un grado de alivio del SII se entendió aquel cuyos síntomas se aliviasen considerable o completamente durante al menos el 50% del periodo de tratamiento, mientras que los pacientes que refiriesen dolor abdominal o incomodidad serían los que experimentasen una mejora del 30% o más en por lo menos el 50% de dicho periodo.
En los datos de 12 semanas, el estudio 1 revela que el 39% de los pacientes tratados con linaclotida, frente al 17% de los tratados con placebo, experimentaron alivio del SII (p < 0,0001), y el 54% de los pacientes tratados con linaclotida, frente al 39% de los que recibieron el placebo, mostraron una respuesta al dolor abdominal y a la incomodidad (p < 0,0001). El estudio 2 pone de manifiesto que el 37% de los pacientes que habían recibido el tratamiento con linaclotida, en comparación con el 19% de los tratados con placebo, manifestaron alivio del SII (p < 0,0001) y el 55% de los tratados con linaclotida, en comparación con el 42% de los tratados con placebo, mostraron respuesta al dolor abdominal y a la incomodidad (p < 0,0002).
En los datos de 26 semanas, el estudio 1 revela que el 37% y el 54% de los pacientes tratados con linaclotida, frente al 17% y el 36% de los tratados con placebo, mostraron alivio del SII (p < 0,0001) y respuesta al dolor abdominal y a la incomodidad (p < 0,0001) respectivamente.
En ambos estudios estas mejoras se observaron ya antes de finalizar la semana 1 y se mantuvieron durante todo el periodo de tratamiento (figuras 1 y 2). Se ha observado que linaclotida no causa efecto rebote cuando el tratamiento se interrumpió al cabo de 3 meses de tratamiento continuo.
Fig 1. Respuesta del paciente al alivio del SII
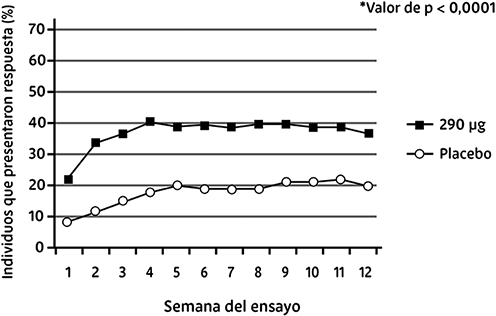
Estudios clínicos combinados de fase III relativos a la eficacia (estudios 1 y 2).
Método: observación de casos (población de intención de tratar).
Fig 2. Respuesta del paciente al dolor abdominal y a la sensación de incomodidad
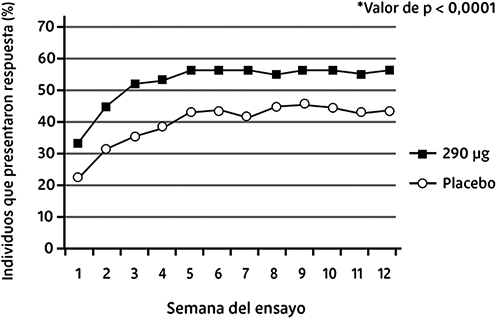
Estudios clínicos combinados de fase III relativos a la eficacia (estudios 1 y 2).
Método: observación de casos (población de intención de tratar).
En comparación con los pacientes tratados con placebo, aquellos a los que se les administró linaclotida experimentaron una mejora (p < 0,0001) en otros signos y síntomas del SII-E (hinchazón, frecuencia de movimientos intestinales espontáneos completos [MIEC], esfuerzo y consistencia de las heces), según se indica en la tabla que figura a continuación. Estos efectos se alcanzaron al cabo de una semana y se mantuvieron a lo largo de la totalidad de los periodos de tratamiento.
Efectos de la linaclotida en los síntomas de SII-E durante las 12 primeras semanas de tratamiento en los estudios clínicos combinados de fase III relativos a la eficacia (estudios 1 y 2)
|
Principales parámetros secundarios de la eficacia |
Placebo (N = 797) |
Linaclotida (N = 805) |
|||||
|
Periodo inicial Media |
12 semanas Media |
Cambio con respecto al periodo inicial Media |
Periodo inicial Media |
12 semanas Media |
Cambio con respecto al periodo inicial Media |
Diferencia media de MC |
|
|
Hinchazón (EPN de 11 puntos) |
6,5 |
5,4 |
-1,0 |
6,7 |
4,6 |
-1,9 |
-0,9* |
|
MIE semana |
0,2 |
1,0 |
0,7 |
0,2 |
2,5 |
2,2 |
1,6* |
|
Consistencia de las heces (puntuación de la escala de heces de Bristol; BSFS) |
2,3 |
3,0 |
0,6 |
2,3 |
4,4 |
2,0 |
1,4* |
|
Esfuerzo (escala ordinal de 5 puntos) |
3,5 |
2,8 |
-0,6 |
3,6 |
2,2 |
-1,3 |
-0,6* |
* p < 0,0001, linaclotida frente a placebo. MC: mínimos cuadrados. MIEC: movimiento intestinal espontáneo completo.
El tratamiento con linaclotida también conllevó una mejora significativa en la medida de la calidad de vida validada y específica para este trastorno (SII-QoL, calidad de vida en el síndrome del intestino irritable; p < 0.0001) y en el EuroQoL (p = 0,001); así, en el 54% de los pacientes tratados con linaclotida se alcanzó una respuesta clínicamente significativa en el SII-QoL (> 14 puntos de diferencia), frente a un 39% en el caso de los pacientes a los que se les administró placebo.
Poblaciones especiales:
Pacientes con insuficiencia renal o hepática:
No es necesario un ajuste de la dosis en los pacientes con insuficiencia hepática o renal.
Pacientes de edad avanzada:
En los pacientes de edad avanzada, aunque no es necesario un ajuste de la dosis, el tratamiento debe vigilarse con atención y controlarse periódicamente.
Población pediátrica:
No se ha establecido todavía la seguridad y eficacia de linaclotida en niños de 0 a 18 años. No se dispone de datos. LINAZIC® no se debe utilizar en niños ni en adolescentes.
CONTRAINDICACIONES:
Hipersensibilidad a linaclotida o a cualquiera de los excipientes.
Pacientes en los que exista certeza o sospecha de obstrucción gastrointestinal mecánica.
Menores de 18 años, embarazo y lactancia.
RESTRICCIONES DE USO DURANTE EL EMBARAZO Y LA LACTANCIA:
Embarazo:
Los datos sobre el uso de linaclotida en mujeres embarazadas son escasos. Los estudios en animales no sugieren efectos perjudiciales directos ni indirectos en términos de toxicidad para la reproducción. LINAZIC® sólo debe utilizarse durante el embarazo si los potenciales beneficios superan a los riesgos.
Lactancia:
No se conoce si linaclotida es excretada a través de la leche humana, pero debido a que la exposición sistémica a linaclotida y su metabolito es mínima, no resulta probable su excreción en la leche materna a las dosis clínicas.
Se debe tener precaución si se administra LINAZIC® en pacientes que amamantan.
REACCIONES SECUNDARIAS Y ADVERSAS:
Resumen del perfil de seguridad:
En estudios clínicos controlados se suministró linaclotida por vía oral a 1166 pacientes afectados de SII-E, de los cuales 892 recibieron linaclotida a la dosis recomendada de 290 microgramos diarios. La exposición total comprendida en el programa de desarrollo clínico fue superior a 1,5 pacientes-año. La reacción adversa notificada con mayor frecuencia asociada al tratamiento con linaclotida fue diarrea, principalmente de intensidad leve a moderada, que se observó en menos del 20% de los pacientes. Raramente en los casos más graves, ésta puede, como consecuencia, conducir a deshidratación, hipopotasemia, disminución de la concentración de bicarbonato en sangre, mareo e hipotensión ortostática.
Otras reacciones adversas frecuentes (> 1%) fueron dolor abdominal, distensión abdominal y flatulencia.
Tabla resumen de las reacciones adversas:
En estudios clínicos en los que se administró la dosis recomendada de 290 microgramos al día, se comunicaron las reacciones adversas enumeradas a continuación, cuya frecuencia se define utilizando el siguiente convenio: muy frecuentes (≥ 1/10), frecuentes (≥ 1/100 a < 1/10), poco frecuentes (≥ 1/1.00 a < 1/100), raras, (≥ 1/1.000), muy raras (< 1/10.000) y frecuencia no conocida (no puedes estimarse a partir de los datos disponibles).
|
Clasificación de órganos del sistema MedDRA |
Muy frecuente |
Frecuentes |
Poco frecuentes |
Raras |
Frecuencia no conocida |
|
Infecciones e infestaciones |
Gastrointeritis vírica |
||||
|
Trastornos del metabolismo y de la nutrición |
Hipopotasemia Deshidratación Disminución del apetito |
||||
|
Trastornos del sistema nervioso |
Mareo |
||||
|
Trastornos vasculares |
Hipotensión ortostática |
||||
|
Trastornos gastrointestinales |
Diarrea |
Dolor abdominal Flatulencia Distensión abdominal |
Incontinencia fecal Urgencia defecatoria Hemorragia digestiva baja. incluida hemorragia hemorroidal y hemorragia rectal Náuseas Vómitos |
Perforación gastrointestinal |
|
|
Trastornos de la piel y del tejido subcutáneo |
Urticaria |
Erupción cutánea |
|||
|
Exploraciones complementarias |
Reducción del bicarbonato en sangre |
Descripción de determinadas reacciones adversas:
La diarrea constituye la reacción adversa más frecuente y responde a la acción farmacológica del principio activo. El 2% de los pacientes tratados experimentaron diarrea grave y el 5% de los pacientes discontinuaron el tratamiento debido a diarrea en los ensayos clínicos.
La mayoría de los casos de diarrea referidos fueron de leves (43%) a moderados (47%); el 2% de los pacientes tratados experimentaron una diarrea grave. Aproximadamente la mitad de los episodios de diarrea comenzaron durante la primera semana de tratamiento.
La diarrea desapareció dentro de los siete días siguientes en aproximadamente un tercio de los pacientes, sin embargo 80 pacientes (el 50%) experimentaron diarrea con una duración de más de 28 días (lo que representa el 9,9% de todos los pacientes tratados con linaclotida). El 5% de los pacientes discontinuaron el tratamiento debido a diarrea en los ensayos clínicos. En los pacientes cuya diarrea motivó la retirada del tratamiento, el trastorno se resolvió al cabo de unos días de la retirada.
En comparación con la población global de individuos afectados de SII-E que se incluyeron en los ensayos clínicos, los pacientes ancianos (> 65 años), hipertensos y diabéticos reportaron diarrea con mayor frecuencia.
PRECAUCIONES EN RELACIÓN CON EFECTOS DE CARCINOGÉNESIS, MUTAGÉNESIS, TERATOGÉNESIS Y SOBRE LA FERTILIDAD:
Carcinogénesis:
En estudios de carcinogenicidad de 2 años, la linaclotida no fue tumorigénica en ratas en dosis de hasta 3500 μg/kg/día o en ratones a dosis de hasta 6000 μg/kg/día. El humano máximo recomendado la dosis es de aproximadamente 5 μg/kg/día en base a un peso corporal de 60 kg. Exposición sistémica limitada a linaclotida y su metabolito activo se logró a los niveles de dosis probados en animales, mientras que no se produjo exposición detectable en humanos.
Por lo tanto, las dosis animales y humanas no debe compararse directamente para evaluar la exposición relativa.
Mutagénesis:
Linaclotida no fue genotóxica en un ensayo de mutación inversa bacteriana in vitro (Ames) o en el ensayo in vitro de aberraciones cromosómicas in vitro en linfocitos de sangre periférica humana cultivados.
Fertilidad:
Linaclotida no tuvo efecto sobre la fertilidad o la función reproductiva en ratas macho y hembra en dosis orales, dosis de hasta 100.000 μg/kg/día.
INTERACCIONES MEDICAMENTOSAS Y DE OTRO GÉNERO:
No se han realizado estudios de interacciones. Linaclotida rara vez resulta detectable en el plasma tras su administración a las dosis clínicas recomendadas, y en estudios realizados in vitro se ha demostrado que no es ni sustrato ni inhibidor/inductor del sistema enzimático del citocromo P450 y no interacciona con los transportadores más relevantes que participan en la captación y eflujo de medicamentos.
Por otro lado, en un estudio clínico sobre interacciones alimentarias llevado a cabo con individuos sanos se puso de manifiesto que, a las dosis terapéuticas, linaclotida no resultaba detectable en plasma tras haber comido ni en ayunas. La toma de linaclotida produjo deposiciones más frecuentes y sueltas, así como más acontecimientos adversos gastrointestinales, tras haber comido que cuando se administró en ayunas. La cápsula debe tomarse 30 minutos antes de una comida.
El tratamiento concomitante con inhibidores de la bomba de protones, laxantes o AINE puede aumentar el riesgo de diarrea.
Se deben tomar precauciones especiales cuando se administre linaclotida de forma concomitante con estos medicamentos.
En los casos de diarrea grave o prolongada es posible que se vea afectada la absorción de otros medicamentos administrados por vía oral. La eficacia de los anticonceptivos orales puede disminuir por lo que se recomienda el uso de un método anticonceptivo adicional que evite el fracaso de la anticoncepción oral (ver la ficha técnica del anticonceptivo oral). Deben tomarse precauciones especiales cuando se prescriban medicamentos que se absorban en el tracto intestinal y con un estrecho índice terapéutico como la levotiroxina ya que su eficacia puede verse reducida.
ALTERACIONES EN LOS RESULTADOS DE PRUEBAS DE LABORATORIO:
No se han demostrado con el uso del producto.
PRECAUCIONES GENERALES:
Pacientes de edad avanzada:
Los datos en pacientes de edad avanzada son escasos. Dado el alto riesgo de padecer diarrea observado en los ensayos clínicos, debe prestarse especial atención a estos pacientes y evaluar cuidadosa y periódicamente la relación beneficio-riesgo.
Población pediátrica:
No se ha estudiado la administración de LINAZIC® en niños y adolescentes, por tanto, no se debe utilizar en esta población. Dado que se tiene constancia de la sobreexpresión del receptor de la guanilato ciclasa C (GC-C) en edades tempranas, los niños menores de dos años pueden ser especialmente sensibles a los efectos de linaclotida.
DOSIS Y VÍA DE ADMINISTRACIÓN:
Vía de administración: Oral.
La cápsula debe tomarse con el estómago vacío al menos treinta minutos antes de la primera comida del día.
No triture ni mastique el contenido de la cápsula. La cápsula debe tragarse entera.
Si se olvida una dosis, se debe omitir la dosis olvidada y tomar la siguiente dosis a la hora habitual. No se deben tomar 2 dosis al mismo tiempo.
En pacientes adultos, con dificultades para tragar, siga las siguientes instrucciones para la administración con puré de manzana o agua. (La aspersión del contenido de la cápsula en otros alimentos blandos o en otros líquidos no ha sido probada).
Para la administración con puré de manzana:
1. Colocar una cucharada de puré de manzana a temperatura ambiente en un recipiente limpio.
2. Abrir la cápsula.
3. Espolvorear todo el contenido sobre puré de manzana.
4. Consumir los contenidos completos de forma inmediata. No masticar los gránulos. No guardar el puré de manzana y los granos para su uso posterior.
Para administración en agua:
1. Verter aproximadamente 30 mL de agua a temperatura ambiente en un recipiente limpio.
2. Abrir la cápsula
3. Espolvorear todo el contenido en el agua
4. Mezclar suavemente durante al menos 10 segundos.
5. Tragar toda la mezcla de granos y agua inmediatamente.
6. Añadir otros 30 ml de agua para los restos que hayan quedado en el vaso, mezclar durante 10 segundos, y tragar inmediatamente.
7. No guardar la mezcla de glóbulos en agua para uso futuro.
Para la administración por sonda nasogástrica/gástrica:
1. Abrir la cápsula y vaciar su contenido en un recipiente limpio con 30 mL de agua a temperatura ambiente.
2. Mezclar girando suavemente durante al menos 10 segundos
3. Pasar la mezcla de agua a una jeringa con punta de catéter de tamaño apropiado y aplicar presión rápida y constante (10 ml/10 segundos) para dispensar el contenido de la jeringa en la sonda.
4. Después de la administración de la mezcla, lavar la sonda nasogástrica/ gástrica con un mínimo de 10 ml de agua.
Después de la administración de linaclotida en puré de manzana o agua, la primera comida del día puede ser consumida 30 minutos más tarde.
Posología:
La dosis recomendada en el SII-C es una cápsula de 290 microgramos, una vez al día.
La dosis recomendada en la CIC es una cápsula de 145 microgramos, una vez al día.
Pacientes con insuficiencia renal o hepática:
No es necesario un ajuste de la dosis en los pacientes con insuficiencia hepática o renal.
Pacientes de edad avanzada:
En los pacientes de edad avanzada, aunque no es necesario un ajuste de la dosis, el tratamiento debe vigilarse con atención y controlarse periódicamente.
Población pediátrica:
No se ha establecido todavía la seguridad y eficacia de linaclotida en niños de 0 a 18 años. No se dispone de datos. LINAZIC® no se debe utilizar en niños ni en adolescentes.
MANIFESTACIONES Y MANEJO DE LA SOBREDOSIFICACIÓN O INGESTA ACCIDENTAL:
La sobredosis puede provocar síntomas resultantes de una exageración de los efectos farmacodinámicos conocidos del medicamento, principalmente diarrea. En un estudio llevado a cabo con voluntarios sanos que recibieron una dosis única de 2897 microgramos (hasta diez veces la dosis terapéutica recomendada), el perfil de seguridad de estos sujetos fue similar al de la población global tratada, siendo la diarrea el acontecimiento adverso comunicado con mayor frecuencia.
En caso de sobredosis, el paciente deberá ser tratado con la terapia y medidas sintomáticas que resulten necesarias.
PRESENTACIONES:
Caja con frasco con 30 cápsulas de 145 μg o 290 μg.
RECOMENDACIONES SOBRE ALMACENAMIENTO:
Consérvese a no más de 25 °C.
Consérvese el frasco bien cerrado.
Protéjase de la luz.
LEYENDAS DE PROTECCIÓN:
Este medicamento solo debe utilizarse bajo estricto control y vigilancia de un profesional de la salud con experiencia. Su venta requiere receta médica. No se deje al alcance de los niños. No se use durante el embarazo y lactancia. No se administre a menores de 18 años. El uso de linaclotida puede causarle: diarrea. Las cápsulas no deben masticarse o fragmentarse. Literatura exclusiva para el médico.
Reporte las sospechas de reacción adversa al correo: farmacovigilancia@cofepris.gob.mx y
farmacovigilancia@asofarma.com.mx
ASOFARMA DE MÉXICO, S.A. de C.V.
Calz. México-Xochimilco No. 43,
Col. San Lorenzo Huipulco,
C.P. 14370, Tlalpan, Ciudad de México, México.
Reg. Núm. 116M2025 SSA IV
®Marca Registrada
