
EVRA
ETINILESTRADIOL, NORELGESTROMINA
Parches
Caja, Bolsa, 3,9,18 Parche transdérmico,
COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Cada PARCHE TRANSDÉRMICO de 20 cm2 contiene:
Norelgestromina (NGMN) 6 mg
Etinilestradiol (EE) 0.6 mg
Excipientes c.s.p.
Cada parche transdérmico libera una media de 203 microgramos de NGMN y 34 microgramos de EE cada 24 horas. La exposición al medicamento se define más adecuadamente a través del perfil farmacocinético (ver sección Propiedades farmacocinéticas).
Para consultar la lista completa de excipientes, ver sección Lista de Excipientes.
INDICACIONES TERAPÉUTICAS
Anticoncepción femenina
EVRA® está indicado en mujeres en edad fértil. Se ha establecido la seguridad y la eficacia en mujeres de edades comprendidas entre los 18 y los 45 años.
La decisión de prescribir EVRA® debe tener en cuenta los factores de riesgo actuales de la mujer en particular, concretamente los de tromboembolismo venoso (TEV), y cómo se compara el riesgo de TEV con EVRA® con el de otros anticonceptivos hormonales combinados (AHCs) (ver secciones Contraindicaciones y Advertencias y precauciones especiales de empleo).
DATOS FARMACÉUTICOS
Lista de excipientes: Poliisobutileno/Polibuteno adhesivo, Lauril Lactato, Crospovidona, Tejido de poliéster sin trama, Filmina de forro y Poliéster de línea de liberación.
Incompatibilidades
No procede.
Período de validez
No utilice este medicamento después de la fecha de vencimiento o expira que aparece en el envase después de “Vence o Expira”. La fecha de caducidad es el último día del mes que se
indica.
Precauciones especiales de conservación
Mantener este medicamento fuera de la vista y del alcance de los niños.
No conservar a más de 30°C.
Conservar en el sobre y envase original.
Naturaleza y contenido del envase
Caja de cartulina x 3, 9 y 18 parches en bolsa de PEBD/Aluminio/Papel.
Precauciones especiales de eliminación y otras manipulaciones Se debe aplicar el parche inmediatamente después de extraerlo del sobre protector.
A fin de evitar interferencias con las propiedades adhesivas de EVRA®, no deben aplicarse cremas, lociones o polvos en el área de la piel donde vaya a ponerse el parche transdérmico EVRA®.
Después de usarlo, el parche transdérmico aún contiene cierta cantidad de principios activos.
La cantidad de principios activos que queda en el parche transdérmico puede tener efectos nocivos en el medio acuático. Por lo tanto, los parches transdérmicos usados se deben desechar con cuidado. La etiqueta destinada a desechar el parche transdérmico se debe despegar, de la parte exterior de la bolsita, de manera que la parte adhesiva cubra la zona sombreada de ésta. Por último, la etiqueta se debe cerrar herméticamente dejando en su interior el parche transdérmico. La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él se realizará de acuerdo con la normativa local.
Los parches transdérmicos usados no se deben arrojar a inodoros convencionales o a sistemas de eliminación de residuos líquidos.
Fabricante
Laboratorio LTS Lohmann Therapie-Systeme AG - Alemania
Producto: Evra® Parche Transdérmico
Nro de registro: EE-04013
Titular del registro sanitario
JOHNSON & JOHNSON DEL PERU S.A.
Av. Canaval y Moreyra N° 480, Int. 901 y 1301
San Isidro-Lima
Version del texto de referencia
EUPI junio 2017
PROPIEDADES FARMACOLÓGICAS
Propiedades farmacodinámicas
Grupo farmacoterapéutico: Hormonas sexuales y moduladores del sistema genital, progestágenos y estrógenos, preparados a dosis fijas, código ATC: G03AA13.
Mecanismo de acción
EVRA® actúa a través del mecanismo de supresión de la gonadotropina por las acciones estrogénica y progestágena del etinilestradiol y de la norelgestromina, respectivamente. El principal mecanismo de acción es la inhibición de la ovulación, pero también pueden contribuir a la eficacia del producto los efectos sobre el moco cervical y el endometrio.
Eficacia clínica y seguridad
|
Índices de Pearl (ver tabla): |
||||||
|
Grupo de estudio |
CONT- 002 EVRA® |
CONT-003 EVRA® |
CONT-003 ACO* |
CONT-004 EVRA® |
CONT-004 ACO** |
Todos los sujetos que recibieron EVRA® |
|
Nº de ciclos |
10.743 |
5.831 |
4.592 |
5.095 |
4.005 |
21.669 |
|
Índices de Pearl globales (IC 95%) |
0.73 (0.15-1.31) |
0,89 (0.02-1.76) |
0,57 (0-1.35) |
1,28 (0.16-2.39) |
2.27 (0.59-3.96) |
0.90 (0.44-1.35) |
|
Índices de Pearl – fallo del método (IC 95%) |
0.61 (0.0-1.14) |
0.67 (0.0- 1.42) |
0.28 (0.0-0.84) |
1.02 0.02-2.02) |
1.30 (0.03-2.57) |
0.72 (0.31-1.13) |
|
* DSG (Desogestrel) 150 µg + 20 µg EE ** 50 µg LNG (Levonorgestrel) + 30 µg EE en los días 1-6, 75 µg LNG + 40 µg EE en los días 7-11, 125 µg LNG + 30 µg EE en los días 12-21 |
||||||
Se realizaron análisis exploratorios para determinar si en los estudios de Fase III (n=3.319) las características de edad, raza y peso de la población estaban asociadas con la incidencia de embarazo.
Los análisis indicaron que no hay asociación de edad y raza con el embarazo. Con respecto al peso, 5 de los 15 embarazos comunicados con EVRA® se produjeron en mujeres con un peso corporal al inicio del ensayo de 90 kg o más, lo que constituía menos del 3 % de la población del ensayo. Por debajo de los 90 kg, no hubo asociación entre peso y embarazo. Aunque sólo un 10–20% de la variabilidad de los datos farmacocinéticos puede atribuirse al peso (ver sección Propiedades farmacocinéticas), la mayor proporción de los embarazos entre las mujeres que pesaban 90 kg o más fue estadísticamente significativa e indica que EVRA® es menos eficaz en estas mujeres.
Con el uso de AOC en dosis mayores (50 microgramos de etinilestradiol) se reduce el riesgo de cáncer de ovario y de endometrio. Queda por confirmar si esto es aplicable a dosis inferiores de anticonceptivos hormonales combinados.
Propiedades farmacocinéticas
Absorción
Tras la aplicación de EVRA®, los niveles de norelgestromina y de etinilestradiol en plasma alcanzan el estado estacionario aproximadamente a las 48 horas. Las concentraciones en estado estacionario (Css) de norelgestromina y EE durante una semana llevando el parche transdérmico son aproximadamente de 0.8 ng/ml y 50 pg/ml, respectivamente. En ensayos de dosis múltiples, las concentraciones plasmáticas y AUC para norelgestromina y EE aumentaron ligeramente con el tiempo comparadas con la semana 1 del ciclo 1.
Se estudió la absorción de la norelgestromina y del etinilestradiol tras la aplicación de EVRA® en condiciones similares a las encontradas en un gimnasio (sauna, jacuzzi, cinta para correr y otros ejercicios aeróbicos) y en un baño de agua fría. Los resultados con norelgestromina indicaron que no hubo efectos significativos del tratamiento sobre la Css o el AUC en comparación con el uso normal. Con EE se observaron aumentos ligeros tras el ejercicio aeróbico y en la cinta para correr; sin embargo, los valores de Css tras el ejercicio estaban dentro de los límites de referencia. No hubo un efecto significativo del baño con agua fría en estos parámetros.
Los resultados de un ensayo para estudiar la prolongación de uso de un único parche transdérmico de EVRA® de 7 a 10 días indicaron que se mantuvo la Css objetivo de norelgestromina y etinilestradiol durante el período adicional de uso de EVRA® de 3 días (10 días). Estos hallazgos sugieren que la eficacia clínica se podría mantener incluso si se olvida cambiar el parche hasta 2 días completos.
Distribución
La norelgestromina y el norgestrel (un metabolito en suero de la norelgestromina) tienen una unión alta (> 97 %) a las proteínas séricas. La norelgestromina se fija a la albúmina y no a la globulina fijadora de las hormonas sexuales (SHBG), mientras que el norgestrel se une principalmente a la globulina fijadora de las hormonas sexuales, lo que limita su actividad biológica. El etinilestradiol se une ampliamente a la albúmina sérica.
Biotransformación
La norelgestromina sufre metabolismo hepático, y entre los metabolitos resultantes se encuentra el norgestrel, que se une principalmente a la globulina fijadora de las hormonas sexuales, y varios metabolitos conjugados e hidroxilados. El etinilestradiol se metaboliza asimismo dando varios productos hidroxilados y sus conjugados de glucorónido y sulfato.
Eliminación
Tras retirar el parche transdérmico, las semividas de eliminación medias de la norelgestromina y del etinilestradiol fueron aproximadamente de 28 horas y 17 horas, respectivamente. Los metabolitos de la norelgestromina y del etinilestradiol se eliminan por vía renal y en las heces.
Anticonceptivos transdérmicos frente a orales
Los perfiles farmacocinéticos de los anticonceptivos transdérmicos hormonales y de los anticonceptivos hormonales combinados orales son distintos y se debe tener precaución cuando se realice una comparación directa de los parámetros farmacocinéticos.
En un ensayo en el cuál se comparó EVRA® con un anticonceptivo oral que contiene 250 microgramos de norgestimato (profármaco de la norelgestromina) y 35 microgramos de etinilestradiol, los valores de Cmáx para norelgestromina y EE fueron el doble en mujeres a las que se administró el anticonceptivo oral en comparación con EVRA®, mientras que la exposición global (AUC y Css) fue comparable. La variabilidad interindividual (% CV) de los parámetros farmacocinéticos tras la administración de EVRA® fue mayor que la variabilidad determinada con el anticonceptivo oral.
EFECTOS DE LA EDAD, PESO CORPORAL Y ÁREA DE SUPERFICIE CORPORAL
Se evaluaron los efectos de la edad, peso corporal y área de superficie corporal sobre la farmacocinética de la norelgestromina y del etinilestradiol en 230 mujeres sanas a partir de nueve ensayos farmacocinéticos de aplicación individual de EVRA® durante 7 días. Tanto para la norelgestromina como para el EE, el aumento de edad, peso corporal y área de superficie corporal estaban asociados con ligeros descensos de los valores de Css y AUC. Sin embargo, sólo una pequeña fracción (10-20 %) de la variabilidad general en la farmacocinética de la norelgestromina y del EE tras la aplicación de EVRA® se puede asociar con alguno o todos los parámetros demográficos anteriores.
Datos preclínicos sobre seguridad
Los datos no clínicos no muestran riesgos especiales para los seres humanos según los estudios convencionales sobre farmacología de seguridad, toxicidad de dosis repetidas, genotoxicidad y potencial carcinogénico. Con respecto a la toxicidad reproductiva, la norelgestromina mostró toxicidad fetal en conejos, pero el margen de seguridad para este efecto fue suficientemente alto. Los datos sobre la toxicidad reproductiva para la combinación de norelgestromina con etinilestradiol no están disponibles. Los datos para la combinación de norgestimato (profármaco de la norelgestromina) con etinilestradiol indican en los animales hembras un descenso en la fertilidad y en la eficiencia de implantación (rata), un aumento en la resorción fetal (rata, conejo) y, a altas dosis, un descenso en la viabilidad y fertilidad de la progenie femenina (rata). No se conoce la relevancia de estos datos para la exposición en humanos, ya que se puede considerar que los efectos están relacionados con acciones farmacodinámicas bien conocidas o son específicos para las especies.
Los estudios realizados para comprobar los efectos de EVRA® en la piel indican que este sistema no tiene potencial para producir sensibilización y sólo causa una irritación leve cuando se aplica en la piel de conejo.
CONTRAINDICACIONES
No se deben utilizar anticonceptivos hormonales combinados (AHC) en las siguientes condiciones. Si se produjera alguna de estas enfermedades durante el uso de EVRA®, se debe suspender el tratamiento con EVRA® de inmediato.
• Presencia o riesgo de tromboembolismo venoso (TEV)
• Tromboembolismo venoso: TEV actual (con anticoagulantes) o antecedentes del mismo (p. ej., trombosis venosa profunda [TVP] o embolia pulmonar [EP]);
• Predisposición hereditaria o adquirida conocida al tromboembolismo venoso, tal como resistencia a la PCA (incluyendo al factor V Leiden), deficiencia de antitrombina III, deficiencia de proteína C, deficiencia de proteína S;
• Cirugía mayor con inmovilización prolongada (ver sección Advertencias y precauciones especiales de empleo);
• Riesgo elevado de tromboembolismo venoso debido a la presencia de varios factores de riesgo (ver sección Advertencias y precauciones especiales de empleo);
• Presencia o riesgo de tromboembolismo arterial (TEA)
• Tromboembolismo arterial: tromboembolismo arterial actual, antecedentes del mismo (por ejemplo, infarto de miocardio) o afección prodrómica (por ejemplo, angina de pecho);
• Enfermedad cerebrovascular: ictus actual, antecedentes de ictus o afección prodrómica (por ejemplo, accidente isquémico transitorio, AIT);
• Predisposición hereditaria o adquirida conocida al tromboembolismo arterial, tal como hiperhomocisteinemia y anticuerpos antifosfolipídicos (anticuerpos anticardiolipina, anticoagulante del lupus);
• Antecedentes de migraña con síntomas neurológicos focales;
• Riesgo elevado de tromboembolismo arterial debido a múltiples factores de riesgo (ver sección Advertencias y precauciones especiales de empleo) o a la presencia de un factor de riesgo grave como:
- diabetes mellitus con síntomas vasculares
- hipertensión grave
- dislipoproteinemia intensa
• Hipersensibilidad a los principios activos o a alguno de los excipientes incluidos en la sección Lista de Excipientes.
• Presencia o sospecha de carcinoma de mama.
• Carcinoma de endometrio o presencia o sospecha de otra neoplasia estrógenodependiente
• Función hepática anormal relacionada con enfermedad hepatocelular crónica o aguda
• Adenomas o carcinomas hepáticos
• Hemorragia genital anormal sin diagnosticar
• Uso concomitante con medicamentos que contienen ombitasvir/paritaprevir/ritonavir y dasabuvir (ver las secciones Advertencias y precauciones especiales de empleo e Interacción con otros medicamentos y otras formas de interacción)
FERTILIDAD, EMBARAZO Y LACTANCIA
Embarazo
EVRA® no está indicado durante el embarazo.
Los estudios epidemiológicos no indican un aumento del riesgo de defectos congénitos en los niños de las mujeres que utilizaron anticonceptivos orales combinados antes del embarazo. La mayoría de los estudios recientes tampoco indican un efecto teratogénico si se utilizan anticonceptivos orales combinados de forma inadvertida al principio del embarazo.
Los datos limitados de los resultados sobre mujeres embarazadas que utilizan EVRA®, no permiten obtener conclusiones sobre su seguridad durante el embarazo.
Estudios en animales han demostrado efectos indeseables durante el embarazo y lactancia (ver sección Datos preclínicos sobre seguridad). Basado en estos datos animales, los efectos indeseables debidos a la acción hormonal de los componentes activos no se pueden excluir. Sin embargo, la experiencia general con anticonceptivos orales combinados durante el embarazo no proporcionó evidencias de efectos indeseables en humanos.
En caso de embarazo durante el uso de EVRA®, se debe interrumpir el uso de EVRA® de inmediato.
El aumento de riesgo de TEV durante el postparto se debe considerar cuando se reinicie el uso de EVRA® (ver secciones Posología y forma de administración y Advertencias y precauciones especiales de empleo).
Lactancia
La lactancia se puede ver afectada por los anticonceptivos hormonales combinados, ya que pueden reducir la cantidad y cambiar la composición de la leche materna. Por lo tanto, no se recomienda el uso de EVRA® hasta que la madre haya dejado de amamantar a su hijo.
Fertilidad
Las mujeres pueden experimentar un retraso en la concepción tras la discontinuación de EVRA®.
EFECTOS SOBRE LA CAPACIDAD PARA CONDUCIR Y UTILIZAR MÁQUINAS
La influencia de EVRA® sobre la capacidad para conducir y utilizar máquinas es nula o insignificante.
REACCIONES ADVERSAS
Resumen del perfil de seguridad
Las reacciones adversas notificadas con más frecuencia en ensayos clínicos fueron dolor de cabeza, náuseas y sensibilidad en las mamas, observándose aproximadamente en un 21.0%, 16.6% y 15.9% de los pacientes, respectivamente. Las reacciones adversas pueden ocurrir al principio del tratamiento, pero normalmente disminuyen después de los tres primeros ciclos, incluidas oligometrorragia, sensibilidad en las mamas y náuseas.
Descripción de ciertas reacciones adversas
Se ha observado un aumento del riesgo de episodios trombóticos y tromboembólicos arteriales y venosos, entre ellos infarto de miocardio, ictus, accidentes isquémicos transitorios, trombosis venosa y embolia pulmonar, en mujeres que utilizan AHCs, que se comentan con más detalle en la sección Advertencias y precauciones especiales de empleo.
Listado tabulado de reacciones adversas
La seguridad fue evaluada en 3 322 mujeres sexualmente activas que participaron en tres ensayos clínicos de Fase III diseñados para evaluar la eficacia anticonceptiva. Estas usuarias recibieron seis o trece ciclos de anticoncepción (EVRA® o anticonceptivo oral comparador), tomaron al menos una dosis del medicamento del estudio y proporcionaron datos de seguridad.
En la tabla 1 indicada más abajo se reflejan las reacciones adversas notificadas en los ensayos clínicos y de la experiencia postcomercialización. Convención MedDRA sobre frecuencia: muy frecuentes (≥ 1/10); frecuentes (≥ 1/100 a <1/10); poco frecuentes (≥ 1/1.000 a < 1/100); raras (≥1/10.000 a < 1/1.000); muy raras (<1/10.000); frecuencia no conocida (no puede estimarse a partir de los datos disponibles).
|
Tabla 1: Frecuencia de las reacciones adversas |
|
|
Clasificación por órganos y sistemas Frecuencia |
Reacción Adversa |
|
Infecciones e infestaciones |
|
|
Frecuentes |
Infección fúngica (vulvo) vaginal Candidiasis vaginal |
|
Raras |
Erupción pustular* Pústulas en el lugar de aplicación |
|
Neoplasias benignas, malignas y no especificadas (incluyendo quistes y pólipos) |
|
|
Raras |
Neoplasia hepática *† Cáncer de mama *† Carcinoma de cérvix *† Adenoma hepático *† Leiomioma uterino Fibroadenoma de mama |
|
Trastornos del sistema inmunológico |
|
|
Poco frecuentes |
Hipersensibilidad |
|
Trastornos del metabolismo y de la nutrición |
|
|
Poco frecuentes |
Hipercolesterolemia Retención de líquidos Aumento del apetito |
|
Raras |
Hiperglucemia* Resistencia a la insulina* |
|
Trastornos psiquiátricos |
|
|
Frecuentes |
Trastornos de ánimo afectividad y ansiedad |
|
Poco frecuentes |
Insomnio Disminución de la líbido |
|
Raras |
Ira* Frustración* Aumento de la líbido |
|
Trastornos del sistema nervioso |
|
|
Muy frecuentes |
Dolor de cabeza |
|
Frecuentes |
Migraña Mareo |
|
Raras |
Accidente cerebrovascular**† Hemorragia cerebral*† Gusto anormal* |
|
Trastornos oculares |
|
|
Raras |
Intolerancia a las lentes de contacto* |
|
Trastornos cardíacos |
|
|
Raras |
Tromboembolismo arterial Infarto (agudo) de miocardio*† |
|
Trastornos vasculares |
|
|
Poco frecuentes |
Hipertensión |
|
Raras |
Crisis hipertensiva* Trombosis arterial**† Trombosis venosa**† Trombosis*† Tromboembolismo venoso |
|
Trastornos respiratorios, torácicos y mediastínicos |
|
|
Raras |
Trombosis de la arteria pulmonar*† Embolia pulmonar† |
|
Trastornos gastrointestinales |
|
|
Muy frecuentes |
Náusea |
|
Frecuentes |
Dolor abdominal Vómitos Diarrea |
|
Raras |
Distensión abdominal Colitis* |
|
Trastornos hepatobiliares |
|
|
Raras |
Colecistitis Colelitiasis† Lesión hepática* Ictericia colestática*† Colestasis*† |
|
Trastornos de la piel y del tejido subcutáneo |
|
|
Frecuentes |
Acné Erupción cutánea Prurito Reacción en la piel Irritación de la piel |
|
Poco frecuentes |
Alopecia Dermatitis alérgica Eccema Reacción de fotosensibilidad Dermatitis de contacto Urticaria Eritema |
|
Raras |
Angioedema* Eritema (multiforme nudoso) * Cloasma† Erupción exfoliativa* Prurito generalizado Erupción (eritematosa prurítica) Dermatitis seborreica* |
|
Trastornos musculoesqueléticos y del tejido conjuntivo |
|
|
Frecuentes |
Espasmos musculares |
|
Trastornos del aparato reproductor y de la mama |
|
|
Muy frecuentes |
Sensibilidad en las mamas |
|
Frecuentes |
Dismenorrea, Sangrado vaginal y trastornos menstruales**† Espasmo uterino Trastornos de la mama Secreción vaginal |
|
Poco frecuentes |
Galactorrea Síndrome premenstrual Sequedad vulvovaginal |
|
Raras |
Displasia cervical* Supresión de la lactancia* Secreción genital |
|
Trastornos generales y alteraciones en el lugar de administración |
|
|
Frecuentes |
Malestar |
|
Poco frecuentes |
Fatiga Reacciones en el lugar de aplicación (eritema, irritación, prurito, erupción cutánea) Edema generalizado Edema periférico Reacciones en el lugar de aplicación** |
|
Raras |
Edema facial* Edema con fóvea* Hinchazón Reacciones en el lugar de aplicación* (por ejemplo, absceso, erosión) Edema localizado* |
|
Exploraciones complementarias |
|
|
Frecuentes |
Aumento de peso |
|
Poco frecuentes |
Aumento de la presión sanguínea Trastornos lipídicos** |
|
Raras |
Disminución de la glucosa en sangre*† Niveles anormales de glucosa en sangre*† |
|
*Notificaciones post comercialización. **Incluyen reacciones adversas notificadas en ensayos clínicos y notificaciones post comercialización. † Ver sección Advertencias y precauciones de especiales de empleo. |
|
Notificación de sospechas de reacciones adversas
Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización.
Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones adversas a través del Centro Nacional de Farmacovigilancia y Tecnovigilancia.
INTERACCIÓN CON OTROS MEDICAMENTOS Y OTRAS FORMAS DE INTERACCIÓN
Nota: Se deben consultar las fichas técnicas de toda la medicación concomitante con el fin de identificar posibles interacciones.
Interacciones farmacodinámicas
El uso concomitante con medicamentos que contienen ombitasvir/ paritaprevir/ ritonavir y dasubuvir, con o sin ribavirina puede aumentar el riesgo de elevaciones de la ALT (ver las secciones Contraindicaciones y Advertencias y precauciones especiales de empleo).
Por lo tanto, las personas que utilizan EVRA® deben cambiar a un método anticonceptivo alternativo (por ejemplo, método anticonceptivo sólo con progestágenos o métodos no hormonales) antes de iniciar el tratamiento con esta farmacoterapia combinada.
EVRA® puede ser reiniciado dos semanas después de la finalización del tratamiento con esta farmacoterapia combinada.
Efectos de otros medicamentos sobre EVRA
Pueden aparecer interacciones con medicamentos inductores de las enzimas microsomales lo cual pueden dar lugar a un aumento en el aclaramiento de las hormonas sexuales pudiendo producir sangrado intermenstrual y/o fallo del tratamiento anticonceptivo. Se han notificado las siguientes interacciones en la bibliografía.
Principios activos que aumentan el aclaramiento de los AHCs (reducción de la eficacia de los AHCs debido a inducción enzimática), por ejemplo: Barbitúricos, bosentán, carbamazepina, fenitoína, primidona, rifampicina, modafinilo y medicamentos para el VIH ritonavir, nevirapina y efavirenz y también posiblemente felbamato, griseofulvina, oxcarbazepina, topiramato y medicamentos a base de plantas medicinales que contengan Hierba de San Juan (Hypericum perforatum).
Forma de empleo
Se puede observar inducción enzimática tras varios días de tratamiento. Generalmente, la máxima inducción enzimática se observa alrededor de los 10 días y se puede mantener durante al menos 4 semanas después de la suspensión del tratamiento farmacológico.
A corto plazo
Las mujeres en tratamiento a corto plazo con medicamentos inductores de enzimas metabolizadoras hepáticas de medicamentos o con los distintos principios activos que inducen estas enzimas deben utilizar de forma temporal un método anticonceptivo de barrera adicional además de EVRA®, es decir, durante el tiempo de la administración concomitante del medicamento y hasta 28 días después de su interrupción.
El siguiente parche transdérmico se debe poner sin intercalar la semana habitual de descanso en el caso de que continúe la administración concomitante de estos medicamentos después del final del período de tres semanas con parche.
A largo plazo
Se recomienda que las mujeres que estén en tratamiento a largo plazo con principios activos que sean inductores enzimáticos, utilicen de forma simultánea otro método anticonceptivo no hormonal fiable.
Principios activos con efectos variables sobre el aclaramiento de los AHCs
Cuando son administrados de forma conjunta con AHCs, algunas combinaciones de inhibidores de la proteasa del VIH e inhibidores de la transcriptasa inversa no nucleosídicos, incluyendo combinaciones de inhibidores del VHC pueden aumentar o disminuir las concentraciones plasmáticas de estrógenos o progestágenos. El efecto neto de estos cambios puede ser clínicamente relevante en algunos casos.
Por tanto, se deben consultar las fichas técnicas de toda la medicación concomitante para el VIH con el fin de identificar potenciales interacciones y cualquier recomendación relacionada.
En caso de duda, las mujeres en tratamiento con inhibidores de la proteasa o inhibidores de la transcriptasa inversa no nucleosídicos deben utilizar un método anticonceptivo de barrera adicional.
Inhibición del metabolismo del etinilestradiol
Se ha demostrado que etoricoxib eleva los niveles plasmáticos de etinilestradiol (50 a 60%) cuando se toma concomitantemente con anticonceptivos hormonales orales trifásicos. Se cree que etoricoxib incrementa los niveles de etinilestradiol porque inhibe la actividad de la sulfotransferasa inhibiendo así el metabolismo del etinilestradiol.
Efecto de EVRA® sobre otros medicamentos
Los anticonceptivos hormonales pueden influir sobre el metabolismo de ciertos principios activos. En consecuencia, las concentraciones plasmáticas y tisulares pueden aumentar (por ejemplo, ciclosporina). Puede ser necesario un ajuste de dosis de los medicamentos concomitantes.
Lamotrigina: Los anticonceptivos hormonales combinados han mostrado un descenso significativo de las concentraciones plasmáticas de lamotrigina cuando se administran de forma conjunta posiblemente debido a la inducción de glucuronidación de la lamotrigina. Esto podría reducir el control de las crisis (convulsiones) y por tanto puede ser necesario un ajuste de dosis de lamotrigina.
Pruebas de laboratorio
La utilización de anticonceptivos esteroideos puede influir en los resultados de ciertas pruebas de laboratorio, incluyendo valores bioquímicos de la función hepática, tiroidea, suprarrenal y renal, niveles plasmáticos de proteínas (transportadoras), por ejemplo, globulina fijadora de corticosteroides y fracciones lipídicas/lipoproteínicas; parámetros del metabolismo de los hidratos de carbono y de la coagulación y fibrinólisis. Generalmente los cambios permanecen dentro del intervalo normal de laboratorio.
ADVERTENCIAS Y PRECAUCIONES ESPECIALES DE EMPLEO
Advertencias
Si alguna de las afecciones o factores de riesgo que se mencionan a continuación está presente, se debe comentar con la mujer la idoneidad de EVRA®.
Si alguna de estas afecciones o alguno de estos factores de riesgo se agrava o aparece por primera vez, se debe aconsejar a la mujer que consulte a su médico para determinar si debe interrumpir el uso de EVRA®.
No hay evidencia clínica que indique que un parche transdérmico sea, en ningún aspecto, más seguro que los anticonceptivos orales combinados.
El uso de EVRA® no está indicado durante el embarazo (ver sección Fertilidad, embarazo y lactancia).
Riesgo de tromboembolismo venoso (TEV)
El uso de cualquier anticonceptivo hormonal combinado incrementa el riesgo de tromboembolismo venoso (TEV), comparado con la no utilización. Los medicamentos que contienen levonorgestrel, norgestimato o noretisterona se asocian con el riesgo más ajo de TEV. Otros medicamentos como EVRA® pueden tener hasta el doble de este nivel de riesgo. La decisión de utilizar cualquier medicamento diferente del que tiene el menor riesgo de TEV se debe tomar solamente después de comentarlo con la mujer para garantizar que comprende el riesgo de TEV con EVRA®, cómo afectan sus actuales factores de riesgo a este riesgo y que su riesgo de TEV es mayor durante el primer año de uso. También existen ciertas evidencias de que el riesgo aumenta cuando se reinicia el AHC después de una interrupción del uso de 4 semanas o más.
Entre las mujeres que no utilizan AHCs y que no están embarazadas, aproximadamente 2 de cada 10 000 presentarán un TEV en el plazo de un año. No obstante, el riesgo puede ser mucho mayor en cada mujer en particular, en función de sus factores de riesgo subyacentes (ver a continuación).
Se estima que de cada 10 000 mujeres que utilizan un AHC de dosis baja que contiene levonorgestrel, unas 61 presentarán un TEV en un año. Ciertos estudios han sugerido que la incidencia de TEV en mujeres que utilizaron EVRA® es hasta el doble de alta que en usuarias de AHCs que contienen levonorgestrel. Esto corresponde a entre unas 6 y 12 TEV en un año entre 10 000 mujeres que utilizan EVRA®.
En ambos casos, el número de TEV por año es inferior al número esperado en mujeres durante el embarazo o en el período posparto.
El TEV puede ser mortal en el 1-2 % de los casos.
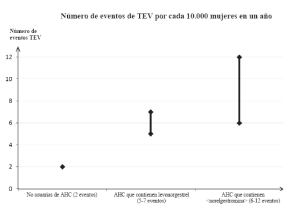
1 Punto medio del intervalo de 5-7 por cada 10.000 AM, basado en un riesgo relativo para los AHC que contienen levonorgestrel frente a la no utilización de aproximadamente 2.3 a 3.6.
Se han notificado casos muy raros en usuarias de anticonceptivos hormonales combinados de trombosis en otros vasos sanguíneos, como arterias y venas hepáticas, mesentéricas, renales, o retinianas.
Factores de riesgo para TEV
El riesgo de complicaciones tromboembólicas venosas en usuarias de AHCs puede aumentar sustancialmente en una mujer con factores de riesgo adicionales, en particular si existen varios factores de riesgo (ver tabla).
EVRA® está contraindicado si una mujer tiene varios factores de riesgo que la ponen en una situación de alto riesgo de trombosis venosa (ver sección Contraindicaciones). Si una mujer tiene más de un factor de riesgo, es posible que el aumento del riesgo sea mayor que la suma de los factores individuales; en este caso se debe tener en cuenta su riesgo total de TEV. Si se considera que la relación beneficio/riesgo es negativa, no se debe prescribir un AHC (ver sección Contraindicaciones).
|
Tabla: Factores de riesgo para TEV |
|
|
Factor de riesgo |
Comentario |
|
Obesidad (índice de masa corporal superior a 30 kg/m2) |
El riesgo aumenta de forma sustancial con el aumento del IMC. Especialmente importante en mujeres con factores de riesgo adicionales. |
|
Inmovilización prolongada, cirugía mayor, cualquier intervención quirúrgica de las piernas o pelvis, neurocirugía o traumatismo importante. Nota: La inmovilización temporal, incluso los viajes en avión > 4 horas, también puede ser un factor de riesgo para TEV, en especial en mujeres con otros factores de riesgo. |
En estas circunstancias es aconsejable interrumpir el uso del parche (en caso de intervención quirúrgica programada, al menos con cuatro semanas de antelación) y no reanudarlo hasta dos semanas después de que se recupere completamente la movilidad. Se debe utilizar otro método anticonceptivo para evitar un embarazo involuntario. Se debe considerar un tratamiento antitrombótico si no se ha interrumpido con antelación el uso de EVRA. |
|
Antecedentes familiares positivos (algún caso de tromboembolismo venoso en un hermano o en un progenitor, especialmente a una edad relativamente temprana). |
Si se sospecha que existe una predisposición hereditaria, la mujer debe ser derivada a un especialista antes de tomar la decisión de usar un AHC. |
|
Otras enfermedades asociadas al TEV |
Cáncer, lupus eritematoso diseminado, síndrome urémico hemolítico, enfermedad inflamatoria intestinal crónica (enfermedad de Crohn o colitis ulcerosa) y anemia drepanocítica. |
|
Aumento de edad |
En especial por encima de los 35 años. |
No hay consenso sobre el posible papel de las venas varicosas y la tromboflebitis superficial en la aparición o progresión de la trombosis venosa.
Es preciso tener en cuenta el aumento del riesgo de tromboembolismo en el embarazo, y en particular en el período de 6 semanas del puerperio (para obtener información sobre “Embarazo y lactancia”, ver sección Fertilidad, embarazo y lactancia).
Síntomas de TEV (trombosis venosa profunda y embolia pulmonar)
En el caso de que se produzcan síntomas, se debe aconsejar a la mujer que busque asistencia médica urgente y que informe al profesional sanitario de que está tomando un AHC.
Los síntomas de trombosis venosa profunda (TVP) pueden incluir:
• hinchazón unilateral de la pierna y/o pie o a lo largo de una vena de la pierna;
• dolor o sensibilidad en la pierna, que tal vez se advierta sólo al ponerse de pie o al caminar;
• aumento de la temperatura en la pierna afectada; enrojecimiento o decoloración de la piel de la pierna;
Los síntomas de embolia pulmonar (EP) pueden incluir:
• aparición repentina de falta de aliento o respiración rápida injustificada;
• tos repentina que puede estar asociada a hemoptisis;
• dolor torácico agudo;
• aturdimiento intenso o mareo;
• latidos cardíacos acelerados o irregulares;
Algunos de estos síntomas (por ejemplo, “falta de aliento”, “tos”) son inespecíficos y se pueden confundir con acontecimientos más frecuentes o menos graves (por ejemplo, infecciones del tracto respiratorio).
Otros signos de oclusión vascular pueden incluir: dolor repentino, hinchazón y ligera coloración azul de una extremidad.
Si la oclusión se produce en el ojo, los síntomas pueden variar desde visión borrosa indolora, que puede evolucionar hasta la pérdida de la visión. A veces la pérdida de la visión se puede producir casi de inmediato.
Riesgo de tromboembolismo arterial (TEA)
Estudios epidemiológicos han asociado el uso de los AHCs con un aumento del riesgo de tromboembolismo arterial (infarto de miocardio) o de accidente cerebrovascular (por ejemplo, accidente isquémico transitorio, ictus). Los episodios tromboembólicos arteriales pueden ser mortales.
Factores de riesgo para TEA
El riesgo de que se produzcan complicaciones tromboembólicas arteriales o un accidente cerebrovascular en las usuarias de AHCs aumenta en mujeres con factores de riesgo (ver tabla). EVRA® está contraindicado si una mujer presenta varios factores de riesgo de TEA o uno grave que la ponen en una situación de alto riesgo de trombosis arterial (ver sección Contraindicaciones). Si una mujer tiene más de un factor de riesgo, es posible que el aumento del riesgo sea mayor que la suma de los factores individuales; en este caso se debe tener en cuenta su riesgo total. Si se considera que la relación beneficio/riesgo es negativa, no se debe prescribir un AHC (ver sección Contraindicaciones).
|
Tabla: Factores de riesgo para TEA |
|
|
Factor de riesgo |
Comentario |
|
Edad |
En especial por encima de los 35 años |
|
Tabaquismo |
Se debe aconsejar a las mujeres que no fumen si desean utilizar un AHC. Se debe aconsejar encarecidamente a las mujeres de más de 35 años que continúan fumando que utilicen un método anticonceptivo diferente. |
|
Hipertensión arterial |
|
|
Obesidad (índice de masa corporal superior a 30 kg/m2) |
El riesgo aumenta de forma sustancial con el aumento del IMC. Especialmente importante en mujeres con factores de riesgo adicionales. |
|
Antecedentes familiares positivos (algún caso de tromboembolismo arterial en un hermano o en un progenitor, especialmente a una edad relativamente temprana (Por ejemplo: antes de los 50 años). |
Si se sospecha que existe una predisposición hereditaria, la mujer se debe derivar a un especialista antes de tomar la decisión de usar un AHC. |
|
Migraña |
Un aumento de la frecuencia o la intensidad de las migrañas durante el uso de AHCs (que puede ser precursor de un acontecimiento cerebrovascular) puede motivar su interrupción inmediata. |
|
Otras enfermedades asociadas a acontecimientos vasculares adversos |
Diabetes mellitus, hiperhomocisteinemia, valvulopatía y fibrilación auricular, dislipoproteinemia y lupus eritematoso sistémico. |
Síntomas de TEA
En el caso de que se produzcan síntomas, se debe aconsejar a la mujer que busque asistencia médica urgente y que informe al profesional sanitario de que está tomando un AHC.
Los síntomas de un accidente cerebrovascular pueden incluir:
• entumecimiento o debilidad repentinos de la cara, brazo o pierna, especialmente en un lado del cuerpo;
• dificultad repentina para caminar, mareo, pérdida del equilibrio o de la coordinación;
• confusión repentina, dificultad para hablar o para comprender;
• dificultad repentina de visión en un ojo o en ambos;
• cefalea repentina, intensa y prolongada sin causa conocida;
• pérdida del conocimiento o desmayo, con o sin convulsiones;
Los síntomas temporales sugieren que el evento es un accidente isquémico transitorio (AIT).
Los síntomas de un infarto de miocardio (IM) pueden incluir:
• dolor, molestias, presión, pesadez, sensación de opresión o plenitud en el tórax, brazo o debajo del esternón;
• malestar que irradia a la espalda, la mandíbula, la garganta, el brazo o el estómago;
• sensación de plenitud, indigestión o ahogo;
• sudoración, náuseas, vómitos o mareo;
• debilidad extrema, ansiedad o falta de aliento;
• latidos cardíacos acelerados o irregulares;
Se debe advertir encarecidamente a las mujeres que toman anticonceptivos combinados que se pongan en contacto con su médico en caso de que observen posibles síntomas de trombosis. En caso de sospecha de trombosis o trombosis confirmada, se debe interrumpir el uso de los anticonceptivos hormonales. Se debe recurrir a un método anticonceptivo apropiado debido a la teratogenicidad de la terapia anticoagulante (cumarinas).
Tumores
En algunos estudios epidemiológicos, se ha notificado un aumento del riesgo de cáncer de cuello uterino en mujeres que utilizaban anticonceptivos orales combinados a largo plazo, pero se mantiene la controversia sobre hasta qué punto este hallazgo se puede atribuir a factores de confusión del comportamiento sexual y otros factores tales como el papilomavirus humano (VPH).
Un metanálisis de 54 estudios epidemiológicos indicó que las mujeres que en la actualidad están tomando anticonceptivos orales combinados tienen un riesgo ligeramente mayor (RR = 1.24) de presentar un diagnóstico de cáncer de mama. El riesgo adicional desaparece gradualmente a lo largo de los 10 años siguientes a haber dejado de tomar los anticonceptivos orales combinados. Ya que el cáncer de mama es raro en mujeres menores de 40 años, el exceso de diagnósticos de cáncer de mama en mujeres que actualmente toman anticonceptivos orales combinados o que los tomaron recientemente es pequeño en relación con el riesgo global de cáncer de mama. Los carcinomas de mama diagnosticados en mujeres que han tomado alguna vez anticonceptivos orales combinados tienden a ser menos avanzados clínicamente que los carcinomas diagnosticados en mujeres que nunca han tomado anticonceptivos orales combinados. El patrón observado de aumento de riesgo se puede deber a un diagnóstico más precoz de cáncer de mama en las usuarias de anticonceptivos orales combinados, a los efectos biológicos de los anticonceptivos orales combinados o a una combinación de los dos factores.
Se han notificado casos raros de tumores hepáticos benignos o con menor frecuencia incluso malignos entre las usuarias de anticonceptivos orales combinados. En casos aislados, estos tumores han dado lugar a hemorragias intra-abdominales que podrían causar la muerte. Por lo tanto, un tumor hepático se debe considerar en el diagnóstico diferencial cuando se produce dolor abdominal superior agudo, aumento del tamaño del hígado o signos de hemorragia intraabdominal en mujeres que usan EVRA®.
Elevación de ALT
Durante ensayos clínicos con pacientes tratados para infecciones por el virus de la hepatitis C (VHC) con medicamentos que contienen ombitasvir/ paritaprevir/ ritonavir y dasabuvir con o sin ribavirina, se produjeron elevaciones de transaminasa (ALT) mayores a 5 veces los límites superiores normales (LSN) con una frecuencia significativamente mayor en mujeres que utilizan medicamentos que contienen etinil-estradiol como los anticonceptivos hormonales combinados (AHCs) (ver las secciones Contraindicaciones e Interacciones con otros medicamentos y otras formas de interacción).
Otras patologías
• La eficacia anticonceptiva puede verse reducida en mujeres que pesan 90 kg o más (ver secciones Posología y forma de administración y Propiedades farmacodinámicas).
• Las mujeres con diagnóstico o historia familiar de hipertrigliceridemia podrían presentar un riesgo mayor de pancreatitis al utilizar anticonceptivos hormonales combinados.
• Aunque se han registrado ligeros aumentos de la presión arterial en muchas mujeres que utilizan anticonceptivos hormonales, son raros los aumentos clínicamente relevantes. No se ha establecido una asociación concluyente entre el uso de anticonceptivos hormonales y la hipertensión clínicamente relevante. Si durante el tratamiento con anticonceptivos hormonales combinados las mujeres hipertensas presentan una elevación constante o aumentos significativos de la tensión y no responden adecuadamente a los antihipertensivos, se debe interrumpir el uso de los anticonceptivos hormonales combinados. Se puede retomar su uso si se alcanzan valores normotensos con antihipertensivos.
• Se han notificado casos nuevos o agravamiento de las siguientes enfermedades tanto con el embarazo como con el uso de anticonceptivos orales combinados, pero la evidencia de su asociación con el uso de anticonceptivos orales combinados no es concluyente: ictericia y/o prurito asociado a colestasis, enfermedades de la vesícula biliar incluyendo colecistitis y colelitiasis, porfiria, lupus eritematoso sistémico, síndrome urémico hemolítico, corea de Sydenham, herpes gestacional, pérdida de audición relacionada con la otosclerosis.
• Las alteraciones graves o crónicas en la función hepática pueden hacer necesaria la interrupción de los anticonceptivos hormonales combinados hasta que los indicadores de la función hepática vuelvan a la normalidad. La recurrencia de prurito relacionado con la colestasis, que haya podido ocurrir en un embarazo anterior o asociado al uso previo de hormonas sexuales esteroídicas hace necesaria la interrupción de los anticonceptivos hormonales combinados.
• Aunque los anticonceptivos hormonales combinados pueden tener un efecto sobre la resistencia periférica a la insulina y la tolerancia a la glucosa, no hay evidencia que apoye la necesidad de modificar el régimen terapéutico en pacientes diabéticas por el uso concomitante de anticonceptivos hormonales combinados. Sin embargo, se debe monitorizar a las mujeres diabéticas, sobre todo en las fases iniciales del tratamiento con EVRA®.
• Durante el uso de anticonceptivos orales combinados, se ha notificado el empeoramiento de la depresión endógena, la epilepsia, la enfermedad de Crohn y la colitis ulcerosa.
• Ocasionalmente pueden darse casos de cloasma con el uso de anticonceptivos hormonales, especialmente en pacientes con una historia de cloasma gravídico. Las mujeres con tendencia al cloasma deben evitar la exposición al sol o a la radiación ultravioleta mientras usen EVRA®. A menudo el cloasma no es enteramente reversible.
Exploración/consulta médica
Antes de iniciar o reanudar el tratamiento con EVRA® se debe realizar una anamnesis completa (incluidos los antecedentes familiares) y descartar un posible embarazo. Se debe medir la tensión arterial y realizar una exploración física, guiada por las contraindicaciones (ver sección Contraindicaciones) y por las advertencias (ver sección Advertencias y precauciones especiales de empleo). Es importante dirigir la atención de la mujer hacia la información sobre la trombosis venosa y arterial, incluido el riesgo de EVRA® en comparación con otros AHCs, los síntomas de TEV y TEA, los factores de riesgo conocidos y qué debe hacer en caso de sospecha de trombosis.
También se debe indicar a la mujer que lea cuidadosamente el prospecto y siga las instrucciones allí descritas. La frecuencia y la naturaleza de las exploraciones se deben basar en las directrices clínicas establecidas y se adaptarán a cada mujer en particular.
Se debe advertir a las mujeres que los anticonceptivos hormonales no protegen frente a la infección por VIH (SIDA) ni frente a otras enfermedades de transmisión sexual.
Irregularidades en la hemorragia
Con todos los anticonceptivos hormonales combinados puede producirse una pérdida de sangre irregular (oligometrorragia o hemorragia intermenstrual), especialmente durante los primeros meses de uso. Por esta razón, sólo será útil una opinión médica sobre las pérdidas de sangre irregulares después de un período de adaptación de aproximadamente 3 ciclos. Si persiste la hemorragia intermenstrual, o se produce después de ciclos previamente regulares, cuando se haya utilizado EVRA® siguiendo el régimen recomendado, se debe considerar otra causa distinta al uso de EVRA®. Se deben considerar causas no hormonales y, si fuera necesario, se deben tomar medidas de diagnóstico adecuadas para descartar enfermedad orgánica o embarazo. Esto puede incluir legrado uterino. En algunas mujeres puede no haber hemorragia por privación durante el período de descanso sin parche transdérmico. Si se ha utilizado EVRA® siguiendo las instrucciones descritas en la sección Posología y forma de administración, es improbable que la mujer esté embarazada. Sin embargo, si no se ha usado EVRA siguiendo estas instrucciones antes de la primera falta de hemorragia por privación, o si hay dos faltas de hemorragia por privación, se debe descartar el embarazo antes de continuar utilizando EVRA®.
Algunas mujeres pueden experimentar amenorrea u oligomenorrea después de interrumpir el uso de los anticonceptivos hormonales, especialmente cuando dicha afección ya existía.
POSOLOGÍA Y FORMA DE ADMINISTRACIÓN
Posología
A fin de que la eficacia anticonceptiva sea máxima, se debe advertir a los pacientes que utilicen EVRA® siguiendo exactamente las instrucciones. Consúltese el apartado “Cómo empezar el tratamiento con EVRA®” para las instrucciones de comienzo del tratamiento.
Los parches transdérmicos deben llevarse sólo de uno en uno.
Cuando se retira un parche transdérmico, se debe sustituir inmediatamente por otro nuevo el mismo día de la semana (Día de Cambio) el Día 8 y Día 15 del ciclo. Los cambios de parche transdérmico se pueden hacer a cualquier hora del Día de Cambio programado. El Día 22 de la cuarta semana comienza la semana de descanso sin parche transdérmico.
El nuevo ciclo anticonceptivo comienza al día siguiente de la semana sin parche transdérmico; el siguiente parche transdérmico EVRA® debe ponerse incluso si no ha habido sangrado por privación o si se continúa con dicho sangrado.
En ningún caso puede haber más de 7 días de descanso sin parche transdérmico entre ciclos de dosificación. Si pasan más de 7 días sin parche transdérmico, la usuaria podría quedar sin protección frente al embarazo. En este caso, se debe usar al mismo tiempo un anticonceptivo no hormonal durante 7 días. El riesgo de ovulación aumenta cada día que pase del período de descanso recomendado. Si ha mantenido relaciones sexuales durante este período prolongado sin parche, debe tener en cuenta la posibilidad de embarazo.
Poblaciones especiales
Peso corporal igual o mayor de 90 kg
La eficacia anticonceptiva puede verse disminuida en mujeres con un peso igual o mayor de 90 kg.
Insuficiencia renal
No se ha estudiado EVRA® en mujeres con insuficiencia renal. A pesar de que en principio no es necesario ajustar la dosis, EVRA® se debe utilizar bajo supervisión en esta población de pacientes dado que la bibliografía sugiere que la fracción libre de etinilestradiol es mayor.
Insuficiencia hepática
No se ha estudiado EVRA® en mujeres con insuficiencia hepática. EVRA® está contraindicado en mujeres con insuficiencia hepática (ver sección Contraindicaciones).
Mujeres postmenopáusicas
EVRA® no está indicado en mujeres postmenopáusicas y no es adecuado como terapia hormonal sustitutiva.
Población pediátrica
La seguridad y la eficacia no han sido establecidas en adolescentes menores de 18 años. No hay un uso relevante de EVRA® en niñas o adolescentes premenárquicas.
Forma de administración
EVRA® debe aplicarse en la piel sana e intacta, sin vello, seca y limpia del glúteo, abdomen, parte exterior del brazo o parte superior del torso, en un lugar donde no roce con la ropa.
EVRA® no debe ponerse en las mamas ni sobre piel que esté enrojecida, irritada o cortada. Cada parche transdérmico consecutivo debe ponerse en un sitio diferente de la piel a fin de evitar una posible irritación, aunque puede ponerse en la misma zona anatómica.
Hay que presionar bien sobre el parche transdérmico hasta que los bordes estén bien pegados. Para que no haya interferencias con las propiedades adhesivas del parche transdérmico, no debe aplicarse maquillaje, cremas, lociones, polvos u otros productos tópicos en la zona de la piel donde esté el parche transdérmico o donde se vaya a poner en breve.
Se recomienda que las usuarias comprueben visualmente el parche transdérmico todos los días para garantizar que sigue bien pegado.
El parche transdérmico de EVRA® no se debe cortar, dañar o modificar de ninguna manera ya que la eficacia anticonceptiva se puede ver afectada.
Los parches transdérmicos usados se deben desechar con cuidado de acuerdo con las instrucciones de la sección Precauciones especiales de eliminación y otras manipulaciones.
Cómo empezar el tratamiento con EVRA
Si no se utilizaban anticonceptivos hormonales en el ciclo anterior
La anticoncepción con EVRA® comienza el primer día de la menstruación. Se coloca un solo parche transdérmico y se lleva durante una semana entera (7 días). El día que se pone el primer parche transdérmico (Día 1/Día de Inicio) determina los Días de Cambio siguientes. El
Día de Cambio del parche transdérmico será este día de cada semana (Días del ciclo 8, 15, 22 y Día 1 del siguiente ciclo). El Día 22 de la cuarta semana comienza la semana de descanso sin parche transdérmico.
Si la terapia del Ciclo 1 comienza después del primer día del ciclo menstrual, deberá usar almismo tiempo un anticonceptivo no hormonal sólo durante los primeros 7 días del primer ciclo de tratamiento.
Si antes se estaba tomando un anticonceptivo oral combinado
El tratamiento con EVRA® debe comenzar el primer día de la hemorragia por privación. En caso de que no haya hemorragia por privación en un plazo de 5 días desde la toma del último comprimido anticonceptivo activo (que contiene hormonas), se debe descartar el embarazo antes de iniciar el tratamiento con EVRA®. Si la terapia comienza después del primer día de la hemorragia por privación, debe usar al mismo tiempo otro método anticonceptivo no hormonal durante 7 días.
Si pasan más de 7 días desde la última toma del comprimido anticonceptivo oral activo, la mujer puede haber ovulado y se le deberá advertir que consulte con un médico antes de iniciar el tratamiento con EVRA® . Si ha mantenido relaciones sexuales durante este período prolongado sin comprimido anticonceptivo, debe tener en cuenta la posibilidad de embarazo.
Si antes se estaba tomando un anticonceptivo basado sólo en progestágenos
Si tomaba el comprimido anticonceptivo basado sólo en progestágenos, la mujer puede cambiar de tratamiento cualquier día (si se trataba de un implante, el día de su extracción, y se trataba de un inyectable, el día que le toque la siguiente inyección), pero debe utilizar simultáneamente un método anticonceptivo de barrera durante los primeros 7 días.
Tras un aborto provocado o espontáneo
Puede utilizar EVRA® inmediatamente después de sufrir un aborto provocado o espontáneo dentro de las primeras 20 semanas de gestación. No es necesario el uso de anticonceptivos adicionales si se comienza con EVRA® de forma inmediata. Tenga en cuenta que la ovulación podrá tener lugar en un plazo de 10 días después de un aborto provocado o espontáneo.
En caso de sufrir un aborto provocado o espontáneo a las 20 semanas de gestación o después, puede comenzar con EVRA® el Día 21 después del aborto o el primer día del siguiente período menstrual espontáneo, lo que primero suceda. Se desconoce la incidencia de la ovulación en el día 21 tras un aborto (a las 20 semanas de gestación).
Después del parto
Las mujeres que decidan no dar el pecho deben empezar el tratamiento anticonceptivo con EVRA® por lo menos 4 semanas después de dar a luz. Si se comienza más tarde, se debe recomendar a la mujer que utilice simultáneamente un método de barrera durante los primeros 7 días. Sin embargo, si ha mantenido relaciones sexuales, deberá excluirse el embarazo antes de comenzar la terapia con EVRA® o la mujer tendrá que esperar a que tenga su primera menstruación.
Para mujeres en período de lactancia, ver sección Fertilidad, embarazo y lactancia.
Qué hacer si el parche transdérmico se despega total o parcialmente
Si el parche transdérmico EVRA® se despega parcial o completamente y se queda despegado, no se liberará cantidad suficiente de principio activo.
En el caso de que EVRA® esté parcialmente despegado:
• menos de un día (hasta 24 horas): se debe volver a poner en el mismo sitio o cambiarse de inmediato por un nuevo parche transdérmico EVRA®. No es necesario tomar otras medidas anticonceptivas. El siguiente parche transdérmico EVRA® se debe poner el “Día de Cambio” habitual.
• más de un día (24 horas o más) o si desconoce cuándo se despegaron los bordes o se despegó el parche transdérmico: la usuaria puede no estar protegida frente al embarazo. Debe parar el ciclo anticonceptivo actual y comenzar inmediatamente un nuevo ciclo colocándose un parche transdérmico EVRA® nuevo. A partir de ahora habrá un nuevo “Día 1” y un nuevo “Día de Cambio”. Debe usar al mismo tiempo otro método anticonceptivo no hormonal sólo durante los primeros 7 días del nuevo ciclo.
El parche transdérmico no se debe volver a poner si ya no pega; se debe poner otro parche transdérmico nuevo de inmediato. No debe utilizar ningún tipo de adhesivo o venda para fijar el parche transdérmico EVRA®.
Si se retrasa el día de cambio del siguiente parche transdérmico EVRA®
Al comienzo de cualquier ciclo de parche transdérmico (Semana Uno/Día 1):
La usuaria puede no estar protegida frente al embarazo. Se debe colocar el primer parche transdérmico del nuevo ciclo en cuanto se acuerde. A partir de ahora habrá un nuevo “Día de Cambio” y un nuevo “Día 1”. Debe usar al mismo tiempo otro método anticonceptivo no hormonal durante los primeros 7 días del nuevo ciclo. Si ha mantenido relaciones sexuales durante este período prolongado sin parche transdérmico, debe tener en cuenta la posibilidad de embarazo.
En la mitad del ciclo (Semana Dos/Día 8 o Semana Tres/Día 15)
• durante uno o dos días (hasta 48 horas): se debe poner un nuevo parche transdérmico EVRA® de inmediato. El siguiente parche transdérmico EVRA® se debe poner el “Día de Cambio” habitual. Si durante los 7 días anteriores al primer día que se olvidó poner el parche transdérmico, éste estuvo aplicado correctamente, no es necesario tomar otras medidas anticonceptivas.
• durante más de dos días (48 horas o más): la usuaria puede no estar protegida frente al embarazo. Debe parar el ciclo anticonceptivo actual y comenzar de inmediato un nuevo ciclo de cuatro semanas colocándose inmediatamente un parche transdérmico EVRA® nuevo. A partir de ahora habrá un nuevo “Día 1” y un nuevo “Día de Cambio”. Debe usar al mismo tiempo otro método anticonceptivo no hormonal durante los primeros 7 días del nuevo ciclo.
Al final del ciclo (Semana Cuatro/Día 22):
• si no se ha quitado el parche transdérmico EVRA® al comienzo de la Semana 4 (Día 22), se lo debe quitar lo antes posible. El siguiente ciclo debe comenzar el “Día de Cambio” habitual, que es al día siguiente del Día 28. No es necesario tomar otras medidas anticonceptivas.
Modificación del Día de Cambio
A fin de posponer un ciclo menstrual, la mujer deberá aplicarse otro parche transdérmico al comienzo de la Semana 4 (Día 22), sin respetar, por lo tanto, la semana de descanso. Se podría producir hemorragia intermenstrual u oligometrorragia. Después de 6 semanas consecutivas con parche transdérmico, debe haber un período de descanso de 7 días.
Después de este descanso, se vuelve a utilizar EVRA® de la forma habitual.
Si quiere modificar el Día de Cambio, debe completar el ciclo actual, quitándose el tercer parche transdérmico EVRA® el día correcto. Durante la semana de descanso, sin parche transdérmico, puede elegir un Día de Cambio nuevo colocándose el primer parche transdérmico EVRA® del siguiente ciclo cuanto antes en ese día elegido. En ningún caso deben transcurrir más de 7 días consecutivos sin parche transdérmico. Cuanto más corto sea el período de descanso, mayor será el riesgo de que la mujer no tenga la hemorragia por privación y pueda experimentar una hemorragia intermenstrual y oligometrorragia durante el siguiente ciclo de tratamiento.
En caso de pequeña irritación cutánea
Si el uso del parche transdérmico produce una irritación incómoda, se puede aplicar otro parche transdérmico nuevo en una zona distinta hasta el siguiente Día de Cambio. Los parches transdérmicos se deben llevar sólo de uno en uno.
SOBREDOSIS
No se han notificado efectos adversos graves tras la ingesta involuntaria de dosis muy altas de anticonceptivos orales. La sobredosis puede causar náuseas y vómitos. En algunas mujeres se puede producir una hemorragia vaginal. En caso de sospecha de sobredosis, se deben retirar todos los sistemas de anticoncepción transdérmica y aplicar un tratamiento sintomático.