
EXELON PATCH
RIVASTIGMINA
Parche transdérmico
Parche transdérmico
DESCRIPCIÓN Y COMPOSICIÓN:
Forma farmacéutica: Parche transdérmico.
Cada PARCHE está constituido por una delgada matriz que consta de tres capas:
El exterior de la capa que sirve de soporte es de color beige y cada uno de los parches está etiquetado de la siguiente manera:
• En el caso de EXELON® Parche 5, con «AMCX»
• En el caso de EXELON® Parche 10, con «BHDI»
• En el caso de EXELON® Parche 15, con «CNFU»
• En el caso de EXELON® Parche 20, con «DSEN»
Principio activo:
Cada PARCHE de 5 cm2 contiene 9 mg de rivastigmina base; tasa de liberación in vivo de 4,6 mg/24 horas.
Cada PARCHE de 10 cm2 contiene 18 mg de rivastigmina base; tasa de liberación in vivo de 9,5 mg/24 horas.
Cada PARCHE de 15 cm2 contiene 27 mg de rivastigmina base; tasa de liberación in vivo de 13,3 mg/24 horas.
Cada PARCHE de 20 cm2 contiene 36 mg de rivastigmina base; tasa de liberación in vivo de 17,4 mg/24 horas.
Es posible que algunas dosis farmacéuticas no estén disponibles en todos los países.
Excipientes: Vitamina E, poli (butilmetacrilato, metil-metacrilato), copolímero de acrílico, aceite de silicona.
Las formulaciones farmacéuticas pueden variar entre los países.
INDICACIONES: Tratamiento de pacientes con demencia entre leve y moderadamente grave de tipo Alzheimer, también denominada «probable enfermedad de Alzheimer» o «enfermedad de Alzheimer».
Tratamiento de pacientes con demencia entre leve y moderadamente grave asociada con la enfermedad de Parkinson.
CONTRAINDICACIONES: El uso de EXELON® está contraindicado en pacientes con antecedentes de hipersensibilidad a la rivastigmina y a otros derivados del carbamato o a componentes de la formulación (véase Descripción y composición: Excipientes).
EMBARAZO Y LACTANCIA:
Embarazo: La rivastigmina no fue teratógena en los estudios con animales. No obstante, aún no se ha confirmado la inocuidad de EXELON®en el embarazo humano y la rivastigmina únicamente debe administrarse a las mujeres embarazadas si los efectos beneficiosos previstos exceden el riesgo que puede correr el feto.
Lactancia: Se ignora si EXELON® se excreta en la leche humana, de modo que las pacientes tratadas con EXELON® no deben amamantar a sus bebés.
REACCIONES ADVERSAS: La incidencia general de acontecimientos adversos en pacientes tratados con parches «EXELON® 10» fue menor que la tasa en pacientes que recibieron el tratamiento con cápsulas duras de EXELON®. Las náuseas y los vómitos fueron los acontecimientos adversos más frecuentes en pacientes que recibieron un tratamiento activo y tuvieron lugar en porcentajes similares entre los grupos tratados con parches «EXELON® 20» y los grupos tratados con cápsulas. Sin embargo, los porcentajes de estos dos acontecimientos fueron sustancialmente inferiores en el grupo tratado con parches «EXELON® 10».
Las reacciones adversas notificadas con mayor frecuencia son gastrointestinales, entre ellas las náuseas y los vómitos, en especial durante el reajuste posológico.
Las siguientes reacciones adversas se notificaron en pacientes con demencia de Alzheimer tratados con parches de EXELON®.
Las reacciones adversas se han ordenado por orden de frecuencia, encabezadas por las más frecuentes, de acuerdo con la siguiente convención: Muy frecuentes (> 1/10); frecuentes (> 1/100, < 1/10); Infrecuentes (> 1/1000, < 1/100); raras (> 1/10 000, < 1/1000); muy raras (< 1/10 000), incluidas las notificaciones aisladas.
|
Tabla 1. Reacciones adversas notificadas en 594 pacientes con demencia de Alzheimer tratados en un estudio clínico específico de 24 semanas, con doble enmascaramiento, comparativo con placebo y fármaco activo, con parches de EXELON® en todas sus dosis (desde «EXELON® 5» hasta «EXELON® 20») |
|
|
Trastornos del metabolismo y de la nutrición |
|
|
Frecuentes: |
Anorexia, disminución del apetito |
|
Infecciones e infestaciones |
|
|
Frecuentes: |
Infecciones del tracto urinario |
|
Trastornos psiquiátricos |
|
|
Frecuentes: |
Ansiedad, depresión, insomnio, delirio |
|
Infrecuentes: |
Agitación, síndrome confusional, alucinaciones |
|
Trastornos del sistema nervioso |
|
|
Frecuentes: |
Mareo, dolor de cabeza |
|
Infrecuentes: |
Accidente cerebrovascular, síncope, somnolencia, síntomas extrapiramidales |
|
Trastornos cardíacos |
|
|
Infrecuentes: |
Arritmia cardíaca (por ejemplo, bradicardia, extrasístole supraventricular) |
|
Trastornos gastrointestinales |
|
|
Muy frecuentes: |
Vómitos, náuseas |
|
Frecuentes: |
Diarrea, dispepsia, dolor abdominal |
|
Infrecuentes: |
Úlcera gástrica, hemorragia gastrointestinal (por ejemplo, duodenitis hemorrágica) |
|
Trastornos cutáneos y subcutáneos |
|
|
Infrecuentes: |
Rash |
|
Trastornos generales y afecciones en el sitio de administración |
|
|
Frecuentes: |
Reacciones en el sitio de aplicación, eritema en el sitio de aplicación, prurito en el sitio de aplicación, irritación, edema, fatiga, astenia, pirexia. |
|
Infrecuentes: |
Dermatitis de contacto, malestar general |
|
Exploraciones complementarias |
|
|
Frecuentes: |
Pérdida de peso |
En el ensayo clínico anteriormente mencionado, con dosis mayores a las que contiene <EXELON® Parche 10>, se observaron con mayor frecuencia mareos, insomnio, agitación, disminución del apetito, fibrilación atrial y fallo cardiaco que con <EXELON® Parche 10> o placebo, lo que sugiere una relación dosis-dependiente. Sin embargo, estos efectos no se produjeron con una mayor frecuencia con <EXELON® Parche 10> que con placebo.
Reacciones adversas procedentes de notificaciones espontáneas: Se han identificado las siguientes reacciones adversas adicionales tomando como base las notificaciones espontáneas realizadas desde la comercialización del fármaco. Dado que estas reacciones adversas son notificaciones voluntarias procedentes de poblaciones de tamaño incierto, no siempre es posible calcular con precisión su frecuencia.
De notificación infrecuente: Hipertensión arterial, hipersensibilidad en el sitio de aplicación, prurito, exantema, eritema, urticaria, ampollas, dermatitis alérgica.
De notificación muy infrecuente: Taquicardia, bloqueo auriculoventricular, fibrilación auricular, taquicardia, pancreatitis, caídas, convulsiones. Se ha observado un empeoramiento de la enfermedad de Parkinson en pacientes diagnosticados de esta dolencia y tratados con parches de EXELON®.
De frecuencia desconocida: Deshidratación, hepatitis, agresiones, agitación y síndrome de disfunción sinusal.
Reacciones adversas adicionales que se han notificado con las cápsulas o la solución oral de EXELON®:
Muy raras: Infección urinaria, vómitos intensos asociados con ruptura del esófago.
Raras: Angina de pecho, infarto de miocardio, úlceras duodenales.
Infrecuentes: Resultados anormales en las pruebas de función hepática.
Frecuentes: Temblores, confusión.
Información procedente de ensayos clínicos en pacientes con demencia de Alzheimer tratados con parches de EXELON®: Se han identificado las siguientes reacciones adversas en pacientes con demencia de Alzheimer tratados con parches de EXELON®.
|
Tabla 2. Acontecimientos adversos 2% en todos los grupos tratados con parches de EXELON®) del ensayo clínico específico de 24 semanas realizado con parches de EXELON® en pacientes con demencia de Alzheimer |
|||||
|
Grupo tratado con parches EXELON® 10 n (%) |
Grupo tratado con parches EXELON® 20 n (%) |
Grupo tratado con cápsulas 12 mg/día n (%) |
Placebo n (%) |
Grupo tratado con todos los parches de EXELON® |
|
|
Número total de pacientes estudiados |
291 |
303 |
294 |
302 |
594 |
|
Total de los pacientes con acontecimientos adversos |
147 (50,5) |
200 (66,0) |
186 (63,3) |
139 (46,0) |
347(58,4) |
|
Náuseas |
21 (7,2) |
64 (21,1) |
68 (23,1) |
15 (5,0) |
85(14,3) |
|
Vómitos |
18 (6,2) |
57 (18,8) |
50 (17,0) |
10 (3,3) |
75(12,6) |
|
Diarrea |
18 (6,2) |
31 (10,2) |
16 (5,4) |
10 (3,3) |
49(8,2) |
|
Pérdida de peso |
8 (2,7) |
23 (7,6) |
16 (5,4) |
4 (1,3) |
31(5,2) |
|
Mareo |
7 (2,4) |
21 (6,9) |
22 (7,5) |
7 (2,3) |
28(4,7) |
|
Pérdida de apetito |
2 (0,7) |
15 (5,0) |
12 (4,1) |
3 (1,0) |
17(2,9) |
|
Cefalea |
10 (3,4) |
13 (4,3) |
18 (6,1) |
5 (1,7) |
23(3,9) |
|
Anorexia |
7 (2,4) |
12 (4,0) |
14 (4,8) |
3 (1,0) |
19(3,2) |
|
Depresión |
11 (3,8) |
12 (4,0) |
13 (4,4) |
4 (1,3) |
23(3,9) |
|
insomnio |
4 (1,4) |
12 (4,0) |
6 (2,0) |
6 (2,0) |
16(2,7) |
|
Dolor abdominal |
7 (2,4) |
11 (3,6) |
4 (1,4) |
2 (0,7) |
18(3,0) |
|
Astenia |
5 (1,7) |
9 (3,0) |
17 (5,8) |
3 (1,0) |
14(2,4) |
|
Ansiedad |
9 (3,1) |
8 (2,6) |
5 (1,7) |
4 (1,3) |
17(2,9) |
|
Fatiga |
5 (1,7) |
7 (2,3) |
2 (0,7) |
4 (1,3) |
12(2,0) |
Irritación cutánea: Cuando se observó, en la irritación cutánea fue casi siempre mínima o de intensidad leve y se la calificó de grave en < 2,2% de las pacientes tratados con parches de EXELON®, frente a < 1,0% de los pacientes a los que se les aplicaron parches de placebo.
CONDUCCIÓN DE VEHÍCULOS Y MANEJO DE MÁQUINAS: La enfermedad de Alzheimer y la demencia en la enfermedad de Parkinson pueden provocar una alteración gradual de la capacidad de conducir vehículos o comprometer la facultad de manejar máquinas. La rivastigmina puede inducir mareo y somnolencia, en especial cuando se inicia el tratamiento o se aumenta la dosis. Por lo tanto, el médico terapeuta debe evaluar periódicamente si los pacientes con demencia tratados con rivastigmina está en condiciones de conducir vehículos o manejar máquinas complejas.
INCOMPATIBILIDADES: Para evitar la interferencia con propiedades adhesivas del parche, no se debe aplicar ninguna crema, loción ni polvo en la zona cutánea donde se aplicará el parche transdérmico de EXELON®.
INTERACCIONES: No se han realizado estudios de interacción específica con los parches de EXELON®.
La hidrólisis por parte de esterasas es la principal vía de transformación metabólica de la rivastigmina. Las principales isoformas del citocromo P450 apenas metabolizan el principio activo; por consiguiente, no cabe esperar que ocurran interacciones farmacocinéticas con otros sustratos farmacológicos de dichas enzimas.
En los estudios con voluntarios sanos no se han detectado interacciones farmacocinéticas entre la rivastigmina y la digoxina, la warfarina, el diazepam o la fluoxetina. El aumento del tiempo de protrombina inducido por la warfarina no se ve afectado por la administración de rivastigmina. Tras la administración simultánea de digoxina y rivastigmina no se han observado efectos adversos en la conducción cardíaca.
La administración simultánea de rivastigmina y otros medicamentos de prescripción habitual, a saber, antiácidos, antieméticos, antidiabéticos, antihipertensivos de acción central, betabloqueantes, antagonistas del calcio, fármacos inótropos, antianginosos, antiinflamatorios no esteroideos, estrógenos, analgésicos, benzodiazepínicos y antihistamínicos, no se acompañó de una alteración de la cinética de rivastigmina ni de un incremento del riesgo de aparición de efectos adversos clínicamente importantes.
En vista de sus efectos farmacodinámicos, la rivastigmina no debe administrarse simultáneamente con otros parasimpaticomiméticos y podría interferir la actividad de los fármacos anticolinérgicos.
Como inhibidor de la colinesterasa, la rivastigmina puede potenciar los efectos de los miorrelajantes de tipo succinilcolínico durante la anestesia.
Teniendo en cuenta las características de su metabolismo, las interacciones metabólicas con otros medicamentos parecen poco probables, aunque la rivastigmina puede inhibir el metabolismo de otras sustancias mediado por la butirilcolinesterasa.
ESTUDIOS CLÍNICOS:
Estudios clínicos en la demencia de alzheimer
Se comprobó la eficacia de los parches de EXELON® en los pacientes con demencia de Alzheimer en un estudio principal de 24 semanas de duración con doble enmascaramiento y en la fase de ampliación del mismo sin enmascaramiento. Los pacientes que participaron en dicho estudio obtuvieron una puntuación de entre 10 y 20 en el miniexamen cognoscitivo (MMSE). Se determinó la eficacia con instrumentos independientes que permitieron evaluar esferas específicas a intervalos periódicos durante el período terapéutico de 24 semanas. Dichos instrumentos fueron: la subescala cognitiva de la escala de evaluación de la enfermedad de Alzheimer o ADAS-Cog (medida de la capacidad intelectual basada en el funcionamiento), la escala ADCS-CGIC (ADCS-CGIC: evaluación global completa del paciente por parte del médico; incluye la opinión del cuidador) y las ADL del ADCS (ADCS-ADL: actividades cotidianas puntuadas por la persona a cargo, como el aseo personal, la alimentación, vestirse, las tareas domésticas, como el hacer las compras, la retención de la capacidad para orientarse con respecto al entorno y la participación en actividades relacionadas con el presupuesto familiar). Los resultados de los tres instrumentos de evaluación en el período de 24 semanas se resumen en la Tabla 3.
|
Tabla 3. Resultados a las 24 semanas de las tres herramientas de evaluación |
||||
|
EXELON® Parche 10 |
EXELON® Parche 20 |
EXELON® Cápsula 12 mg/día |
Placebo |
|
|
Población ITT + LOCF |
N = 251 |
N = 264 |
N = 256 |
N = 282 |
|
ADAS-Cog |
||||
|
(n = 248) |
(n = 262) |
(n = 253) |
(n = 281) |
|
|
Media inicial ± DE |
27,0 ± 10,3 |
27,4 ± 9,7 |
27,9 ± 9,4 |
28,6 ± 9,9 |
|
Media del cambio a las 24 semanas ± DE |
-0,6 ± 6,4 |
-1,6 ± 6,5 |
-0,6 ± 6,2 |
1,0 ± 6,8 |
|
Valor de p frente al placebo |
0,005*1 |
<0,001*1 |
0,003*1 |
|
|
ADCS-CGIC |
||||
|
(n = 248) |
(n=260) |
(n = 253) |
(n = 278) |
|
|
Media inicial ± DE |
3,9 ± 1,20 |
4,0 ± 1,27 |
3,9 ± 1,25 |
4,2 ± 1,26 |
|
Valor de p frente al placebo |
0,010*2 |
0,0542 |
0,009*2 |
|
|
ADCS-ADL |
||||
|
(n = 247) |
(n = 263) |
(n = 254) |
(n = 281) |
|
|
Media inicial ± DE |
50,1 ± 16,3 |
47,6 ±15,7 |
49,3 ± 15,8 |
49,2 ± 16,0 |
|
Media del cambio a las 24 semanas ± DE |
-0,1 ± 9,1 |
0,0 ± 11,6 |
-0,5 ± 9,5 |
-2,3 ± 9,4 |
|
Valor de p frente al placebo |
0,013*1 |
0,017*1 |
0,039*1 |
|
|
* Valor de p s0,05 frente al placebo. ITT: Intención de tratar, LOCF (Last Observation Carried Forward): traslación de los datos de la última observación disponible. 1 Basado en un ANCOVA, con el tratamiento y el país como factores y el valor inicial como covariable Las cifras negativas de la ADAS-Cog indican una mejoría. Las cifras positivas de las ADCS-ADL indican una mejoría. 2 Basado en el examen CMH (examen de Van Elteren) con bloques por país. Las puntuaciones de ADCS-CGIC < 4 indican una mejoría. |
||||
En la Tabla 4 se muestran los resultados del estudio de 24 semanas obtenidos en los pacientes que respondieron clínicamente al tratamiento. La mejoría clínicamente importante se definió a priori como un progreso de 4 puntos como mínimo en la escala ADAS-cog y ningún deterioro en la ADCS-CGIC ni en las ADCS-ADL.
|
Tabla 4. Resultado de pacientes con una respuesta clínica importante en el estudio de 24 semanas |
|||
|
Pacientes cuya respuesta fue clínicamente significativa (%) |
|||
|
Población ITT-LOCF |
EXELON® Parche 10 |
EXELON® en cápsula |
Placebo |
|
N=251 |
N=256 |
N=282 |
|
|
Progreso de 4 puntos como mínimo en la ADAS-Cog y ningún deterioro en la ADCS-CGIC ni en las ADCS-ADL |
17,4* |
19,0.004*0** |
10,5 |
|
Valor p versus placebo |
0.037* |
||
|
*p<0.05 versus placebo |
|||
Según la modelización compartimental, con EXELON® 10 parche transdérmico se alcanzó una exposición similar a la obtenida con una dosis oral de 12 mg/día.
Demencia asociada a la enfermedad de Parkinson: La eficacia y la inocuidad de la rivastigmina se ha comprobado con las cápsulas duras de EXELON® en pacientes con demencia asociada a la enfermedad de Parkinson, pero no se ha hecho ningún estudio con los parches de EXELON®.
Los resultados del modelo farmacocinético de un estudio que se llevó a cabo con parches de EXELON® en pacientes con enfermedad de Alzheimer indicaron que la exposición diaria total (AUC) del parche de EXELON® 10 es aproximadamente equivalente a la que se logra con la dosis de 6 mg administrada en cápsulas dos veces al día. Esta última fue la mayor dosis utilizada en los pacientes con demencia debida a la enfermedad de Parkinson. La dosis media diaria de mantenimiento en cápsulas que resultó más eficaz que el placebo en las escalas ADAS-Cog y ADCS-CGIC fue de 8,7 mg de rivastigmina. Estos indicios avalan el uso de los parches de EXELON® en pacientes con demencia asociada a la enfermedad de Parkinson.
DATOS SOBRE TOXICIDAD PRECLÍNICA:
Toxicidad tras dosis única: Los valores estimados de dosis letal intermedia (LD50) en ratones fueron de 5,6 mg de base/kg en los machos y de 13,8 mg de base/kg en las hembras. Los valores estimados de dosis letal intermedia (LD50) en las ratas fueron de 8,1 mg de base/kg en los machos y de 13,8 mg de base/kg en las hembras.
Toxicidad tras dosis repetidas: Los estudios de toxicidad tras dosis repetidas por vía oral o tópica efectuados en ratones, ratas, conejos, perros y cerdos Minipig revelaron solamente los efectos asociados con una actividad farmacológica exagerada. No se observó toxicidad en órganos afectados. En los estudios con animales, la administración oral y tópica fue limitada debido a la sensibilidad de los modelos animales utilizados.
Mutagenia: La rivastigmina careció de poder mutágeno en los ensayos de mutación génica, daños primarios del ADN y aberraciones cromosómicas in vivo. En los ensayos de aberraciones cromosómicas in vitro se observó un ligero aumento del número de células portadoras de aberraciones cromosómicas cuando se utilizaron concentraciones muy altas. Sin embargo, como no se observaron indicios de actividad clastógena en la prueba más importante de daño cromosómico in vivo (el ensayo de micronúcleos), es bastante probable que los resultados observados in vitro fuesen falsos positivos.
Carcinogenia: No se observaron indicios de poder cancerígeno en estudios con administración oral y tópica en ratones y en un estudio con administración oral en ratas en las dosis máximas toleradas. La exposición a la rivastigmina y a sus metabolitos fue aproximadamente igual a la exposición humana que se logra con las dosis más altas de rivastigmina administradas en forma de cápsulas y en parches transdérmicos.
Toxicidad en la reproducción: Los estudios por vía oral en ratas y conejas grávidas con dosis de hasta 2,3 mg de base/kg/día no exhibieron indicios de que la rivastigmina tenga potencial teratógeno. Tampoco hubo indicios de que la rivastigmina ejerza efectos tóxicos en la fertilidad, la función reproductora o el crecimiento y el desarrollo, tanto en el útero como en el período posnatal, en dosis de hasta 1,1 mg de base/kg/día. No se han llevado a cabo estudios dérmicos específicos en hembras grávidas de animales.
Toxicidad dérmica: Los parches de rivastigmina no fueron fototóxicos. En otros estudios de toxicidad dérmica, se apreció un leve efecto irritante en la piel de los animales de laboratorio, también en los testigos. Ello podría indicar que los parches de EXELON® tienen la capacidad de inducir un eritema leve en los pacientes. Cuando se administró enojos de conejos en estudios primarios de irritación ocular, la rivastigmina causó enrojecimiento e inflamación de la conjuntiva, opacidad correal y miosis que persistió durante 7 días. En consecuencia, tanto el paciente como su cuidador deben evitar el contacto con los ojos tras manipular el parche.
ADVERTENCIAS Y PRECAUCIONES: La incidencia y la intensidad de los acontecimientos adversos normalmente aumentan al incrementar la dosis, especialmente cuando se modifica ésta. Si el tratamiento se interrumpe durante varios días, deberá reanudarse con «EXELON® Parche 5».
Cuando se inicia el tratamiento o se aumenta la dosis pueden aparecer trastornos gastrointestinales, como náuseas, vómitos y diarrea. Dichos trastornos pueden responder a la reducción de la dosis. En otros casos se ha interrumpido el uso de EXELON®. Los pacientes que muestran signos o síntomas de deshidratación a causa de vómitos o diarrea prolongados pueden tratarse con líquidos por vía intravenosa y reducción o interrupción de la dosis si se diagnostican con prontitud. La deshidratación puede asociarse a desenlaces graves (véase Reacciones adversas).
Los pacientes con enfermedad de Alzheimer pueden perder peso durante el tratamiento con inhibidores de la colinesterasa, entre ellos la rivastigmina. Durante el tratamiento con los parches de EXELON® debe controlarse el peso de los pacientes.
Como en el caso de otras sustancias colinérgicas, se ha de tener cuidado a la hora de prescribir los parches de EXELON®:
• Pacientes afectos de un síndrome de disfunción sinusal o de trastornos de la conducción cardíaca (bloqueo sinoauricular o auriculoventricular) (véase Reacciones adversas).
• Pacientes que padecen úlceras duodenales o gástricas activas o que son susceptibles de padecerlas debido a un posible aumento de las secreciones de ácido gástrico.
• Pacientes susceptibles de padecer convulsiones u obstrucción urinaria debido a que los parasimpaticomiméticos pueden inducir o agravar dichos trastornos.
• Pacientes con antecedentes de asma o enfermedad pulmonar obstructiva.
Al igual que otros parasimpaticomiméticos, la rivastigmina puede exacerbar los síntomas extrapiramidales. En los pacientes con demencia asociada a la enfermedad de Parkinson que recibieron tratamiento con cápsulas duras de EXELON®, se ha observado un recrudecimiento de los síntomas parkinsonianos, especialmente de los temblores. Tales acontecimientos adversos también pueden sobrevenir con los parches de EXELON®, sobre todo con los parches de «EXELON® 15» y «EXELON® 20», que proporcionan una mayor exposición (AUC) que las cápsulas de 6 mg de EXELON® administradas dos veces al día.
Debe evitarse el contacto con los ojos tras manipular EXELON® Parches transdérmicos. Poblaciones especiales
• Los pacientes con un peso corporal inferior a 50 kg pueden experimentar más acontecimientos adversos y es más probable que interrumpan el tratamiento a causa de éstos. Es preciso proceder con suma cautela al reajuste de la dosis en estos pacientes por encima de la dosis de mantenimiento recomendada de un parche de «EXELON® 10».
• Disfunción hepática: los pacientes con disfunción hepática clínicamente significativa pueden presentar más acontecimientos adversos. Es preciso proceder con suma cautela al reajuste de la dosis en estos pacientes por encima de la dosis de mantenimiento recomendada de un parche de «EXELON® 10» (véase Farmacocinética).
POSOLOGÍA Y ADMINISTRACIÓN:
Posología:
|
Parches |
Dosis de rivastigmina base |
Tasa de liberación de rivastigminabase en 24 horas in vivo |
|
EXELON® parche 5 |
9 mg |
4,6 mg |
|
EXELON® parche 10 |
18 mg |
9,5 mg |
|
EXELON® parche 15 |
27 mg |
13,3 mg |
|
EXELON® parche 20 |
36 mg |
17,4 mg |
Dosis inicial: El tratamiento se inicia con «EXELON® Parche 5» una vez al día.
Al cabo de un mínimo de cuatro semanas de tratamiento y si la dosis se tolera bien, se puede administrar «EXELON® Parche 10», que contiene la dosis eficaz recomendada.
Dosis de mantenimiento: «EXELON® Parche 10» contiene la dosis de mantenimiento diaria recomendada y puede administrarse mientras proporcione un beneficio terapéutico al paciente.
• La reacción individual a la rivastigmina puede variar y algunos pacientes probablemente obtengan un mayor beneficio con dosis más altas. La administración subsiguiente de «EXELON® Parche 15» y luego de «EXELON® Parche 20» siempre dependerá de la adecuada tolerabilidad del parche anterior y se hará únicamente tras un período terapéutico mínimo de cuatro semanas con el parche precedente.
• Si se observan reacciones adversas gastrointestinales o una agravación de los síntomas extrapiramidales existentes (por ejemplo: temblores) se debe interrumpir momentáneamente el tratamiento hasta que dichos efectos hayan desaparecido. El tratamiento con un parche dado se puede reanudar en la misma dosis si se ha interrumpido más de unos días. En caso contrario, se debe reinstaurar el tratamiento con «EXELON® Parche 5».
• Si las reacciones adversas persisten, se debe reducir la dosis diaria a la dosis anterior que se toleraba bien.
Reemplazo de las cápsulas o de la solución oral: Las cápsulas o la solución oral de EXELON® pueden sustituirse por los parches de EXELON® tal como se indica a continuación:
• El paciente que recibe una dosis de menos de 3 mg al día de rivastigmina debe recibir «EXELON® Parche 5».
• El paciente que recibe una dosis de menos de 6 mg al día de rivastigmina oral debe recibir «EXELON® Parche 5».
• El paciente que recibe una dosis de menos de 9 mg al día de rivastigmina debe recibir «EXELON® Parche 10».
• El paciente que recibe una dosis de menos de 12 mg al día de rivastigmina oral debe recibir directamente «EXELON® Parche 10».
Tras el cambio a «EXELON® Parche 5» y asegurándose de que se toleran bien durante un mínimo de cuatro semanas de tratamiento, la dosis correspondiente a «EXELON® Parche 5» se debe aumentar a «EXELON® Parche 10», que es la dosis terapéutica recomendada.
Se recomienda aplicar el primer parche al día siguiente de la última dosis oral.
Forma de administración: Los parches transdérmicos de rivastigmina se deben aplicar una vez al día sobre la piel sana, lampiña, seca y limpia, en la parte superior o inferior de la espalda, en el brazo o en el pecho, sin que roce la ropa ajustada. El parche no debe aplicarse sobre la piel enrojecida, irritada o herida. Se recomienda cambiar el sitio de aplicación a diario para evitar problemas de irritación, aunque el parche siguiente puede aplicarse sobre el mismo sitio.
No se recomienda aplicar el parche transdérmico ni en el muslo ni en el abdomen, debido a que se ha observado una disminución de la biodisponibilidad de rivastigmina cuando el parche transdérmico se utiliza en estas zonas del cuerpo.
Se debe presionar firmemente el parche hasta que sus bordes se hayan adherido bien. Los parches se pueden utilizar en cualquier situación de la vida diaria, incluso durante el baño y en clima cálido.
Al cabo de 24 horas hay que sustituir el parche por uno nuevo. Se colocará únicamente un solo parche cada vez (véase Sobredosis). No se debe cortar el parche en dos trozos. Es necesario instruir a los pacientes y a sus cuidadores al respecto.
Población especial: (Véase Advertencias y precauciones).
• Disfunción renal: No es necesario ajustar la dosis en los pacientes con disfunción renal (véase Farmacocinética).
• Pacientes pediátricos:
— Niños y adolescentes (menores de 18 años de edad): No se recomienda el uso pediátrico de la rivastigmina.
INSTRUCCIONES DE USO Y MANIPULACIÓN:
Importante: Se colocará únicamente un solo parche cada vez. Usted debe quitarse el parche de EXELON® del día anterior antes de aplicarse uno nuevo. No corte el parche en trozos.
Dónde aplicar un parche de EXELON®:
• Antes de aplicar el parche de EXELON®, asegúrese que su piel:
— Esté limpia y seca y no tenga vello.
— No contenga polvo, aceite, humectante o loción (que podría impedir que el parche se adhiera a su piel correctamente).
— No esté herida, no tenga sarpullido ni tenga irritaciones.
• Por favor, retire delicadamente cualquier parche de EXELON® que lleve puesto antes de aplicarse uno nuevo. El hecho de llevar varios parches en el cuerpo hará que usted se exponga a una cantidad excesiva y potencialmente peligrosa de medicamento.
• Aplique únicamente un parche al día sólo en uno de los lugares siguientes (que se muestran en las imágenes aquí abajo):
— La parte superior del brazo, izquierdo o derecho, o
— La parte superior del pecho, a la izquierda o a la derecha, o
— La parte superior de la espalda, a la izquierda o a la derecha, o
— La parte inferior de la espalda, a la izquierda o a la derecha.
Evite aquellos lugares que estén en estrecho contacto con la prenda de vestir, pues el parche puede despegarse.
Cuando cambie de parche, aplique el nuevo parche en otra zona de la piel (por ejemplo, del lado derecho del cuerpo un día, y del lado izquierdo al día siguiente). No aplique un parche nuevo en el mismo lugar antes de haber dejado transcurrir una semana como mínimo.
Cómo aplicar un parche de EXELON®:
El parche es un producto delgado, opaco y de plástico que se adhiere a la piel. Cada parche se acondiciona en un sobre sellado que lo protege hasta que usted está listo para ponérselo. Abra el sobre y extraiga el parche justo antes de su aplicación solamente.
|
Cada parche se acondiciona en su propio sobre protector sellado. |
|
|
No abra el sobre hasta que vaya a aplicarse el parche. |
|
|
Desgarre o corte el sobre por la hendidura y saque el parche. |
|
|
Una membrana de protección recubre la parte adhesiva del parche. |
|
|
Desprenda la mitad de la membrana y no toque la parte adhesiva del parche con los dedos. |
|
|
Apoye el lado adherente del parche contra la parte superior o inferior de la espalda, la parte superior del brazo o el pecho y posteriormente desprenda la otra mitad de la membrana de protección. |
|
|
Luego, presione firmemente el parche con la mano hasta que los bordes se adhieran bien. |
|
|
Si le parece útil, puede escribir sobre el parche de EXELON® (el día de la semana, por ejemplo) con un bolígrafo de punta fina. |
|
El parche de EXELON® debe llevarse siempre puesto hasta el momento de su reemplazo por uno nuevo. Puede usted probar a ponerse el parche nuevo en distintas zonas hasta encontrar las que le resulten más cómodas y donde el parche no roce la ropa.
Cómo quitarse un parche de EXELON®: Tire suavemente del borde del parche hasta desprender el parche por completo. Cómo desechar un parche de EXELON®.
Una vez que ha despegado el parche, dóblelo por la mitad con los flancos adherentes hacia adentro y presiónelos. Coloque el parche utilizado en su sobre original y elimínelo con cuidado fuera del alcance y de la vista de los niños. Lávese las manos con jabón y agua después de desechar el parche.
¿Puede usted mantener el parche en su piel cuando se baña, va a nadar o a tomar el sol?
• El baño, la natación o la ducha no deberían dañar el parche. Si usted va a nadar, puede llevarlo adherido bajo el traje de baño. Asegúrese de que el parche no se afloje cuando realiza dichas actividades.
• No exponga el parche a ninguna fuente de calor externo (luz solar intensa, saunas, solarios) durante largos períodos.
¿Qué hacer si el parche se despega?
Si el parche se despega, póngase uno nuevo hasta que finalice el día y luego reemplácelo al día siguiente a la hora habitual.
Fabricante: Véase el envase exterior.
Información publicada en: Noviembre de 2010
NOVARTIS PHARMA AG, Basilea (Suiza)
®= Marca registrada
SOBREDOSIS:
Síntomas: La mayoría de los casos de sobredosis accidental no se han asociado con ningún signo clínico ni con síntomas y casi todos los pacientes concernidos continuaron su tratamiento con rivastigmina. Los síntomas, cuando los hubo, podían ser náuseas, vómitos, diarrea, hipertensión arterial y alucinaciones. Debido al conocido efecto vagotónico de los inhibidores de la colinesterasa sobre la frecuencia cardíaca, también puede sobrevenir bradicardia o síncope.
La ingestión de 46 mg ocurrió una vez; tras un tratamiento conservador, el paciente se recuperó por completo en el espacio de 24 horas.
Se han registrado casos de sobredosis con los parches de EXELON® como resultado de errores de uso o de medicación (aplicación de varios parches al mismo tiempo) tras la comercialización del producto. Los síntomas comunicados en dichos casos suelen ser semejantes a los que se observan cuando se ingiere una sobredosis de EXELON® en formulación oral.
Tratamiento: Dado que la rivastigmina posee una semivida plasmática de alrededor de 3,4 horas y una duración de inhibición de la acetilcolinesterasa de en torno a las 9 horas, se recomienda que en casos de sobredosis asintomática se quiten inmediatamente los parches de EXELON® y no se apliquen de nuevo durante las siguientes 24 horas. Si la sobredosis se acompaña de náuseas y vómitos intensos, se debe considerar la posibilidad de administrar antieméticos. Se administrará tratamiento sintomático si ocurren otros acontecimientos adversos, según proceda.
En caso de sobredosis masiva se puede usar atropina. Se recomienda una dosis inicial de 0,03 mg/kg de sulfato de atropina por vía intravenosa, que luego se puede modificar en función de la respuesta clínica. No se recomienda el uso de escopolamina como antídoto.
FARMACOLOGÍA CLÍNICA:
Modo de acción: Farmacodinamia
Los cambios patológicos asociados a la demencia, como la enfermedad de Alzheimer, afectan las vías neuronales colinérgicas que se extienden desde el prosencéfalo hasta la corteza cerebral y el hipocampo. Estas vías guardan relación con la atención, el aprendizaje y la memoria, así como con otros procesos cognitivos. La rivastigmina, un derivado cerebroselectivo del carbamato que inhibe las enzimas acetilcolinesterasa y butirilcolinesterasa, parece facilitar la neurotransmisión colinérgica mediante la ralentización de la degradación de la acetilcolina liberada por las neuronas colinérgicas funcionalmente activas. Los estudios en animales indican que la rivastigmina aumenta de forma selectiva la disponibilidad de acetilcolina en la corteza y el hipocampo. Por consiguiente, EXELON® puede mejorar los déficits cognitivos que se asocian por vía colinérgica con la enfermedad de Alzheimer y la enfermedad de Parkinson. Además, existen indicios de que la inhibición de la colinesterasa podría ralentizar la formación de los fragmentos amiloidógenos de la proteína precursora del amiloide 3 y, por ende, de las placas amiloides, que son una de las principales características patológicas de la enfermedad de Alzheimer.
La rivastigmina interactúa con sus enzimas diana y forma un complejo unido covalentemente que las inactiva de forma pasajera. En los varones jóvenes sanos, una dosis oral de 3,0 mg disminuye la actividad de la acetilcolinesterasa en el líquido cefalorraquídeo en aproximadamente un 40% durante la hora y media que sigue a la administración. La actividad de la enzima recupera su nivel inicial cerca de 9 horas después de que se alcanza el efecto inhibitorio máximo. En los voluntarios jóvenes sanos, la actividad butirilcolinesterásica en el líquido cefalorraquídeo se inhibía transitoriamente y al cabo de unas 3,6 horas ya no se diferenciaba de la inicial. En los pacientes con enfermedad de Alzheimer, la inhibición de la acetilcolinesterasa por parte de la rivastigmina en el líquido cefalorraquídeo resultó proporcional a la dosis hasta los 6 mg dos veces al día, que fue la dosis más alta estudiada. La inhibición de la actividad butirilcolinesterásica por parte de la rivastigmina en el líquido cefalorraquídeo de los pacientes con enfermedad de Alzheimer era equiparable a la de la acetilcolinesterasa, observándose un cambio de más del 60% con respecto al inicio tras la administración de 6 mg dos veces al día. El efecto de la rivastigmina sobre la actividad de la acetilcolinesterasa y la butirilcolinesterasa en el líquido cefalorraquídeo se mantuvo durante más de 12 meses de administración, que fue el mayor tiempo estudiado. Se encontraron correlaciones estadísticamente significativas entre el grado de inhibición de la acetilcolinesterasa y la butirilcolinesterasa por parte de la rivastigmina en el líquido cefalorraquídeo y los cambios de una variable compuesta de actividad cognitiva en los pacientes con enfermedad de Alzheimer; sin embargo, únicamente la inhibición de la butirilcolinesterasa en el líquido cefalorraquídeo se correlacionaba de manera significativa y sistemática con mejoras en las pruebas secundarias de rapidez, atención y memoria.
Farmacocinética:
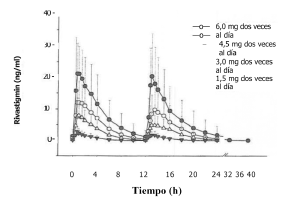
• Absorción: La rivastigmina de los parches de EXELON® se absorbe lentamente. Después de administrar la primera dosis, las concentraciones del principio activo en el plasma se detectan con un retraso de entre media hora y una hora. Luego, las concentraciones plasmáticas aumentan paulatinamente hasta alcanzar su valor máximo (Cmáx) normalmente después de 8 horas, pero con frecuencia después de entre 10 horas y 16 horas. A partir de ese momento, las concentraciones plasmáticas descienden suavemente a lo largo del período de aplicación de 24 horas. Con la administración repetida (en el estado estacionario), justo después de reemplazar el parche anterior por uno nuevo, las concentraciones plasmáticas descienden de forma lenta durante unos 40 minutos en promedio, hasta que la velocidad de absorción del principio activo liberado por el nuevo parche supera a la de eliminación, momento en que dichas concentraciones aumentan nuevamente hasta alcanzar un nuevo máximo en tomo a las 8 horas. En el estado estacionario, las concentraciones mínimas son aproximadamente la mitad (el 50%) de las cifras máximas, contrariamente a lo que sucede en la administración oral, en que las concentraciones decaen hasta ser prácticamente indetectables en el intervalo entre dos tomas (véanse las Figuras 1 y 2). Se observa el mismo curso de concentraciones plasmáticas con todos los parches (tamaños) investigados de EXELON® (parches de 5 a 20). La exposición a la rivastigmina (Cm y AUC), si bien es menos pronunciada que con la formulación oral, aumenta de forma más que proporcional a la dosis conforme se utilizan parches de dosis más altas. Con la aplicación sucesiva de parches de mayor tamaño (de «EXELON® 5» a «EXELON® 20»), el aumento relativo del AUC de rivastigmina (con respecto a la dosis inferior del parche «EXELON® 5») resultaba unas 2,6, 4,9 y 7,8 veces mayor con los parches de 10, 15 y 20, respectivamente. El índice de fluctuación (IF), que es una medida de la diferencia relativa entre las concentraciones máximas y las concentraciones mínimas ([Cmu-Cmid/Cavg), variaba entre 0,57 y 0,77 con un parche, de modo que la fluctuación entre las concentraciones máxima y mínima es mucho menor que la que se observa con la formulación oral (FI = de 3,96 a 6,24). A juzgar por el modelo de compartimentos, el parche de EXELON® 20 suministra una exposición (AUC24h) al paciente típico equivalente a la de una dosis oral de 9 a 10 mg dos veces al día (es decir, 18 a 20 mg/día), mientras que el parche de 10 proporciona una exposición equivalente a la de una dosis oral de alrededor de 6 mg dos veces al día (es decir, 12 mg/día).
Figura 1. Concentraciones plasmáticas de rivastigmina después de la aplicación dérmica del parche durante 24 horas
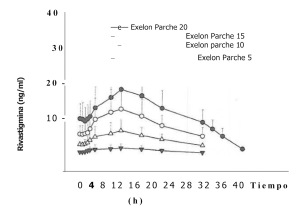
Figura 2. Concentraciones plasmáticas de rivastigmina después de la administración de cápsulas dos veces al día por vía oral
En un estudio de administración de dosis únicas en que el parche se comparó directamente con la cápsula, la variabilidad interindividual de las magnitudes farmacocinéticas de rivastigmina (normalizada en: dosis/kg de peso corporal) fue del 43% (Cmáx) y del 49% (AUC0-24 h) con el parche, frente a 74 y 103%, respectivamente, con la cápsula oral. En un estudio de administración repetida en el estado estacionario en pacientes con demencia de Alzheimer se observó asimismo una menor variabilidad interindividual de las magnitudes farmacocinéticas de rivastigmina con el parche que con la cápsula oral. La variabilidad interindividual fue como máximo del 45% (Cmáx) y el 43% (AUC0-24h) con el parche, y del 71 y 73%, respectivamente, con la forma oral.
En los pacientes con demencia de Alzheimer, la exposición farmacológica (a la rivastigmina y al metabolito NAP226-90) en el estado estacionario se correlaciona con el peso corporal. Tomando como referencia un paciente de 65 kg de peso, las concentraciones de rivastigmina en el estado estacionario de un paciente de 35 kg serán aproximadamente del doble y las de un paciente de 100 kg aproximadamente iguales a la mitad. El efecto del peso corporal sobre la exposición farmacológica exige prestar una atención especial a la hora de aumentar la dosis en pacientes de peso reducido (véase Posología y administración).
La rivastigmina se libera adecuadamente del parche transdérmico en el plazo de 24 horas de aplicación dérmica; se libera del sistema aproximadamente el 50% de la carga de fármaco.
La exposición (AUCA) a la rivastigmina (y al metabolito NAP266-90) es máxima cuando se aplica el parche en la parte superior de la espalda, el pecho o el brazo. Llegado el caso de que no fuera posible aplicar el parche en alguno de esos tres sitios, todavía se puede aplicar sobre el abdomen o el muslo, aunque el médico debe tener presente que la exposición plasmática a la rivastigmina asociada con dichos sitios es entre 20 y 30% menor.
No se apreció ninguna acumulación importante de rivastigmina o del metabolito NAP226-90 en el plasma de los pacientes con enfermedad de Alzheimer, salvo que las concentraciones plasmáticas del segundo día eran mayores que las del primero con los parches.
• Distribución: La rivastigmina se une débilmente a las proteínas plasmáticas (aproximadamente el 40%). Atraviesa prontamente la barrera hematoencefálica y tiene un volumen aparente de distribución de 1,8-2,7 1/kg.
• Metabolismo: La rivastigmina se metaboliza de forma rápida y extensa con una semivida de eliminación aparente en el plasma aproximadamente igual a 3,4 horas tras la retirada de un parche. La eliminación se ve constreñida por la velocidad de absorción (cinéticaflip-flop), lo cual explica la mayor semivida que se logra con la aplicación del parche (ty, de 3,4 h) que con la administración oral o intravenosa (ty, de 1,4 h a 1,7 h). El fármaco se transforma principalmente en el metabolito descarbamilado mediante una reacción de hidrólisis catalizada por la colinesterasa. Dicho metabolito produce una inhibición mínima de la acetilcolinesterasa in vitro (< 10%). Los estudios realizados in vitro y en animales indican que las principales isoformas del citocromo P450 desempeñan un papel mínimo en el metabolismo de la rivastigmina. La depuración (clearance) total plasmática de rivastigmina fue de unos 130 litros/h tras una dosis intravenosa de 0,2 mg y de 70 litros/h tras una dosis intravenosa de 2,7 mg, lo cual es coherente con una farmacocinética de rivastigmina no lineal y sobreproporcional debido a la saturación de su eliminación.
La razón de AUC, entre el metabolito y el compuesto original fue de 0,7 con el parche y de 3,5 con la administración oral, lo cual revela que la transformación metabólica es mucho menor con el tratamiento dérmico. Se forma una cantidad menor de NAP226-90 tras la aplicación de un parche, presuntamente debida a la falta de metabolismo presistémico (primer paso por el hígado).
• Eliminación: Se detectan cantidades ínfimas de rivastigmina inalterada en la orina; la excreción renal de metabolitos es la vía de eliminación principal. Tras la administración de "C-rivastigmina, la eliminación renal durante 24 horas es rápida y prácticamente completa (> 90%). Menos del 1% de la dosis administrada se excreta en las heces.
Pacientes ancianos: La edad no afectó la exposición a la rivastigmina en los pacientes con enfermedad de Alzheimer tratados con parches de EXELON®.
Pacientes con disfunción hepática: No se realizó ningún estudio con parches de EXELON® en individuos aquejados de disfunción hepática. Tras la administración oral, la Cmá y el AUC de rivastigmina fueron un 60% superior y más de dos veces mayores, respectivamente, en los individuos con disfunción hepática entre leve y moderada que en los individuos sanos.
Pacientes con disfunción renal: No se realizó ningún estudio con parches de EXELON® en individuos aquejados de disfunción renal. Tras la administración oral, la Cmá, y el AUC de rivastigmina fueron más de dos veces mayores, respectivamente, en los pacientes con alzheimer y disfunción renal moderada que en los individuos sanos; no obstante, no se apreciaron cambios en la Cmffi, ni en el AUC de rivastigmina en los pacientes con alzheimer y disfunción renal grave.
CONSERVACIÓN: Véase el envase exterior.
Los parches de EXELON® no deberán utilizarse a partir de la fecha de caducidad («EXP») indicada en el envase.
Los parches de EXELON® deben conservarse fuera del alcance y la vista de los niños.