
LUCENTIS
RANIBIZUMAB
Solución inyectable
Caja, 1 Vial(es), Solución inyectable, 0,23 Mililitros
DESCRIPCIÓN Y COMPOSICIÓN:
Forma farmacéutica: Solución inyectable.
Solución acuosa, límpida, incolora o algo amarillenta, estéril y sin conservantes.
Sustancia farmacéutica: Un mL contiene 10 mg de ranibizumab.
Cada VIAL [frasco ampolla] contiene 2,3 mg de ranibizumab en 0,23 ml de solución.
El ranibizumab es un fragmento de anticuerpo monoclonal humanizado producido en células de Escherichia coli mediante tecnología de ADN recombinante.
Principio activo: Ranibizumab.
Excipientes: α,α-trehalosa dihidrato, clorhidrato de L-histidina monohidrato; L-histidina; polisorbato 20; agua para preparaciones inyectables.
INDICACIONES:
LUCENTIS® está indicado para el tratamiento de:
• La degeneración macular asociada a la edad (DMAE) de tipo neovascular («húmeda»);
• La disfunción visual debida a edema macular diabético (EMD);
• La disfunción visual debida a edema macular secundario a oclusión de vena retiniana (OVR) (oclusión de rama venosa retiniana –ORVR– u oclusión de la vena central de la retina –OVCR–);
• La disfunción visual debida a neovascularización coroidea (NVC) secundaria a miopía patológica (MP).
PROPIEDADES FARMACOLÓGICAS:
Propiedades farmacodinámicas: Grupo farmacoterapéutico: Oftalmológicos, agentes antineovascularización. Código ATC: S01LA04.
El ranibizumab es un fragmento de anticuerpo monoclonal recombinado humanizado dirigido contra el factor de crecimiento del endotelio vascular de tipo A (VEGF-A). Tiene gran afinidad por las isoformas del VEGF-A (p. ej., VEGF110, VEGF121 y VEGF165), por lo que impide que el VEGF-A se una a sus receptores VEGFR-1 y VEGFR-2.
La unión del VEGF-A a sus receptores promueve la proliferación de células endoteliales, la neovascularización y la hiperpermeabilidad vascular, y todo ello contribuye a la progresión de la forma neovascular de la degeneración macular asociada a la edad y al edema macular causante de disfunción visual en la diabetes y la oclusión de vena retiniana.
Tratamiento de la DMAE húmeda: En la DMAE húmeda, la eficacia y seguridad clínicas de LUCENTIS® se han evaluado en tres ensayos aleatorizados, doble ciego, controlados con tratamiento simulado (sham) o con tratamiento activo de 24 meses de duración, en pacientes con DMAE neovascular. En estos ensayos fueron reclutados un total de 1.323 pacientes (879 con tratamiento activo y 444 con control).
En el ensayo FVF2598g (MARINA), 716 pacientes con neovascularización coroidea (NVC) mínimamente clásica u oculta sin componente clásico recibieron inyecciones intravítreas de LUCENTIS® 0,3 mg (n=238) ó 0,5 mg (n=240) o inyecciones simuladas (n=238) una vez al mes.
En el estudio FVF2587g (ANCHOR), 423 pacientes con lesiones de neovascularización coroidea de tipo predominantemente clásico recibieron: 1) inyecciones intravítreas mensuales de 0,3 mg de ranibizumab y TFD simulada (n=140); 2) inyecciones intravítreas mensuales de 0,5 mg de ranibizumab TFD simulada (n=140); 3) inyecciones intravítreas simuladas y TFD activa con verteporfina (n=143). Se administró TFD simulada o activa con verteporfina junto con la inyección inicial de LUCENTIS® y luego cada tres meses, si la angiografía fluoresceínica indicaba persistencia o recurrencia de la hiperpermeabilidad vascular.
En las Tablas 1, 2 y en la Figura 1 se resumen los resultados clave.
|
Tabla 1. Resultados a los 12 meses y a los 24 meses |
|||
|
Medida del resultado |
Mes |
Tratamiento simulado o sham (n=238) |
LUCENTIS® 0,5 mg (n=240) |
|
Pérdida de agudeza visual <15 letras (%)a (conservación de la visión, variable primaria) |
Mes 12 |
62% |
95% |
|
Mes 24 |
53% |
90% |
|
|
Mejora de la agudeza visual ≥15 letras (%)a |
Mes 12 |
5% |
34% |
|
Mes 24 |
4% |
33% |
|
|
Variación media de la agudeza visual (letras) (desviación estándar)a |
Mes 12 |
–10,5 (16,6) |
+7,2 (14,4) |
|
Mes 24 |
–14,9 (18,7) |
+6,6 (16,5) |
|
|
a p<0,01 |
|||
|
Tabla 2. Resultados a los 12 meses y a los 24 meses en el estudio FVF2587g (ANCHOR) |
|||
|
Medida del resultado |
Mes |
TDF con verteporfina (n=143) |
LUCENTIS® 0,5 mg (n=140) |
|
Pérdida de agudeza visual <15 letras (%)a (mantenimiento de la visión) (variable primaria) |
Mes 12 |
64% |
96% |
|
Mes 24 |
66% |
90% |
|
|
Ganancia de ≥15 letras de agudeza visual (%)a |
Mes 12 |
6% |
40% |
|
Mes 24 |
6% |
41% |
|
|
Cambio medio de la agudeza visual (letras) (desviación estándar)a |
Mes 12 |
–9,5 (16,4) |
+11,3 (14,6) |
|
Mes 24 |
–9,8 (17,6) |
+10,7 (16,5) |
|
|
a p<0,01 |
|||
Figura 1. Cambio medio de la agudeza visual entre el inicio y los 24 meses en el estudio FVF2598g (MARINA) y el estudio FVF2587g (ANCHOR):
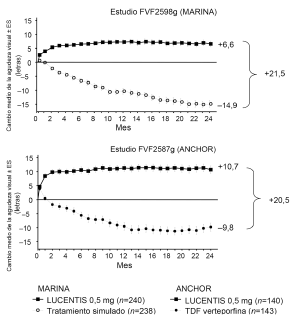
Los resultados de ambos ensayos indicaban que el tratamiento continuo con ranibizumab podía resultar beneficioso también en los pacientes que habían perdido ≥15 letras de agudeza visual con corrección (AVC) en el primer año de tratamiento.
No se ha estudiado el uso de LUCENTIS® después de 36 meses.
El estudio FVF3192g (PIER) fue un ensayo aleatorizado, doble ciego, controlado con tratamiento simulado o sham, concebido para evaluar la seguridad y la eficacia de LUCENTIS® en 184 pacientes con todas las formas de DMAE neovascular. Los pacientes recibieron inyecciones intravítreas de 0,3 mg (n=60) ó 0,5 mg (n=61) de ranibizumab o inyecciones simuladas (sham) (n=63) una vez al mes, en 3 dosis consecutivas, seguido de la administración de una dosis una vez cada 3 meses.
A partir del 14º mes del estudio, se permitió que los pacientes que habían recibido el tratamiento simulado (sham) cambiaran al tratamiento con ranibizumab, y a partir del 19º mes fue posible administrar tratamientos más frecuentes. Los pacientes tratados con LUCENTIS® en el estudio PIER recibieron un promedio de 10 tratamientos.
La variable primaria de eficacia fue el cambio medio en la agudeza visual al cabo de 12 meses comparado con la basal. En general, tras un incremento inicial en la agudeza visual (después de la dosificación mensual), la agudeza visual de los pacientes disminuyó con la dosis trimestral, volviendo al valor basal en el Mes 12 y este efecto se mantuvo al Mes 24 en la mayoría de los pacientes tratados con ranibizumab (82%). Los datos de un número limitado de sujetos que tras más de un año de haber recibido tratamiento simulado pasaron a recibir ranibizumab, sugirieron que el inicio temprano del tratamiento puede asociarse a una mejor conservación de la agudeza visual.
En ambos estudios MARINA y ANCHOR, la mejora de la agudeza visual observada con 0,5 mg de ranibizumab a los 12 meses se acompañaba de beneficios percibidos por los pacientes, los cuales se evaluaron con el cuestionario de función visual (Visual Function Questionnaire, VFQ-25) del National Eye Institute de los Estados Unidos. Las diferencias entre el grupo tratado con 0,5 mg de ranibizumab y los dos grupos de control se evaluaron con valores de p comprendidos entre 0,009 y <0,0001.
La eficacia de LUCENTIS® en el tratamiento de la DMAE húmeda ha sido además confirmada en los ensayos de DMAE finalizados después de la autorización de comercialización. Los datos de los ensayos (MONT BLANC, BPD952A2308 y DENALI, BPD952A2309) no demostraron un efecto adicional en la administración combinada de verteporfina (Visudyne TFD) y LUCENTIS® comparado con LUCENTIS® en monoterapia.
Tratamiento de la alteración visual debida a EMD: La eficacia y seguridad de LUCENTIS® se han evaluado en dos ensayos aleatorizados, doble ciego, controlados con tratamiento simulado (sham) o con tratamiento activo de 12 meses de duración, en pacientes con alteración visual debida al edema macular diabético. En estos ensayos fueron reclutados un total de 496 pacientes (336 con tratamiento activo y 160 con control), la mayoría tenían diabetes tipo II, 28 pacientes tratados con ranibizumab tenían diabetes tipo I.
En el estudio de fase II D2201 (RESOLVE), 151 pacientes que presentaban lesiones maculares centrales causantes de disfunción visual recibieron ranibizumab (6 mg/ml, n=51, 10 mg/ml, n=51) o tratamiento simulado (n=49) en forma de inyecciones intravítreas mensuales hasta que se cumplieran los criterios predefinidos de interrupción del tratamiento.
La dosis inicial de ranibizumab (0,3 mg o 0,5 mg) podía duplicarse en cualquier momento del estudio después de la primera inyección. La fotocoagulación con láser se permitió como tratamiento de rescate desde el Mes 3 en ambos brazos de tratamiento. El estudio tenía dos partes: una parte exploratoria (los primeros 42 pacientes analizados al Mes 6) y una parte confirmatoria (los restantes 109 pacientes analizados al mes 12).
Los resultados clave de la parte confirmatoria del estudio (2/3 de los pacientes) se resumen en la Tabla 3.
|
Tabla 3. Resultados del estudio D2201 (RESOLVE) a los |
||
|
Medida de resultado |
Ranibizumab (ambos grupos) (n=102) |
Tratamiento simulado (n=49) |
|
Cambio medio en la AVMC desde el mes 1 hasta el mes 12 comparado con el inicioa (letras) (desviación estándar) (variable primaria) |
+7,8 (7,72) |
–0,1 (9,77) |
|
Cambio medio en la AVMC al Mes 12ª (letras) (desviación estándar) |
+10,3 (9,14) |
–1,4 (14,16) |
|
Ganancia de ≥ 10 letras en AVMC (%) al Mes 12a |
60,8 |
18,4 |
|
Ganacia de ≥15 letras en AVMC (%) al mes 12 |
32,4 |
10,2 |
|
valor p |
0,0043 |
|
|
a p<0,0001 |
||
En el ensayo de fase III D2301 (RESTORE), se aleatorizaron 345 pacientes con alteración visual debida a edema macular para recibir o bien inyección intravítrea de ranibizumab 0,5 mg en monoterapia y fotocoagulación con láser simulada (n=116), o ranibizumab 0,5 mg y fotocoagulación con láser combinados (n=118), o inyección simulada y fotocoagulación con láser (n=111). El tratamiento con ranibizumab se inició con inyecciones intravítreas mensuales y continuó hasta que la agudeza visual era estable durante un mínimo de tres controles mensuales consecutivos. El tratamiento se reiniciaba cuando se observaba una reducción de la AVMC debida a progresión del EMD. La fotocoagulación con láser se aplicaba al inicio en el mismo día, como mínimo 30 minutos antes de la inyección de ranibizumab, y después según necesidad basándose en los criterios ETDRS.
En la Tabla 4 y la Figura 2 se resumen los resultados clave.
|
Tabla 4. Resultados del estudio D2301 (RESTORE) a los 12 meses |
|||
|
Medida del resultado comparado con el valor inicial |
Ranibizumab 0,5 mg (n=115) |
Ranibizumab 0,5 mg + láser (n=118) |
Láser (n=110) |
|
Cambio medio en la AVMC desde el mes 1 al mes 12a (±desviación estándar) |
6,1 (6,4) |
5,9 (7,9) |
0,8 (8,6) |
|
Ganancia de ≥10 letras o AVMC ≥84a (%) |
37,4 |
43,2 |
15,5 |
|
Ganancia de ≥15 letras o AVMC ≥84 (%) |
22,6 |
22,9 |
8,2 |
|
valor p |
0,0032 |
0,0021 |
|
|
a p<0,0001 |
|||
Figura 2. Cambio medio en la agudeza visual en el tiempo desde el inicio, en el estudio D2301 (RESTORE)
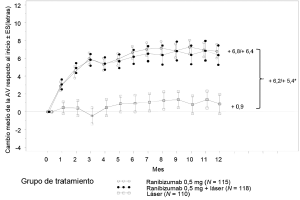
BL=Valor inicial; ES= error estándar de la media.
* Diferencia de medias de mínimos cuadrados, p<0,0001/0,0004 basado en el test bilateral de Cochran-Mantel-Haenszel.
El efecto fue consistente en la mayoría de subgrupos. Sin embargo, sujetos con una AVMC bastante buena al inicio (>73 letras) y con un edema macular con un grosor de la retina central de <300 µm, no parecían beneficiarse del tratamiento con ranibizumab comparado con la fotocoagulación con láser.
La mejora en la agudeza visual observada con LUCENTIS® 0,5 mg a los 12 meses se acompañó de beneficios notificados por el mismo paciente en lo que respecta a las funciones más relacionadas con la visión, medidos según las puntuaciones del Cuestionario de Función Visual del National Eye Institute (VFQ-25). Para las otras subescalas de este cuestionario no pudieron establecerse diferencias ligadas al tratamiento. La diferencia entre LUCENTIS® 0,5 mg y el grupo control fue evaluada con valores de p de 0,0137 (ranibizumab monoterapia) y de 0,0041 (ranibizumab + láser) para la puntuación compuesta del VFQ-25.
En ambos estudios la mejora de la visión se acompañó de una disminución continua en el edema macular medido según el grosor de la retina central (CRT).
Tratamiento de la alteración visual debida al edema macular secundario a OVR: La seguridad y eficacia clínicas de LUCENTIS® en pacientes con alteración visual debida al edema macular secundario a OVR se han evaluado en los ensayos BRAVO y CRUISE, controlados, aleatorizados, doble ciego que reclutaron sujetos con ORVR (n=397) y con OVCR (n=392), respectivamente. En ambos ensayos, los sujetos recibieron o bien ranibizumab intravítreo 0,3 mg o 0,5 mg o inyecciones simuladas. Después de 6 meses, los pacientes en los grupos control con inyección simulada se cambiaron a ranibizumab 0,5 mg.
En el ensayo BRAVO, se permitió la fotocoagulación con láser como rescate en todos los grupos desde el Mes 3.
En las Tablas 5 y 6 y las Figuras 3 y 4 se resumen los resultados clave de los ensayos BRAVO y CRUISE.
|
Tabla 5. Resultados a los 6 meses y a los 12 meses (BRAVO) |
||
|
Tratamiento Simulado/LUCENTIS® 0,5 mg (n=132) |
LUCENTIS® 0,5 mg (n=131) |
|
|
Cambio medio en la agudeza visual a los 6 mesesa (letras) (desviación estándar) (variable primaria) |
7,3 (13,0) |
18,3 (13,2) |
|
Cambio medio en la AVMC a los 12 meses (letras) (desviación estándar). |
12,1 (14,4) |
18,3 (14,6) |
|
Ganancia de ≥15 letras a los 6 mesesa (%) |
28,8% |
61,1% |
|
Ganancia de ≥15 letras en agudeza visual a los 12 meses (%) |
43,9% |
60,3% |
|
Proporción (%) que recibió rescate con láser en 12 meses |
61,4% |
34,4% |
|
a p<0,0001 |
||
Figura 3. Cambio medio en la AVMC desde el inicio en el tiempo hasta el mes 6 y el mes 12 (BRAVO)
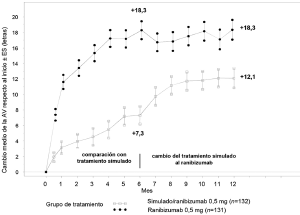
BL=valor inicial; ES = error estándar de la media
|
Tabla 6. Resultados a los 6 meses y a los 12 meses (CRUISE) |
||
|
Tratamiento s simulado/LUCENTIS® 0,5 mg (n=130) |
LUCENTIS® 0,5 mg (n=130) |
|
|
Cambio medio en la agudeza visual a los 6 mesesa (letras) (desviación estándar) (variable primaria) |
0,8 (16,2) |
14,9 (13,2) |
|
Cambio medio en la AVMC a los 12 meses (letras) (desviación estándar) |
7,3 (15,9) |
13,9 (14,2) |
|
Ganancia de ≥15 letras en agudeza visual a los 6 mesesa (%) |
16,9% |
47,7% |
|
Ganancia de ≥15 letras en agudeza visual a los 12 meses (%) |
33,1% |
50,8% |
|
a p<0,0001 |
||
Figura 4. Cambio medio en la AVMC desde el inicio en el tiempo a los 6 meses y a los 12 meses (CRUISE)
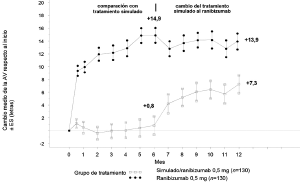
BL= valor inicial; ES = error estándar de la media.
En ambos estudios, la mejora de la visión se acompañó de una reducción continua y significativa del edema macular medido según el grosor central de la retina.
En pacientes con ORVR (BRAVO y extensión HORIZON): Después de 2 años, los sujetos que fueron tratados con tratamiento simulado en los primeros 6 meses y posteriormente cambiados al tratamiento con ranibizumab habían alcanzado ganancias comparables en AV (~15 letras) en comparación con los sujetos que fueron tratados con ranibizumab desde el inicio del ensayo (~16 letras). Sin embargo, el número de pacientes que completaron 2 años fue limitado y en HORIZON sólo se programaron visitas de monitorización trimestrales. Por tanto, en la actualidad no existe evidencia suficiente para recomendar cuándo debe iniciarse el tratamiento con ranibizumab en pacientes con ORVR.
En pacientes con OVCR (CRUISE y ensayo de extensión HORIZON): Después de 2 años, los sujetos que fueron tratados con tratamiento simulado en los primeros 6 meses y posteriormente cambiados al tratamiento con ranibizumab no alcanzaron ganancias comparables en AV (~6 letras) en comparación con los sujetos que fueron tratados con ranibizumab desde el inicio del ensayo (~12 letras).
La mejora en la agudeza visual observada con el tratamiento con ranibizumab a los 6 y 12 meses se acompañó de beneficios notificados por el mismo paciente medido según las subescalas del Cuestionario de Función Visual del National Eye Institute (NEI VFQ-25) relativas a la actividad de cerca y de lejos. La diferencia entre LUCENTIS® 0,5 mg y el grupo control fue evaluada al Mes 6 con valores p entre 0,02 y 0,0002.
Tratamiento de la alteración visual debida a la NVC secundario a MP: Se han evaluado la seguridad y la eficacia clínicas de LUCENTIS® en pacientes con disfunción visual por NVC secundaria a MP, basándose para ello en los datos de los 12 meses del estudio fundamental (pivotal) F2301 (RADIANCE), controlado, aleatorizado, doble ciego. Este ensayo se diseñó para evaluar dos regímenes de tratamiento diferentes de ranibizumab 0,5 mg administrados en forma de inyección intravítrea en comparación con TFD con verteporfina (TFDv, terapia fotodinámica con Visudyne).
Los 277 pacientes fueron asignados aleatoriamente a uno de los grupos siguientes:
• Grupo I (ranibizumab, 0,5 mg; pauta posológica basada en el criterio de «estabilidad», definido como la ausencia de variación de la AVC respecto a las dos evaluaciones mensuales anteriores).
• Grupo II (ranibizumab, 0,5 mg; pauta posológica basada en el criterio de «actividad de la enfermedad», definido como un deterioro de la visión atribuible a la existencia de líquido intrarretiniano o subretiniano o a una fuga activa debida a la lesión de NVC según la TCO, la AF o ambas exploraciones).
• Grupo III (TFDv: desde el final de tercer mes en adelante se permitió a los pacientes recibir ranibizumab)
Durante los 12 primeros meses del estudio, los pacientes recibieron una media de 4,6 inyecciones (mínimo 1 y máximo 11) en el grupo I y 3,5 inyecciones en el grupo II (mínimo 1 y máximo 12). En el grupo II (en el que los pacientes recibieron la pauta terapéutica recomendada según la actividad de la enfermedad, véase Posología y administración), durante el período de estudio de 12 meses, el 50,9% de los pacientes necesitaron 1 o 2 inyecciones, el 34,5%, 3 a 5 inyecciones, y el 14,7%, entre 6 y 12 inyecciones. Siempre en el grupo II, durante el segundo período de 6 meses del estudio, el 62,9% de los pacientes no necesitaron inyecciones.
En la tabla 7 y la figura 5 se resumen los principales resultados del estudio RADIANCE.
|
Tabla 7. Resultados a los 3 meses y a los 12 meses (RADIANCE) |
|||
|
Grupo I Ranibizumab 0,5 mg |
Grupo II Ranibizumab 0,5 mg |
Grupo III TFDv* (n=55) |
|
|
Mes 3 |
|||
|
Cambio medio en la AVMC desde el mes 1 hasta el mes 3 comparada con el inicioa (letras) |
+10,5 |
+10,6
|
+2,2 |
|
Proporción de pacientes que ganaron: |
|||
|
≥ 10 letras, o alcanzaron ≥ 84 letras en la AVMC |
61,9% |
65,5% |
27,3% |
|
≥ 15 letras, o alcanzaron ≥ 84 letras en la AVMC |
38,1% |
43,1% |
14,5% |
|
Mes 12 Número de inyecciones hasta el mes 12: |
|||
|
Media |
4,6 |
3,5 |
NP |
|
Mediana |
4,0 |
2,0 |
NP |
|
Cambio medio en la AVMC desde el mes 1 hasta el mes 12 comparada con el inicio (letras) |
+12,8 |
+12,5 |
NP |
|
Proporción de pacientes que ganaron: |
|||
|
≥ 10 letras, o alcanzaron ≥ 84 letras en la AVMC |
69,5% |
69,0% |
NP |
|
≥ 15 letras, o alcanzaron ≥ 84 letras en la AVMC |
53,3% |
51,7% |
NP |
|
* Grupo comparativo de control hasta el tercer mes. Desde el final del tercer mes en adelante, a los pacientes asignados aleatoriamente al grupo tratado con TFDv se les permitió recibir ranibizumab (en el grupo III, 38 pacientes recibieron ranibizumab desde el final del tercer mes en adelante). a: p <0,00001 en la comparación con el grupo de control de la TFDv. NP: no procede. |
|||
Figura 5. Cambio medio en la AVMC respecto de la inicial a lo largo del tiempo hasta los 12 meses (RADIANCE)
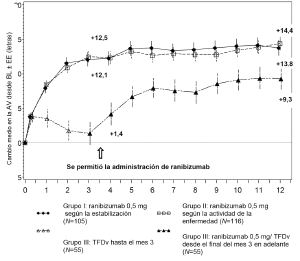
La mejora de la visión se acompañó de una reducción del espesor de la retina central.
Los beneficios comunicados por el paciente se observaron más en los brazos de tratamiento con ranibizumab en comparación con la TFDv (valor de p<0,05), en términos de mejora en la puntuación compuesta y varias subescalas (visión general, actividades de visión cercana, salud mental y dependencia) del NEI VFQ-25).
Población pediátrica: La seguridad y eficacia de ranibizumab aún no han sido estudiadas en pacientes pediátricos.
La Agencia Europea de Medicamentos ha eximido al titular de la obligación de presentar los resultados de los ensayos realizados con LUCENTIS® en los diferentes grupos de la población pediátrica en la DMAE neovascular, la alteración visual debida al EMD, la alteración visual debida al edema macular secundario a la OVR y la alteración visual debida a la NVC secundaria a MP.
Propiedades farmacocinéticas: Tras la administración intravítrea mensual de LUCENTIS® a pacientes con DMAE neovascular, las concentraciones séricas de ranibizumab fueron en general bajas; con niveles máximos (Cmáx) por debajo de la concentración de ranibizumab necesaria para inhibir la actividad biológica de VEGF en un 50% (entre 11 y 27 ng/ml, determinada en un ensayo de proliferación celular in vitro). La Cmáx fue proporcional a la dosis en el intervalo posológico comprendido entre 0,05 y 1,0 mg/ojo., Las concentraciones séricas de ranibizumab en pacientes con OVR fueron similares o ligeramente superiores en comparación con las observadas en los pacientes con DMAE neovascular.
Los análisis de farmacocinética poblacional y la desaparición del ranibizumab del suero en los pacientes con DMAE neovascular que recibieron la dosis de 0,5 mg indican que la semivida de eliminación vítrea del ranibizumab es de unos 9 días en promedio. Tras la administración intravítrea mensual de LUCENTIS® 0,5 mg/ojo, se prevé que la Cmax de ranibizumab sérica alcanzada aproximadamente 1 día después de la administración, varíe en general en un rango de entre 0,79 y 2,90 ng/ml, y que la Cmin varíe en general en un rango de entre 0,07 y 0,49 ng/ml. Se prevé que las concentraciones séricas de ranibizumab es unas 90 000 veces menor que la exposición intravítrea al fármaco.
Poblaciones especiales:
• Disfunción renal: No se han llevado a cabo estudios formales para examinar la farmacocinética de LUCENTIS® en pacientes con disfunción renal. En un análisis de farmacocinética poblacional llevado a cabo en pacientes con DMAE neovascular, el 68% de ellos (136 de 200) tenían insuficiencia renal (leve [50-80 ml/min] en el 46,5%, moderada [30-50 ml/min] en el 20% y grave [<30 ml/min] en el 1,5%). Entre los pacientes con OVR, el 48,2% (253 de 525) tenían insuficiencia renal (leve en el 36,4%, moderada en el 9,5% y grave en el 2,3%). La depuración sistémica fue levemente inferior, pero sin que ello llegara a ser clínicamente significativo.
• Disfunción hepática: No se han llevado a cabo estudios formales para examinar la farmacocinética de LUCENTIS® en pacientes con disfunción hepática.
Datos preclínicos sobre seguridad: La administración intravítrea bilateral de ranibizumab en dosis de entre 0,25 y 2,0 mg/ojo a macacos una vez cada 2 semanas durante 26 semanas produjo efectos oculares dependientes de la dosis.
A nivel intraocular, se registraron aumentos del exudado proteínico (flare) y la celularidad de la cámara anterior dependientes de la dosis, que alcanzaban el máximo dos días después de la inyección. En general, la intensidad de la reacción inflamatoria disminuyó con las inyecciones posteriores o durante la recuperación. En el segmento posterior se observaron infiltración celular y cuerpos flotantes en el vítreo, que también tendían a ser dependientes de la dosis y generalmente persistían al final del período de tratamiento. En el estudio de 26 semanas, la intensidad de la inflamación vítrea aumentó con el número de inyecciones. Sin embargo, se observaron signos de reversibilidad tras la recuperación. La naturaleza y la cronología de la inflamación en el segmento posterior apuntan a una reacción inmunitaria mediada por anticuerpos que puede no tener trascendencia clínica. En algunos animales se observó la formación de cataratas al cabo de un período relativamente largo de intensa inflamación, lo que parece indicar que las alteraciones cristalinianas eran secundarias a inflamación grave. Con independencia de la dosis, tras la inyección intravítrea se observaba un incremento pasajero de la presión intraocular.
Las alteraciones oculares microscópicas estaban relacionadas con la inflamación y no eran indicativas de procesos degenerativos. En la papila de algunos ojos se observaron alteraciones inflamatorias granulomatosas. Estas alteraciones en el segmento posterior cedieron (y en algunos casos se resolvieron) durante el período de recuperación.
Tras la administración intravítrea no se observaron signos de toxicidad sistémica. Se detectaron anticuerpos contra el ranibizumab en el suero y el vítreo de un subgrupo de animales tratados.
No se dispone de datos de carcinogenia ni de mutagenia.
En hembras de mono preñadas, el tratamiento con ranibizumab intravítreo resultando en exposiciones sistémicas máximas 0,9 – 7 veces la peor exposición clínica, no provocó toxicidad en el desarrollo ni teratogenicidad y no tuvo ningún efecto sobre el peso o la estructura de la placenta, aunque en base a su efecto farmacológico, ranibizumab debe considerarse potencialmente teratogénico y embrio/fetotóxico.
La ausencia de efectos mediados por ranibizumab sobre el desarrollo embrio-fetal está plausiblemente relacionado principalmente con la incapacidad del fragmento Fab de atravesar la placenta. Sin embargo, se describió un caso de niveles séricos de ranibizumab materno elevados y presencia de ranibizumab en el suero fetal lo que sugiere que el anticuerpo contra ranibizumab actuó como proteína transportadora (conteniendo la región Fc) para ranibizumab, disminuyendo de ese modo su aclaramiento sérico materno y permitiendo su paso a la placenta. Dado que las investigaciones en el desarrollo embrio-fetal se llevaron a cabo en animales preñados sanos y las enfermedades (tales como la diabetes) pueden modificar la permeabilidad de la placenta para el fragmento Fab, el estudio debe interpretarse con cautela.
CONTRAINDICACIONES: Hipersensibilidad al principio activo o a cualquiera de los excipientes.
Pacientes con infecciones oculares o perioculares en actividad o sospecha de ellas.
Pacientes con inflamación intraocular grave.
EFECTOS SOBRE LA CAPACIDAD PARA CONDUCIR Y UTILIZAR MÁQUINAS: El procedimiento de tratamiento con LUCENTIS® puede producir alteraciones visuales transitorias, que pueden afectar la capacidad para conducir o utilizar máquinas. Los pacientes que experimenten signos no deben conducir ni utilizar máquinas hasta que dichas alteraciones visuales transitorias remitan.
REACCIONES ADVERSAS:
Resumen del perfil de seguridad: La mayoría de las reacciones adversas notificadas tras la administración de LUCENTIS® están relacionadas con el procedimiento de inyección intravítrea.
Las reacciones adversas oculares tras la inyección de LUCENTIS® notificadas más frecuentemente son: dolor ocular, hiperemia ocular, aumento de la presión intraocular, vítritis, desprendimiento de vítreo, hemorragia retiniana, alteración visual, partículas flotantes en el vítreo, hemorragia conjuntival, irritación ocular, sensación de cuerpo extraño en los ojos, aumento del lagrimeo, blefaritis, ojo seco y prurito ocular.
Las reacciones adversas no oculares notificadas más frecuentemente son cefalea, nasofaringitis y artralgia.
Las reacciones adversas notificadas con menor frecuencia, pero de mayor gravedad, incluyen endoftalmitis, ceguera, desprendimiento de retina, desgarro retiniano y catarata traumática iatrogénica.
Se debe informar a los pacientes de los síntomas de estas reacciones adversas potenciales e instruirlos para que informen a su médico en caso de aparición de signos tales como dolor ocular o aumento del malestar en el ojo, empeoramiento del enrojecimiento del ojo, visión borrosa o disminución de la visión, aumento del número de pequeñas manchas en su visión o aumento de la sensibilidad a la luz.
En la siguiente tabla se resumen las reacciones adversas ocurridas tras la administración de LUCENTIS® en los ensayos clínicos.
Listado tabulado de reacciones adversas:#
Las reacciones adversas se listan con un sistema de clasificación de órganos y frecuencia usando el siguiente criterio: muy frecuentes (≥1/10), frecuentes (≥1/100 a <1/10), poco frecuentes (≥1/1000 a <1/100), raras (≥1/10 000 a <1/1000), muy raras (<1/10 000),frecuencia no conocida (no puede estimarse a partir de los datos disponibles). Las reacciones adversas se enumeran en orden decreciente de gravedad dentro de cada intervalo frecuencia.
|
Infecciones e infestaciones |
|
|
Muy frecuentes |
Nasofaringitis |
|
Frecuentes |
Infección de las vías urinarias* |
|
Trastornos de la sangre y del sistema linfático |
|
|
Frecuentes |
Anemia |
|
Trastornos del sistema inmunológico |
|
|
Frecuentes |
Hipersensibilidad |
|
Trastornos psiquiátricos |
|
|
Frecuentes |
Ansiedad |
|
Trastornos del sistema nervioso |
|
|
Muy frecuentes |
Cefalea |
|
Trastornos oculares |
|
|
Muy frecuentes |
Vitritis, desprendimiento de vítreo, hemorragia retiniana, alteración visual, dolor ocular, partículas flotantes en el vítreo, hemorragia conjuntival, irritación ocular, sensación de cuerpo extraño en los ojos, aumento del lagrimeo, blefaritis, ojo seco, hiperemia ocular, prurito ocular. |
|
Frecuentes |
Degeneración retiniana, trastorno retiniano, desprendimiento de retina, desgarro retiniano, desprendimiento del epitelio pigmentario retiniano, desgarro del epitelio pigmentario retiniano, agudeza visual reducida, hemorragia vítrea, trastorno del cuerpo vítreo, uveítis, iritis, iridociclitis, catarata, catarata subcapsular, opacificación de la cápsula posterior, queratitis punctata, abrasión corneal, células flotantes en la cámara anterior, visión borrosa, hemorragia en el lugar de la inyección, hemorragia ocular, conjuntivitis, conjuntivitis alérgica, secreción ocular, fotopsia, fotofobia, molestia ocular, edema palpebral, dolor palpebral, hiperemia conjuntival. |
|
Poco frecuentes |
Ceguera, endoftalmitis, hipopion, hipema, queratopatía, adhesión del iris, depósitos corneales, edema corneal, estrías corneales, dolor en el lugar de inyección, irritación en el lugar de inyección, sensación anormal en el ojo, irritación palpebral. |
|
Trastornos respiratorios, torácicos y mediastínicos |
|
|
Frecuentes |
Tos |
|
Trastornos gastrointestinales |
|
|
Frecuentes |
Náuseas |
|
Trastornos de la piel y del tejido subcutáneo |
|
|
Frecuentes |
Reacciones alérgicas (erupción, urticaria, prurito, eritema). |
|
Trastornos musculoesqueléticos y del tejido conjuntivo |
|
|
Muy frecuentes |
Artralgia |
|
Exploraciones complementarias |
|
|
Muy frecuentes |
Aumento de la presión intraocular |
|
# Las reacciones adversas se definieron como acontecimientos adversos (en al menos 0,5 puntos porcentuales de pacientes) que ocurrieron con una frecuencia superior (como mínimo 2 puntos porcentuales) en pacientes que recibieron el tratamiento con LUCENTIS® 0,5 mg respecto a los que recibieron el tratamiento control (tratamiento simulado (sham) o TFD con verteporfina). * Observado sólo en población con EMD |
|
Reacciones adversas de clase terapéutica: En los ensayos fase III en DMAE húmeda, la frecuencia global de hemorragias no oculares, un efecto adverso potencialmente relacionado con la inhibición sistémica del VEGF (factor de crecimiento endotelial vascular), fue ligeramente superior a los pacientes tratados con ranibizumab.
Sin embargo, no hubo un patrón consistente entre las distintas hemorragias. Tras el uso intravítreo de inhibidores del VEGF existe un riesgo teórico de acontecimientos tromboembólicos arteriales, incluyendo accidente cerebrovascular e infarto de miocardio. En los ensayos clínicos con LUCENTIS® se observó una incidencia baja de acontecimientos tromboembólicos arteriales en pacientes con DMAE, EMD, OVR y MP y no hubo ninguna diferencia destacable entre los grupos tratados con ranibizumab comparado con el control.
Notificación de sospechas de reacciones adversas: Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento.
INCOMPATIBILIDADES: Dada la ausencia de estudios de compatibilidad, Lucentis no se debe mezclar con otros medicamentos.
INTERACCIONES: No se han efectuado estudios de interacción propiamente dichos.
El uso conjunto de la TFD con verteporfina y LUCENTIS® en la DMAE húmeda y la MP se aborda en el apartado Propiedades farmacodinámicas.
El uso conjunto de la fotocoagulación con láser y LUCENTIS® en el EMD y la ORVR se aborda en los apartados Posología y modo de administración, y Propiedades farmacodinámicas.
ADVERTENCIAS Y PRECAUCIONES ESPECIALES DE EMPLEO:
Reacciones relacionadas con la inyección intravítrea: Las inyecciones intravítreas, como las de LUCENTIS®, se han asociado con endoftalmitis, inflamación intraocular, desprendimiento de retina regmatógeno, desgarros retinianos y catarata traumática iatrogénica (véase Reacciones adversas). Siempre que se administre LUCENTIS® se deben emplear técnicas asépticas adecuadas. Además, debe vigilarse a los pacientes durante la semana posterior a la inyección para poder administrar tratamiento temprano en caso de infección. Es preciso instruirlos para que notifiquen sin demora todo síntoma indicativo de endoftalmitis o cualquiera de los problemas mencionados.
Aumento de la presión intraocular: Se han observado aumentos transitorios de la presión intraocular (PIO) en los 60 minutos siguientes a la inyección de LUCENTIS® (véase Reacciones adversas). También se han descrito aumentos sostenidos de la PIO. Se deben vigilar la presión intraocular y la perfusión de la papila del nervio óptico y, en su caso, tratarlas adecuadamente.
Tratamiento bilateral: No se ha estudiado la seguridad y eficacia de la terapia con LUCENTIS® administrada en los dos ojos de forma concurrente. Si se lleva a cabo el tratamiento bilateral a la vez, esto podría conllevar un incremento de la exposición sistémica, lo cual podría aumentar el riesgo de efectos adversos sistémicos.
Inmunogenicidad: Hay un potencial de inmunogenicidad con LUCENTIS®. Dado que en sujetos con EMD existe un potencial para una exposición sistémica incrementada, no puede excluirse un mayor riesgo para desarrollar hipersensibilidad en esta población de pacientes. También se deberá instruir a los pacientes sobre la necesidad de notificar si la inflamación intraocular incrementa en su gravedad, lo que puede ser un signo clínico atribuible a la formación de anticuerpos intraoculares.
Uso concomitante con otros anti-VEGF (factor de crecimiento endotelial vascular): LUCENTIS® no se deberá administrar de forma concurrente con otros medicamentos anti-VEGF (sistémicos u oculares).
Aplazamiento del tratamiento con LUCENTIS®: La administración se deberá aplazar y el tratamiento no deberá reanudarse antes del siguiente tratamiento programado en caso de:
• Una disminución en la agudeza visual mejor corregida (AVMC) de ≥ 30 letras comparado con la última evaluación de la agudeza visual;
• Una presión intraocular de ≥ 30 mmHg;
• Una rotura retiniana
• Una hemorragia subretiniana que afecte al centro de la fóvea, o, si el tamaño de la hemorragia es ≥ 50% del área total de la lesión;
• Cirugía intraocular realizada en los 28 días previos o previstos durante los 28 días posteriores.
Desgarro del epitelio pigmentario de la retina: Los factores de riesgo asociados con el desarrollo de un desgarro del epitelio pigmentario de la retina tras la terapia con anti-VEGF para la DMAE exudativa, incluyen un desprendimiento del epitelio pigmentario de la retina extenso y/o elevado. Cuando se inicie la terapia con LUCENTIS® se debe tener precaución en pacientes con estos factores de riesgo de desarrollar desgarros del epitelio pigmentario de la retina.
Desprendimiento de retina regmatógeno o agujeros maculares: El tratamiento se debe interrumpir en sujetos con desprendimiento de retina regmatógeno o agujeros maculares en estadíos 3 ó 4.
Poblaciones con datos limitados: Sólo existe experiencia limitada en el tratamiento de sujetos con EMD debido a diabetes tipo I. LUCENTIS® no ha sido estudiado en pacientes que hayan recibido previamente inyecciones intravítreas, en pacientes con infecciones sistémicas activas, retinopatía diabética proliferativa, ni en pacientes con enfermedades oculares simultáneas tales como desprendimiento de retina o agujero macular. Tampoco existe experiencia en el tratamiento con LUCENTIS® en pacientes diabéticos con un HbA1c por encima del 12% e hipertensión no controlada. El médico debe tener en cuenta esta falta de información al tratar a tales pacientes.
En pacientes con MP, hay datos limitados del efecto de LUCENTIS® en pacientes que han sido sometidos previamente a un tratamiento de terapia fotodinámica con verteporfina (TFDv) sin éxito. Además, mientras que en sujetos con lesiones subfoveales y yuxtafoveales se observó un efecto consistente, no hay datos suficientes para establecer conclusiones sobre el efecto de LUCENTIS® en sujetos con MP y lesiones extrafoveales.
Efectos sistémicos tras el uso intravítreo: Se han notificado acontecimientos adversos sistémicos, incluyendo hemorragias no oculares y acontecimientos tromboembólicos arteriales tras la inyección intravítrea de inhibidores del VEGF.
Existen datos limitados sobre seguridad en el tratamiento de pacientes con EMD, edema macular debido a OVR y NVC secundaria a MP que tengan antecedentes de accidente cerebrovascular o ataques isquémicos transitorios. Se debe tener precaución cuando se traten tales pacientes.
Episodios previos de OVR, oclusión de la rama venosa retiniana y oclusión de la vena central retiniana isquémicas: Existe experiencia limitada en el tratamiento de pacientes con episodios previos de OVR y de pacientes con oclusión de la rama venosa retiniana (ORVR) y oclusión de la vena central retiniana (OVCR) isquémicas. No se recomienda el tratamiento en pacientes con OVR que presentan signos clínicos de pérdida irreversible de la función visual isquémica.
INSTRUCCIONES DE USO Y MANIPULACIÓN:
Los viales son únicamente para un solo uso (véase Posología y modo de administración).
Para preparar LUCENTIS® para la administración intravítrea, siga las instrucciones que se indican a continuación:
|
A
|
1. Antes de extraer la solución, desinfecte la parte externa del tapón de goma del vial [frasco ampolla]. 2. Monte la aguja de filtro de 5 µm (suministrada) en la jeringa de 1 ml (suministrada) utilizando una técnica aséptica. Perfore el centro del tapón del vial con la aguja de filtro roma hasta que la punta toque el fondo del vial. 3. Extraiga todo el líquido del vial manteniendo este en posición vertical e inclinándolo ligeramente para facilitar la extracción completa. |
|
B
|
4. Al vaciar el vial, asegúrese de retraer el émbolo de la jeringa lo suficiente para vaciar por completo la aguja de filtro. 5. Deje la aguja de filtro roma en el vial y desacople de ella la jeringa. Una vez extraído el contenido del vial, la aguja de filtro debe desecharse y no utilizarse para la inyección intravítrea. |
|
C
|
6. Con una técnica aséptica, monte firmemente la aguja de inyección (suministrada) en la jeringa. 7. Retire con cuidado el capuchón de la aguja de inyección sin desacoplar esta de la jeringa. Nota: Mientras retira el capuchón, sujete la aguja de inyección por el cono amarillo. |
|
D
|
8. Expulse cuidadosamente el aire contenido en la jeringa y ajuste la dosis a la marca de 0,05 ml que figura en la jeringa. La jeringa ya está preparada para la inyección. Nota: No limpie la aguja de inyección. No tire del émbolo hacia atrás. |
Todo el producto que no se haya utilizado y el material de desecho deben eliminarse con arreglo a la normativa local.
Nota: LUCENTIS® debe conservarse fuera del alcance y de la vista de los niños.
POSOLOGÍA Y MODO DE ADMINISTRACIÓN:
Posología: Viales [frascos ampolla] de un solo uso, únicamente para administración intravítrea.
Administrar más de una inyección a partir de un mismo vial entraña riesgo de contaminación y de una ulterior infección.
LUCENTIS® debe ser administrado por un oftalmólogo cualificado y con experiencia en inyecciones intravítreas.
La dosis recomendada de LUCENTIS® es de 0,5 mg administrados como una única inyección intravítrea. Ello corresponde a un volumen de inyección de 0,05 ml. El intervalo entre dosis no debe ser inferior a un mes.
Población destinataria general:
• Tratamiento de la DMAE neovascular («húmeda»): La dosis recomendada de LUCENTIS® es 0,5 mg administrada mensualmente en forma de inyección intravítrea única. Esto corresponde a un volumen de inyección de 0,05 mL.
El tratamiento se administra mensualmente y de forma continuada hasta alcanzar la agudeza visual máxima, es decir hasta que la agudeza visual de los pacientes es estable durante tres controles mensuales consecutivos realizados durante el tratamiento con ranibizumab.
A partir de ese momento se debe controlar la agudeza visual de los pacientes mensualmente.
El tratamiento se reanuda cuando el control indique una pérdida de agudeza visual debida a DMAE húmeda. Entonces se deben administrar inyecciones mensuales hasta alcanzar nuevamente una agudeza visual estable durante tres controles mensuales colectivos (lo que implica un mínimo de dos inyecciones). El intervalo entre dos dosis no debe ser inferior a un mes.
• Tratamiento de la disfunción visual por EMD o a edema macular secundario a OVR: La dosis recomendada de LUCENTIS® es 0,5 mg administrada mensualmente en forma de inyección intravítrea única. Esto corresponde a un volumen de inyección de 0,05 mL.
El tratamiento se administra mensualmente y de forma continuada hasta alcanzar la agudeza visual máxima es decir, hasta que la agudeza visual de los pacientes es estable durante tres controles mensuales consecutivos realizados durante el tratamiento con ranibizumab. Si no hay ninguna mejora en la agudeza visual en el transcurso de las primeras tres inyecciones, no se recomienda continuar con el tratamiento.
A partir de ese momento se debe controlar la agudeza visual de los pacientes mensualmente.
El tratamiento se reanuda cuando el control indique una pérdida de agudeza visual debida a EMD o a edema macular secundario a OVR. Entonces se deben administrar inyecciones mensuales hasta alcanzar nuevamente una agudeza visual estable durante tres controles mensuales consecutivos (lo que implica un mínimo de dos inyecciones). El intervalo entre dos dosis no debe ser inferior a un mes.
— LUCENTIS® y fotocoagulación con láser en EMD y en edema macular secundario a oclusión de la rama venosa retiniana (ORVR): Existe alguna experiencia con LUCENTIS® administrado concomitantemente con fotocoagulación con láser. Cuando se administren en el mismo día, LUCENTIS® se debe administrar como mínimo 30 minutos después de la fotocoagulación con láser previamente. LUCENTIS® puede administrarse en pacientes que han recibido fotocoagulación con láser previamente.
• Tratamiento de la disfunción visual por NVC secundaria a MP: El tratamiento se inicia con una sola inyección.
Si el control indica signos de actividad de la enfermedad, p. ej. Disminución de la agudeza visual y/o signos de actividad de la lesión, se recomienda continuar con el tratamiento.
El seguimiento de la actividad de la enfermedad puede incluir examen clínico, tomografía de coherencia óptica (OCT) o angiografía con fluoresceína (AF).
Mientras que muchos pacientes pueden necesitar únicamente una o dos inyecciones durante el primer año, algunos pacientes pueden necesitar tratamiento con mayor frecuencia. Por lo tanto, se recomienda un seguimiento mensual durante los dos primeros meses y a partir de entonces como mínimo cada tres meses durante el primer año. Después del primer año, el médico deberá determinar la frecuencia de seguimiento.
El intervalo entre dos dosis no debe ser inferior a un mes.
— LUCENTIS® y la terapia fotodinámica con Visudyne en la NVC secundaria a MP: No hay experiencia en la administración concomitante de LUCENTIS® y Visudyne.
Poblaciones especiales:
• Insuficiencia hepática: LUCENTIS® no ha sido estudiado en pacientes con insuficiencia hepática. Sin embargo, no es necesaria ninguna consideración especial en esta población.
• Insuficiencia renal: No es necesario ningún ajuste de la dosis en pacientes con insuficiencia renal.
• Pacientes de edad avanzada: No se requiere ningún ajuste de la dosis en pacientes de edad avanzada. Existe experiencia limitada en pacientes con EMD mayores de 75 años.
• Población pediátrica: No se ha establecido la seguridad y eficacia de LUCENTIS® en niños y adolescentes menores de 18 años de edad. No se dispone de datos.
Forma de administración: Vial para un solo uso. Únicamente para vía intravítrea.
Antes de la administración de LUCENTIS® se debe comprobar visualmente la ausencia de partículas y decoloración.
Antes del tratamiento, se debe instruir al paciente en la autoadministración de gotas antimicrobianas (cuatro veces al día durante 3 días, antes y después de cada inyección).
El procedimiento de inyección deberá llevarse a cabo bajo condiciones asépticas, que incluyen el lavado quirúrgico de las manos, el uso de guantes estériles, un campo estéril, un blefaróstato estéril para los párpados (o equivalente) y la disponibilidad de una paracentesis estéril (en caso necesario).
Antes de realizar el procedimiento de inyección intravítrea, se deberá evaluar detalladamente la historia clínica del paciente en cuanto a reacciones de hipersensibilidad. Antes de la inyección se debe desinfectar la piel de la zona periocular, párpado y superficie ocular, y se debe administrar una anestesia adecuada y un microbicida tópico de amplio espectro.
Para la información relativa a la preparación de LUCENTIS®, ver Instrucciones de uso y manipulación.
La aguja para inyección se deberá introducir 3,5 – 4,0 mm por detrás del limbo en la cavidad vítrea, evitando el meridiano horizontal y en dirección al centro del globo. Seguidamente debe liberarse el volumen de inyección de 0,05 mL; las inyecciones siguientes deberán aplicarse cada vez en un punto escleral distinto.
SOBREDOSIS: Se han notificado casos de sobredosis accidental en los estudios clínicos de la DMAE húmeda y en la farmacovigilancia posterior a la comercialización. Las reacciones adversas asociadas con mayor frecuencia a estos casos notificados fueron aumento de la presión intraocular, ceguera transitoria, agudeza visual reducida, edema corneal, dolor corneal y dolor ocular. En caso de sobredosis, se debe realizar un seguimiento y tratamiento de la presión intraocular, y tratarla si el médico responsable lo considera necesario.
MUJERES EN EDAD DE PROCREAR, EMBARAZO, LACTANCIA Y FECUNDIDAD:
Mujeres en edad de procrear: Las mujeres en edad de procrear deben utilizar métodos anticonceptivos eficaces durante el tratamiento.
Embarazo: No se dispone de datos clínicos sobre la exposición de mujeres embarazadas al ranibizumab.
Los estudios en monos cinomolgos no indican que el ranibizumab tenga efectos perjudiciales directos ni indirectos sobre el embarazo o el desarrollo embriofetal (véase Datos sobre toxicidad preclínica). La exposición sistémica al ranibizumab es baja tras la administración intraocular, pero debido a su mecanismo de acción, este fármaco debe considerarse potencialmente teratógeno, embriotóxico y fetotóxico. Por consiguiente, no debe administrarse ranibizumab durante el embarazo a no ser que los beneficios previstos justifiquen los posibles riesgos para el feto. En el caso de las mujeres que deseen quedar embarazadas y hayan sido tratadas con ranibizumab, se recomienda que esperen al menos 3 meses desde la última dosis antes de concebir.
Lactancia: No se sabe si el ranibizumab (LUCENTIS®) se excreta en la leche humana. Como medida de precaución, se recomienda no amamantar durante el tratamiento con LUCENTIS®.
Fecundidad: No se dispone de datos sobre la fecundidad.
FORMA DE PRESENTACIÓN:
Caja con un vial de vidrio tipo I incoloro x 0.23 mL de solución inyectable.
Caja con un vial x 0.23 mL + 01 aguja con filtro 18G 1 ½” + 01 aguja 30G ½” + 01 jeringa de 1 mL.
Fabricante: Véase el envase exterior.
Prospecto internacional
Fecha de distribución de la información: mayo de 2013
NOVARTIS PHARMA AG, Basilea (Suiza)
® Marca registrada
CONSERVACIÓN: Véase el envase exterior.
Conservar en condiciones refrigeradas (entre 2 °C y 8 °C).
No congelar.
No usar LUCENTIS® después de la fecha de caducidad que figura en el envase («EXP»).